El estimulador carotídeo es un dispositivo que activa eléctricamente el mecanismo barorreflejo. Esto tiene el efecto de debilitar el tono simpático y amortiguar el sistema renina-angiotensina-aldosterona, provocando una reducción de la presión arterial y de la frecuencia cardiaca. La terapia de activación barorrefleja (BAT) produce una reducción media permanente de la presión arterial sistólica de 40-50 mmHg al cabo de cuatro años. Además del efecto reductor de la presión arterial, se observó una reducción del grosor del músculo cardiaco en los pacientes. Actualmente se está probando su efecto en pacientes con insuficiencia cardiaca. La implantación del dispositivo se considera segura. El estimulador carotídeo ya está disponible en varios países europeos.
La hipertensión arterial, definida como una presión arterial sistólica superior a 140 mmHg o una presión arterial diastólica superior a 90 mmHg, afecta a más del 30% de los adultos del mundo occidental. Un tratamiento eficaz de la tensión arterial conlleva una reducción sustancial del riesgo de ictus, infarto de miocardio e insuficiencia cardiaca [1,2]. A pesar del tratamiento farmacológico optimizado y de los cambios en el estilo de vida, sólo entre el 25 y el 34% de los pacientes alcanzan un objetivo de tensión arterial de 140/90 mmHg o inferior [3]. Muchos pacientes tienen una hipertensión refractaria a la terapia o sufren efectos secundarios inducidos por la medicación.
La farmacoterapia es y sigue siendo el pilar más importante del tratamiento de la hipertensión arterial. En los últimos diez años, sin embargo, se han hecho públicas otras formas de terapia además del tratamiento puramente medicinal:
- La estimulación eléctrica de los barorreceptores
- Biorretroalimentación y otros tratamientos psicosomáticos
- Denervación de la arteria renal
- La vacuna contra la tensión arterial (anticuerpos contra la angiotensina)
- La estimulación eléctrica del nervio vago.
Tanto la denervación de la arteria renal como la vacunación contra la presión arterial no lograron ser aceptadas [4,5]. Y hace poco, en el último Congreso de la ESC 2014 celebrado en Barcelona, se presentaron los resultados del estudio NECTAR-HF, que demuestran que la estimulación del nervio vago no mejora la función cardiaca [6].
Por otro lado, la terapia de activación barorrefleja mediante un estimulador carotídeo pudo demostrar una reducción sostenida de la presión arterial en pacientes con hipertensión arterial refractaria.
Sobre la historia
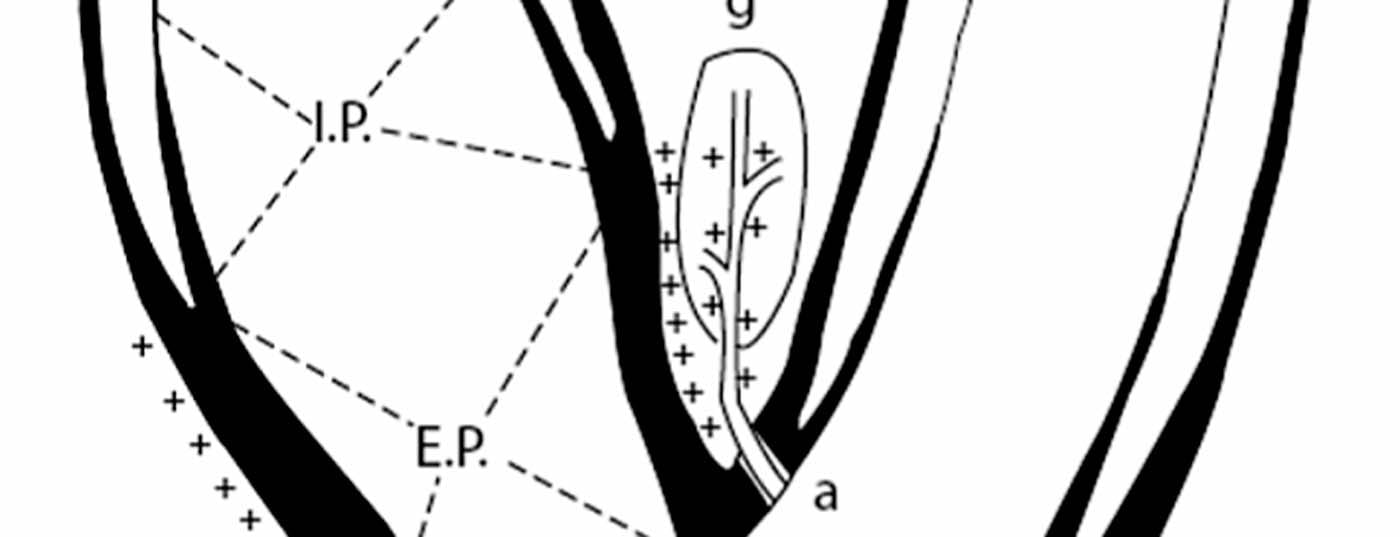
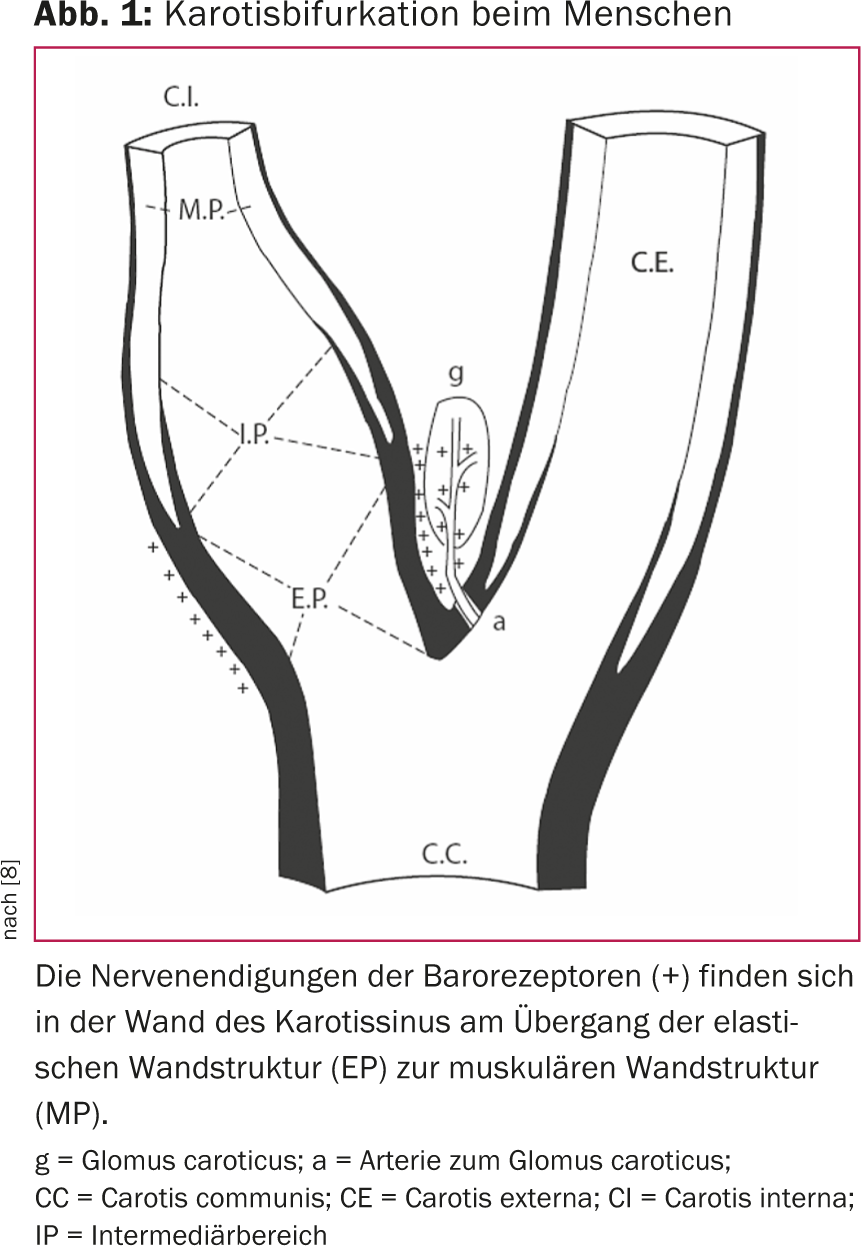
La importancia del barorreflejo para la regulación de la presión arterial se reconoció hace más de 80 años [7]. En los seres humanos, los llamados sensores de la presión sanguínea, es decir, los barorreceptores, están situados principalmente en el arco aórtico, en las arterias subclavias y en la zona del seno carotídeo. Los barorreceptores del seno carotídeo parecen ser dominantes. La distribución y el mecanismo de retroalimentación de las fibras nerviosas barorreceptoras se han estudiado intensamente (Fig. 1) [8]. Esencialmente, un aumento de la presión sanguínea provoca un aumento de la tensión de la pared del seno carotídeo. Esto activa los barorreceptores de la pared del seno carotídeo, lo que se manifiesta en un aumento de la frecuencia y la amplitud de los impulsos nerviosos aferentes. Los impulsos están interconectados en el cerebro y conducen, tanto neurohumoralmente como a través de la modulación del sistema nervioso autónomo, a una amortiguación del tono simpático. En consecuencia, la presión arterial se ve influida a continuación por la función cardiaca, por los riñones y por la resistencia vascular periférica (Fig. 2).
Ya en los años sesenta se utilizaron estimuladores carotídeos en un estudio en pacientes con hipertensión arterial refractaria [9]. Sin embargo, por razones técnicas y porque se han desarrollado mejores fármacos para la tensión arterial, se ha abandonado este enfoque terapéutico y la industria ha dirigido su atención al desarrollo de marcapasos. La idea de la estimulación eléctrica de los barorreceptores no se retomó hasta principios de este siglo. Tanto los estudios en animales como los estudios a largo plazo en humanos han demostrado un efecto positivo y duradero en la regulación de la presión arterial [10,11].
Especificación del dispositivo y técnica de implantación
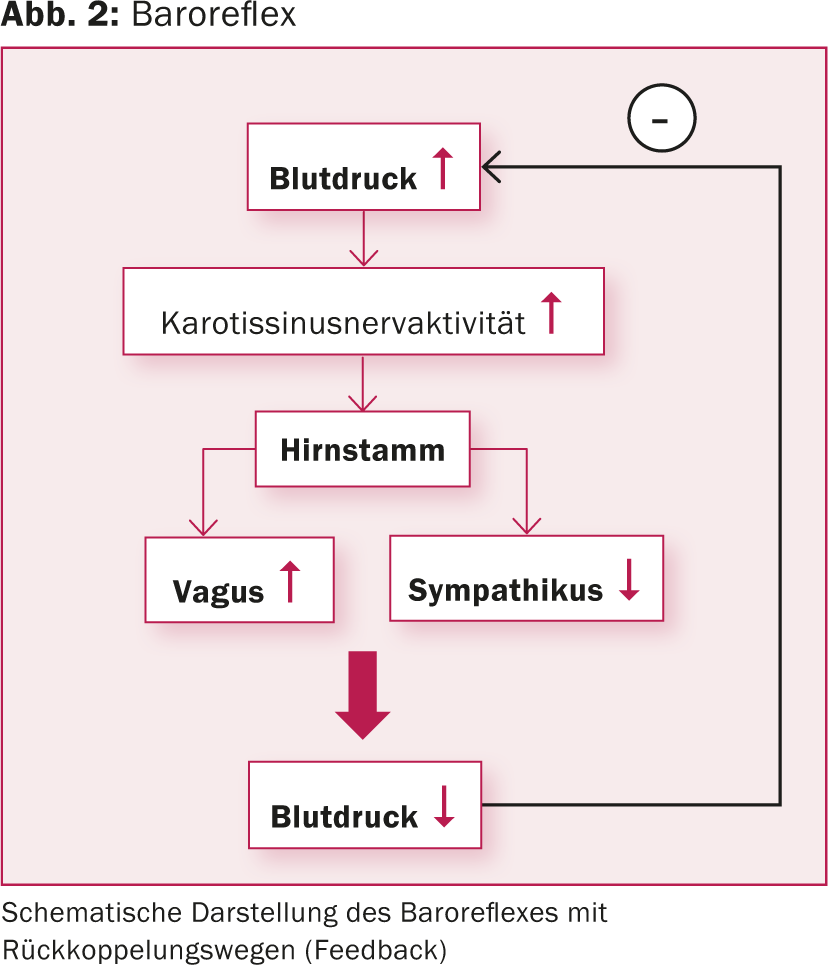
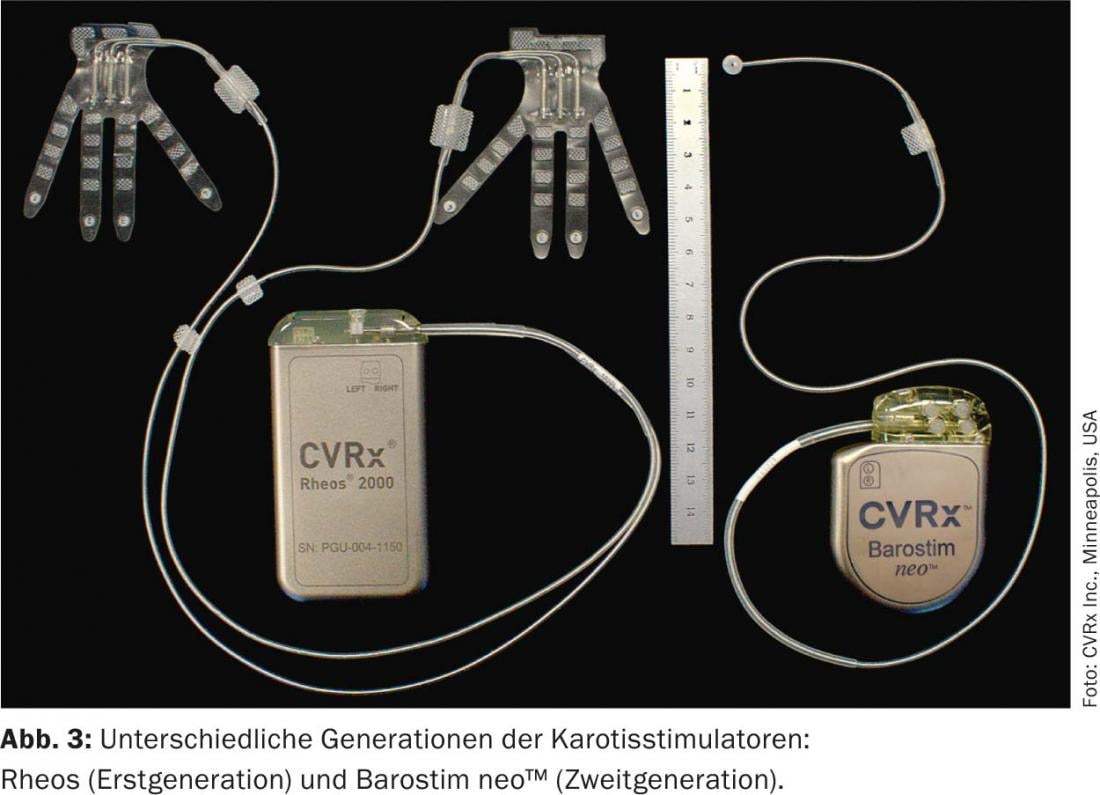
El dispositivo de primera generación (Rheos-System Baroreflex Activation Therapy Device®, CVRx Inc., Minneapolis, MN, EE.UU.) requirió la implantación de un generador y dos sondas. Los electrodos se colocaron alrededor del seno carotídeo en ambos lados. El dispositivo de nueva generación (Barostim neo™), en cambio, sólo tiene una sonda, que se implanta preferentemente en el lado derecho. Además, se ha reducido considerablemente el tamaño del generador y del electrodo y se ha prolongado la vida útil de la batería hasta los 48 meses de media. En la estimulación monopolar, el generador sirve de electrodo activo (fig. 3 y 4). Además, ahora la corriente se aplica de forma constante y ya no intermitente.
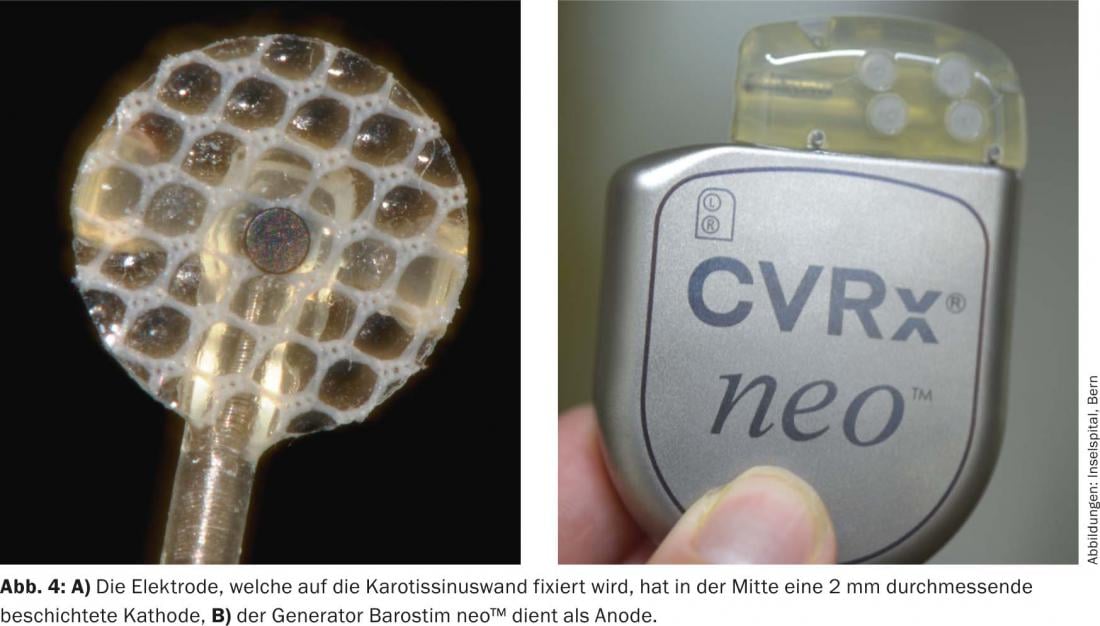
La implantación del dispositivo se realiza bajo anestesia. El procedimiento dura entre 60 y 90 minutos. La bifurcación carotídea y la pared anterior del seno carotídeo se visualizan mediante un abordaje quirúrgico a través de la bifurcación carotídea derecha. A continuación, compruebe qué zona del seno carotídeo presenta la respuesta más fuerte (es decir, disminución de la presión arterial sistólica y/o del pulso). A continuación, se fija el electrodo con suturas finas. Se forma un bolsillo para el generador infraclavicularmente a la derecha, de forma similar a la implantación de un marcapasos. El electrodo se tuneliza a lo largo de la arteria carótida hasta el nivel del yugulum y luego por vía subcutánea hasta el bolsillo del generador y se conecta a éste. Se forma un bucle de alivio en la zona de la arteria carótida común , que debería evitar la tracción del electrodo cuando se gira la cabeza. La anestesia debe planificarse específicamente, ya que los anestésicos inhalatorios en particular pueden amortiguar el barorreflejo. La operación no es estresante y puede realizarse bien durante una corta hospitalización. El dispositivo sólo se enciende entre dos y cuatro semanas después de la implantación. La medicación antihipertensiva debe continuarse y, en función de la respuesta de la presión arterial a la estimulación de los barorreceptores, puede reducirse gradualmente con el tiempo.
Estudios clínicos
Dentro de un estudio agudo (BRASS, BaroReceptor Activation System Study), activamos eléctricamente el barorreflejo durante la cirugía de la carótida común [12]. Bajo una estimulación creciente, se pudo lograr una reducción significativa de la presión sanguínea y del pulso dependiente del voltaje. La respuesta más fuerte se detectó cuando se estimuló con 4-6 voltios. Esto demostró de forma reproducible que la estimulación eléctrica del barorreflejo provoca un cambio inmediato en la presión arterial. Se trata de un estudio importante en relación con la implantación permanente del dispositivo para reducir la presión arterial en pacientes con hipertensión refractaria.
Pacientes con hipertensión refractaria
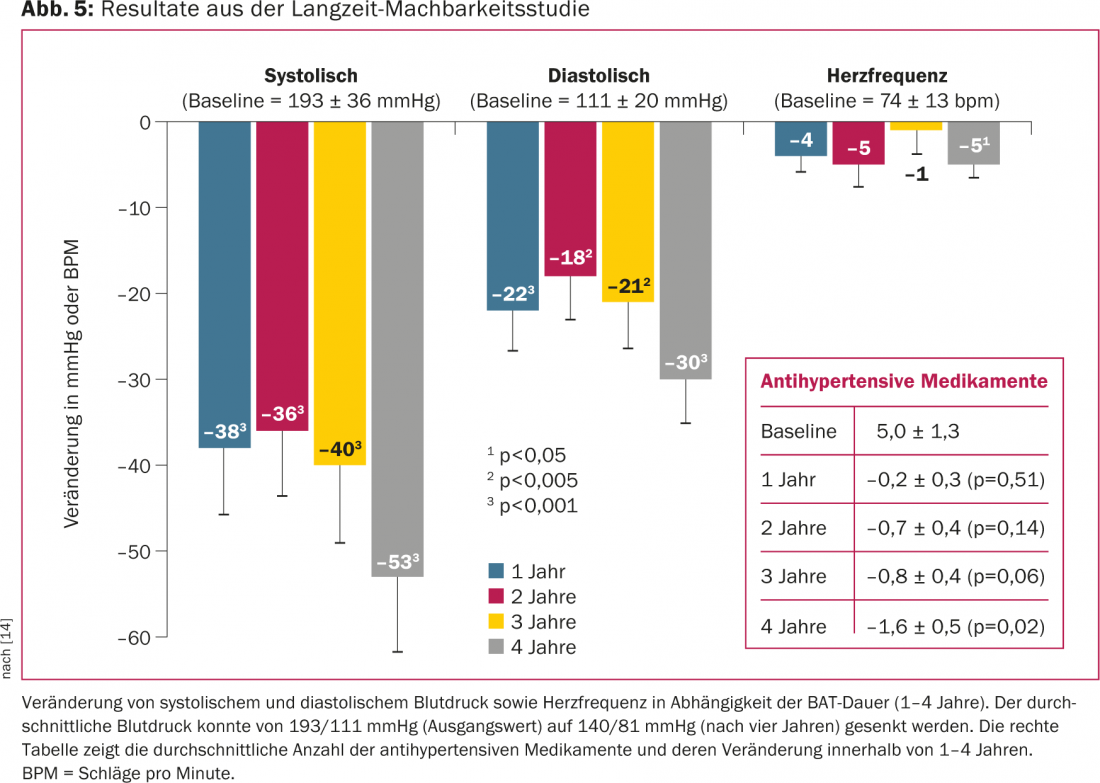
El estudio DEBuT-HT(Device Based Therapyin Hypertension Trial) fue un estudio multicéntrico europeo prospectivo, no aleatorizado, que investigó la seguridad y viabilidad del estimulador carotídeo en 45 pacientes de con hipertensión refractaria. El criterio de inclusión fue una presión arterial sistólica superior a 160 mmHg a pesar de un régimen farmacológico con tres fármacos antihipertensivos, uno de los cuales debía ser un diurético [13]. La medicación antihipertensiva no se modificó durante el periodo de estudio. El criterio de valoración principal fue una reducción de la presión arterial sistólica de al menos 10 mmHg tres meses después de la MTD. A lo largo de tres años, se controlaron todos los acontecimientos graves y todas las complicaciones relacionadas con la implantación y el dispositivo. Antes de la implantación, la presión arterial sistólica media y la frecuencia del pulso eran de casi 180 mmHg y 180 mmHg, respectivamente. 80 latidos por minuto con una ingesta media de 5,5 fármacos antihipertensivos por paciente. Después de tres meses, la presión arterial media se redujo una media de más de 20 mmHg. En todo caso, la reducción de la presión arterial fue aún mayor tras dos y tres años de seguimiento [13]. Después de cuatro años, la presión arterial sistólica se redujo incluso una media de 53 mmHg (Fig. 5) [14]. El procedimiento de implantación demostró ser seguro. La colocación del electrodo alrededor del seno carotídeo no produjo estenosis de la arteria carótida. La satisfacción de los pacientes fue muy alta y éstos declararon una mejor calidad del sueño, menos dolores de cabeza y una mayor concentración.
Se inició un ensayo de fase III (Rheos Pivotal Trial) con 265 pacientes en EE.UU. y Europa. Se trató de un ensayo aleatorizado doble ciego controlado con placebo en pacientes con hipertensión refractaria. Un mes después de la implantación del sistema Rheos, los pacientes fueron aleatorizados 2:1, es decir, en dos tercios de los pacientes el dispositivo se encendió inmediatamente después de la aleatorización y en el resto sólo después de seis meses. Se realizó un seguimiento de ambos grupos de pacientes durante doce meses después de la aleatorización. El estudio mostró una reducción de la presión arterial sistólica media de 35 mmHg al cabo de doce meses. Más del 50% de los pacientes alcanzaron un valor objetivo de presión arterial ≤140 mmHg [15,16]. Se observó un ligero descenso inicial de la tasa de filtración glomerular tras encender el dispositivo. Esto se interpretó como una reacción a la reducción de la presión arterial. Sin embargo, en el curso a largo plazo, la función renal permaneció estable [17].
En un análisis de subgrupos del estudio DEBuT-HT, se investigó el efecto de la alteración de la presión arterial sobre la regulación autonómica cardiaca en 21 pacientes [18]. Se observó un cambio en la variabilidad de la frecuencia cardiaca, que se correlacionó con la atenuación simpática o la activación parasimpática con la correspondiente reducción de la presión arterial. Otro estudio demostró que la MTD provoca una remodelación inversa del ventrículo izquierdo y las aurículas y una mejora de la distensibilidad arterial [19]. Además, se ha observado que los pacientes con insuficiencia cardiaca sintomática que toman MTD mejoran su rendimiento funcional en más de un 37% (medido por la prueba de la marcha de 6 minutos). Además, la ecocardiografía reveló una reducción significativa de la masa ventricular izquierda y del grosor de la pared posterior como signo de “remodelación inversa” del ventrículo izquierdo [20].
Todos los estudios mencionados se realizaron con la primera generación de dispositivos para bajar la tensión arterial (Rheos). En un estudio reciente con el implante de segunda generación (Barostim neo™), se consiguió el mismo efecto en la reducción de la presión arterial que con el sistema Rheos [21].
Contrariamente al temor de que la MTD pudiera provocar un embotamiento del barorreflejo (“reajuste del barorreflejo”), se observó una reducción sostenida y dependiente de la dosis de la presión arterial y la frecuencia cardiaca en pacientes con hipertensión refractaria [22].
Los resultados del estudio hasta ahora han llevado a incluir la MTD como opción de tratamiento en las directrices sobre hipertensión de la ESH/ESC en 2013. Se recomienda considerar la MTD en pacientes con hipertensión refractaria (clase de recomendación IIb, nivel de evidencia C). Al mismo tiempo, sin embargo, se recomendó que el estimulador barorreceptor sólo fuera implantado por especialistas experimentados y en centros seleccionados de tratamiento de la hipertensión hasta que se disponga de más pruebas sobre la eficacia y la seguridad a largo plazo (Clase I, Nivel C) [23].
La rentabilidad de la MTD se analizó en otro estudio con pacientes que sufrían hipertensión refractaria. Al mismo tiempo, también se investigó la influencia de la terapia en la morbilidad y mortalidad cardiovasculares [24]. En este estudio realizado en Alemania, los autores concluyeron que en pacientes con hipertensión refractaria, la estimulación barorreceptora de por vida reducía el riesgo de ictus en un 35%, de infarto de miocardio en un 19% y de insuficiencia renal que requiriera diálisis en un 23%. Por término medio, los pacientes vivirían 1,66 años más, con un aumento de 2,17 años de vida ajustados por calidad (AVAC). El coste de un AVAC se estimó en 7797 euros. Este valor es muy inferior al umbral de rentabilidad generalmente aceptado de 35.000 euros por un AVAC [25]. Se concluyó que la MTD puede ser rentable en comparación con el tratamiento farmacológico óptimo de la hipertensión en pacientes con hipertensión refractaria.
BAT en pacientes con insuficiencia cardíaca
Dado que la MTD no sólo reduce la presión arterial sino que también tiene un efecto beneficioso sobre la función cardiaca, se han realizado estudios en pacientes con insuficiencia cardiaca. Recientemente se ha publicado un estudio de once pacientes con insuficiencia cardiaca (clase III de la NYHA, FE <40%) en los que no fue posible la terapia de resincronización cardiaca. Durante seis meses, se utilizó la MTD en paralelo con la terapia farmacológica óptima. La eficacia del tratamiento se midió por el cambio en la actividad nerviosa simpática muscular. Además, se recogieron parámetros clínicos de calidad de vida y rendimiento funcional. Los pacientes mostraron una atenuación significativa de la actividad nerviosa muscular simpática con mejoras significativas en la sensibilidad barorrefleja, la fracción de eyección, la clase NYHA, la calidad de vida y la prueba de la marcha de 6 minutos. Además, el número de rehospitalizaciones por empeoramiento de la insuficiencia cardiaca se redujo significativamente [26]. La MTD demostró ser compatible con el desfibrilador cardioversor implantable (DAI) y las dos terapias parecieron funcionar de forma complementaria [27].
En abril de 2013, se inició un estudio sobre insuficiencia cardiaca que incluye a pacientes con una fracción de eyección ventricular izquierda ≤35% y una clase III de la NYHA (Barostim Health Outcomes Prospective Evaluation for Heart Failure, Barostim HOPE4HF). Se trata de un ensayo de fase II que prueba la eficacia y seguridad del sistema Barostim neo™ en pacientes con insuficiencia cardiaca. Este estudio multicéntrico prospectivo aleatorizado y controlado reclutará a 140 pacientes en EE.UU. y Europa con la intención de comparar la terapia Barostim neo™ con la terapia estándar para la insuficiencia cardiaca. Los criterios de valoración del estudio son los cambios en la fracción de eyección, la prueba de la marcha de 6 minutos, la clasificación de la NYHA, la calidad de vida y la función renal y otros parámetros. Los primeros resultados después de seis meses se esperan en breve.
Situación actual
A principios de septiembre de 2014, se habían implantado en todo el mundo un total de 420 dispositivos Rheos y 380 estimuladores Barostim neo™. La implantación demostró ser segura y los riesgos de implantación son comparables a los de otros dispositivos implantables como los marcapasos o los DAI.
En Europa, Barostim neo™ cuenta con la certificación CE y está disponible en Italia, Alemania, Suiza y Holanda. La compensación económica aún no está regulada universalmente, pero se están haciendo esfuerzos en este sentido, a sabiendas de que la MTD puede ser rentable en pacientes con hipertensión refractaria [24].
Resumen
El estimulador carotídeo puede implantarse con poco riesgo y produce una reducción significativa y sostenida de la presión arterial en pacientes con hipertensión refractaria. La eficacia hemodinámica es mayor de lo esperado e incluso se mantiene durante más de cinco años. El objetivo del tratamiento es modular el sistema nervioso autónomo y amortiguar así el tono simpático. Además de la reducción de la presión arterial, también se observa una remodelación cardiaca con disminución del grosor de la pared miocárdica del ventrículo izquierdo. Todos estos resultados han llevado a integrar la MTD en las directrices ESH/ESC de 2013 sobre hipertensión arterial. La eficacia de este tratamiento en pacientes con insuficiencia cardiaca se está investigando actualmente en ensayos; sin embargo, ya se han demostrado efectos positivos en poblaciones de pacientes seleccionadas.
Literatura:
- Fields LE, et al: La carga de la hipertensión en adultos en Estados Unidos de 1999 a 2000: una marea creciente. Hipertensión 2004; 44: 398-404.
- Hajjar I, Kotchen TA: Tendencias en la prevalencia, concienciación, tratamiento y control de la hipertensión en Estados Unidos, 1988-2000. JAMA : la revista de la Asociación Médica Americana 2003; 290: 199-206.
- Chobanian AV, et al: Séptimo informe del Comité Nacional Conjunto sobre Prevención, Detección, Evaluación y Tratamiento de la Hipertensión Arterial: el informe JNC 7. JAMA : la revista de la Asociación Médica Americana 2003; 289: 2560-2572.
- Campbell DJ: Vacunación contra la hipertensión arterial. Diseño farmacéutico actual 2012; 18: 1005-1010.
- Wienemann H, et al: Tratamiento de la hipertensión resistente con nuevos dispositivos. Minerva cardioangiologica 2014; 62: 235-241.
- Zannad F, et al: Estimulación vagal crónica para el tratamiento de la insuficiencia cardiaca con baja fracción de eyección: resultados del ensayo controlado aleatorizado de terapia cardiaca neural para la insuficiencia cardiaca (NECTAR-HF). Revista europea del corazón 2014 [Epub ahead of print].
- Koch E: El autocontrol reflejo de la circulación. Dresde, Steinkopff 1931.
- Muratori G: Observaciones histológicas sobre la estructura del seno carotídeo en el hombre y los mamíferos. Oxford, Pergamon 1967.
- Brest AN, Wiener L, Bachrach B: Estimulación del nervio del seno carotídeo bilateral en el tratamiento de la hipertensión. The American journal of cardiology 1972; 29: 821-825.
- Lohmeier TE, et al: La activación prolongada del barorreflejo produce hipotensión sostenida. Hipertensión 2004; 43: 306-311.
- Scheffers IJM, et al: Reducción sostenida de la presión arterial mediante terapia de hipertensión barorrefleja con un sistema implantado crónicamente: datos de 3 años del estudio Rheos DEBuT en pacientes con hipertensión resistente. J Hypertens 2009; 27: S421.
- Schmidli J, et al: Reducción aguda de la presión arterial basada en dispositivos: activación eléctrica del barorreflejo carotídeo en pacientes sometidos a cirugía electiva de la carótida. Vascular 2007; 15: 63-69.
- Scheffers IJ, et al: Novedosa terapia de activación barorrefleja en la hipertensión resistente: resultados de un estudio europeo multicéntrico de viabilidad. Revista del Colegio Americano de Cardiología 2010; 56: 1254-1258.
- Kroon AA, et al: Sistema implantado crónicamente: datos de 4 años del estudio Rheos® DEBUT-HT en pacientes con hipertensión resistente. Revista de hipertensión 2010; 28: 278.
- Bakris GL, et al: La terapia de activación barorrefleja proporciona un beneficio duradero en pacientes con hipertensión resistente: resultados del seguimiento a largo plazo en el ensayo pivotal Rheos. Revista de la Sociedad Americana de Hipertensión: JASH 2012; 6: 152-158.
- Bisognano JD, et al: La terapia de activación barorrefleja reduce la presión arterial en pacientes con hipertensión resistente: resultados del ensayo pivotal rheos, doble ciego, aleatorizado y controlado con placebo. Revista del Colegio Americano de Cardiología 2011; 58: 765-773.
- Alnima T, et al: Respuestas renales a la terapia de activación del barorreflejo carotídeo a largo plazo en pacientes con hipertensión resistente a los fármacos. Hipertensión 2013; 61: 1334-1339.
- Wustmann K, et al.: Efectos de la estimulación barorreceptora crónica sobre la regulación autonómica cardiovascular en pacientes con hipertensión arterial resistente a los fármacos. Hipertensión 2009; 54: 530-536.
- Bisognano JD, et al: Mejora de la estructura y la función cardiacas con el tratamiento crónico mediante un dispositivo implantable en la hipertensión resistente: resultados de los ensayos europeos y estadounidenses del sistema Rheos. Revista del Colegio Americano de Cardiología 2011; 57: 1787-1788.
- Mohaupt MG, Schmidli J, Luft FC: Tratamiento de la hipertensión incontrolable con un dispositivo de estimulación del seno carotídeo. Hipertensión 2007; 50: 825-828.
- Hoppe UC, et al: Un sistema mínimamente invasivo para la terapia de activación del barorreflejo reduce de forma crónica la presión arterial con un perfil de seguridad similar al de un marcapasos: resultados del ensayo Barostim neo. Revista de la Sociedad Americana de Hipertensión: JASH 2012; 6: 270-276.
- Alnima T, et al: Descenso agudo sostenido de la presión arterial dependiente del voltaje con activación prolongada del barorreflejo carotídeo en la hipertensión resistente al tratamiento. Revista de hipertensión 2012; 30: 1665-1670.
- Task Force for the Management of Arterial Hypertension of the European Society Of H, Task Force for the Management of Arterial Hypertension of the European Society Of C: 2013 ESH/ESC Guidelines for the Management of Arterial Hypertension. Presión arterial 2013; 22: 193-278.
- Borisenko O, et al.: Rentabilidad de la terapia con Barostim para el tratamiento de la hipertensión resistente en entornos europeos. Revista de hipertensión 2014; 32: 681-692.
- Eichler HG, et al.: Utilización del análisis coste-eficacia en la toma de decisiones sobre la asignación de recursos sanitarios: ¿cómo se espera que surjan los umbrales coste-eficacia? Value Health 2004; 7: 518-528.
- Gronda E, et al: Efectos de la activación barorrefleja crónica sobre el tráfico nervioso simpático, la función barorrefleja y la hemodinámica cardiaca en la insuficiencia cardiaca: un estudio de prueba de concepto. Revista europea de insuficiencia cardiaca 2014; 16: 977-983.
- Madershahian N, et al: Terapia de activación barorrefleja en pacientes con desfibrilador cardioversor implantable preexistente: terapias compatibles y complementarias. Europace 2014; 16: 861-865.
CARDIOVASC 2014; 13(6): 6-11