Han pasado muchas cosas desde la desensibilización al polen en los años sesenta. Un tour d’horizon con los hitos históricos médicos más importantes de varias décadas de investigación y práctica alergológica.
Introducción: el pabellón de alergia de Zúrich
En 1948, el Prof. Hans Stork (1910-1983), como profesor privado recién licenciado – conferencia inaugural sobre el tema “Importancia de la alergia en el proceso de la enfermedad” [1] – fundó una “sala de alergia con horas de consulta para pacientes con alergias de las vías respiratorias (rinitis polinosa et alérgica, asma bronquial, dermatitis atópica)” en la Clínica Dermatológica Universitaria bajo la dirección del entonces director de la clínica, el Prof. Guido Miescher. Guido Miescher – una “sala de alergias” con horas de consulta para pacientes con alergias de las vías respiratorias (rinitis polínica y alérgica, asma bronquial), neurodermatitis, anafilaxia, alergias alimentarias, alergias a picaduras de insectos, etc. Este centro fue la primera policlínica de alergia de Europa. En los años de la posguerra, Stork había estudiado la teoría de la alergia en varios centros de alergia de EE.UU. y había estudiado allí las prácticas de la “terapia de desensibilización”. Para el diagnóstico y la terapia, se importaron de EE.UU. extractos acuosos de alérgenos (Hollister-Stier Lab, Spokane).
Tras completar mis estudios de medicina en Zúrich de 1956 a 1963, trabajé como médico adjunto en el Departamento Médico del Hospital Municipal de Lugano de 1963 a 1964 y comencé mi formación especializada como dermatólogo en 1965 en la Clínica Dermatológica Universitaria de Zúrich. Como parte de la rotación, llegué a la sala de alergia en 1968 como joven residente. Allí encontré mi “nicho ecológico”. Apenas un año después fui ascendido a médico superior i.V. 1; en 1971 a médico superior (Fig. 1). y en 1975, tras mi habilitación, a su jefe, cargo que ocupé hasta mi jubilación en 2003 y posteriormente dirigí una consulta de alergología en Zollikerberg hasta 2013. De este modo, he vivido casi 60 años de alergología muy de cerca y he podido seguir los hitos de la alergología práctica y la investigación sobre alergias durante este periodo.

Sin duda, una nueva era en la alergología quedó marcada en 1967-1968 por el descubrimiento de una nueva clase de inmunoglobulinas, las IgE, como portadoras de actividad reagínica, y la puesta a disposición de métodos radioinmunológicos sensibles (RIST y RAST) para su detección [2–4]. Gracias al descubrimiento de la IgE y su cuantificación, la alergología también se convirtió en “esperanza” para los inmunólogos.
Desensibilización al polen en la sala de alergia en los años 60
Los pacientes alérgicos al polen formaban una parte considerable de la población de pacientes de la sala de alergia en aquella época. Los pacientes se sometieron a pruebas de punción exhaustivas con extractos acuosos (diluidos 1:1000) en ambas extremidades anteriores y, en caso negativo, a pruebas intracutáneas con la misma concentración en la parte superior de los brazos. Todos los pólenes positivos a las pruebas se consideraron para la “desensibilización” en un extracto mixto, que puede contener más de 40 (!) especies de polen, entre ellas arce, sauce, jazmín, lila, acacia negra, tilo, juncia y otras. El tratamiento se administró de forma ambulatoria; la dosis inicial fue de 1:100.000 millones de la solución madre, incrementada con inyecciones subcutáneas tres veces por semana durante tres a cinco meses hasta alcanzar una dosis de mantenimiento de 0,2 ml (1:100.000), administrada cada dos a cuatro semanas durante tres a cuatro años. No sin razón, a los alergólogos se les llamaba entonces “médicos de las inyecciones” y esta práctica fue recibida con escepticismo por los titulares de las cátedras de medicina interna y pediatría, que calificaban de “homeopáticas” las dosis administradas.
El punto de inflexión: Semidepotextos, polen guía y desensibilización hasta la dosis máxima
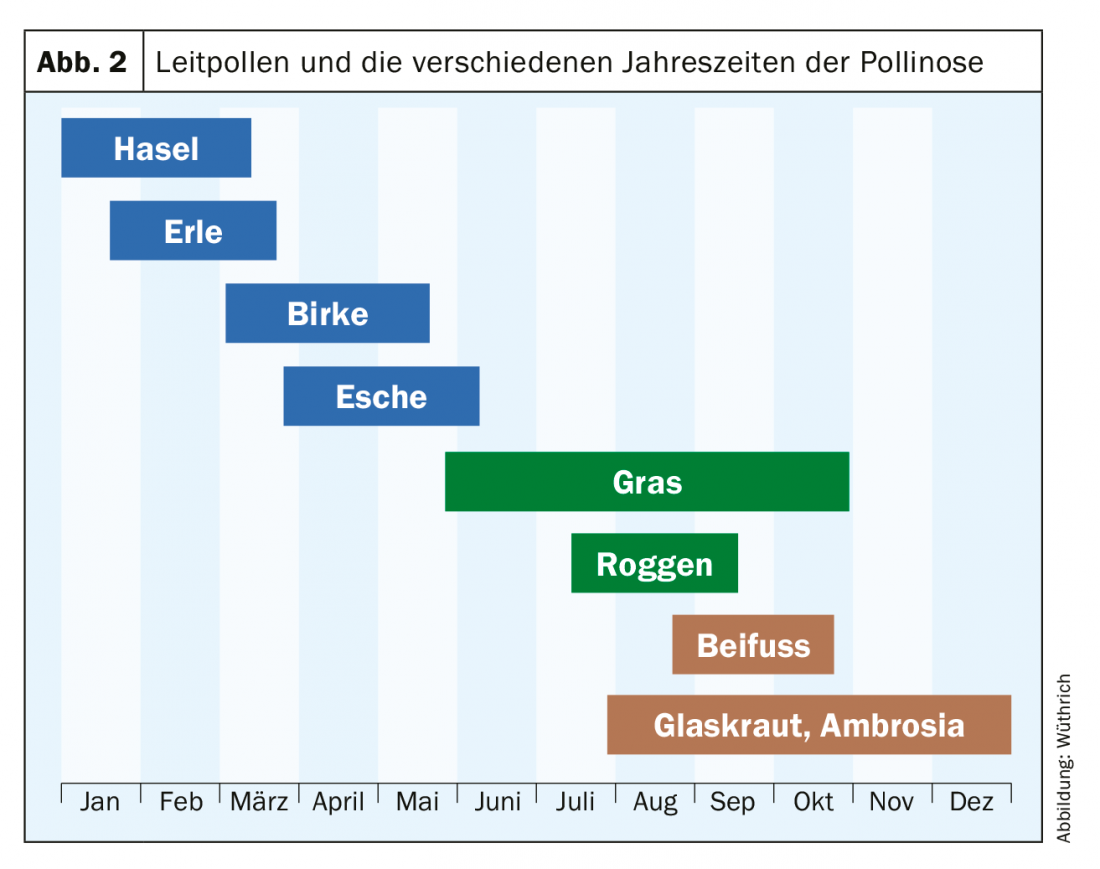
Un avance decisivo en la práctica de la terapia de desensibilización fue la introducción de alérgenos extraídos con piridina y adsorbidos en hidróxido de aluminio (los llamados semidepotextractos), que permitieron administrar la vacuna sólo cada 14 días. Los preparados originales de la marca Allpyral procedentes de EE.UU. se introdujeron en Suiza hacia 1965 con una selección limitada de alérgenos (mezcla de árboles del norte de polen de avellano, aliso y abedul, mezcla de gramíneas y artemisa, entre otros): Los primeros resultados de la desensibilización al polen con estos preparados semi-depot en Suiza fueron publicados en 1967 por Ferdinand Wortmann, de Basilea, y en 1968 por Wüthrich y Storck, de Zúrich, respectivamente. [5,6]. La normalización de los alérgenos se basó en el contenido proteínico en PNU (Unidades de Nitrógeno Proteínico). Comenzando con 20 a 50 PNU, la dosis se incrementó hasta la dosis máxima de 10.000 PNU, o hasta la concentración más alta tolerada. Esta concentración de alérgenos era mucho mayor que con la desensibilización “homeopática” con extractos acuosos. Las conclusiones de los dos estudios suizos fueron que el tratamiento con extractos de polen mediopot era un método de desensibilización eficaz (tasa de éxito en el primer año del 65-70%, en los años siguientes del 75-85%) y, debido al menor número de inyecciones, representaba un gran avance para médicos y pacientes. Basándose en el calendario de quejas y en el espectro de sensibilización de los pólenes anemófilos presentes en número suficiente en el aire, se introdujo el concepto de pólenes líderes (avellano, aliso, abedul para la polinosis primaveral, gramíneas/cereales para la polinosis estival y artemisa para la polinosis de finales de verano/otoño). (Fig. 2). La empresa Allergomed AG (nombre actual de la empresa: Allergopharma AG), Therwil suministró soluciones de prueba bien estandarizadas y duraderas en glicerina para las pruebas prick, así como semidepotextos y preparados orales para la desensibilización subcutánea y oral de la empresa Allergopharma en Reinbeck (Alemania) a partir de 1973. Novo-Helisen-Depot® con los alérgenos de inhalación más importantes representó un nuevo preparado de alérgenos en el que se utilizó un procedimiento de extracción en dos pasos sin piridina. En 1977 se publicaron nuestras experiencias de desensibilización al polen con Novo-Helisen-Depot® [7]. En un trabajo posterior, pudimos demostrar la sostenibilidad del método de desensibilización con extractos semidepotados; especialmente también con respecto al asma al polen [8].
Los extractos semidespotables para la desensibilización de las enfermedades alérgicas -hoy en día esta terapia se denomina inmunoterapia alergeno-específica (ASIT)-, sustituyeron a la larga “desensibilización” con extractos acuosos, que estaba plagada de muchos efectos secundarios, y sólo tuvieron en cuenta en la solución terapéutica los principales pólenes clínicamente eficaces del abedul, el avellano, el aliso, las gramíneas y la artemisa. No fue hasta principios de los noventa cuando nuestro grupo de trabajo demostró la importancia del polen de fresno para la polinosis primaveral [9]. Con pequeñas modificaciones, la TIE con hemidepoxtractos sigue siendo la inmunoterapia de elección, como confirma un metaanálisis [10].
La inmunoterapia con polen hoy: diagnóstico basado en los componentes alergénicos para su indicación
Basándose en el calendario de quejas, el polen desencadenante también puede determinarse fácilmente de forma anamnésica. En consecuencia, se distingue entre la polinosis primaveral (avellano, aliso, abedul y fresno) de enero/febrero a marzo/abril y la polinosis de principios de verano (principalmente polen de gramíneas y cereales) y, de importancia para las regiones meridionales, la polinosis de finales de verano (artemisa, vidriera, bogweed). [Parietaria officinalis] y ambrosía [Ambrosia artemifolia]). Con respecto al inicio de una inmunoterapia específica (SIT) a finales de los meses de otoño/invierno, hoy en día está indicado un esclarecimiento alergológico no sólo mediante pruebas cutáneas, sino también serológicas con determinación de IgE para alérgenos polínicos recombinantes. Por ejemplo, el avellano de floración temprana, el aliso y el abedul pertenecen a la familia de las Fagales (al igual que el haya y el roble, entre otras) y tienen un alto grado de reactividad cruzada entre sí debido al alergeno principal del polen de abedul Bet v 1. Para la inmunoterapia específica de la polinosis primaveral, ahora se recomienda determinar la sIgE para el polen de abedul, así como para el rBet v 1 y el r Bet v4/rtBet v 12 (alérgenos menores). Las posibilidades de éxito de la inmunoterapia específica están fuertemente ligadas a la presencia de sensibilización a los alérgenos principales. Son sólo espec. Si se detectan anticuerpos IgE contra los alérgenos secundarios profilina (rBet v 2) y proteína de unión al Ca (rBet v 4), existe una alta probabilidad de que la TIE no tenga éxito. Sin embargo, si el paciente presenta espec. anticuerpos IgE frente a los principales alérgenos, las posibilidades de éxito de la TIE son altas. Debido a la elevada reactividad cruzada dentro del polen de Fagales, suele ser suficiente una TIE con sólo un extracto de polen de abedul. Sin embargo, como los fresnos no son abedules, este tipo de polen, procedente de Fraxinus excelsior y no de Fraxinus americana [11], debe analizarse siempre. Serológicamente, se puede determinar Fraxinus excelsior o nOle e 1, una proteína inhibidora de la tripsina, el principal alérgeno del polen de olivo (Olea europea ) con una amplia reactividad cruzada con el polen de fresno. Si el resultado es claramente positivo (>= CAP clase 2), la ceniza debe incluirse en el extracto SIT.
En el caso de una alergia al polen de gramíneas/cereales, es suficiente – debido a la alta reactividad cruzada dentro de la familia de las gramíneas (Poaceae, antes Gramineae) – determinar los alérgenos de la hierba timotea (Phleum pratense ) rPhl p 1/ rPhl p 5b (g215) y rPhl p 7/rPhl p 12 (g214). Si sólo se detectan anticuerpos IgE específicos contra los alérgenos secundarios proteína de unión al Ca (rPhl p 7) y profilina (rPhl p 12), las perspectivas de éxito del tratamiento son escasas. Sin embargo, si el paciente tiene anticuerpos IgE específicos contra los alérgenos principales (aquí rPhl p 1+ rPhl p 5b), cabe esperar una buena respuesta a la TIE.
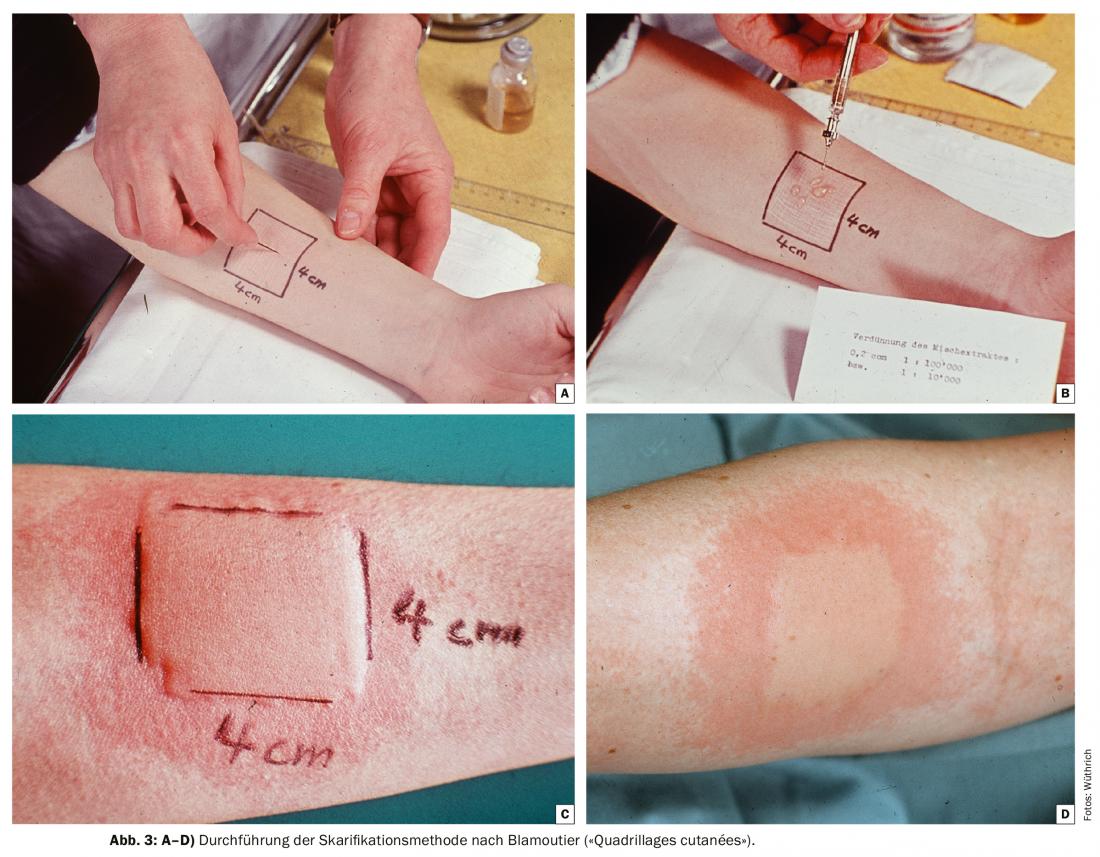
El método de escarificación coestacional según Blamoutier (“Quadrillages cutanées”)
Desde finales de los años 50 hasta principios de los 80, sólo se disponía de antihistamínicos sedantes de primera generación y esteroides sistémicos (orales e intramusculares) para el tratamiento sintomático de la fiebre del heno. La introducción y el triunfo mundial de la terfenadina, el primer antihistamínico no sedante de segunda generación, no comenzó hasta la década de 1980. La homologación en Suiza tuvo lugar en 1981.
En esta “era preantihistamínica”, el método de escarificación co-estacional según Blamoutier [12] gozaba de gran popularidad en las policlínicas de alergia de Suiza. Los alergólogos franceses introdujeron los “quadrillages cutanés” en 1959-1961. Se indicó a los alérgicos al polen que se presentaran al tratamiento cuando aparecieran los primeros síntomas en la conjuntiva y la mucosa nasal, y que repitieran el tratamiento si los síntomas reaparecían. Los intervalos solían ser de una semana, pero podían variar entre tres días y tres semanas en función del recuento de polen. Esto se traducía normalmente en entre seis y doce sesiones por temporada. El procedimiento se muestra en las figuras 3A-D. Curiosamente, varios pacientes informaron de la ausencia de síntomas inmediatamente después de la formación de las ronchas. Un estudio clínico de Zúrich mostró un éxito del tratamiento del 84% [13]. El mecanismo del éxito del tratamiento no estaba claro; en cualquier caso, no pudo observarse ninguna disminución de los anticuerpos IgE específicos (RAST) en el suero inmediatamente después del cuadrillaje ni 24 horas después. Incluso tras la introducción de los antihistamínicos no sedantes y los esteroides tópicos, los pacientes siguieron acudiendo a la sala de alergia con el deseo de someterse a este método de tratamiento hasta finales de los años ochenta. Hoy ha caído en el olvido.
La “desensibilización” al veneno de abeja con extractos de cuerpo entero: gran desilusión
La desensibilización para las reacciones alérgicas tras las picaduras de insectos fue el pan de cada día de los alergólogos durante muchos años, junto con la desensibilización al polen. Se realizó con extractos de cuerpo entero (GKE) de abejas (B) y avispas (W), basándose en un estudio de 1930 [14]: los investigadores estadounidenses informaron de un apicultor con alergia respiratoria al polvo de abeja tras entrar en el colmenar y urticaria con edema de Quincke tras picaduras de abeja, que había sido desensibilizado con éxito con un extracto de cuerpo entero de abejas (BGKE). Desde este estudio, se ha practicado en todo el mundo la desensibilización con GKE B y W acuosos, y más tarde con extractos semidepotados, en la mayoría de los casos de por vida. Informamos de que “la profilaxis mediante desensibilización específica con GKE había resultado exitosa en nuestra población de pacientes, mostrando una tasa de fracaso con GKE acuosa de “sólo” el 24% (n=54), y de “sólo” el 17% (n=60) con semidepotextractos” [15]. La desilusión llegó en 1978, cuando un artículo de Hunt et al. se demostró que, a diferencia del veneno de abeja puro, la aplicación de BGKE no era más eficaz que el tratamiento con placebo [16]. Hoy en día, la TIE con veneno puro de abeja y avispa es una historia de éxito.
Desensibilización oral para alergias a inhalantes
Además de la inmunoterapia subcutánea, la sala de alergia probó intensamente el efecto de la desensibilización oral para las alergias a inhalantes, especialmente en niños. A los niños o a sus madres se les dijo que las “gotas de desensibilización”, extractos de glicerina (principalmente de polen) debían tomarse por la mañana en ayunas, no simplemente tragarlas sino mantenerlas en la boca durante unos minutos. Se trataba, por tanto, de lo que hoy se conoce como inmunoterapia sublingual (SLIT). En un informe de campo sobre esta terapia, que debía llevarse a cabo durante al menos 3 años, concluimos que “algunos médicos y clínicos se muestran escépticos ante la desensibilización peroral, aunque este método ha demostrado tener éxito en niños de hasta unos 10-12 años [17] . De hecho, la desensibilización peroral tiene las ventajas de ser fácil de realizar y económica gracias a su administración por la madre, de ser inocua en cuanto a incidentes y efectos secundarios y, por último, pero no por ello menos importante, de ser suave con el paciente infantil, que no tiene que sufrir el trauma de muchos años de inyecciones y visitas al médico” [17]. Desgraciadamente, este tratamiento resultó ser ineficaz basándose en ensayos individuales controlados con placebo, pero sólo duró 1-2 años, por lo que se abandonó temporalmente. No fue hasta los años 1990-2002 cuando el SLIT experimentó un renacimiento, debido principalmente a los estudios procedentes de la región mediterránea. Mientras tanto, la SLIT está bien establecida gracias también a preparados mejorados y estandarizados, también en forma de comprimidos, basados en numerosos estudios controlados con placebo [18].
Desensibilización oral para la alergia a la leche de vaca: antes rechazada, ahora establecida
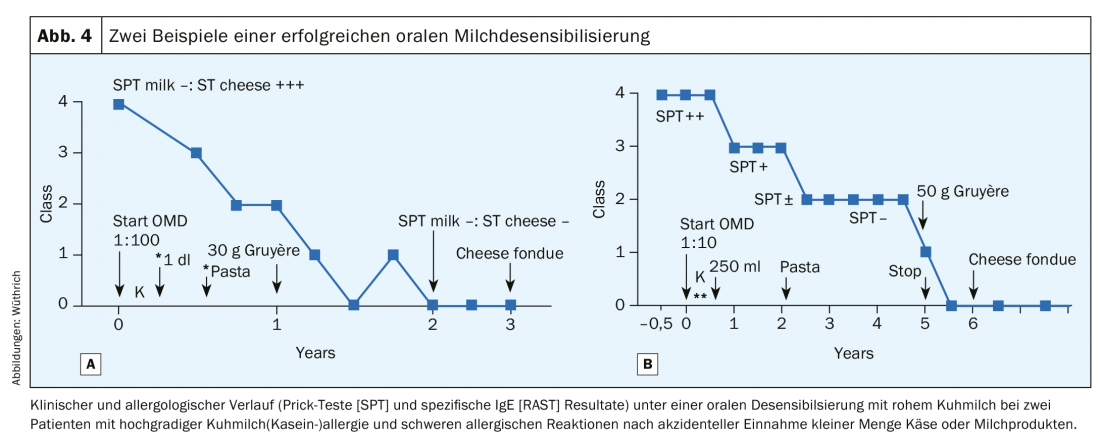
Desde la década de 1980, hemos trabajado ampliamente en la desensibilización oral (DO) de las alergias alimentarias, especialmente la alergia a la leche de vaca en adultos, y hemos descrito repetidamente la metodología en detalle [19,20]. Pudimos demostrar que en el 50% de los casos sometidos a desensibilización oral a la leche, se podía inducir una tolerancia completa (es decir, una verdadera desensibilización) a la leche y al queso tras un periodo de tratamiento de 3 a 5 años. [20] (Fig. 4A y B). Al menos se produjo una tolerancia parcial en el 25%, de modo que ya no se produjeron incidentes graves tras las comidas fuera de casa. Sin embargo, en el 25% de los casos, la hiposensibilización oral tuvo que interrumpirse a causa de reacciones alérgicas repetidas, incluso con reducción de dosis y terapia concomitante con fármacos antialérgicos [20]. Durante la fase inicial de la terapia de mantenimiento de la DO, debe tomarse diariamente 1 dl de leche de vaca, ya que una interrupción podría romper de nuevo la tolerancia alcanzada. Esta primera fase corresponde, pues, a la inducción de la tolerancia: sin embargo, si la aplicación diaria de la dosis de mantenimiento se prolonga durante meses, incluso años, se produce una verdadera desensibilización; se detecta la negatividad de las pruebas cutáneas y de las determinaciones de IgE específicas para las proteínas lácteas y las caseínas. Este método fue rechazado alegando que no existían estudios doble ciego controlados con placebo y, por tanto, ninguna prueba científica de su eficacia (¡!) [21]. Ahora este método ha sido redescubierto por los pediatras [22–23], pero se busca en vano nuestro trabajo en la bibliografía [24–26].
Nuevas estrategias para mejorar la inmunoterapia alergeno-específica
El progreso de la ASIT en los últimos años se basa esencialmente en una mejor normalización de los extractos de alérgenos, en el desarrollo de extractos terapéuticos modificados (alergoides, por ejemplo Allergovit® o Polvac®) [27] y en la caracterización molecular-biológica de los alérgenos naturales hasta la ingeniería genética de importantes alérgenos recombinantes [28–29]. También se muestran perspectivas en el uso combinado de la TIE con vacunas anti-IgE (rhuMab-E25, omazulimab, Xolair) [30]. En cualquier caso, la ASIT y la SLIT mantendrán o incluso ampliarán su papel en el tratamiento de las enfermedades mediadas por IgE en un futuro próximo [31].
Literatura:
- Storck H: Importancia de la alergia en el proceso de la enfermedad. Schweiz Rundschau Med [PRAXIS] 1948, nº 32 (separata).
- Johansson SGO: Niveles elevados de una nueva clase de inmunoglobulina (IgND) en el asma. Lancet 1967; 2(7523): 951.
- Ishizaka K, Ishizaka T: Anticuerpos reagínicos humanos e inmunoglobulina E. J. Allergy 1968; 42: 330.
- Wide L, Bennich H, Johansson SGO: Diagnóstico de la alergia mediante una prueba in vitro de anticuerpos contra alérgenos. Lancet 1967: 2(7526): 1105-1107.
- Wortmann F: Resultados de la desensibilización del polen con extractos de piridina precipitados con alumbre (Allpyral). Schweiz Med Wschr 1967; 97: 489.
- Wüthrich B, Storck H: Resultados de la desensibilización en pacientes alérgicos al polen con alipiral y con extractos acuosos. Schweiz Med Wschr 1968; 98: 653-658.
- Wüthrich B: Sobre la hiposensibilización específica de la polinosis. Resultados de un estudio de dos años con un nuevo preparado alergénico Novo-Helisen-Depot. Schweiz Rundschau Med [PRAXIS] 1977; 66: 260-266.
- Wüthrich B, Günthard HP: Resultados tardíos de la terapia de hiposensibilización de la polinosis Seguimiento de 328 casos entre 2 y 5 años después de finalizar el tratamiento con jeringuillas con extractos acuosos o semidepósitos de alérgenos. Schweiz Med Wschr 1974; 104: 713-717.
- Schmid-Grendelmeier P, Peters A, Wahl R, Wüthrich B: Sobre la importancia de la alergia al polen de fresno. Alergología 1994; 17: 535-542.
- Compalati E, et al.: Inmunoterapia específica para la alergia respiratoria: estado de la técnica según los metaanálisis actuales. Ann Allergy Asthma Immunol 2009; 102: 22-28.
- Wüthrich B: La ceniza no es ceniza. Alergología 2006; 29: 231-235.
- Blamoutier P, Blamoutier J, Guibert L: Traitement co-saisonier de la pollinose par l’application d’extraits de pollens sur des quadrillages cutanés: Résultats obtenus en 1959 et 1960. Revue francaise d’allergie 1961; 1: 112-120.
- Eichenberger H, Stork H: Desensibilización coestacional de la polinosis con el método de escarificación de Blamoutier. Acta Allergol 1966; 21(3): 261-267.
- Benson RL, Semenov HZ: La alergia en su relación con la picadura de abeja. J Allergy 1930; 1: 105.
- Wüthrich B, Häberlin G, Aeberhard M, Ott F, Zisiadis S: Resultados de la desensibilización con extractos acuosos y semidepoxtractos en la alergia al veneno de insectos. Schweiz med Wschr 1977; 107: 1497-1505.
- Hunt KJ, et al: Un ensayo controlado de inmunoterapia en la hipersensibilidad a los insectos. New England J Med 1978; 299(4): 157-161.
- Lätsch C, Wüthrich B: Sobre la desensibilización peroral de las alergias a inhalantes en la infancia. Resultados del tratamiento. Schweiz Med Wschr 1973: 103: 342-347.
- Bergmann K-Ch: Eficacia y seguridad de la inmunoterapia sublingual (SLIT) – una evaluación detallada del estado. Neumología 2006; 60: 241-247.
- Wüthrich B, Hofer T: Alergias alimentarias. III. Terapia: dieta de eliminación, sintomática, profilaxis farmacológica e hiposensibilización específica. Schweiz Med Wschr 1986; 116: 1401-1410 & 1446-1449.
- Wüthrich B: Desensibilización oral con leche de vaca en la alergia a la leche de vaca. ¡Pro! En: Wüthrich B, Ortolani C (eds), Aspectos destacados de la alergia alimentaria. Monogr Allergy 1996, 32; 36-240. Basilea: Karger.
- Bahna SL: Desensibilización oral con leche de vaca en la alergia a la leche de vaca mediada por IgE, ¡contra! En: Wüthrich B, Ortolani C (eds), Aspectos destacados de la alergia alimentaria. Monogr Alergia 1996; 32, 233-235. Basilea: Karger.
- Staden U, et al: Inmunoterapia oral de urgencia en niños con alergia persistente a la leche de vaca. J Allergy Clinical Immunol 2008; 122: 418-419. doi: 10.1016/j.jaci.2008.06.002. Epub 2008 jul 7.
- Keet CA, et al: Seguridad y eficacia de la inmunoterapia sublingual y oral para la alergia a la leche. J Allergy Clin Immunol 2012; 129: 448-455. 455.e1-5. doi: 10.1016/j.jaci.2011.10.023. Epub 2011 Nov 30.
- Wüthrich B: Aspectos más novedosos del diagnóstico y la terapia de la alergia alimentaria. Presentado a partir de estudios de casos seleccionados de alergia a la leche. Alergología 1987; 10: 370-376.
- Wüthrich B, Stäger J: Allergie au lait de vache chez l’adulte et désensibilisation spécifique au lait par voie orale. Méd & Hyg 1988: 46: 1899-1905.
- Bucher C, Wüthrich B: Desensibilización oral en la alergia a la leche de vaca. Giorn it allergol immunol clin 2000; 10: 119-120.
- Mühlethaler K, et al: Sobre la hiposensibilización de la polinosis. Resultados de un estudio controlado durante tres años con dos extractos de polen de gramíneas alergoides de depósito: alergoide adsorbido con hidróxido de aluminio (AGD) y alergoide adsorbido con tirosina (TA). Schweiz Rundschau Med [PRAXIS] 1990; 79: 430-436.
- Valenta R, et al: El concepto basado en alérgenos recombinantes de diagnóstico e inmunoterapia con componentes resueltos (CRD&CRIT). Clin Exp Allergy 1999; 29: 896-904.
- Valenta R, Linhart B, Swoboda I, Niederberger V: Alérgenos recombinantes para la inmunoterapia específica con alérgenos: 10 años de inmunoterapia con alérgenos recombinantes. Alergia 2011; 66: 775-783.
- Kuehr J, et al: Eficacia del tratamiento combinado con anti-IgE más inmunoterapia específica en niños y adolescentes polisensibilizados con rinitis alérgica estacional. J Allergy Clin Immunol 2002; 109: 274-280.
- Nedergaard Larsen J, Broge L, Jacobi H: Inmunoterapia de la alergia: el futuro del tratamiento de la alergia. Drug Discovery Today 2016; 21: 26-37.
PRÁCTICA DERMATOLÓGICA 2019; 29(5): 8-12