Las reacciones adversas a los medicamentos se dividen en reacciones de tipo A y de tipo B. Las reacciones de tipo A se basan en el mecanismo de acción del fármaco. Las reacciones de tipo B (alergias a fármacos) son menos frecuentes pero potencialmente peligrosas y están causadas por una reacción inmunológica al fármaco.
Las alergias a los medicamentos (AM) suelen producirse de forma imprevisible. Las manifestaciones son clínicamente muy variables y potencialmente peligrosas. Los mecanismos subyacentes son heterogéneos y encontrar las causas es difícil. Datos recientes han demostrado que la estimulación inmunológica en la AM se desencadena por tres mecanismos distintos que difieren en la velocidad de manifestación, la dependencia de la dosis, las opciones de aclaración y la genética [3]. La atribución de una reacción se complica por el hecho de que muchos pacientes reciben varios fármacos al mismo tiempo. Si se sospecha de MA, se requiere una aclaración cuidadosa. Si se trata de un AM, el paciente afectado debe ser informado adecuadamente sobre su estado. Se recomienda un pasaporte de alergia de la SGAI (Sociedad Suiza de Alergología e Inmunología); contiene información sobre la gravedad de la alergia, los medicamentos alternativos tolerados e información general sobre el diagnóstico de la alergia. El pasaporte para alérgicos está disponible en el Centro Suizo de Alergia (www.aha.ch).
“Reacción adversa a un medicamento”
Las reacciones adversas a los medicamentos (RAM) se dividen en reacciones de tipo A y de tipo B [1,2]. Las reacciones de tipo A son frecuentes (85%) y se deben a reacciones farmacológicas (por ejemplo, fatiga tras dosis altas de bloqueantes anti-H1, gastritis erosiva tras AINE, etc.). Las reacciones de tipo B (alrededor del 15%) son aquellas reacciones de hipersensibilidad cuyos síntomas no corresponden al mecanismo de acción del medicamento, sino que están causadas por reacciones inmunitarias: un exantema tras la amoxicilina no tiene nada que ver con el mecanismo de acción del antibiótico, sino que está causado por una reacción inmunitaria a la amoxicilina.
Reacciones de hipersensibilidad: Reacción de tipo B
Formación de un nuevo antígeno/alérgeno (modelo hapteno): Un fármaco químicamente reactivo (por ejemplo, la penicilina) se une a una proteína mediante enlace covalente (mecanismo del hapteno): el complejo hapteno-proteína es reconocido como un nuevo antígeno por el sistema inmunitario, contra el que se desarrolla una reacción inmunitaria compleja basada en diferentes simulaciones de células B o T. Clínicamente, dependiendo del tipo de estimulación inmunológica, existen diferentes síntomas como anafilaxia de aparición rápida (mediada por IgE), eccema y exantema (ambos mediados por células T) que sólo se manifiestan al cabo de días, o hemólisis (IgG/IgM). Esta reacción inmunoalérgica sigue los principios de la estimulación inmunológica frente a las proteínas y puede detectarse con pruebas cutáneas y pruebas in vitro. El número de fármacos que estimulan claramente a través del mecanismo del hapteno es manejable. Algunos fármacos sólo se convierten en reactivos tras su metabolización (por ejemplo, las sulfanilamidas) (Tab. 1).

p-i (interacción farmacológica con los receptores inmunitarios): Este concepto, desarrollado en el grupo de investigación sobre alergia a medicamentos del Inselspital, combina la farmacología con la inmunología [4]. Los fármacos tienden a unirse a las proteínas mediante enlaces de hidrógeno, interacciones electrostáticas y fuerzas de van der Waals, como ocurre con las interacciones normales entre ligando y receptor. En parte, estas interacciones no covalentes conducen al bloqueo o la estimulación de receptores que son importantes para la activación de las células T. En el mecanismo p-i, estas interacciones “farmacológicas” implican a los receptores inmunitarios HLA y TCR. A diferencia del modelo del hapteno, en el p-i sólo se produce una estimulación selectiva de las células T. Hay una serie de fármacos que estimulan principalmente a través del mecanismo p-i, y estas reacciones suelen ser clínicamente problemáticas (hepatitis, DRESS, SJS/TEN) (Tabla 1).
En el caso de los fármacos abacavir, carbamazepina o alopurinol, la unión por afinidad relativa se produce principal o exclusivamente a determinados alelos HLA: por ejemplo, el metabolito principal del alopurinol (oxipurinol) puede unirse fuertemente al alelo HLA-B*58:01, el abacavir al B*57:01 y la carbamazepina al B*15:01 o al A*31:01. Las personas que tienen estos alelos HLA son especialmente susceptibles de padecer NW graves como el SJS o el DRESS: la tipificación HLA puede utilizarse para detectar el riesgo de NW graves, lo que se hace a menudo para el abacavir y la carbamazepina en personas del sudeste asiático, ya que el HLA-B*15:02 es relativamente común en esta región. Alternativamente, el fármaco puede unirse directamente al TCR, que reconoce péptidos en el HLA: este es el caso, por ejemplo, de las alergias al sulfametoxazol, en las que se han identificado diferentes sitios de unión en el TCR [4]. El diagnóstico se basa en la detección de reacciones de las células T en la piel o en una prueba in vitro (citolistesis).
Efectos secundarios pseudoalérgicos: Se deben a la estimulación directa de las células efectoras del sistema inmunitario. El mejor estudiado es la estimulación de los mastocitos a través del receptor MRGPRX2 mediante la unión de quinolonas o relajantes musculares [5]. Explica la aparición de urticaria y anafilaxia con estos fármacos. Las más importantes son las reacciones pseudoalérgicas a los AINE, parte de las cuales pueden atribuirse al aumento de la producción de leucotrienos [6]. Se produce una activación de los eosinófilos y los basófilos, así como una estimulación de los mastocitos. Los síntomas son rinosinusitis y broncoespasmo en el sentido de asma sensible a la aspirina, y/o urticaria y anafilaxia. Las NW pseudoalérgicas son frecuentes. Dado que no hay afectación del sistema inmunitario específico (células B y T), las pruebas inmunológicas (pruebas cutáneas, BAT, citolitotina) son negativas (tab. 1) . El diagnóstico se basa en pruebas de provocación, así como en la anamnesis y la observación de la evolución con respecto a la cuestión de qué fármacos se toleran o desencadenan los síntomas.
¿Reacciones de tipo inmediato o de tipo tardío?
Las siguientes preguntas son importantes para el clínico: ¿Podría tratarse de una alergia a un medicamento? ¿Distinción entre reacciones de tipo inmediato y tardío? ¿Señales de peligro? ¿Qué fármaco es el desencadenante? A menudo se piensa en la AM de forma tardía en el diagnóstico diferencial, ya que las manifestaciones clínicas de la AM imitan varias otras enfermedades inmunológicas o autoinmunes víricas o bacterianas. En el caso de enfermedades que no puedan explicarse, la AM debe incluirse siempre en el diagnóstico diferencial. Los indicios de MA como causa de los síntomas son: Conexión con una medicación recién recetada (desde <1-45 días) o síntomas típicos de erupción pruriginosa (exantema), urticaria, anafilaxia o eosinofilia.
Es importante distinguir las reacciones de tipo inmediato de las de tipo tardío. Las reacciones que se producen en la hora siguiente a la administración del fármaco (a veces peragudas, en cuestión de minutos) son mediadas por IgE o pseudoalérgicas. Se manifiestan como flash, picor (típicamente palmar, plantar, del cuero cabelludo, axilar, genital), urticaria y, si también se ven afectados órganos internos, adicionalmente como anafilaxia (broncoespasmo, vómitos, diarrea, hipotensión, shock cardiogénico). La mayoría de las reacciones no se producen hasta pasadas seis horas (normalmente no hasta pasados cuatro días). Con la amoxicilina, el desencadenante más frecuente de la MA en Suiza (2-8% de los tratados), el exantema a menudo sólo aparece tras un periodo de tratamiento de 7-12 días, a veces sólo tras la interrupción del fármaco. El exantema es clínicamente relativamente heterogéneo y en su mayoría está causado por células T estimuladas por fármacos.
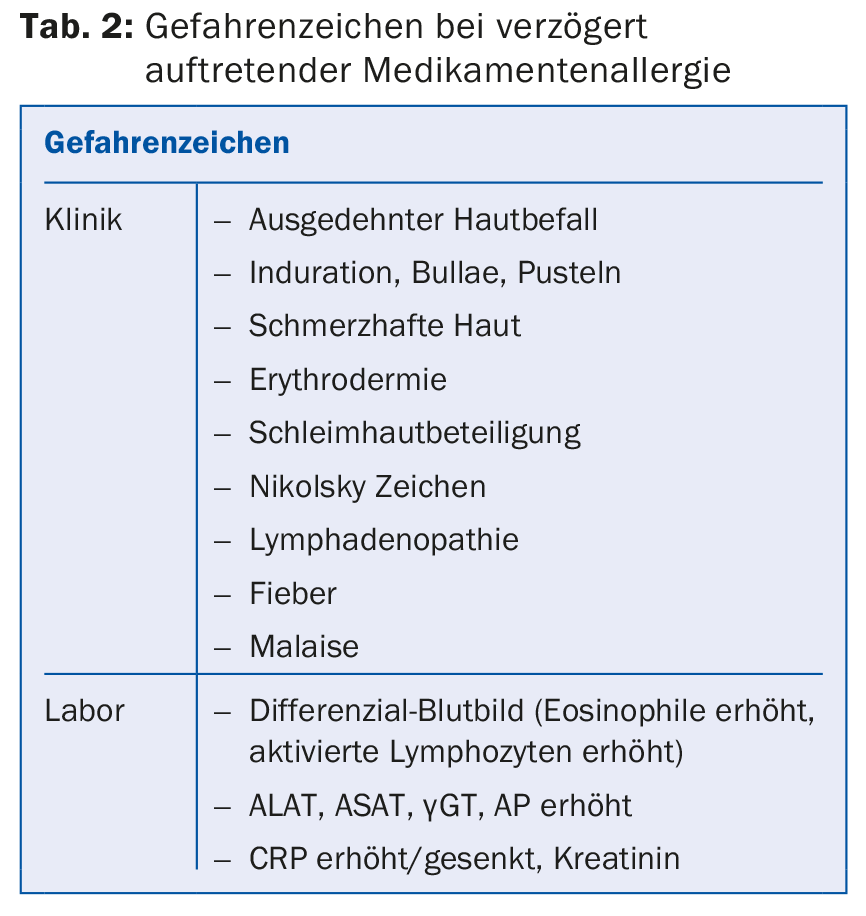
Las reacciones de tipo tardío están dominadas por el exantema macular, urticarial y maculopapular. La hepatitis de leve a moderada no es infrecuente, y la pleuresía, la pancreatitis, etc. son raras. Las reacciones cutáneas ampollosas y las reacciones de las mucosas (conjuntivitis, úlceras orales o genitales/aftas), que caracterizan el SJS/TEN y tienen una letalidad del 10-30%, deben clasificarse siempre como peligrosas. Son típicos y por tanto indicativos los aumentos masivos de eosinofilia (a menudo >1 G/l) y linfoblastos (como en la infección por el virus de Epstein-Barr), que a menudo se ignoran: Si se sospecha de MA, haga siempre un hemograma diferencial o busque linfoblastos y, en caso de exantema generalizado, determine siempre también los valores hepáticos (SGOT/SGPT, LDH, AP, γGT) para detectar la afectación hepática; informe sobre los signos de peligro Cuadro 2. En raras ocasiones, pueden producirse NW hematológicos (trombocitopenia, anemia hemolítica, agranulocitosis). Éstas están mediadas en gran medida por las IgG.
¿Qué fármaco es el desencadenante?
Identificar los factores desencadenantes del AM es muy complejo. La documentación de la medicación con la mayor precisión posible en cuanto a la duración, la dosis y el momento de los primeros síntomas de MA son fundamentales para el esclarecimiento; en particular, si se conoce el tipo de MA con la medicación correspondiente y de qué tipo. A veces esto es suficiente para tener éxito en la demarcación y la clasificación. Dado que muchos pacientes reciben una terapia combinada, la historia clínica suele ser difícil y poco concluyente. El diagnóstico de una alergia a un fármaco debe realizarse con la menor probabilidad de error posible, ya que las consecuencias asociadas pueden incluir la supresión de un grupo importante de fármacos y un aumento del coste o empeoramiento de la terapia.
Pruebas cutáneas e in vitro: En la clarificación in vivo deben tenerse en cuenta las concentraciones, la solubilidad, la disponibilidad de medicamentos estériles, así como la ingesta simultánea de medicamentos durante la prueba y mucho más, para que la clarificación tenga lugar con el alergólogo. También hay que tener en cuenta los posibles mecanismos inmunológicos, es decir, si la reacción podría estar relacionada con las IgE o con las células T. Si se sospecha un mecanismo mediado por IgE, pueden realizarse pruebas cutáneas por punción con sustancias solubles y pruebas intradérmicas con fármacos solubles estériles. Para unos pocos fármacos, existe una prueba de laboratorio para detectar la IgE específica del fármaco mediante serología (método ImmunoCap). Las reacciones de las células T contra el fármaco pueden detectarse mediante pruebas cutáneas (prueba intradérmica y prueba epicutánea). Las posibilidades de clarificación in vitro han mejorado recientemente: Si se sospecha una reacción mediada por IgE, se utiliza la BAT. Para las reacciones tardías, la cito-LTT in vitro es la más adecuada para detectar la sensibilización.
Reacciones de tipo inmediato: Prueba de activación de basófilos: La MTD es adecuada para el esclarecimiento diagnóstico de una reacción de tipo inmediato (normalmente unos minutos/horas después de tomar la medicación). En la MTD, la reacción que se produce en el organismo se “recrea” en el laboratorio. La sangre se incuba con el presunto fármaco desencadenante en sustancia pura y en concentración ascendente, con lo que los basófilos presentes en la sangre se activan en caso de sensibilización. Además de la liberación de mediadores (histamina, heparina), también se expresan diversos marcadores de activación en la superficie de los basófilos, que pueden cuantificarse mediante citometría de flujo. Como la prueba requiere células vivas, es esencial que el tiempo de transporte de la muestra sea rápido (<24h). La prueba también debe registrarse en el laboratorio. El material de prueba necesario son al menos 4 ml de sangre EDTA.
Los siguientes grupos de medicamentos han demostrado ser adecuados para el esclarecimiento de una MA de tipo inmediato con la MTD (experiencia de ADR-AC): penicilinas, cefalosporinas, relajantes musculares, IBP, fluoroquinolonas y diversos desinfectantes. Si se prueban otras drogas, la prueba debe seguir considerándose experimental. Al igual que ocurre con la prueba cutánea, la sensibilidad de la BAT disminuye con la distancia al evento. De este modo, lo óptimo es que la MTD se lleve a cabo en el plazo de un año tras la reacción alérgica.
Reacciones de tipo tardío: Prueba de transformación linfocitaria de citoquinas (cito-LTT): Para el esclarecimiento diagnóstico de las reacciones alérgicas de tipo tardío mediante diagnósticos de laboratorio in vitro, la cito-LTT ha demostrado ser útil y -según datos anteriores- superior a la prueba cutánea y a la LTT normal: En un cultivo celular de 7 días de las células del paciente con el fármaco, se estimulan células T específicas que segregan citoquinas: El análisis de determinados mediadores en sobrenadantes de cultivos celulares, a saber, IL-5, IL-13, IFN-y, granzima B y granulisina es adecuado para detectar los distintos tipos de reacciones. En función del patrón de distribución de las citocinas, se pueden sacar incluso conclusiones sobre el patrón de la enfermedad. Por ejemplo, los pacientes con exantema maculopapular tienden a mostrar un aumento de los niveles de IL-5 e IL-13, mientras que los mecanismos de respuesta citotóxica como el AGEP o el DRESS muestran un aumento de las citocinas citotóxicas. La cyto-LTT requiere 4050 ml de sangre con heparina, siendo el momento óptimo de recogida entre dos semanas y 1-2 años después de que se haya resuelto la respuesta, excepto en SJS/TEN, en los que la prueba debe realizarse lo antes posible. Se puede probar un amplio espectro de sustancias activas en el cito-LTT. Esto incluye los desencadenantes típicos más importantes de las reacciones de tipo tardío mediadas por fármacos (más detalles en www.adr-ac.ch).
Evolución de los síntomas y medidas
Como primera medida, debe suspenderse la medicación que se ha administrado recientemente. Esto se debe a que es poco probable que un medicamento que ya se ha tomado durante mucho tiempo (por ejemplo, un año) desencadene una alergia. Dependiendo de la gravedad de los síntomas (tab. 2), es necesario adoptar otras medidas. El síndrome DRESS es una reacción sistémica clínicamente grave (exantema masivo, malestar, hinchazón facial, hepatitis y a menudo eosinofilia) y es desencadenada principalmente por algunos fármacos específicos (tab. 3). El síndrome DRESS suele aparecer tras varias semanas de terapia y puede provocar fallos orgánicos letales (carditis, hepatitis). Los pacientes con exantema grave y DRESS pueden seguir desarrollando durante años una nueva MA frente a nuevos fármacos (“hipersensibilidad múltiple a fármacos”, MDH) [7]. En la MA leve, es suficiente la terapia a corto plazo con bloqueantes anti-H1, complementada con esteroides tópicos. Los esteroides sistémicos se utilizan para la MA grave. La hospitalización y la participación de especialistas son necesarias y útiles en las enfermedades bullosas de la piel (SJS/TEN), en el DRESS y sobre todo en la AGEP, ya que los cursos son a menudo sorprendentes y la experiencia con estas MA graves es importante. El seguimiento de los pacientes con DRESS es complicado, ya que muchos de ellos presentan reacciones de “reagudización” a pesar de haber dejado los desencadenantes y algunos pacientes desarrollan HMD.

La duración de la sensibilización tras la MA no ha sido suficientemente estudiada. Se observaron casos que seguían reaccionando de forma fuertemente positiva al fármaco en la prueba cutánea o LTT después de más de 12-20 años, por lo que debe suponerse una MA permanente: Esto es especialmente cierto en el caso de MA graves como DRESS, SJS/TEN y hepatitis. En la anafilaxia, la detección de alergia es mayor en el primer año tras el suceso que después, ya que se ha observado repetidamente una disminución espontánea de la IgE específica del fármaco. Sin embargo, esta disminución no es segura, por lo que -si se va a volver a utilizar el mismo fármaco- primero se administra una dosis de prueba: El fármaco se administra entre 1/100 y 1/10 de la dosis diaria y después se aumenta rápidamente a la dosis normal en un plazo de 3 a 6 horas (“desafío graduado”). La reexposición (“pruebas de provocación”/provocación) con la dosis completa está contraindicada en caso de reacciones graves. En el caso de las reacciones tardías frecuentes y originalmente leves (exantema), la reexposición tras >2 años sería posible si se trata de una clase de fármaco importante.
Mensajes para llevarse a casa
- Las reacciones adversas a los medicamentos se dividen en reacciones de tipo A y de tipo B [1,2]. Las reacciones de tipo A se basan en el mecanismo de acción del fármaco. Las reacciones de tipo B (alergias a fármacos) son menos frecuentes pero potencialmente peligrosas y están causadas por una reacción inmunológica al fármaco.
- Las alergias a los medicamentos pueden clasificarse en inmunoalérgicas, p-i y pseudoalérgicas en función del mecanismo de acción del fármaco con las células inmunitarias e inflamatorias. Las características distintivas están relacionadas con la velocidad de manifestación, la dependencia de la dosis, las opciones de aclaración y la genética.
- Además, hay que distinguir las reacciones de tipo inmediato de las de tipo tardío. Además de la anamnesis y la observación del curso de la enfermedad, un hemograma diferencial puede proporcionar pistas para el diagnóstico. Identificar los fármacos que desencadenan la enfermedad es complicado. Las nuevas pruebas in vitro facilitan la detección del desencadenante tanto para las reacciones inmediatas (prueba de activación de basófilos, BAT) como para las reacciones tardías (cito-LTT).
Literatura:
- Rawlins MD, Thompson JW: Patogénesis de las reacciones adversas a los medicamentos. En: Davies DM, ed. Libro de texto de reacciones adversas a los medicamentos. Oxford: Oxford University Press, 1977: 10-17.
- Rawlins MD: Farmacología clínica: reacciones adversas a los medicamentos. BMJ 1981; 282: 974-976.
- Pichler WJ, Hausmann O: Clasificación de la hipersensibilidad a fármacos en formas alérgica, p-i y pseudoalérgica. Int Arch Allergy Immunol 2016; 171 (3-4): 166-179.
- Pichler WJ, et al.: Hipersensibilidad a los fármacos: cómo estimulan los fármacos las células T a través de la interacción farmacológica con los receptores inmunitarios. Intern Arch Allerg Clin Immunol 2015; 168(1): 13-24.
- McNeil BD, et al: Identificación de un receptor específico de los mastocitos crucial para las reacciones pseudoalérgicas a fármacos. Nature 2015; 519 (7542): 237-241. doi: 10.1038/nature14022.
- Kowalski ML, et al: Clasificación y enfoque práctico del diagnóstico y tratamiento de la hipersensibilidad a los antiinflamatorios no esteroideos. Alergia 2013; 68(10): 1219-1232.
- Pichler WJ, Srinoulprasert Y, Yun J, Hausmann O: Hipersensibilidad a múltiples fármacos. Int Arch Allergy Immunol 2017; 172(3): 129-138.
PRÁCTICA GP 2018; 13(10): 12-16