Los procedimientos de resección en el tratamiento del linfedema llevan desarrollándose desde principios del siglo pasado. Son invasivas y tienen muchas complicaciones. Con el avance de la microcirugía, las anastomosis linfovenosas desempeñan un papel importante en la mejora de la calidad de vida del paciente.
Los procedimientos de resección en el tratamiento del linfedema son métodos que eliminan quirúrgicamente el exceso de tejido. Desde finales del siglo XIX se han descrito diversos procedimientos, en parte históricos, para la terapia quirúrgica del linfedema (Tab. 1).
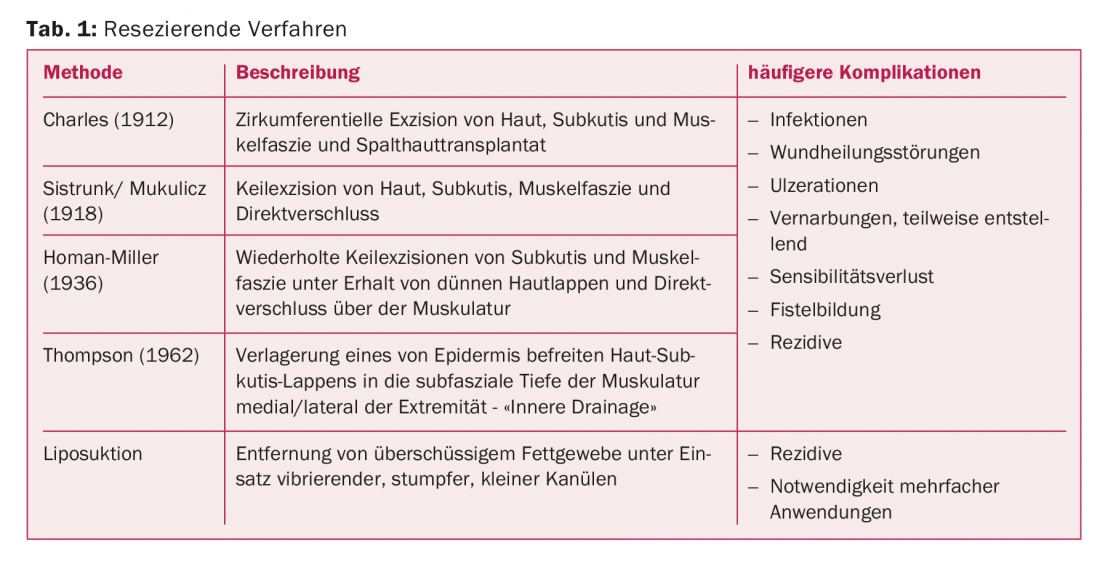
En 1912 se desarrolló el procedimiento Charles, en el que la piel, el subcutis y la fascia muscular se extirpan circunferencialmente y se cubren con piel dividida [1]. Según Sistrunk, las escisiones en cuña de piel, subcutis y fascia muscular se realizan con cierre directo, mientras que en el procedimiento según Homan la piel se preservaba por primera vez y se cerraba sobre el defecto de tejido resecado [2]. Este procedimiento se repite hasta alcanzar la circunferencia deseada. La idea de conectar los linfáticos superficiales y profundos se estableció por primera vez en 1962, cuando Thompson resecó tejido subcutáneo y reubicó un delgado colgajo subcutáneo de piel profunda en la profundidad subfascial de la musculatura. Como resultado, no sólo se producen cicatrices desfigurantes, sino también frecuentes fístulas linfáticas y sinusoides pilonidales [3].
El proceso de cicatrización suele complicarse por las infecciones y la formación de cicatrices inestables durante los procedimientos de resección. Estos métodos deben explorarse en casos de discapacidad y fracaso del tratamiento en la fase final del linfedema y pueden aumentar la eficacia de las terapias causales al reducir la llamada “carga linfática”. Pueden combinarse con métodos reconstructivos. En el edema genital, estos procedimientos suelen plantearse antes.
Liposucción
La liposucción es un procedimiento de resección especial que puede reducir eficazmente la circunferencia del linfedema de las extremidades. La liposucción es la eliminación del exceso de tejido graso mediante succión con cánulas vibrantes, romas y pequeñas. La transformación del linfedema en tejido adiposo (la llamada transformación grasa) tiene lugar muy a menudo en el curso posterior de la enfermedad. El cirujano sueco Hakan Brorson fue pionero en el uso de la liposucción para el linfedema de las extremidades y ha publicado resultados prometedores en los últimos años. En un estudio prospectivo de 56 pacientes con linfedema (29 primario, 27 secundario tras terapia oncológica), la circunferencia de la extremidad inferior tratada mediante liposucción seguía siendo significativamente similar a la del lado sano al cabo de diez años [4]. Sin embargo, las personas afectadas siguieron llevando medias de compresión continuamente. En otro estudio prospectivo de 146 pacientes con cáncer de mama que habían desarrollado linfedema en las extremidades superiores, el exceso de volumen se eliminó eficazmente y la circunferencia reducida de las extremidades se mantuvo a largo plazo mediante el uso constante de medias de compresión [5]. Un amplio estudio mediante encuesta reveló un alto nivel de satisfacción psicológica y física entre las personas que recibían tratamiento [6].
El riesgo de daño adicional de los vasos linfáticos debido a la liposucción aún no se ha observado ni experimental ni clínicamente. Los exámenes anatómicos tras la aspiración en sentido longitudinal de las extremidades no pudieron demostrar ningún daño en los vasos linfáticos epifasciales. Por regla general, no se aspiran más de cuatro litros de grasa por intervención para evitar problemas circulatorios y desplazamientos electrolíticos. Pueden ser necesarias varias intervenciones.
Anastomosis linfovenosas (LVA)
Aunque el interés por el papel del sistema linfático en los procesos fisiológicos y patológicos ha crecido en los últimos años, el conocimiento del sistema linfático sigue siendo limitado en comparación con el conocimiento del sistema cardiovascular. En la actualidad se investigan cada vez más los mecanismos patológicos del linfedema y las posibilidades de tratamiento quirúrgico se amplían constantemente. Para restablecer el drenaje linfático de forma fisiológica, se crean supermicrosúrgicamente anastomosis linfovenosas que permiten el drenaje linfático de forma extraanatómica. La supermicrocirugía es una nueva técnica y un perfeccionamiento de la microcirugía que permite preparar y suturar vasos muy pequeños con un diámetro inferior a 1 mm (0,3-0,8 mm). Se fabrican especialmente instrumentos quirúrgicos muy finos y se utilizan microscopios de hasta 40 aumentos. Se utilizan materiales de sutura muy finos, que tienen un grosor de 12-0 según la clasificación USP (< 0,1 mm grosor del hilo). Estas delicadas anastomosis suelen insertarse bajo anestesia general para mayor comodidad del paciente, pero en principio también pueden insertarse bajo anestesia local.
Los propios vasos linfáticos son difíciles de visualizar en su conjunto porque son de pequeño calibre y transportan principalmente líquido linfático claro y casi sin células. La mayoría de las técnicas de visualización se basan en la capacidad natural de los vasos linfáticos para absorber los trazadores inyectados en el espacio tisular. A continuación, el trazador se transporta y se concentra en el vaso linfático, lo que permite diversas modalidades de obtención de imágenes.
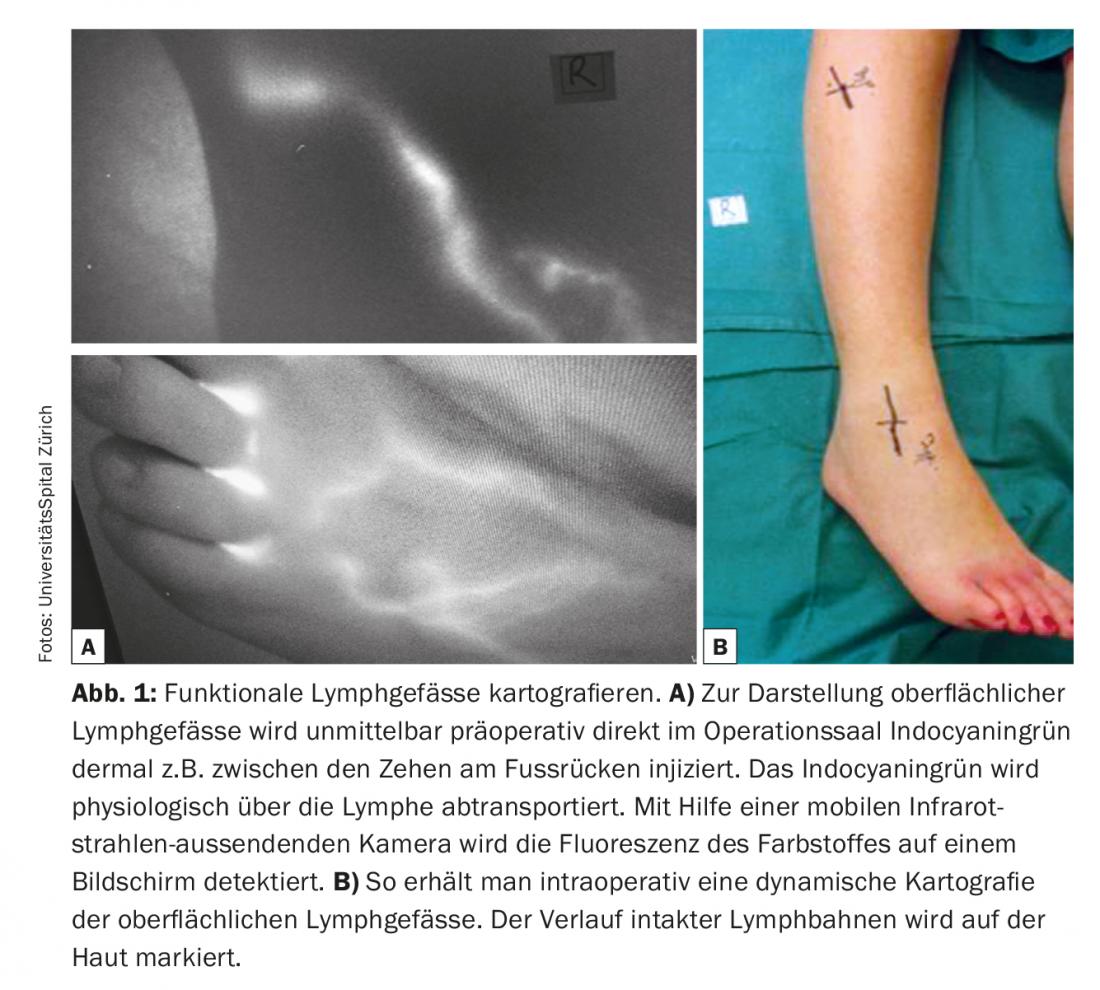
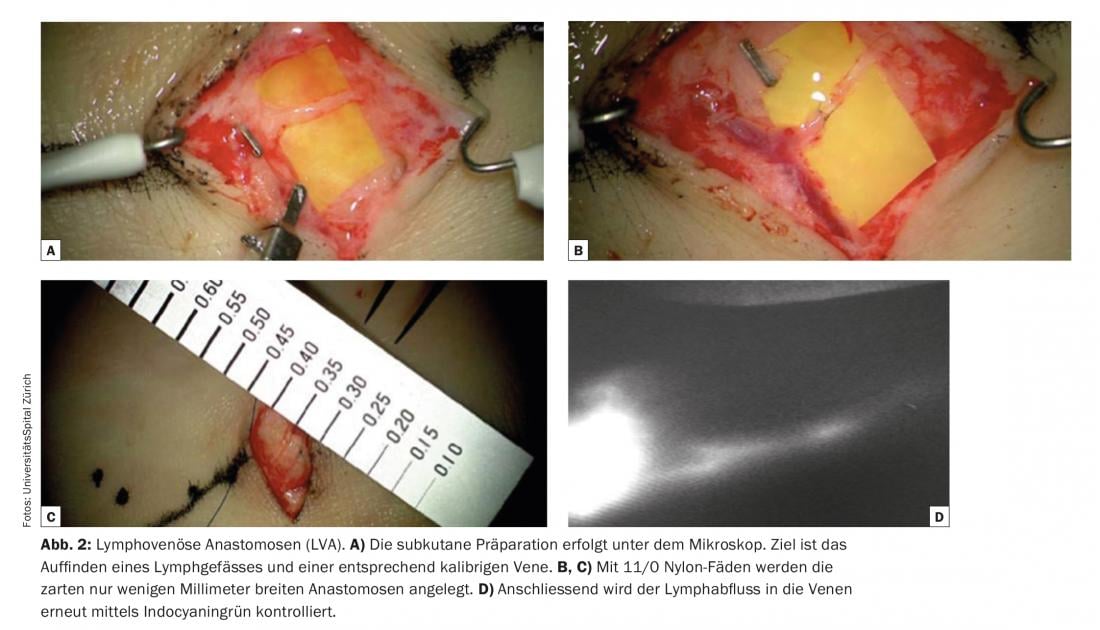
Una de las condiciones elementales para el éxito de las anastomosis linfovenosas es la identificación de vasos linfáticos adecuados que no sean fibróticos y tengan una gran capacidad de transporte. La linfangiografía con verde de indocianina (ICG) se utiliza actualmente como técnica comparativamente sencilla y rápidamente informativa para obtener imágenes de los vasos linfáticos. En los vasos linfáticos funcionales -por ejemplo, de las extremidades- el verde de indocianina se absorbe rápidamente y se transporta velozmente por los canales linfáticos lineales hasta la ingle o la axila. A menudo puede observarse incluso el peristaltismo. La ICG se utiliza como una navegación pre e intraoperatoria viable y rentable. El verde de indocianina se inyecta por vía dérmica inmediatamente antes de la operación en el quirófano para visualizar los vasos linfáticos superficiales, por ejemplo, entre los dedos en el dorso del pie, y se marca en la piel el curso de los vasos linfáticos. (Fig. 1). La preparación subcutánea se realiza bajo el microscopio (Fig. 2). El objetivo es encontrar un vaso linfático y una vena del calibre correspondiente. Las anastomosis se crean con hilos de nailon 11/0 o 12/0. Posteriormente, se comprueba de nuevo el drenaje linfático en la vena mediante ICG. A menudo, los vasos linfáticos adicionales de una determinada zona quirúrgica, que no fueron visualizados ni registrados por la ICG antes de la operación, sólo se detectan intraoperatoriamente. Estos vasos adicionales suelen tener un diámetro mayor y casi más adecuado. El drenaje linfático es parcialmente visible a simple vista. Estos vasos linfáticos denominados ICG-negativos se utilizan cada vez más para generar anastomosis adicionales en la zona quirúrgica y potenciar la función de drenaje.
Hasta ahora, estas observaciones clínicas no se han descrito en la literatura. En general, la investigación experimental en este campo es muy limitada. Las funciones de transporte diferencial entre dos vasos colectores se demostraron en un modelo de rata [7]. Se cree que existen patrones de drenaje linfático preferencial de modo que, para un espacio tisular determinado, el drenaje linfático es responsabilidad principal de un solo vaso, y que los vasos adicionales de la zona sólo sirven cuando el sistema está sobrecargado o como ruta de transporte de reserva para grandes cargas linfáticas [7]. Las diferencias en la profundidad y el diámetro de los vasos pueden favorecer el drenaje linfático a través de un vaso linfático concreto [7]. Los efectos del verde de indocianina sobre la contractilidad linfática normal y la función de drenaje también pueden causar un artefacto significativo [8].
La identificación de las venas pequeñas también es problemática en los pacientes con linfedema porque la grasa subcutánea suele estar engrosada y el tejido, fibrótico. Debe existir una vena adecuada en las inmediaciones de un vaso linfático funcional detectado. En la literatura se describen como prometedores los sistemas de visualización sin contacto para la identificación preoperatoria de vénulas subcutáneas con un diámetro de aproximadamente 0,5-1,0 mm [9].
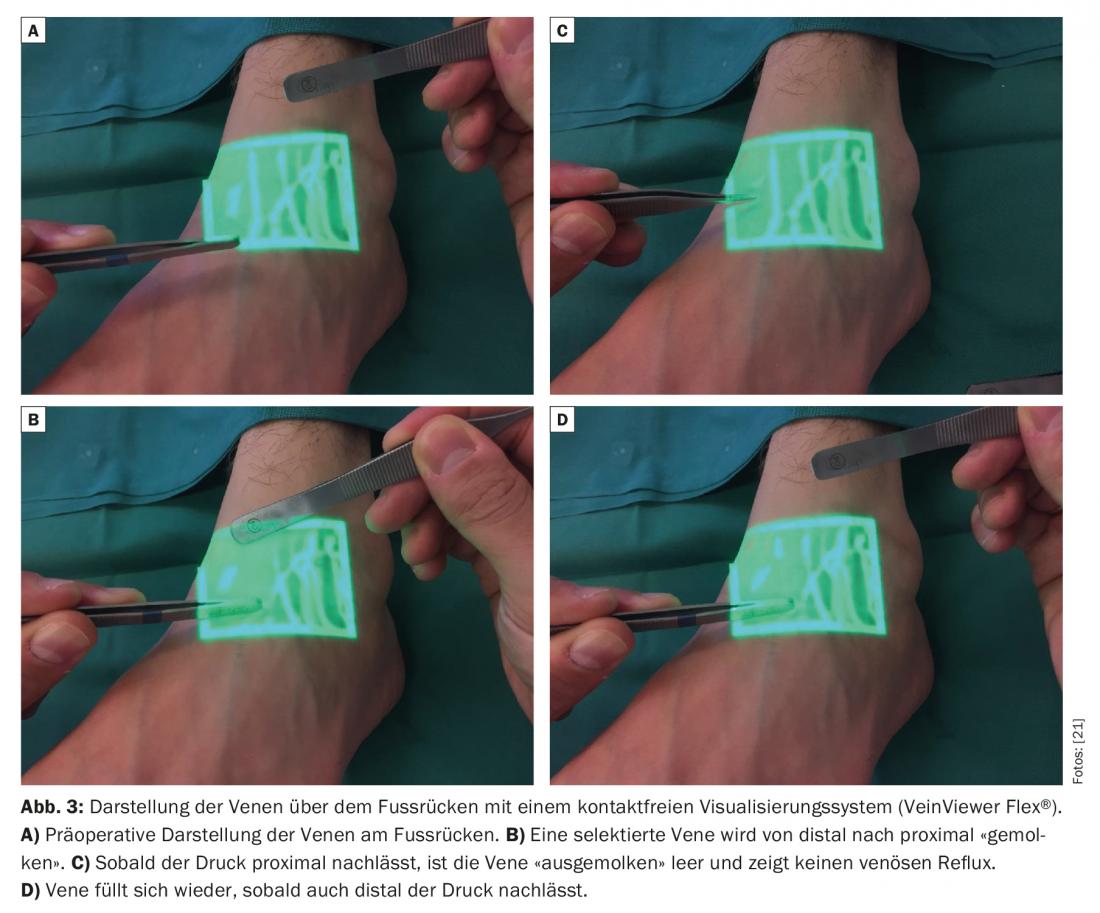
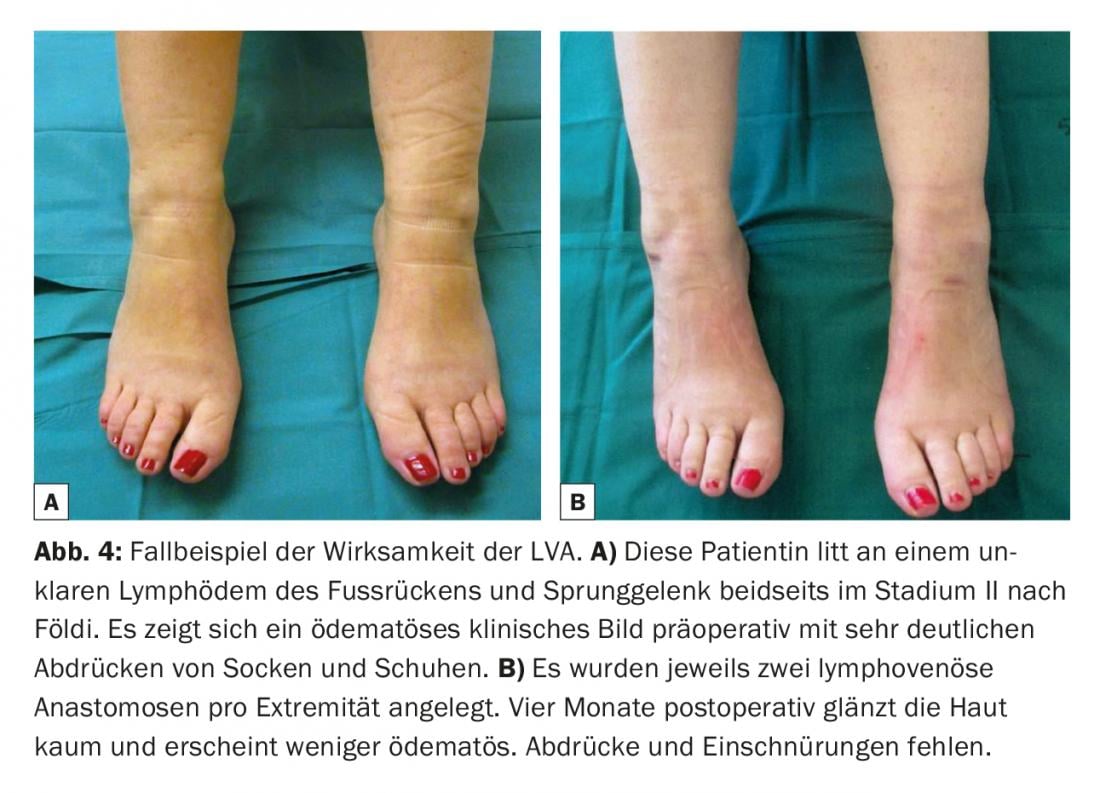
La presión venosa suele ser mayor que en el sistema linfático [10,11]. Por lo tanto, la ausencia de reflujo venoso también tiene una importancia elemental. Si la vena tiene un sistema de válvulas inadecuado o un curso desfavorable, puede producirse un reflujo venoso hacia el vaso linfático. Así, la trombosis y la fibrosis de las anastomosis pueden limitar significativamente la longevidad de las anastomosis [12]. Por lo tanto, los sistemas de visualización estándar sin contacto se utilizan cada vez más para obtener una cartografía venosa rápida e identificar bifurcaciones ocultas, así como válvulas desfavorablemente situadas en las venas que podrían influir negativamente en la calidad de las anastomosis linfovenosas creadas. (Fig.3). En el postoperatorio, se lleva un vendaje de compresión ligera para no poner en peligro las delicadas anastomosis recién aplicadas. Los pacientes permanecen hospitalizados durante una noche. De este modo, podrían reducirse las lesiones cutáneas en las supervivientes de cáncer de mama con linfedema en las extremidades superiores [13]. Muchos estudios clínicos informan de una reducción de la circunferencia de entre el 35% y el 50% en pacientes con cáncer de mama y linfedema en el brazo un año después de colocar estas anastomosis [14–16]. La discrepancia en estos resultados se debe muy probablemente a los resultados retrospectivos con sólo un pequeño número de casos. En un estudio prospectivo más amplio con 100 casos, los investigadores determinaron más recientemente una reducción de la circunferencia de hasta el 38% al cabo de tres años y demostraron que también se producía un alivio significativo de los síntomas desde el punto de vista subjetivo [17]. El dolor asociado al linfoedema se alivió [18]. En otro estudio clínico con 49 pacientes que sufrían linfedema secundario de las extremidades inferiores, se descubrió que la combinación de anastomosis linfovenosas con liposucción también puede reducir significativamente la textura de la piel, así como la circunferencia [19]. En general, se postula que la eficacia de la LVA aumenta en las primeras fases (Fig. 4) . Existen en la literatura informes de casos y revisiones que demuestran que la aparición de linfedema tras una linfadenectomía puede reducirse significativamente mediante la colocación profiláctica de anastomosis linfovenosas [20].
En resumen, los procedimientos de resección son invasivos y están plagados de complicaciones, por lo que sólo se consideran en las fases finales de la enfermedad. La liposucción es un procedimiento de resección especial porque es menos invasivo y ha dado excelentes resultados en muchos estudios clínicos. Los procedimientos de resección pueden combinarse con la creación de anastomosis linfovenosas en determinados casos. La creación de anastomosis linfovenosas es un procedimiento quirúrgico seguro hasta la fecha y ha mostrado resultados de mejora de la calidad de la piel y de reducción de la circunferencia en los estudios clínicos y experimentales disponibles hasta la fecha, aunque aún están pendientes los resultados a largo plazo. En definitiva, en el futuro serán necesarios más estudios experimentales y estudios clínico-prospectivos a largo plazo con un mayor número de pacientes para poder demostrar mejor la evidencia de esta terapia y optimizar continuamente el procedimiento desde el punto de vista técnico.
Las anastomosis linfovenosas están reconocidas internacionalmente como parte integrante de la terapia quirúrgica del linfedema.
Mensajes para llevarse a casa
- Los procedimientos de resección son invasivos y están plagados de complicaciones. Sólo se consideran en las fases finales de la enfermedad.
- La creación de anastomosis linfovenosas es un procedimiento quirúrgico seguro hasta la fecha y ha mostrado resultados de mejora de la calidad de la piel y reducción de la circunferencia en los estudios clínicos y experimentales disponibles.
- Las anastomosis linfovenosas están reconocidas internacionalmente como parte integrante de la terapia quirúrgica del linfedema.
Literatura:
- Charles H: Elefantiasis de la pierna. En: Latham A, English TC, editores. Un sistema de tratamiento. Vol. Londres: Churchill 1912: 516.
- Sistrunk WE: Contribución a la cirugía plástica: eliminación de cicatrices por etapas; una operación abierta para la laceración extensa del esfínter anal; la operación Kondoleon para la elefantiasis. Ann surg 1927; 85: 185-193.
- Thompson N: Operación de colgajo dérmico enterrado para el linfedema crónico de las extremidades. Plast Reconstr Surg 1970; 45: 541-548.
- Brorson H: La liposucción normaliza la hipertrofia del tejido adiposo inducida por el linfedema en la elefantiasis de la pierna. Plast Reconstr Surg 2015; 136 (4): 133-134.
- Brorson H: Reducción completa del linfedema de brazo tras un cáncer de mama – Un estudio prospectivo de veintiún años. Plast Reconstr Surg 2015; 136 (4): 134-135.
- Hoffner M, et al: El SF-36 muestra un aumento de la calidad de vida tras la reducción completa del linfedema postmastectomía con liposucción. Lymphat Res Biol 2017; 15 (1): 87-98.
- Gashev AA et al: El verde de indocianina y la imagen linfática: problemas actuales. Investigación y Biología Linfática. 2010; 8 (2): 127-130.
- Weiler M, Dixon JB: Función de transporte diferencial de los vasos linfáticos en el modelo de cola de rata y los efectos a largo plazo del verde de indocianina evaluados con imágenes de infrarrojo cercano. Fronteras de la fisiología. 2013; 4: 215.
- Makoto M, et al: Linfedema de miembros inferiores tratado con anastomosis linfático-venosa basada en linfografía icg preoperatoria e intraoperatoria y visualización de venas sin contacto: informe de un caso. Microcirugía 2012; 32: 227-230.
- Wardhan R, Shelley K: Onda de presión venosa periférica. Curr Opin Anaesthesiol 2009; 22: 814-821
- Munn LL: Mecanobiología de las contracciones linfáticas. Semin Cell Dev Biol 2015; 38: 67-74.
- Yamamoto T, Koshima I: Neovalvuloplastia para supermicrocirugía linfática. JPlast Reconstr Aesthet Surg 2014; 67: 587-588.
- Jeremy ST, et al: La derivación linfático-venosa disminuye los cambios patológicos de la piel en el cáncer de mama de las extremidades superiores rel. Linfedema. Lymphatic Res Biol. 2015; 13: 46-53.
- Koshima I, et al: Anastomosis linfáticovenular supermicroquirúrgica para el tratamiento del linfedema en las extremidades superiores. J Reconstr Microsurg 2000; 16: 437-442
- Furukawa H, et al: Implantación linfático-venosa microquirúrgica dirigida al reflujo linfático dérmico mediante linfografía por fluorescencia verde de indocianina en el tratamiento del linfedema postmastectomía. Plast Reconstr Surg 2011; 127: 1804-1811.
- Chang DW: Derivación linfático-venular para el tratamiento del linfedema en pacientes con cáncer de mama: un estudio prospectivo. Plast Reconstr Surg 2010; 126: 752-758.
- Chang DW, et al: Un análisis prospectove de 100 casos consecutivos de bypass linfovenoso para el tratamiento del linfedema de las extremidades. Plastic Reconst Surg 2013; 132: 1305-1314.
- Mihara M, et al: La anastomosis linfático-venosa libera el dolor asociado al linfedema de las extremidades inferiores. Plast Reconst Surg Global Open. 2017; 5 (1): e1205.
- Chang K1, et al: Liposucción combinada con anastomosis linfático-venosa para el tratamiento del linfedema secundario de las extremidades inferiores: informe de 49 casos. Zhonghua Wai Ke Za Zhi 2017; 55 (4): 274-278.
- Jorgensen MG, et al: El efecto de la anastomosis linfovenosa profiláctica y las derivaciones para prevenir el linfedema relacionado con el cáncer: una revisión sistemática y metaanálisis. Microsurg 2017; 00: 1-10.
- Scaglioni M, et al: Optimización de los resultados de la supermicrocirugía de anastomosis linfático-venosa (LVA) mediante la identificación preoperatoria de la vena libre de reflujo: elija bien la vena. Manuscrito enviado a Microsurgery, 2017.
CARDIOVASC 2017; 16(5): 11-15