La investigación en nuevos productos biológicos está contribuyendo a ofrecer alternativas de tratamiento para la psoriasis en placas de moderada a grave cuando hay falta de respuesta o pérdida de eficacia [1]. Los datos publicados en 2019 por la Red Suiza de Dermatología de Terapias Dirigidas (SDTT) muestran que la rápida mejoría de los síntomas cutáneos y la ausencia de lesiones se encuentran entre los criterios más importantes para los pacientes, según la doctora Julia-Tatjana Maul, del Hospital Universitario de Zúrich [2,3].
Volver a “Noticias sobre dermatitis atópica y psoriasis”.
El inhibidor de la interleucina-23 risankizumab (SKYRIZITM) está aprobado en Suiza desde abril de 2019 para la psoriasis en placas de moderada a grave tras el fracaso del tratamiento sistémico convencional [4]. Desde el 1 de agosto de 2019, el anticuerpo monoclonal humanizado también ha sido aprobado para su uso por los fondos de seguros sanitarios [5]. El risankizumab se inyecta por vía subcutánea (150 mg; 2× 75 mg); tras la primera administración a intervalos de cuatro semanas y posteriormente a intervalos de doce semanas cada uno [4]. Se ha confirmado clínicamente su eficacia elevada y duradera con una respuesta rápida, así como su buena tolerabilidad [6–8].
Datos a largo plazo: Conclusión positiva
Su alta eficacia, practicabilidad y tolerabilidad contribuyen a mejorar la calidad de vida, que es también un objetivo terapéutico importante, según el Prof. Peter Häusermann, del Hospital Universitario de Basilea. Gracias a la rápida tasa de respuesta -alivio significativo de los síntomas en un plazo de 4 a 8 semanas- se puede reducir la fase de deterioro de la vida cotidiana relacionada con la psoriasis. El experto subrayó que la eficacia del risankizumab no disminuye incluso con un uso prolongado [9]. Esto también lo confirman los datos de varios estudios de fase III [6–8].
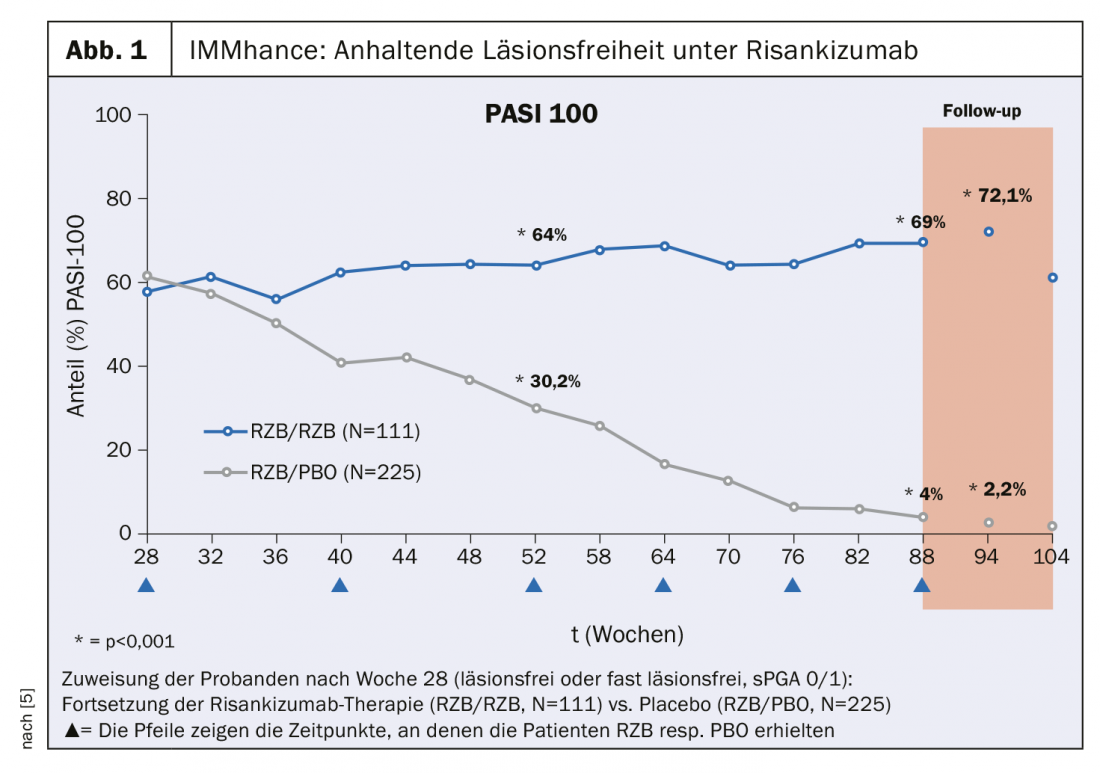
El estudio IMMhance investigó los efectos a largo plazo de la interrupción del tratamiento con risankizumab en pacientes con psoriasis en placas de moderada a grave. Aquellos que consiguieron un estado libre o casi libre de lesiones en la semana 28 tras el inicio del tratamiento (Static Physician Global Assessment, sPGA 0/1) fueron asignados aleatoriamente a las condiciones de continuación del tratamiento con risankizumab (n=111) frente a placebo (n=225). En el grupo de participantes del estudio que seguían en tratamiento con risankizumab, más del 70% logró una curación completa de la piel según el índice de gravedad del área de psoriasis (PASI) 100 en la semana 94 (Fig. 1). Sin embargo, en el grupo al que se cambió a placebo, la respuesta PASI 100 empeoró del 61,3% al 2,2% [6]. En los ensayos UltIMMa-1 y UltIMMa-2, el 75,1% y el 81,3% de los pacientes tratados con risankizumab (n=598) alcanzaron un PASI 90 tras 16 y 52 semanas de tratamiento, respectivamente, según un análisis integrado de ambos ensayos, lo que supone una cifra significativamente superior a la del grupo de ustekinumab, en el que menos del 50% de los 199 sujetos alcanzaron un PASI 90 en ambos puntos temporales [8].
Controversia económica sanitaria
El risankizumab está indicado para el tratamiento de la psoriasis en placas de moderada a grave en adultos que hayan tenido una respuesta inadecuada a otras terapias sistémicas [4]. En concreto, al menos una terapia sistémica convencional (ciclosporina, metotrexato, acitretina o UVB y PUVA) debe haber fracasado tras 16 semanas de tratamiento [5]. No hay consenso sobre cuántos ensayos de terapia sistémica con no biológicos deben probarse primero. En general, sin embargo, se propaga una estrategia de terapia personalizada. Se valora de forma diferente si se debe interrumpir la terapia cuando se alcanza un PASI de 100 y qué se considera un criterio para cambiar a otro biológico. El Prof. Häusermann tiene la visión de que en unos cinco años la clase de sustancia innovadora de los inhibidores de la IL-23 se utilizará de forma rutinaria. Hasta entonces, también podría ser posible reducir la diferencia de precio respecto a la terapéutica sistémica convencional, que actualmente es un dilema económico sanitario de estos fármacos altamente eficaces [9].
Volver a “Noticias sobre dermatitis atópica y psoriasis”.
Literatura:
- Birchler T: Risankizumab como opción terapéutica para la psoriasis. Presentación de diapositivas. Thomas Birchler, AbbVie AG, asesor médico, mesa redonda con los medios de comunicación, Iaculis GmbH & AbbVie AG, 29.10.2019, Zúrich.
- Maul JT: Risankizumab como opción terapéutica para la psoriasis. Presentación de diapositivas. Julia-Tatjana Maul, MD, Mesa redonda con los medios de comunicación, Iaculis GmbH & AbbVie AG, 29.10.2019, Zúrich.
- Maul JT et al. El sexo y la edad determinan de forma significativa las necesidades del paciente y los objetivos del tratamiento en la psoriasis: una lección para la práctica. J Eur Acad Dermatol Venereol, 2019. 33(4): p. 700-708.
- Información técnica actual sobre SKYRIZITM en www.swissmedicinfo.ch.
- Lista de especialidades 2019 de la Oficina Federal de Salud Pública FOPH. www.spezialitaetenliste.ch, en agosto de 2019.
- Blauvelt A, Leonardi, C., Gooderham, M., Papp, K. Eficacia y seguridad del risankizumab Q12W continuo frente a la retirada del tratamiento: resultados a doble ciego durante 2 años del ensayo de fase 3 IMMhance. presentado en el 24º Congreso Mundial de Dermatología. Milán, Italia, del 10 al 15 de junio de 2019.
- Gordon KB et al. Eficacia y seguridad del risankizumab en la psoriasis en placas de moderada a grave (UltIMMa-1 y UltIMMa-2): resultados de dos ensayos de fase 3 doble ciego, aleatorizados, controlados con placebo y ustekinumab. Lancet, 2018. 392(10148): p. 650-661.
- Lebwohl M et al. Eficacia y seguridad del risankizumab en la psoriasis en placas de moderada a grave: un análisis integrado de UltIMMa-1 y UltIMMa-2. P8108, presentado en la Reunión Anual de la Academia Americana de Dermatología, Washington DC, del 1 al 5 de marzo de 2019.
- Häusermann P: Risankizumab como opción terapéutica para la psoriasis. Presentación de diapositivas. Prof. Dr. med. Peter Häusermann, Mesa redonda con los medios de comunicación, Iaculis GmbH & AbbVie AG, 29.10.2019, Zúrich.
Adaptado de: DERMATOLOGIE PRAXIS 2019; 29(6): 26











