El carcinoma de próstata es el tumor masculino más frecuente en los países occidentales y es la segunda causa de muerte relacionada con el cáncer en Suiza. En concreto, el cáncer de próstata resistente a la castración metastásico (CPRCm) es un reto que puede abordarse terapéuticamente de muchas maneras en la actualidad. La situación actual de los datos sobre las nuevas sustancias activas se debatió en el Simposio sobre Próstata celebrado en St.
“¿Qué prometen los nuevos fármacos y avances en el campo del carcinoma de próstata metastásico?” fue la pregunta que planteó el doctor Aurelius Omlin, del Hospital Cantonal de St. “No hace mucho tiempo que la quimioterapia con docetaxel era la única opción de tratamiento que ofrecía un beneficio de supervivencia global a los pacientes con cáncer de próstata metastásico resistente a la castración (progresión a pesar de la supresión de la testosterona) (CPRCm).
Esto sólo cambió en los últimos cuatro años, cuando se pudo demostrar la eficacia de los siguientes fármacos en ensayos prospectivos aleatorizados: la inmunoterapia con sipuleucel-T, una quimioterapia de unión a la tubulina análoga al docetaxel con cabazitaxel, el nuevo inhibidor de la síntesis hormonal abiraterona, el radionúclido radio-223 y el nuevo antagonista del receptor androgénico enzalutamida (Tabla 1)”.

Cabazitaxel: Está aprobado en Suiza tras el fracaso de la quimioterapia con docetaxel. En combinación con prednisona, muestra una ventaja significativa en la supervivencia global sobre la combinación con mitoxantrona [1].
Abiraterona: Está aprobada en Suiza después y, como única de las nuevas sustancias, también antes de la quimioterapia con docetaxel. En combinación con prednisona, muestra una ventaja significativa en la supervivencia global en comparación con placebo más prednisona, después de una terapia de primera línea con docetaxel [2]. En combinación con prednisona, también mejora significativamente la supervivencia libre de progresión como terapia de primera línea en comparación con placebo más prednisona y muestra una tendencia en la supervivencia global [3].
Enzalutamida: Aún no está aprobada en Suiza, pero se espera para 2014. Tras la quimioterapia, muestra una ventaja significativa sobre el placebo en la supervivencia global [4].
Radio-223: Actualmente está disponible en Suiza como parte de un programa de acceso ampliado.
Seguimiento y uso secuencial
“El nivel de PSA puede aumentar con las nuevas terapias en las primeras doce semanas, por lo que la medición del PSA debe realizarse con precaución durante este tiempo. Después, sin embargo, debe hacerse cada tres o cuatro semanas”, dice el Dr. Omlin. El seguimiento también incluye:
- TAC y gammagrafía cada doce semanas
- Resonancia magnética de columna larga en caso de afectación ósea extensa: Línea de base y si está clínicamente indicado (dolor, déficits neurológicos).
Actualmente no se dispone de datos recopilados prospectivamente sobre el uso secuencial y la posible resistencia cruzada de las nuevas sustancias. Sin embargo, hay estudios más pequeños con una potencia limitada, por ejemplo, los que investigan el docetaxel después de la abiraterona: La actividad del docetaxel fue inferior a la esperada tras la abiraterona y no hubo respuesta significativa del PSA o de los tejidos blandos en ocho pacientes que tampoco habían respondido a la abiraterona o que habían progresado durante la terapia con abiraterona. [5]. La enzalutamida mostró un beneficio significativo en unos pocos pacientes de forma secuencial tras docetaxel y abiraterona [6]; de forma similar, la abiraterona parece tener un efecto moderado tras docetaxel y enzalutamida [7]. En la actualidad se carece de factores predictivos que permitan una selección terapéutica individualizada.
“En general, pues, hay muchas opciones terapéuticas nuevas con tasas de supervivencia mejoradas, lo que a su vez hace que la gestión de los efectos secundarios y la prevención de las complicaciones (eventos óseos) sean aún más importantes. El seguimiento de las terapias es exigente en cualquier caso, la resistencia cruzada de las nuevas terapias es de esperar en algunos casos y, lo que tampoco debe olvidarse: los costes de las nuevas terapias son considerables”, concluyó su conferencia el Dr. Omlin. “Debido al aumento de las posibilidades y la complejidad, los pacientes con cáncer de próstata resistente a la castración deben ser discutidos de forma interdisciplinar y, si es posible, también incluidos en ensayos clínicos para lograr nuevos avances en el tratamiento de esta enfermedad.”
¿Cómo tratar las metástasis óseas?
El PD Dr. med. Dr. Friedemann Honecker del ZeTuP de St. Gallen habló sobre el tema de las metástasis óseas y el tratamiento dirigido a los huesos: “Más del 90% de todos los pacientes con CPRCm desarrollan metástasis óseas. Esto se asocia a una importante mortalidad y morbilidad. Estas metástasis osteoblásticas mayoritarias provocan una mayor tasa de eventos óseos (“eventos relacionados con el esqueleto”, SRE). Las posibles complicaciones son: Dolor, inmovilización, fracturas patológicas, hipercalcemia o compresión nerviosa/espinal”.
Dado que las sustancias mensajeras PTHrP, RANKL, TGF-β, FGF, MET y VEGF en el lado tumoral y TNF-α y ET-1 en el lado óseo están implicadas de forma significativa en la metástasis esquelética, también representan posibles dianas para la terapia dirigida.
Por ejemplo, el denosumab, un anticuerpo anti-RANKL, ya se utiliza específicamente para tratar las metástasis óseas. Es especialmente eficaz para reducir el riesgo de SRE. En un estudio de fase III, se consiguió una reducción relativa de aproximadamente el 18% en comparación con el zoledronato (Fig. 1) [8].
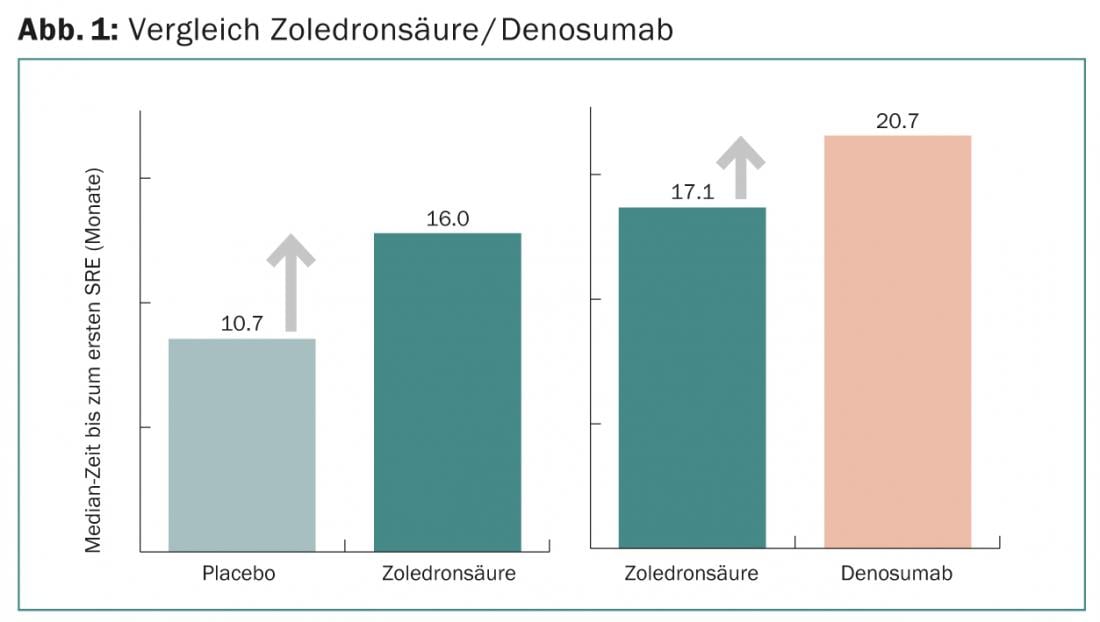
Sin embargo, el bifosfonato zoledronato también previno de forma significativa los SRE en comparación con el placebo [9]. “Las reacciones adversas a los bifosfonatos incluyen síntomas parecidos a los de la gripe (reacción de fase aguda) en el 10-20% de los casos, efectos secundarios renales (disminución del aclaramiento de creatinina), hipocalcemia (disminución del nivel de calcio sérico) y osteonecrosis de la mandíbula (acontecimiento multifactorial). El aclaramiento de creatinina debe comprobarse siempre antes de cada infusión; si aumenta, debe ajustarse la dosis. La duración de la infusión no debe acortarse, sino retenerse o prolongarse. La recomendación al paciente de que beba 1-2 l de agua el día de la infusión es sensata”, explicó el Dr. Honecker.
El radio-223 mostró incluso un efecto positivo sobre la supervivencia global en pacientes sintomáticos con metástasis óseas, por lo que actualmente se está estudiando su aprobación en Suiza. Por último, la sustancia ya aprobada abiraterona también muestra una buena eficacia con respecto a la aparición de ERE, así como para paliar el dolor óseo.
El cabozantinib, un inhibidor de VEGFR2/MET, es particularmente prometedor entre los agentes activos completamente nuevos y aún no aprobados e indujo una respuesta muy clara de las metástasis óseas en la gammagrafía esquelética en un 60-70% y un alivio del dolor en un buen 50% de los pacientes parcialmente pretratados en estudios de fase II. El compuesto se encuentra actualmente en ensayos de fase III. También deben tenerse en cuenta los efectos secundarios, a veces graves, del cabozantinib en particular.
Radio-223
Por último, el Dr. Joachim Müller, del Hospital Cantonal de St. Gallen, entró en más detalles sobre el radionucleido radio-223 (nuevo nombre comercial Xofigo®): “Es el primer radiofármaco emisor de partículas alfa disponible clínicamente para la terapia médica nuclear de las metástasis óseas en la CPRCm.
En comparación con los emisores beta (estroncio-89, samario-153, renio-188) que se han utilizado durante mucho tiempo, que permiten una terapia paliativa del dolor pero no prolongan la supervivencia, los emisores alfa presentan algunas ventajas físicas: transfieren su energía al tejido de la forma más corta posible, por lo que las zonas vecinas, como la médula ósea adyacente, no reciben ninguna dosis de radiación o sólo una dosis muy baja.”
El conocido ensayo de fase III ALSYMPCA [10] condujo recientemente a la aprobación de la FDA. La supervivencia global se prolongó significativamente en comparación con el placebo, al igual que el intervalo de tiempo hasta el primer evento esquelético. Los efectos secundarios sólo fueron leves e incluyeron diarrea y náuseas. La hemotoxicidad de grado 3-4 es rara: Neutropenia 2%, trombocitopenia 3%, anemia 6%.
Aún no se han determinado las posibles combinaciones con otros medicamentos.
Fuente: 5º Simposio Interdisciplinario sobre el Cáncer de Próstata, 7 de noviembre de 2013, St.
Literatura:
- De Bono JS, et al: Prednisona más cabazitaxel o mitoxantrona para el cáncer de próstata metastásico resistente a la castración que progresa tras el tratamiento con docetaxel: un ensayo aleatorizado abierto. The Lancet 2010; 376(9747): 1147-1154. doi:10.1016/S0140-6736(10)61389-X.
- De Bono JS, et al: Abiraterona y aumento de la supervivencia en el cáncer de próstata metastásico. N Engl J Med 2011; 364: 1995-2005. doi: 10.1056/NEJMoa1014618.
- Ryan CJ, et al: Abiraterona en el cáncer de próstata metastásico sin quimioterapia previa. N Engl J Med 2013; 368: 138-48. doi: 10.1056/NEJMoa120909.
- Scher HI, et al: Aumento de la supervivencia con enzalutamida en el cáncer de próstata tras la quimioterapia. N Engl J Med 2012 Sep 27; 367(13): 1187-97. Epub 2012 Aug 15.
- Mezynski J, et al: Actividad antitumoral del docetaxel tras el tratamiento con el inhibidor de CYP17A1 abiraterona: ¿pruebas clínicas de resistencia cruzada? Ann Oncol 2012 Nov; 23(11): 2943-7. doi: 10.1093/annonc/mds119. Epub 2012 Jul 5.
- Schrader AJ, et al: Enzalutamida en pacientes con cáncer de próstata resistente a la castración que progresan tras docetaxel y abiraterona. Eur Urol 2013 jul 2. pii: S0302 2838(13)00657-X. doi: 10.1016/j.eururo.2013.06.042. [Epub ahead of print].
- Noonan KL, et al: Actividad clínica del acetato de abiraterona en pacientes con cáncer de próstata metastásico resistente a la castración que progresa tras enzalutamida. Ann Oncol 2013. doi: 10.1093/annonc/mdt138 Primera publicación en línea: 12 de abril de 2013.
- Fizazi K, et al: Denosumab frente a ácido zoledrónico para el tratamiento de las metástasis óseas en hombres con cáncer de próstata resistente a la castración: un estudio aleatorizado a doble ciego. Lancet 2011 mar 5; 377(9768): 813-22. doi: 10.1016/S0140-6736(10)62344-6. Epub 2011 Feb 25.
- Saad F, et al: Ensayo aleatorizado controlado con placebo de ácido zoledrónico en pacientes con carcinoma de próstata metastásico refractario a las hormonas. J Natl Cancer Inst 2002 Oct 2; 94(19): 1458-68.
- Parker C, et al: El emisor alfa radio-223 y la supervivencia en el cáncer de próstata metastásico. N Engl J Med 2013; 369: 213-23. doi: 10.1056/NEJMoa1213755.
InFo Oncología y Hematología 2013; 1(1): 33-36