Existen nuevos enfoques terapéuticos para el mieloma múltiple. Por ejemplo, se está investigando la eficacia y la seguridad de las células CAR-T. En particular, podrían ser aplicables en la situación refractaria y recidivante en el futuro.
La lenalidomida se utiliza cada vez más para la terapia de inducción en pacientes con mieloma múltiple. Sin embargo, debido a la resistencia a la lenalidomida en el mieloma múltiple, que a menudo se produce en el curso posterior del tratamiento, la búsqueda de terapias de seguimiento eficaces es médicamente necesaria.
OPTIMISMM: Demostrado que es más que puro optimismo
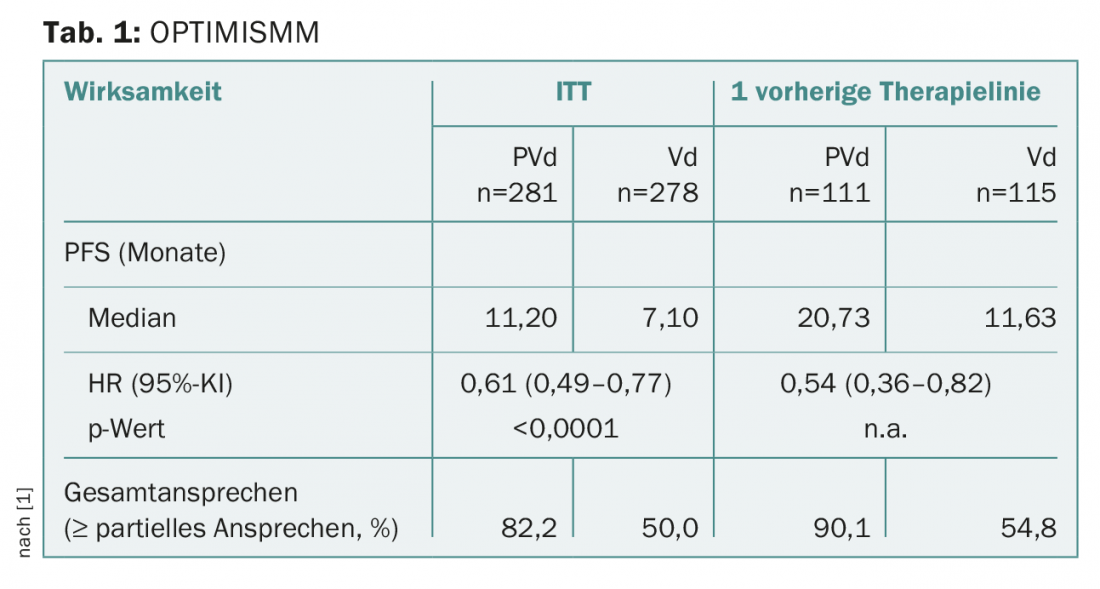
En la actualidad, la pomalidomida se utiliza habitualmente en el tratamiento del mieloma múltiple en recaída/refractario, e incluso se ha demostrado a menudo su eficacia contra las células resistentes a la lenalidomida [1]. El estudio de fase III presentado, denominado OPTIMISMM, en pacientes tratados con lenalidomida con mieloma múltiple en recaída/refractario (de los cuales cerca del 70% eran previamente refractarios a la lenalidomida) reveló, entre otras cosas, una prolongación significativa de la supervivencia libre de progresión: En la población por intención de tratar, pero también tras un único tratamiento previo (incluida la lenalidomida), tanto la SLP como la tasa de respuesta global (TRG) fueron mejores para la pomalidomida, el bortezomib y la dexametasona a dosis bajas en comparación con el bortezomib y la dexametasona solos. (Tab. 1) [1].
¿Respuesta sostenida al tratamiento gracias a la inmunoterapia?
En el congreso de la EHA de este año también se debatió muy animadamente otro novedoso enfoque terapéutico para el mieloma múltiple, la inmuno-oncología mediante células CAR-T. La inmunoterapia podría ser una opción de tratamiento en el futuro, especialmente para los pacientes con MM refractario muy pretratados.
Como diana terapéutica, el antígeno de maduración de las células B (abreviado BCMA) parece actualmente muy prometedor. El BCMA se expresa predominantemente en la superficie de las células plasmáticas y se encuentra en muy pocos otros tejidos del cuerpo humano. Esto lo convierte en un marcador tumoral adecuado y en una posible diana para la inmunoterapia [2].
En un primer ensayo multicéntrico de fase I [2], los hematólogos están utilizando bb2121, células T con receptores de antígenos quiméricos (CAR) de segunda generación que pueden reconocer con precisión el BCMA. La fase de escalada de dosis del estudio ya ha proporcionado resultados prometedores en cuanto a la eficacia y seguridad del bb2121 en pacientes con mieloma múltiple en recaída/refractario.
Una buena mitad de los pacientes presentados participaron en la fase de escalada. Anteriormente, tenían que haberse sometido al menos a tres terapias (incluidos un inhibidor del proteasoma y un inmunomodulador) o ser doblemente refractarios a la terapia. En sus células plasmáticas, estos pacientes portaban BCMA en ≥50% de los casos [2]. La segunda parte del estudio en curso, la denominada fase de expansión de dosis, preconizaba la preterapia con daratumumab para el resto de pacientes presentados. Además, la enfermedad tenía que ser refractaria a la última terapia. Por el contrario, ya no se requería una expresión de BCMA demostrada.
Los resultados mostraron que el bb2121 funcionaba de forma muy prometedora a dosis de ≥150 × 106 células CAR-T (Tab. 2) [2]:
- Hubo una respuesta sostenida a la terapia, la neurotoxicidad y el síndrome de liberación de citoquinas (SRC) fueron controlables como grado 1-2 principalmente.
- En general, la terapia de células T CAR contra el BCMA con bb2121 parece representar sin duda una nueva opción de tratamiento para los pacientes con mieloma múltiple en recaída/refractario.

Tema candente: la inmunoterapia
Desde el punto de vista genético, el mieloma múltiple es muy heterogéneo, lo que lo convierte en una enfermedad compleja. Hoy en día, la secuenciación de próxima generación (NGS) ya va mucho más allá de la importancia diagnóstica de la citogenética convencional y ha ayudado, entre otras cosas, a descifrar importantes vías de señalización y procesos de mutación que pueden influir en el pronóstico de un paciente con mieloma múltiple. Al mismo tiempo, los avances dentro del diagnóstico genético son el punto de partida de nuevos procedimientos terapéuticos como la inmunoterapia, que por supuesto incluye el procedimiento de células CAR-T o el anticuerpo anti-CD38 daratumumab.
El anticuerpo monoclonal anti-CD38 daratumumab es ya un factor importante en la lucha contra el mieloma múltiple. El mecanismo de acción es tan sencillo como eficaz: el anticuerpo anti-CD38 induce la muerte celular de las células del mieloma, por un lado, mediante efectos inmunológicos directos y, por otro, mediante la eliminación de las células inmunosupresoras. Los estudios también demostraron que las combinaciones de anticuerpos monoclonales como daratumumab o elotuzumab y fármacos inmunomoduladores o inhibidores del proteasoma pueden aumentar su eficacia terapéutica, pero sin provocar más efectos tóxicos.
En el futuro, se espera que la gama de inmunoterapias para el mieloma múltiple aumente aún más, según los expertos del congreso de la EHA. Por ejemplo, se está hablando de conjugados formados por un anticuerpo y un fármaco o del uso de inhibidores de puntos de control para el tratamiento del mieloma múltiple [3].
Los hematólogos y oncólogos deben tenerlo en cuenta
En los últimos años se han producido algunos avances notables en el campo de las opciones de tratamiento del mieloma múltiple. Sin embargo, no hay que olvidar que el MM sigue siendo una enfermedad tumoral que no puede tratarse de forma curativa. Especialmente en el mieloma múltiple recidivante/refractario, la elección de opciones de tratamiento se considera limitada. La inmunoterapia podría ofrecer nuevas posibilidades en este sentido en el futuro, pero muchos enfoques para el tratamiento del MM, incluidas las células CAR-T, se encuentran todavía en fase de desarrollo y, por tanto, lamentablemente aún no están disponibles para la práctica diaria.
La aprobación de varias combinaciones nuevas de fármacos (por ejemplo, carfilzomib-lenalidomida-dexametasona, daratumumab-lenalidomida-dexametasona o elotuzumab-lenalidomida-dexametasona, así como bortezomib-dexametasona-daratumumab) ha mejorado la terapia de los pacientes con mieloma múltiple en recaída/refractario. Sin embargo, esto también complicó el proceso de toma de decisiones terapéuticas por parte de médicos y pacientes. En cualquier caso, la terapia debe optimizarse para cada paciente, especialmente en caso de recaída [3].
Fuente: Congreso de la EHA, 14-17 de junio de 2018, Estocolmo
Literatura:
- Richardson P, et al: OPTIMISMM: ensayo de fase 3 de pomalidomida, bortezomib y dosis bajas de dexametasona frente a bortezomib y dosis bajas de dexametasona en pacientes expuestos a lenalidomida con mieloma múltiple en recaída/refractario. EHA 2018; Resumen S847.
- Raje N, et al: bb2121 anti-bcma car t cell therapy in patients with relapsed/refractory multiple myeloma: updated results from a multicenter phase I study. EHA 2018; Resumen S138.
- Van de Donk N: Inmunoterapia en el mieloma: ¿por qué, cuándo y cómo? Tema: 3ec Mieloma de células plasmáticas (mieloma múltiple). EHA 2018; 219162.
InFo ONCOLOGÍA Y HEMATOLOGÍA 2018; 6(4): 39-40.