Una vez que se ha producido el daño articular en el curso de la artritis reumatoide, ya no puede revertirse con medicación. Por lo tanto, es importante utilizar la terapéutica básica lo antes posible. Si las sustancias convencionales no funcionan lo suficiente o no se toleran, entran en juego las biológicas. El siguiente artículo ofrece una visión general de las estrategias terapéuticas.
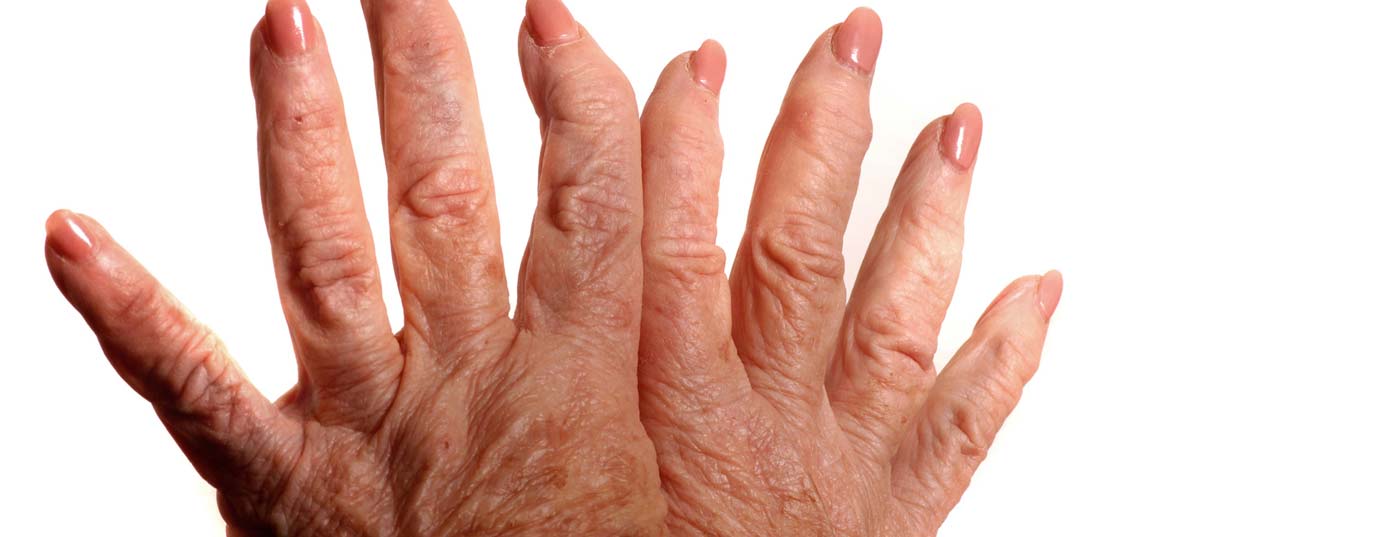
La destrucción de las articulaciones relacionada con la inflamación en la artritis reumatoide (AR) comienza muy pronto en el curso de la enfermedad, normalmente en los primeros meses. El daño articular o artrosis secundaria (Fig. 1) es irreversible y no puede revertirse con medicación. Cuanto antes se utilice la terapéutica básica, mejor será la respuesta.
Para una buena gestión, es esencial la cooperación interdisciplinar con la fisioterapia, la terapia ocupacional y, a veces, la cirugía del reumatismo. La coordinación de las medidas de tratamiento dentro de estos ámbitos debe hacerse con cuidado, especialmente en la interacción entre el proveedor de atención primaria y el reumatólogo.

Diagnóstico precoz
Hoy en día, la remisión completa es un objetivo bastante realista y puede alcanzarse más fácilmente al principio que al final del curso. Dado que lo ideal es iniciar la terapia básica en los tres primeros meses tras la aparición de los síntomas, el diagnóstico precoz es crucial. Al principio de la enfermedad, se necesita mucha experiencia para realizar correctamente el diagnóstico mediante los síntomas típicos, el patrón de afectación articular y los exámenes complementarios (laboratorio con autoanticuerpos, artrosonografía, radiografías).
Enfoques de tratamiento
Medicamentos básicos: Los medicamentos básicos son esenciales para un control adecuado de la actividad de la enfermedad en la mayoría de los casos. A largo plazo, son mucho menos tóxicos que los glucocorticoides, siempre que se utilicen con habilidad. No sólo reducen los síntomas de la inflamación, sino que, en el mejor de los casos, ralentizan y detienen el proceso erosivo-destructivo. Con las sustancias sintéticas convencionales, el efecto suele aparecer con una latencia de unos dos o tres meses.
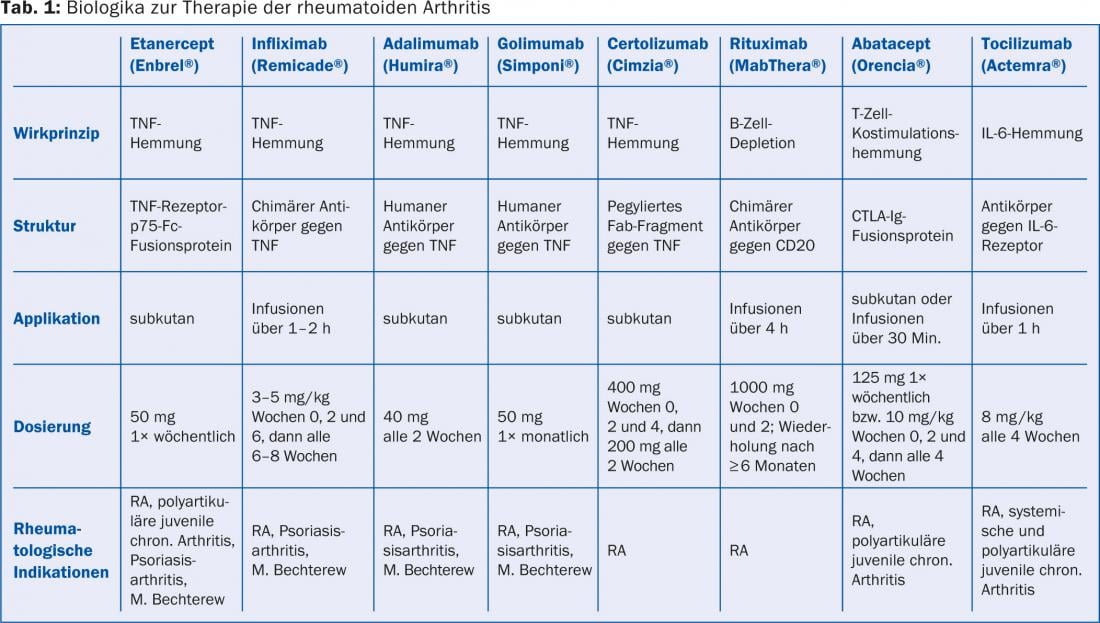
La gama de terapéuticas básicas aumenta constantemente. Los fármacos de base sintética más utilizados son el metotrexato, la leflunomida (Arava® y genéricos), la sulfasalazina (Salazopyrin® ES) y la hidroxicloroquina (Plaquenil®). Recientemente, también está disponible el fármaco sintético selectivo tofacitinib (Xeljanz®), que inhibe las enzimas intracelulares, concretamente las denominadas Janus quinasas. Se utiliza por vía peroral con o sin fármacos básicos convencionales (por ejemplo, metotrexato). Además, están los biológicos (Tabla 1) , que han supuesto una auténtica revolución en el tratamiento de la AR en los últimos 15 años: Hoy en día, se puede encontrar una medicación bien eficaz y tolerable para la mayoría de los pacientes, pero a menudo son necesarias las combinaciones. Hoy en día, lograr la remisión es un objetivo bastante realista.
Adaptar la terapia a las necesidades individuales de los pacientes es todo un reto. Requiere mucha experiencia. Por ello, el tratamiento debe realizarse siempre junto con un especialista en reumatología.
El metotrexato suele ser la primera opción, aunque es mejor administrarlo junto con, por ejemplo, hidroxicloroquina, leflunomida o biológicos (combinaciones de dos fármacos). También son posibles combinaciones de tres o incluso de cuatro. Los diferentes mecanismos de acción de las sustancias individuales consiguen un efecto aditivo y a veces incluso sinérgico, lo que permite mantener la dosis de las sustancias individuales más baja (menos efectos secundarios). Las terapias combinadas requieren mucha experiencia, incluido el seguimiento.
El metotrexato, la leflunomida, el tofacitinib y todos los biológicos tienen un efecto inmunosupresor. Para evitar un aumento excesivo del riesgo de infección, las terapias combinadas no deben contener más de dos de estos inmunosupresores ni más de un biológico. También deben evitarse las dosis elevadas de esteroides. Es esencial instruir al paciente para que informe rápidamente si sospecha síntomas de infección y para que suspenda cualquier biológico. Si una sospecha de infección se confirma por un aumento de la PCR, es aconsejable la hospitalización inmediata si el foco de la infección sigue sin estar claro o se requiere terapia antibiótica parenteral o monitorización.
Los biológicos intervienen específicamente en el proceso inflamatorio a nivel molecular. Los posibles tratamientos incluyen la inhibición del TNF (inhibidores del TNF) o de la coestimulación de las células T (Abatacept), la reducción de la actividad de la interleucina-6 (Tocilizumab) y el agotamiento de las células B (Rituximab). La experiencia más larga ha sido con los inhibidores del TNF. Clínicamente, son sólo marginalmente mejores que el metotrexato en monoterapia, pero su inicio de acción es mucho más rápido: la actividad inflamatoria sistémica (humoral) se suprime en sólo dos días, lo que a menudo se manifiesta en una mejora brusca de los síntomas generales (fatiga, agotamiento e inapetencia).
El efecto antierosivo de los inhibidores del TNF es claramente superior al del metotrexato. También pueden combinarse muy bien con fármacos básicos sintéticos y especialmente con metotrexato, lo que por término medio conduce a un efecto clínico y antierosivo aún mejor.
Los inhibidores del TNF se inyectan por vía subcutánea o se infunden por vía intravenosa. En la mayoría de los casos se toleran bien. Los efectos secundarios más importantes incluyen reacciones cutáneas en el lugar de la inyección o reacciones a la infusión. El riesgo de infección se duplica aproximadamente bajo la inhibición del TNF, y es posible que se produzcan infecciones oportunistas, especialmente con patógenos intracelulares. Dado que puede producirse una reactivación de la tuberculosis, es necesario un cribado previo de la tuberculosis. Las vacunas antineumocócica y anual contra la gripe son útiles. Los posibles lugares de entrada como la periodontitis o las lesiones cutáneas (también micosis) deben eliminarse antes de iniciar la terapia.
Tras el fracaso de la terapia básica convencional, también pueden considerarse el abatacept y el tocilizumab en lugar de los inhibidores del TNF. Otra indicación de estas dos sustancias, así como del rituximab, es el efecto insuficiente de la terapia anti-TNF. Abatacept tiene un perfil de tolerabilidad excelente. El tocilizumab es el que más suprime la actividad inflamatoria sistémica (humoral) de todos los biológicos. El rituximab tiene la ventaja de que sus ciclos de tratamiento no necesitan ser más frecuentes que seis meses, y funciona mejor en pacientes positivos al factor reumatoide y a los anticuerpos anti-CCP. En el caso del abatacept, el tocilizumab y el rituximab, se aplican precauciones similares a las de los inhibidores del TNF, pero las infecciones oportunistas son menos frecuentes. A tener en cuenta: Un aumento de la PCR relacionado con la infección puede ser inhibido por el tocilizumab (subestimación de la gravedad de la infección por CAVE).
Los productos biológicos son caros debido a su compleja producción, por lo que sólo se aprueban si una terapia previa con sustancias convencionales ha resultado insuficiente. Debe obtenerse previamente una aprobación de los costes por parte de la compañía de seguros médicos.
Glucocorticoides: Los corticoides sólo están indicados como puente a corto plazo hasta el inicio de la acción de los fármacos básicos y para el uso a largo plazo a dosis bajas (por ejemplo, prednisona ≤ 7,5 mg/día) si la eficacia de los fármacos básicos es insuficiente. Recientemente se ha comercializado una forma de prednisona de liberación sostenida (Lodotra®). Se toma antes de acostarse y libera la prednisona con un retraso de varias horas, de modo que ya es plenamente eficaz al levantarse por la mañana. El rápido y fuerte efecto antiinflamatorio tienta a las personas a utilizar glucocorticoides en dosis más altas durante periodos más largos. Sin embargo, la monoterapia con glucocorticoides está obsoleta hoy en día, ya que su uso a largo plazo en dosis más elevadas se asocia a una toxicidad grave (por ejemplo, osteoporosis). Si las articulaciones individuales son dominantes, las inyecciones intraarticulares de esteroides son apropiadas.
Seguimiento para la optimización de la terapia
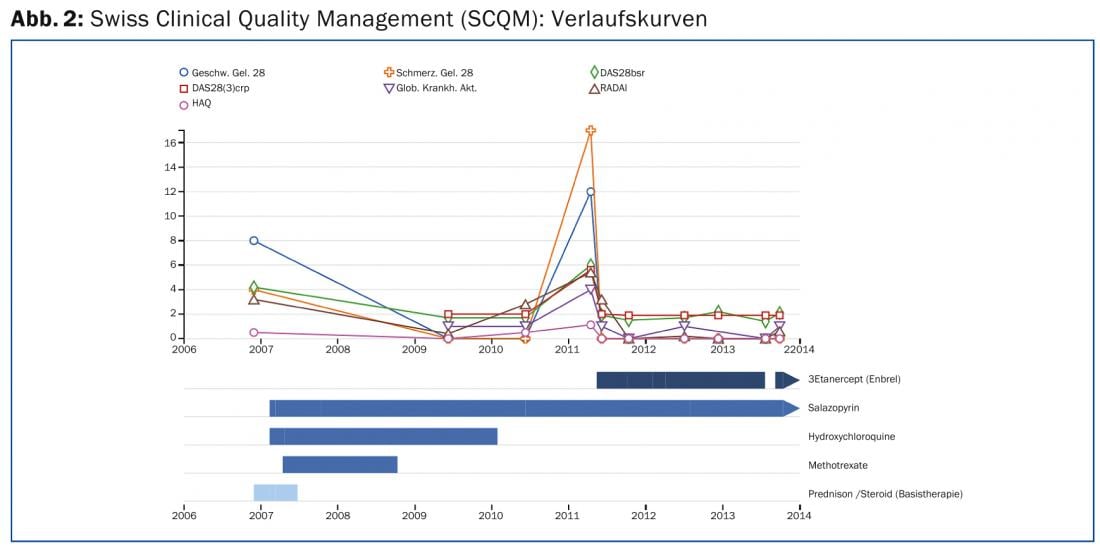
En cualquier caso, es necesario supervisar y ajustar continuamente la medicación junto con un especialista en reumatología, lo que se hace mejor en el marco de una gestión de calidad. En Suiza, el registro SCQM (Swiss Clinical Quality Management in Rheumatic Diseases) está disponible para este fin (www.scqm.ch). Como sistema de mejora de la medición, el SCQM es muy utilizable en la práctica y proporciona valiosos datos de registro de la “vida real”. Mediante cuestionarios, que el paciente y el reumatólogo rellenan regularmente en internet o en papel, se puede registrar de forma estandarizada el curso de la actividad inflamatoria, el daño articular y los efectos de la enfermedad. Los rayos X y las pruebas de laboratorio también forman parte de la evaluación. Las evaluaciones centralizadas permiten optimizar continuamente la terapia (Fig. 2) . Las directrices de la Sociedad Suiza de Reumatología (www.rheuma-net.ch/Richtlinien) ofrecen un resumen de las medidas de seguimiento necesarias para cada uno de los medicamentos básicos.
Comorbilidades
La osteoporosis y la arteriosclerosis son las enfermedades concomitantes más importantes. Los bifosfonatos ya se utilizan bajo tratamiento continuo con esteroides cuando existe osteopenia de moderada a grave, es decir, no sólo cuando hay indicios de osteoporosis (recomendaciones “Osteoporosis por esteroides” en www.rheuma-net.ch/Richtlinien). En la AR, se produce una aceleración de la arteriosclerosis. Los episodios cardiovasculares se producen aproximadamente el doble de veces que en la población normal, por lo que es necesario centrarse en los factores de riesgo (diabetes, tabaquismo, hipertensión e hipercolesterolemia) y combatirlos de forma agresiva.
Dr. Adrian Forster
Literatura:
- Schneider M, Krüger K: Artritis reumatoide: diagnóstico precoz y tratamiento de la enfermedad. Dtsch Ärztebl Int 2013; 110: 477-484.
- Smolen JS, et al: Recomendaciones de la EULAR para el tratamiento de la artritis reumatoide con fármacos antirreumáticos modificadores de la enfermedad sintéticos y biológicos: actualización de 2013. Ann Rheum Dis 2014; 73: 492-509.
- Bykerk VP, Schoels MM: Estrategias de tratamiento para la artritis reumatoide temprana. Curr Opin Rheumatol 2013; 25: 375-383.
- Gramling A, O’Dell JR: Tratamiento inicial de la artritis reumatoide. Rheum Dis Clin North Am 2012; 38: 311-325.
CONCLUSIÓN PARA LA PRÁCTICA
- Iniciar la terapia básica lo antes posible es fundamental para el pronóstico. El objetivo del tratamiento es la remisión.
- Si los fármacos básicos convencionales no son suficientemente eficaces, están indicados los biológicos o el tofacitinib.
- La monoterapia con esteroides está descartada.
- Es crucial que el riesgo de enfermedades concomitantes como la osteoporosis o la arteriosclerosis se detecte y reduzca en una fase temprana.
A RETENIR
- Un tratamiento de base instaurado lo antes posible es crucial para el pronóstico. El objetivo del tratamiento es la remisión.
- Si los medicamentos de base clásicos no son suficientemente eficaces, se indican los agentes biológicos o el tofacitinib.
- La monothérapie par des stéroïdes n’est plus d’actualité.
- Es crucial evaluar y reducir el riesgo de comorbilidades como la osteoporosis o la artritis.
PRÁCTICA GP 2014; 9(4): 12-15