La infección del revestimiento del estómago por la bacteria Helicobacter provoca inflamación estomacal y también aumenta el riesgo de cáncer de estómago. Un equipo de investigación de la Charité – Universitätsmedizin de Berlín y del Centro Max Delbrück de Medicina Molecular de la Asociación Helmholtz (MDC) ha logrado ahora dilucidar los cambios característicos de las glándulas gástricas en el curso de una infección. Los científicos han encontrado un mecanismo desconocido hasta ahora que limita la división celular en los tejidos sanos y protege así contra el desarrollo del cáncer. Sin embargo, una infección estomacal anula esto, de modo que las células pueden crecer sin control.
La colonización del estómago por Helicobacter pylori se produce en aproximadamente la mitad de la humanidad en todo el mundo. Esto la convierte en una de las infecciones bacterianas crónicas más comunes. Como resultado, puede desarrollarse una inflamación del estómago o un cáncer de estómago. Debido al contacto constante con el ácido gástrico, el revestimiento sano del estómago se renueva completamente en pocas semanas, mientras que su estructura y composición permanecen siempre inalteradas. “Hasta ahora se suponía que una infección por Helicobacter daña directamente las células glandulares de la mucosa gástrica”, explica el Prof. Dr. Michael Sigal, jefe del grupo de investigación Emmy Noether de la Clínica Médica Charité, especializado en hepatología y gastroenterología, y del Instituto de Biología de Sistemas Médicos de Berlín (BIMSB), que forma parte del Centro Max Delbrück de Medicina Molecular de la Asociación Helmholtz (MDC). “Nuestro equipo ha descubierto ahora que las complejas interacciones de diferentes células y señales que garantizan la estabilidad de los tejidos se ven alteradas por la infección”.
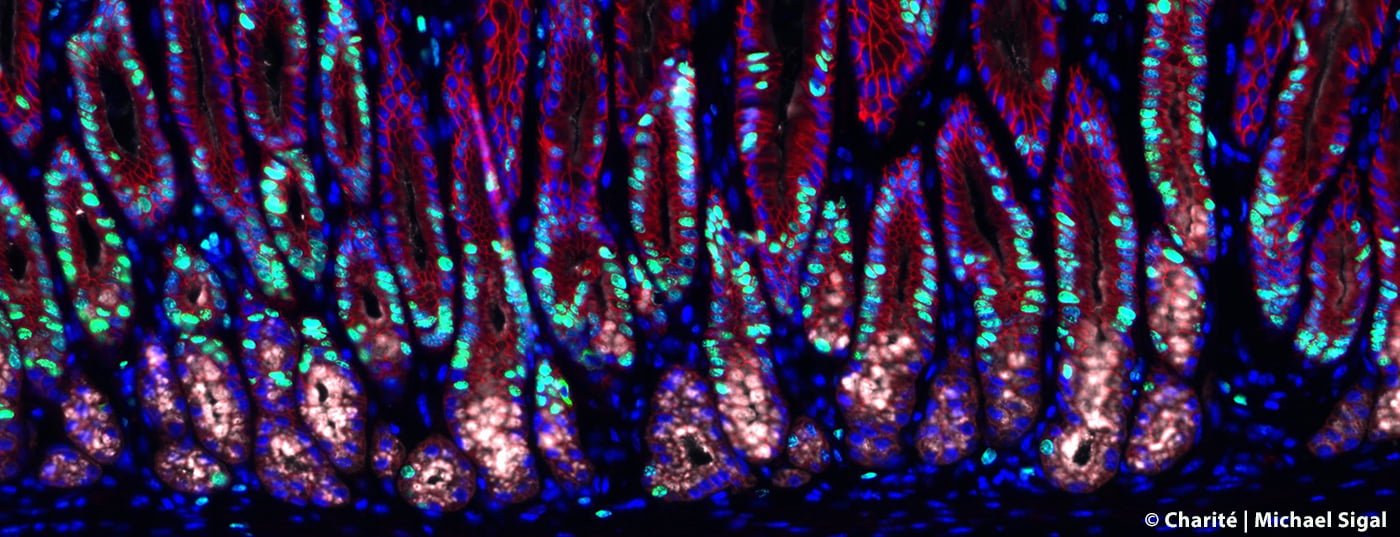
Para rastrear los cambios en las glándulas gástricas causados por la infección por Helicobacter, el equipo de investigación, junto con científicos del Instituto Max Planck de Biología de las Infecciones, utilizó complejos modelos de ratón en los que se pueden visualizar, aislar y estudiar en detalle células específicas de las glándulas gástricas mediante tecnologías de vanguardia como la obtención de imágenes y la secuenciación unicelular en tejidos. Además, desarrollaron microestructuras especiales similares a órganos -los llamados organoides- en el laboratorio para poder limitar el uso de modelos animales. Con la ayuda de estos diminutos estómagos en miniatura, pudieron recrear muchas de las propiedades de las glándulas e investigar la influencia de diversas señales sobre las células madre allí presentes, que pueden dar lugar a diferentes tipos celulares.
“Hemos descubierto que las llamadas células estromales que rodean las glándulas no son -como se pensaba anteriormente- las únicas responsables de la estabilidad mecánica. También producen sustancias mensajeras que tienen una influencia significativa en el comportamiento de las glándulas”, describe el Prof. Sigal. Estas sustancias mensajeras también incluyen la “proteína morfogenética ósea” (BMP), que es importante para el desarrollo de los tejidos. Los investigadores pudieron demostrar que las células estromales que rodean la base de la glándula suprimen continuamente la vía de señalización de las BMP y estimulan así la división de las células madre allí presentes. Por el contrario, las células estromales de la punta de la glándula activan la vía de señalización e impiden así la división celular en esa zona. Esta influencia del entorno es la base de la estructura estable de la glándula. La infección por Helicobacter provoca la liberación de sustancias inflamatorias como el interferón-gamma (IFN-γ). En el curso de esta reacción inflamatoria, ahora se producen más sustancias mensajeras que estimulan la división celular de las células madre de las glándulas. Esto acaba provocando lo que se denomina hiperplasia, es decir, el tejido se agranda y pueden desarrollarse lesiones precancerosas.
“Nuestros hallazgos demuestran que la infección y la inflamación asociada tienen muchos más efectos en los tejidos de lo que se pensaba: las sustancias inflamatorias clásicas como el IFN-γ no sólo tienen un efecto antimicrobiano directo, sino que también influyen en la división celular y en el comportamiento de las células madre de los tejidos. En caso de daño tisular, la rápida división celular puede ser muy útil para permitir una rápida cicatrización. Sin embargo, en el caso de una inflamación crónica en el curso de una infección por Helicobacter, podría favorecer el desarrollo de precursores de cáncer”, resume el Prof. Sigal. Las vías de señalización en la interacción entre el sistema inmunitario y las células madre, que también podrían ser importantes para otros órganos además del estómago, representan así un punto de partida para nuevas terapias, tanto en la prevención del cáncer como en la medicina regenerativa.
Fuente original:
Kapalczynska M, et al.: Schmidt F, et al.: El bucle de avance de las BMP promueve la diferenciación terminal en las glándulas gástricas y se interrumpe por la inflamación impulsada por H. pylori. Nature Communication 2022; doi: 10.1038/s41467-022-29176-w.