Aunque muchas personas de entre 60 y 80 años padecen hiperplasia prostática, sólo alrededor del 40% de ellas muestran síntomas que incluyen micciones obstructivas e irritativas. El siguiente artículo analiza qué exploraciones son posibles y útiles en la consulta del médico de cabecera y cuándo debe consultarse a un urólogo. Además, analiza las ventajas e inconvenientes de los procedimientos terapéuticos medicinales, intervencionistas y quirúrgicos. En este caso, la enucleación de la próstata con láser de holmio en particular muestra buenos resultados en órganos grandes.
La hiperplasia de próstata es un problema antiguo. En la antigua Grecia, Hipócrates de Kos ya distinguía entre disuria, estranguria e ischuria. Las primeras sondas, entonces todavía de bronce, datan del año 1000 a.C. se han descrito en Egipto.
El juramento hipocrático de no realizar intervenciones quirúrgicas y la falta de acceso a estudios anatómicos mediante disecciones de cadáveres hacen necesaria una primera descripción anatómica de la próstata por Herófilo de Calcedonia sólo hacia el año 300 a.C.
El análisis de orina según Galenos de Pérgamo (hacia 131 a 201 d.C.) en función de la densidad, el color, el olor, el sabor y el sedimento en combinación con los síntomas y el sexo del paciente se conoce hasta el siglo XVII . Estándar.
No fue hasta que el fundador de la patología Giovanni Morgagni (1683-1771) describió la anatomía y la patología del tracto urogenital y, en este contexto, la hiperplasia prostática en su obra en cinco volúmenes “Vom Sitz und den Ursachen der Krankenheiten” (De sedibus et causis morborum).
La evolución demográfica, así como una mayor conciencia corporal con escasa disposición al sufrimiento, hacen de la hiperplasia de próstata un problema que afecta al 80% de los hombres de 60 a 80 años. Sin embargo, sólo alrededor del 40% de estos pacientes son sintomáticos.
Etiología y fisiopatología
Los carcinomas de próstata se desarrollan en un 70% en la cápsula prostática, en un 10% en la zona central y en un 20% en la zona de transición entre ambas. La hiperplasia prostática benigna (HPB) también se desarrolla en esta zona de transición y en las glándulas periuretrales. Macroscópicamente, a veces se distingue entre una configuración bilobular (sólo lóbulos laterales) y trilobular (lóbulos laterales y lóbulos medios).
Histológicamente, se distingue entre hiperplasia glandular (adenoma) e hiperplasia fibromuscular (estroma). El término hiperplasia es sólo parcialmente correcto, ya que se trata de una verdadera proliferación numérica de células. Hasta la fecha se desconoce la génesis definitiva de la HBP. Se discuten los cambios hormonales en la relación estrógeno/testosterona en la vejez.
Existen diferencias étnicas y geográficas en la frecuencia del tratamiento: los asiáticos, por ejemplo, tienen un riesgo significativamente menor de necesitar cirugía para la HBP en comparación con los estadounidenses blancos y negros. Se analizan la hiperalimentación (consumo de carne y grasa, así como la inactividad física), el estreñimiento y las diferencias en la actividad sexual. Los hermanos varones de pacientes con HBP clínica tienen un riesgo seis veces mayor de desarrollar también HBP.
Sintomatología
Los síntomas clínicos de la HBP no se correlacionan con las condiciones patoanatómicas. En general, hay que distinguir entre trastornos obstructivos e irritativos del vaciado de la vejiga.
Los trastornos obstructivos de la micción incluyen:
- chorro de orina debilitado
- micción prolongada
- Llovizna
- Sensación de orina residual.
- Los trastornos irritativos de la micción incluyen:
- Pollakiuria
- Nocturia
- Dsyurie
- Urgencia (síntomas de incontinencia de urgencia).
La hipertrofia del trusor terminal de la vejiga debida a presiones de micción elevadas puede provocar polaquiuria, al igual que el aumento de la formación de orina residual con la correspondiente disminución del volumen vesical efectivamente utilizable. Si los músculos de la vejiga se agotan, puede desarrollarse una incontinencia por rebosamiento (ischuria paradoxa) o una retención urinaria. Los exámenes ecográficos están indicados en consecuencia. La puesta en escena según Alken se muestra en el recuadro.
Las infecciones urinarias recurrentes, la epididimitis o la hematuria deben remitirse para una evaluación urológica, ya que pueden ser síntomas de aumento de la presión de micción intravesical con formación consecutiva de orina residual, hemorragia varicosa prostática e inflamación ascendente.
Del mismo modo, tiene sentido remitir a los pacientes para su examen a tiempo si existe alguna sospecha, ya que las molestias irritativas en particular pueden persistir durante mucho tiempo si se retrasa el diagnóstico y la terapia, incluso después de una operación.
Exámenes del médico de familia
Historial miccional preciso: Debe tener en cuenta los posibles efectos de la administración de diuréticos o de la insuficiencia cardiaca (nicturia cardiaca) sobre el comportamiento miccional. Para una diferenciación exacta, se puede llevar un registro de medición de la bebida durante varios días.
Tacto rectal (TDR): Es la medida diagnóstica más sencilla con buena información sobre el tamaño y el estado (dureza, nódulos, delimitación, simetría) de la próstata. La DRU también proporciona una buena información sobre posibles hemorroides o tumores rectales y ofrece una evaluación orientativa de un trastorno neurogénico de la vejiga, por ejemplo, a través del tono del esfínter anal y el reflejo bulbocavernoso, así como de la sensibilidad perianal.
Laboratorio: estipe de orina y creatinina sérica para excluir infección e insuficiencia postrenal.
PSA: El PSA forma parte integrante del diagnóstico rutinario de los pacientes con HBP. Como proteína, la expresan las células epiteliales benignas y malignas de la próstata, por lo que no es un marcador tumoral sino tisular. Los puntos débiles de la determinación del PSA son conocidos, pero sin embargo es indispensable como indicador de una biopsia de próstata necesaria para excluir una génesis maligna de las molestias miccionales. Por lo tanto, a partir de un PSA de 3,0 ng/ml y una relación PSA libre/total ≤12%, debe asignarse a los pacientes la determinación del tamaño de la próstata mediante ecografía transrectal y correlacionar el valor del PSA con éste. Esto se hace con la ayuda de un cálculo del riesgo prostático.
El Centro de Próstata de Aarau, en colaboración con el Hospital Mount Sinai de Toronto, está llevando a cabo una intensa investigación sobre nuevos marcadores tumorales más específicos para el cáncer.
Exámenes complementarios del urólogo
Ecografía: La orina residual no debe superar el 10-20% del volumen de micción. Ecografía de los riñones para excluir un sistema hueco dilatado.
TRUS (ecografía transrectal): Para las próstatas grandes en DRU, porque a partir de un tamaño de adenoma de 60- 70 cc, la TUR-P ya no es la terapia de elección, sino la enucleación de la próstata con láser de holmio (HoLEP).
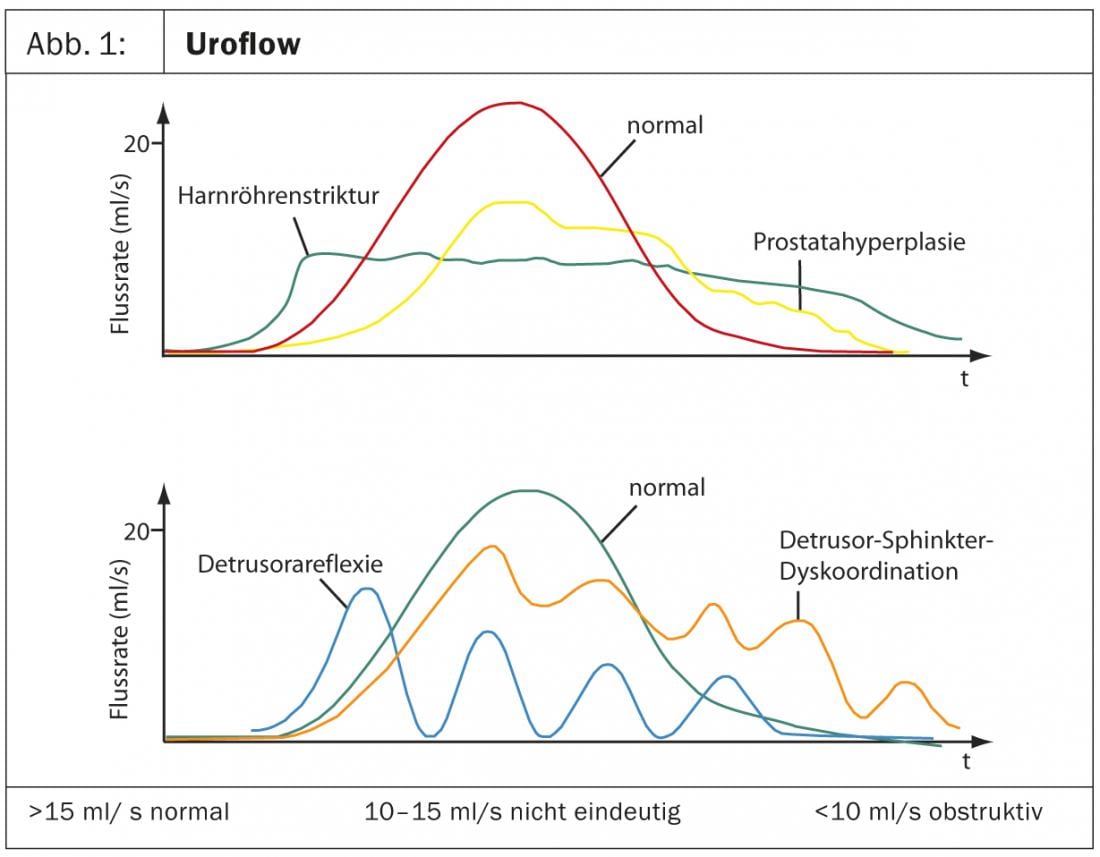
Uroflujo: Tiene sentido pedir a los pacientes que acudan al urólogo con la vejiga llena cuando sean remitidos, para poder realizar primero un uroflujo. Un criterio importante es el flujo máximo, que debe ser superior a 15 ml/s. La representación gráfica del caudal a lo largo del tiempo permite realizar diagnósticos diferenciales de trastornos del vaciado vesical, además de la sospecha de HBP (Fig. 1) . Si es necesario, un uroflujo llamativo con sospecha de componente neurogénico/disinergia del detrusor-esfínter debe ir seguido de una cistomanometría/videourodinámica.
Uretrocistoscopia: Además de las estenosis uretrales, también pueden diagnosticarse hiperplasia prostática bi o trilobular, esclerosis del cuello vesical, trabecularización de la vejiga o divertículos. Una gran ventaja es la posibilidad técnica de mostrar directamente al paciente el problema fisiopatológico de sus síntomas a través de un monitor de paciente e ilustrar la indicación quirúrgica y anatómica.
Tratamiento farmacológico
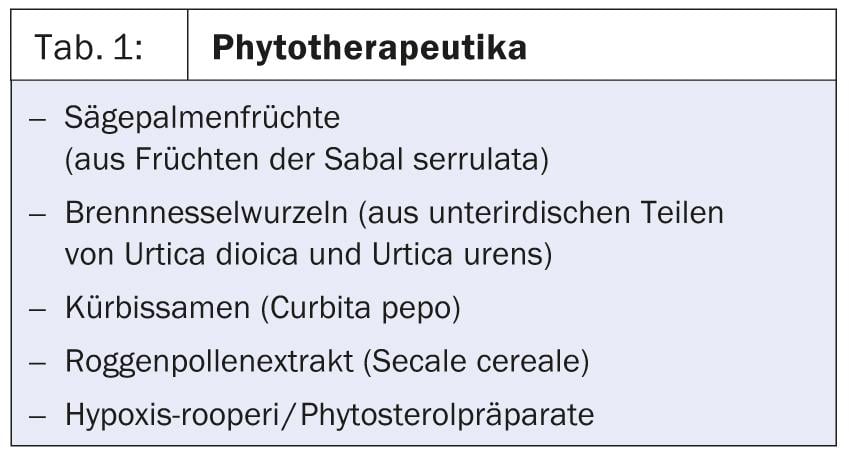
Fitoterapéuticos (Tab. 1): Los ingredientes de los fitofármacos responsables de los efectos terapéuticos, así como sus principios de acción, no han sido aclarados sin lugar a dudas. Así pues, el valor de los extractos vegetales sigue siendo controvertido. Se sospecha de un efecto placebo significativo, ya que los síntomas de micción mejoraron en algunos estudios, pero los parámetros medibles como el flujo máximo y la orina residual no mejoraron significativamente. Si los síntomas son leves y no hay orina residual, no está de más intentarlo. A pesar de la falta de criterios objetivos, a menudo es cierto que quien cura siempre tiene razón.
Bloqueantes de los receptores α: los receptores α1 y α1a están presentes tanto en el cuello de la vejiga como en la próstata, y su activación provoca la contracción del músculo liso. Al bloquear estos receptores, se puede relajar el componente dinámico de la obstrucción. El medicamento está indicado al inicio de la HBP y con síntomas poco pronunciados, especialmente irritativos. La duración de la acción varía, al igual que los efectos secundarios. La eficacia de la medicación requiere el control del flujo y de la orina residual. El fármaco tamsulosina tiene la mayor selectividad del receptor α1a y, por tanto, los mejores resultados clínicos, pero un ensayo terapéutico con alfuzosina o terazusina está igualmente justificado.
Los efectos secundarios comunicados con frecuencia son ortostatismo, mareos y eyaculación retrógrada, y ocasionalmente pérdida de libido/potencia.
Modulación hormonal: La testosterona es una prohormona en la próstata y es convertida por la 5α-reductasa en la forma activa real dihidrotestosterona, que se une al receptor de andrógenos. Los inhibidores de la 5α-reductasa inhiben la influencia proliferativa de la DHT. Por ejemplo, puede conseguirse una reducción de volumen del 20-30% con finasterida tomada durante meses (Höfner et al. 2000). Sin embargo, principalmente se alivian los síntomas obstructivos de la HBP, y sólo se produjo una mejora de 1,4-1,9 ml/s en el flujo urinario máximo en comparación con el placebo. Los preparados combinados de tamsulosina y dutasterida en una cápsula se han publicitado más intensamente en los últimos tiempos, pero la combinación de principios activos no es nada nuevo en sí misma. Resultados más recientes (estudio Combat) justifican un ensayo también con volúmenes prostáticos más pequeños (entre 30-50 ml), pero el efecto es menor en este caso. Los inhibidores de la 5α-reductasa tienen como efecto secundario más frecuente la disfunción eréctil, así como la pérdida de libido en un 5-15% y la reducción del volumen de eyaculación.
El efecto completo puede esperarse al cabo de 6-12 meses. Los pacientes con dolencias avanzadas a menudo no pueden esperar ese tiempo.
Los inhibidores de la 5α-reductasa conducen a una reducción del PSA de alrededor del 50%. Un paciente en tratamiento con un inhibidor de la 5α-reductasa tiene un valor umbral de PSA correspondiente no de 3, sino de 1,5 ug/l, por lo que debe someterse antes al cribado del carcinoma.

Procedimientos de intervención
Incrustación de endoprótesis: Incrustación de aleaciones metálicas recubiertas de platino, titanio o polietileno. La ventaja es que puede utilizarse en casos de multimorbilidad. El inconveniente, aparte de la necesidad de cambiar algunos preparados, es la frecuencia de las infecciones y la sensación de necesidad constante de orinar en un gran número de pacientes.
Procedimientos térmicos: Con la TUMT de alta energía (termoterapia transuretral microvellar inducida), los síntomas deberían alcanzar los resultados de la RTU-P en un año, pero esta terapia es significativamente peor en cuanto a los resultados del flujo urinario. En la TUNA (ablación transuretral de la próstata con aguja), la termonecrosis se produce en el cuerpo de la glándula mediante la generación de calor intersticial (aprox. 90°C). Esto provoca una mejora significativa de los síntomas de la HBP, pero tiene malos resultados en cuanto al flujo urinario y requiere tratamientos repetidos en el 42% de los casos.
Todos estos no son procedimientos estándar y no están recomendados en las directrices nacionales e internacionales.
Procedimientos operativos
RTU-P: La norma de referencia ha sido durante mucho tiempo la resección transuretral de la próstata (RTU-P). Diferentes fabricantes tienen buenos sistemas en el mercado. Las modulaciones de la corriente en intensidad o frecuencia, así como la distinción entre sistema monopolar (retorno de la corriente a través de un electrodo adhesivo en el muslo) o bipolar (retorno de la corriente en el propio dispositivo transuretral) no suponen una gran diferencia en el resultado funcional final. La ventaja de la resección bipolar se observa en la posibilidad de utilizar soluciones salinas fisiológicas como medio de irrigación y da lugar a menos desplazamientos electrolíticos debidos a la reabsorción del agua de irrigación. Se calcula que la pérdida media de sangre intraoperatoria es de unos 500 ml, las tasas de transfusión son del 0-20%, pero de facto ocurren muy raramente en nuestra clínica. Marcoumar®, Xarelto® o Plavix® deben suspenderse de antemano. pasarse a heparina de bajo peso molecular por vía subcutánea, el AAS no es un obstáculo.
Vaporización con láser KTP: La llamada vaporización con láser KTP (láser de luz verde) vaporiza el tejido prostático sobrante con luz láser en el rango visible de 532 nm (verde). La ventaja es que la operación está casi exenta de hemorragias, incluso bajo anticoagulación, ya que los vasos sanguíneos pueden coagularse directamente. Con potentes láseres de 120 W, la eficacia es comparable a la de la TUR-P en >0,5 g/min. La desventaja es que no se dispone de histología debido a la vaporización y, en consecuencia, no se detectan las incidencias de carcinoma. La tasa de reoperación debida a masas detríticas obstructivas es del 17%. Además, a menudo se produce una macrohematuria retardada en el curso de la descamación.
Enucleación prostática con láser de holmio (HoLEP): La RTU-P ya no debe realizarse en adenomas grandes debido a la carga de volumen que supone para la circulación la reabsorción del líquido de irrigación. En muchos lugares, la enucleación transabdominal y transvesical de un adenoma (análoga a la de Freyer) o la enucleación transabdominal y extravesical de un adenoma (análoga a la de Milin) es el procedimiento habitual para los adenomas con un tamaño de 100 g o más. Desde hace unos ocho años se dispone de un nuevo procedimiento láser en forma de enucleación prostática con láser de holmio, o HoLEP por sus siglas en inglés. Muestra resultados igualmente excelentes para todos los tamaños de próstata, pero sus ventajas entran realmente en juego a partir de un tamaño de órgano de >50-60 g. Los lóbulos laterales obstructivos ± lóbulos medios se extirpan completamente en bloque por vía transuretral y se introducen en la vejiga. La base de resección se coagula directamente con el láser de holmio, por lo que apenas hay pérdida de sangre y tampoco se produce una reabsorción significativa. A continuación, los bloques de tejido enucleado se extraen de la vejiga mediante un morcelador y están disponibles para el examen histológico necesario.
Debido a la extirpación completa del adenoma, los resultados funcionales a largo plazo son los mismos que con la cirugía abierta y, con una tasa de reintervención de <1% en un plazo de siete años, significativamente mejores que con la RTU-P convencional (aprox. 15%).
El enfoque mínimamente invasivo reduce el tiempo de hospitalización en unos cinco días, con una pérdida de sangre y unas necesidades de medicación significativamente menores, por lo que desde 2011 ya no se realizan enucleaciones abiertas de adenomas en el Centro de Próstata.
CONCLUSIÓN PARA LA PRÁCTICA
- Hasta el 80% de las personas de 60-80 años padecen HBP, pero sólo el 40% son sintomáticas.
- Los pacientes deben recibir una aclaración urológica en una fase temprana.
- La medicación mejora los síntomas más que los parámetros medibles.
- La RTUP sigue siendo la norma de referencia.
- La enucleación de la próstata con láser de holmio se está convirtiendo en la norma de oro, sobre todo para órganos grandes.
Bibliografía con el autor
PRÁCTICA GP 2013; 8(11): 12-16