Las estrategias terapéuticas actuales para la enfermedad inflamatoria intestinal (EII) han alcanzado una meseta en cuanto a las tasas de respuesta y/o remisión logradas con un único agente terapéutico. En consecuencia, la terapia combinada avanzada (TCA) ha surgido como un nuevo concepto de tratamiento. Un grupo de investigadores analizó estudios recientes en los que se comparaban las TCA con las monoterapias.
Las terapias biológicas se han convertido en el tratamiento de referencia de la enfermedad inflamatoria intestinal (EII) activa de moderada a grave, incluidas la enfermedad de Crohn (EC) y la colitis ulcerosa (CU). A pesar de estos avances, los enfoques terapéuticos actuales para la EII se han estancado en términos de tasas de respuesta y/o remisión. El arsenal existente de terapias avanzadas da como resultado unas tasas de remisión clínica global de sólo alrededor del 50%. Además, aproximadamente el 50% de los pacientes que responden inicialmente a la terapia biológica o de moléculas pequeñas pierden esta respuesta con el tiempo. En consecuencia, los pacientes con EII que no responden o han perdido la respuesta a una terapia biológica concreta deben cambiar a una molécula diferente, lo que reduce sus posibilidades de lograr la remisión de la enfermedad a largo plazo.
El novedoso enfoque de la terapia combinada avanzada (TCA ) ha surgido como una prometedora estrategia de tratamiento para la EII. Implica el uso de dos terapias dirigidas diferentes, biológicas o de moléculas pequeñas, con el objetivo principal de superar la meseta terapéutica. Recientemente se han obtenido datos sobre el ACT a partir del ensayo aleatorizado y controlado VEGA: El Dr. Panu Wetwittayakhlang, del Departamento de Gastroenterología y Hepatología de la Universidad Príncipe de Songkla, Hat Yai, Tailandia, y el Dr. Peter L. Lakatos, del Departamento de Gastroenterología y Hepatología del Centro de Salud de la Universidad McGill, Montreal, revisaron las pruebas actuales (a febrero de 2024) sobre el ACT y su impacto en la superación del techo terapéutico en el tratamiento de la EII [1].
La combinación a corto plazo de dos biológicos puede ayudar a los pacientes con CU a lograr un mejor control de la enfermedad
El ECA de fase 2a VEGA investigó la eficacia de la terapia de inducción combinada con el inhibidor selectivo de la interleucina (IL)-23 guselkumab y el inhibidor del TNF-alfa golimumab en comparación con la monoterapia con guselkumab o golimumab en pacientes con CU de moderada a gravemente activa. Un total de 214 pacientes que no habían respondido a la terapia anti-TNF y no respondieron o no toleraron la terapia convencional fueron asignados aleatoriamente a uno de los siguientes tratamientos:
- Guselkumab 200 mg i.v. en las semanas 0, 4 y 8 (n=71),
- Golimumab 200 mg s.c. en la semana 0, luego 100 mg s.c. en las semanas 2, 6 y 10 (n=72)
- o una combinación de 200 mg de guselkumab i.v. más 200 mg de golimumab s.c. en la semana 0; 100 mg de golimumab s.c. en las semanas 2, 6 y 10 y 200 mg de guselkumab i.v. en las semanas 4 y 8 (n=71).
En la fase de mantenimiento, los pacientes del brazo de combinación pasaron a monoterapia con guselkumab al inicio de la semana 12.
En pacientes con CU no tratados biológicamente, el estudio indica una mayor tasa de remisión clínica y mejoría endoscópica en el brazo de combinación (terapia de inducción con golimumab y guselkumab) frente a las monoterapias con golimumab o guselkumab. Sin embargo, los autores señalan que el estudio VEGA no incluyó a pacientes con CU con exposición previa o fracaso a biológicos anteriores. Por lo tanto, los datos procedentes de ensayos clínicos sobre la eficacia del ACT en pacientes con CU refractarios al tratamiento biológico siguen siendo limitados. Los datos disponibles sobre el ACT en pacientes con enfermedad de Crohn también son limitados, lo que plantea un reto particular en pacientes con enfermedad complicada.
La terapia combinada condujo a la remisión clínica en el 54,5% de los pacientes
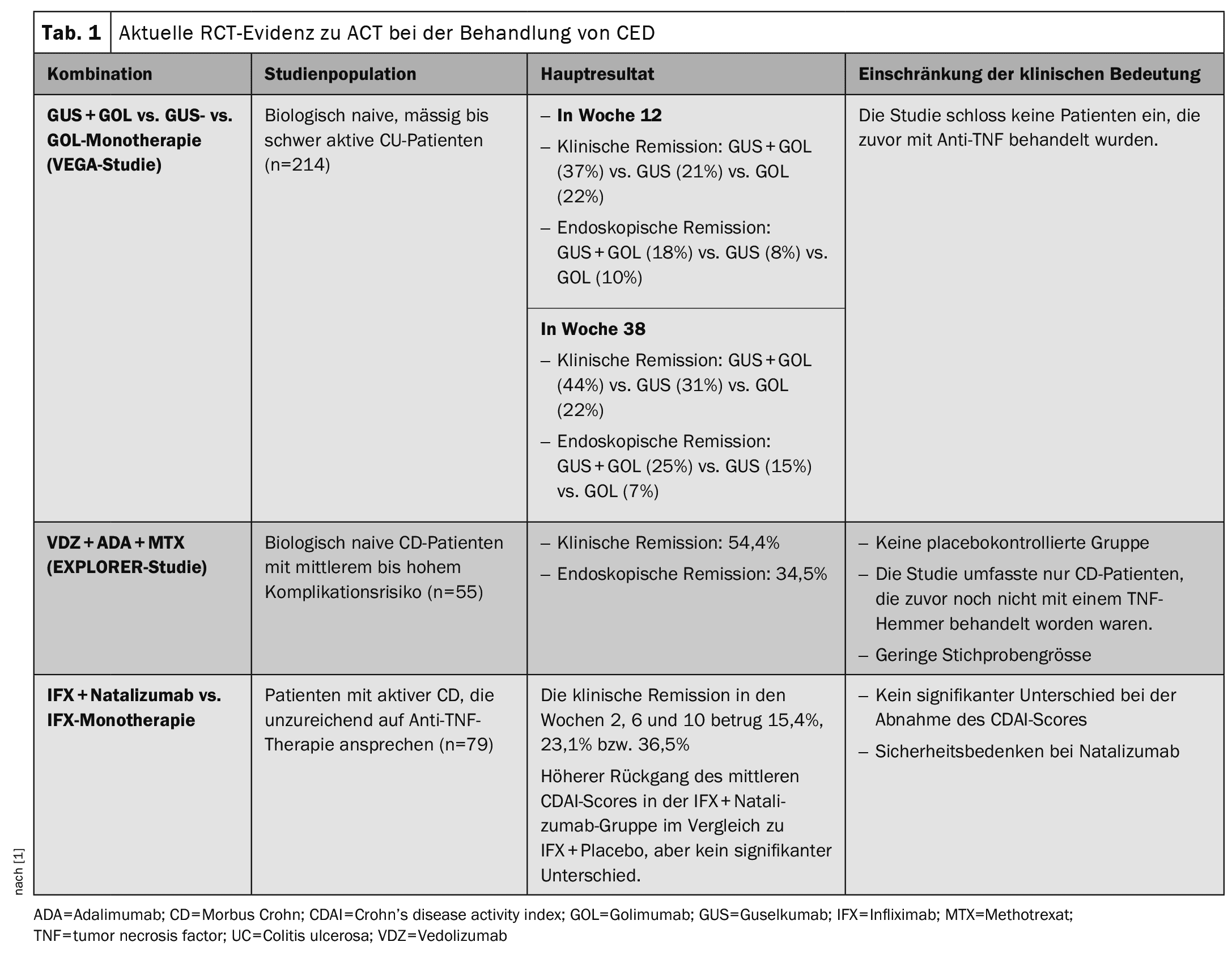
> >El estudio abierto de fase 4 EXPLORER investigó la eficacia de una terapia combinada triple de vedolizumab, adalimumab y metotrexato en pacientes no tratados biológicamente con enfermedad de Crohn (EC) con un riesgo de moderado a alto, determinado por una puntuación endoscópica para EC (SES-CD) 7 (o 4 para la enfermedad ileal aislada). Se consideró que los pacientes elegibles con enfermedad de Crohn tenían un riesgo de complicaciones de medio a alto. Se realizó un análisis provisional de 55 pacientes tratados con la terapia triple (vedolizumab 300 mg i.v. el día 1 y las semanas 2 y 6 y después cada 8 semanas; adalimumab 160 mg s.c. el día 2, 80 mg la semana 2 y después 40 mg cada 2 semanas hasta la semana 26; metotrexato 15 mg por vía oral semanalmente hasta la semana 34). Después de la triple y hasta la semana 34, cada paciente recibió vedolizumab en monoterapia hasta la semana 102. En la semana 26, se observaron respuesta clínica y remisión endoscópica en el 54,4% y el 34,5%, respectivamente. No hubo señales de seguridad asociadas a la terapia triple. Las pruebas actuales de ECA sobre el ACT en el tratamiento de la EII se resumen enla tabla 1 .
El ensayo EXPLORER sugiere la eficacia de una combinación de vedolizumab, adalimumab y metotrexato para mejorar la respuesta endoscópica y la remisión en pacientes con EC no tratados con biológicos y con un riesgo de complicaciones de intermedio a alto. Sin embargo, la falta de un brazo controlado en el estudio impide obtener pruebas claras de la eficacia terapéutica del ACT en la EC, señalaron los doctores Wetwittayakhlang y Lakatos.
Pruebas débiles de estudios en el mundo real
En cuanto a los datos observacionales del mundo real, un gran estudio multicéntrico informó sobre 98 pacientes que iniciaron una terapia combinada para la EII activa (67%), enfermedades inflamatorias inmunomediadas activas (IMID) o manifestaciones extraintestinales (EIM, 22%) o ambas (10%) después de que hubieran fracasado en ellos múltiples biológicos. La actividad de la enfermedad de la EII mejoró clínicamente en el 70% de los pacientes, y en el 81% de los pacientes con IMID/EIM. Otro estudio retrospectivo informó sobre 92 pacientes que recibieron terapia biológica combinada para la EII activa o los EIM. Las combinaciones más comunes fueron vedolizumab y ustekinumab (32%) o vedolizumab y anti-TNF (31%). Las tasas de respuesta clínica a los 3 y 6 meses fueron del 46% y el 34% respectivamente. Un estudio retrospectivo de Glassner et al. examinó a 50 pacientes con EII que fueron tratados con diversas combinaciones de terapias biológicas o de moléculas pequeñas. Aproximadamente el 50% recibió vedolizumab más anti-IL-12 e IL-23 (ustekinumab) por actividad persistente de la enfermedad (n=47) o enfermedad reumatológica o dermatológica concurrente (n=3). Después de 4 meses, un número significativamente mayor de pacientes se encontraba en remisión clínica (50% frente a 14%, p=0,0018) y después de 8 meses en remisión endoscópica (34% frente a 6%, p=0,0039) que al inicio.
Otra serie de casos demostró que la terapia biológica dual era segura y eficaz en 22 pacientes con EC refractaria grave que habían recibido un total de 24 tratamientos biológicos duales tras múltiples terapias biológicas fallidas. Se observó respuesta clínica y remisión clínica en el 50% y el 41% de los pacientes, respectivamente. La mejoría endoscópica y la remisión se observaron en el 43% y el 26%, respectivamente. La presencia de fístula perianal activa disminuyó del 50% al inicio al 33% tras el tratamiento. Asimismo, en dos estudios retrospectivos de cohortes se informó de la eficacia de combinar tofacitinib con otras terapias biológicas.
Un metaanálisis de Alayo et al. evaluó la eficacia del ACT con diferentes regímenes combinados. En los pacientes que recibieron vedolizumab más tofacitinib, las tasas agrupadas de respuesta clínica y remisión fueron del 59,9% (IC del 95%: 37,2-80,8) y del 47,8% (IC del 95%: 19,0-77,4), respectivamente. En el caso de vedolizumab más ustekinumab, las tasas agrupadas de respuesta clínica y remisión fueron del 83,9% (IC del 95%: 66,4-96,8) y del 47,0% (IC del 95%: 14,5-80,7), respectivamente. Los pacientes que recibieron vedolizumab más anti-TNF tuvieron unas tasas conjuntas de respuesta y remisión endoscópica/radiológica del 38,2% (IC 95%: 19,5-58,4) y del 18,0% (IC 95%: 1,6-41,8), respectivamente. Y en los pacientes tratados con tofacitinib más vedolizumab, las tasas correspondientes fueron del 46,2% (IC 95%: 20,4-73,0) y el 24,6% (IC 95%: 6,4-47,6).
Según el Dr. Wetwittayakhlang y el Dr. Lakatos, los estudios observacionales del mundo real son informativos pero dejan abierto si el ACT puede elevar el techo terapéutico en la EII en las complejidades de un entorno clínico real, ya que la mayoría de los pacientes que reciben ACT no han respondido o han respondido inadecuadamente a la terapia biológica. Por lo tanto, deben tenerse en cuenta los datos disponibles más fiables, principalmente los procedentes de un número limitado de ensayos clínicos en los que participaron pacientes con TCA que aún no habían recibido agentes biológicos.
Opción terapéutica prometedora para un control eficaz de la enfermedad
El ACT ha surgido como una nueva estrategia terapéutica potencial destinada a mejorar la eficacia terapéutica y superar la meseta observada con las terapias actualmente disponibles. En pacientes muy seleccionados con un fenotipo de enfermedad de alto riesgo (como los pacientes con una amplia afectación del intestino delgado en la enfermedad de Crohn o los pacientes que no responden a múltiples terapias), el uso del ACT para el control precoz de la enfermedad puede ser útil para prevenir la progresión de la enfermedad y las complicaciones. Durante la fase de inducción, puede utilizarse la coinducción simultánea con una combinación de biológicos o moléculas pequeñas para maximizar el control de la enfermedad mediante efectos sinérgicos. Una vez alcanzada la remisión de la enfermedad, puede utilizarse la monoterapia con uno de los agentes combinados para mantener la remisión de la enfermedad.
Otro aspecto, según los autores, que debe tenerse en cuenta al aplicar la estrategia ACT en la práctica clínica es la posibilidad de que se produzcan cambios en las señales de seguridad con la exposición prolongada a múltiples inmunosupresores. Aunque hasta la fecha no se ha prestado gran atención a los problemas de seguridad, es importante reconocer que los datos disponibles proceden de estudios pequeños con periodos de seguimiento limitados. Por lo tanto, se necesitan más estudios prospectivos de gran tamaño con periodos de seguimiento más largos para comprender plenamente la eficacia y la seguridad de esta estrategia. También persiste la incertidumbre sobre si la combinación debe utilizarse exclusivamente para la fase de inducción o extenderse a la terapia de mantenimiento.
Los resultados actuales, como los del estudio VEGA, muestran que la combinación de biológicos novedosos logra una eficacia terapéutica superior en pacientes biológicamente naïve con CU de moderada a gravemente activa, tanto clínica como endoscópicamente, en comparación con la terapia monobiológica. Sin embargo, los datos suelen ser limitados. De cara al futuro, estudios en curso como los ensayos DUET-CD y DUET-UC (que evalúan la combinación de guselkumab y golimumab en pacientes con EII refractaria) y el ensayo VICTRIVA (que evalúa la combinación de vedolizumab y upadacitinib) prometen aportar datos adicionales sobre la eficacia del ACT en pacientes con enfermedad de Crohn y colitis ulcerosa en los que ha fracasado la terapia biológica, concluyó el Dr. Wetwittayakhlang. Wetwittayakhlang y el Dr. Lakatos.
Literatura:
- Wetwittayakhlang P, Lakatos PL: Terapia combinada avanzada: ¿es la mejor forma de romper el techo terapéutico? Avances terapéuticos en gastroenterología 2024; 17; doi: 10.1177/17562848241272995.
PRÁCTICA DE LA GASTROENTEROLOGÍA 2024; 2(2): 22-23