La fibrilación auricular es un trastorno dinámico del ritmo que requiere aclaraciones y enfoques terapéuticos individuales y amplios. El tratamiento integral de los pacientes con fibrilación auricular se basa en cinco pilares: 1. prevención de eventos tromboembólicos; 2. control de los síntomas; 3. Si es posible, restaure o mantenga el ritmo sinusal; 4. Por lo demás, buen control de la frecuencia; 5. tratamiento de la cardiopatía subyacente y de los factores predisponentes.
La fibrilación auricular afecta al 1-2% de toda la población, lo que la convierte en la arritmia cardiaca más común [1–3]. Debido a la creciente prevalencia de factores de riesgo y enfermedades cardiovasculares, y al aumento de la edad media de la población general, nos enfrentamos a un número cada vez mayor de pacientes con fibrilación auricular en la práctica clínica [1–3]. El tratamiento integral es un reto. Además de mantener la calidad de vida, es importante reducir el riesgo de tromboembolismo y el aumento general del riesgo de morbilidad y mortalidad asociado a la fibrilación auricular [1,2]. Los hallazgos de la investigación epidemiológica y clínica, la llegada de nuevos anticoagulantes orales (“anticoagulantes orales no antagonistas de la vitamina K” (NOAC) y los avances en el campo de la electrofisiología intervencionista han revolucionado el tratamiento de la FA. Este artículo pretende ofrecer una visión general de los principales conceptos y los últimos paradigmas en el tratamiento de la fibrilación auricular.
Aclaraciones iniciales y estratificación del riesgo
Además de una evaluación clínica y de laboratorio, los pacientes con fibrilación auricular recién detectada y documentada electrocardiográficamente también deben ser evaluados mediante ecocardiografía y, si es necesario, un ECG a largo plazo [1,2]. La historia y los hallazgos constituyen la base para clasificar el tipo de fibrilación auricular (paroxística, persistente, de larga persistencia [>1 año] o permanente), graduar los síntomas y evaluar el riesgo de tromboembolia y hemorragia. El proceso de evaluación y tratamiento primario se resume a grandes rasgos en la figura 1. Cabe señalar que la puntuación CHA2DS2-VASc ha sustituido de hecho a la puntuación CHADS2 para el riesgo de ictus [4].

Profilaxis de la tromboembolia en la fibrilación auricular
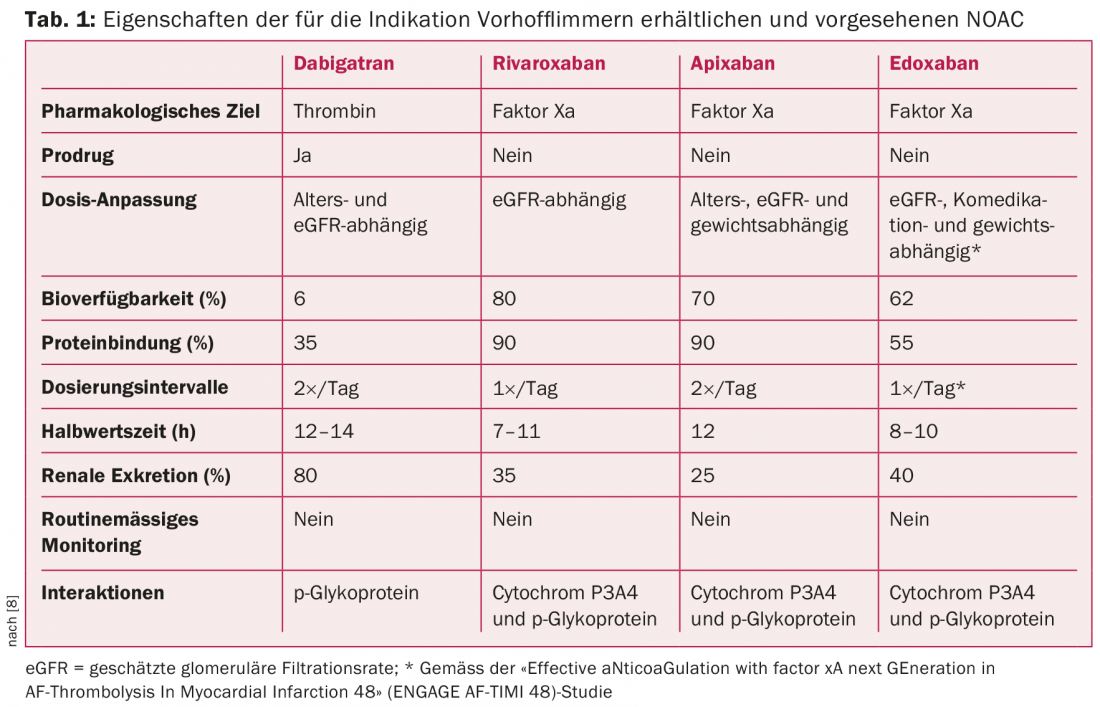
Simultáneamente a la introducción de la puntuación CHA2DS2-VASc, hace unos años se produjo un cambio de paradigma en la anticoagulación para la FA [1,2,4]. Esta reorientación estuvo marcada de forma decisiva por la aparición del NOAC [4,5]. Hasta la fecha, tres NOAC -apixabán, dabigatrán y rivaroxabán (en orden alfabético)- se han establecido en la práctica clínica habitual para la profilaxis de acontecimientos tromboembólicos [4–7]. Con el edoxaban, está a punto de lanzarse un cuarto preparado (nota del editor: ya aprobado) (Tab. 1) [7]. Los NOAC han revolucionado y simplificado la anticoagulación.
Además, se ha redefinido el papel de los antiagregantes plaquetarios para la prevención del ictus en la fibrilación auricular [1,2]. Hoy en día, en general no se recomienda prescribir aspirina para la profilaxis del ictus en pacientes con fibrilación auricular, ya que no garantiza una profilaxis suficiente del tromboembolismo y, al mismo tiempo, aumenta significativamente el riesgo de hemorragia [1,4].
Ensayos aleatorizados muy amplios han demostrado que los NOAC son equivalentes o incluso superiores a los antagonistas de la vitamina K (AVK) en pacientes con FA [1,5–8]. En particular, la superioridad en términos de riesgo de hemorragia intracraneal es una característica importante de los NOAC [1,5–8]. En general, debe tenerse en cuenta que antes de iniciar la terapia anticoagulante, debe evaluarse el riesgo de interacción, hemorragia y complicaciones generales, incluyendo puntuaciones de riesgo (por ejemplo, la puntuación HAS-BLED) si es necesario. En vista de la creciente prevalencia de los NOAC, es importante tener en cuenta que una reducción de la función renal también puede provocar una acumulación de anticoagulantes. El grado de acumulación se correlaciona con la gravedad de la disfunción renal y también depende de la sustancia utilizada (Tab. 1). También hay que estar preparado para las posibles interacciones farmacológicas y saber que -al igual que los AVK- los NOAC también pueden verse influidos de forma relevante en su metabolismo por la medicación conjunta y la función hepática (Tab.1) [4,5].
A veces, los pacientes con fibrilación auricular y un alto riesgo de tromboembolia, pero que corren riesgo de hemorragia o que no corren riesgo de tromboembolia, pueden ser tratados con un fármaco. -complicaciones no son elegibles para la anticoagulación. Ahora se sabe que la orejuela auricular izquierda es una fuente central de formación de trombos en la fibrilación auricular [9,10]. Para los pacientes bien seleccionados que no pueden optar a la anticoagulación debido a contraindicaciones, en los últimos años ha surgido una alternativa con la introducción de los llamados sistemas de cierre del apéndice auricular para reducir el riesgo de ictus o de muerte relacionada con el ictus. para contener el riesgo de hemorragia [1,2,9,10]. Varios estudios ya han demostrado que estos sistemas de cierre auricular pueden ser una opción de tratamiento eficaz [9,10].
Control del ritmo – Opciones de fármacos
Además de la profilaxis de la tromboembolia, el segundo elemento central para los pacientes con fibrilación auricular es la terapia de la arritmia per se. La estrategia de tratamiento debe basarse en las circunstancias individuales y, por lo tanto, está orientada a los síntomas del paciente, la duración del episodio de fibrilación auricular y la situación clínica general.
En la figura 2 se enumeran las posibles estrategias para el control del ritmo en pacientes con FA paroxística o persistente. Los pacientes sintomáticos, así como los pacientes con una función cardiaca reducida en la fibrilación auricular (por ejemplo, taquicardiomiopatía), suelen beneficiarse de la terapia de control del ritmo [2,3,11]. Dependiendo de los síntomas y de la duración del episodio de fibrilación auricular, una vez aclarada la necesidad de anticoagulación o de terapia anticoagulante, el paciente puede ser ingresado en el hospital. Tras la exclusión de un trombo intracardiaco, debe intentarse la medicación o la cardioversión eléctrica. En general, si la FA ha persistido durante más de 48 horas o más, debe establecerse la anticoagulación durante al menos tres semanas antes de la cardioversión y luego continuarla durante al menos cuatro semanas y después indefinidamente en función de la puntuación CHA2DS2 VASc [1,2].
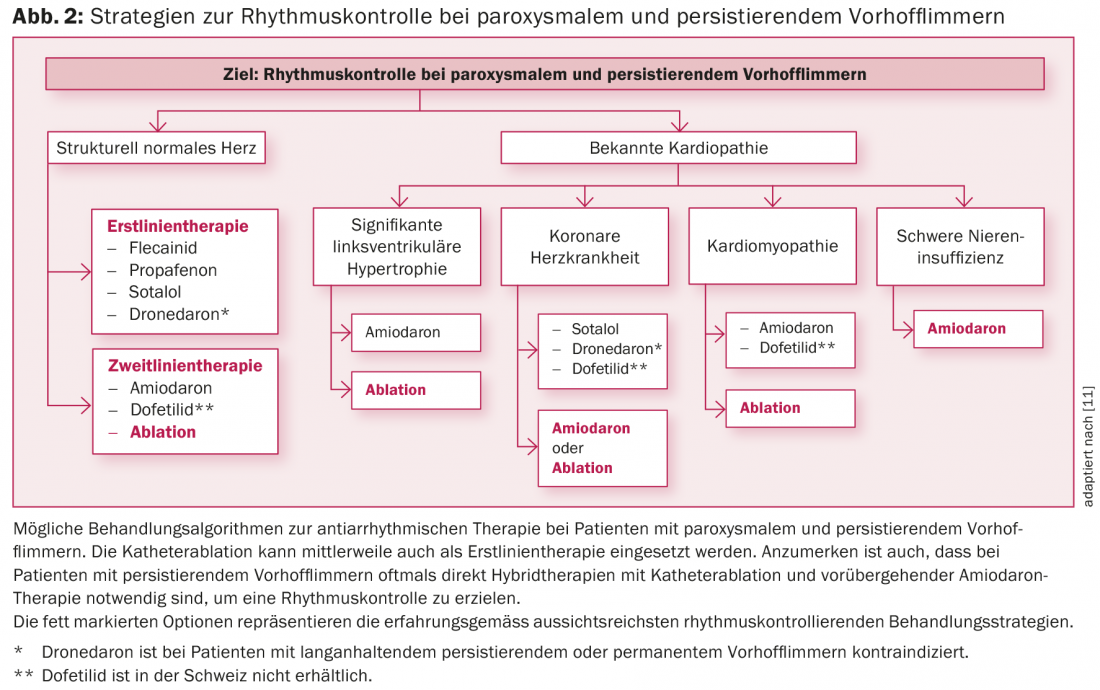
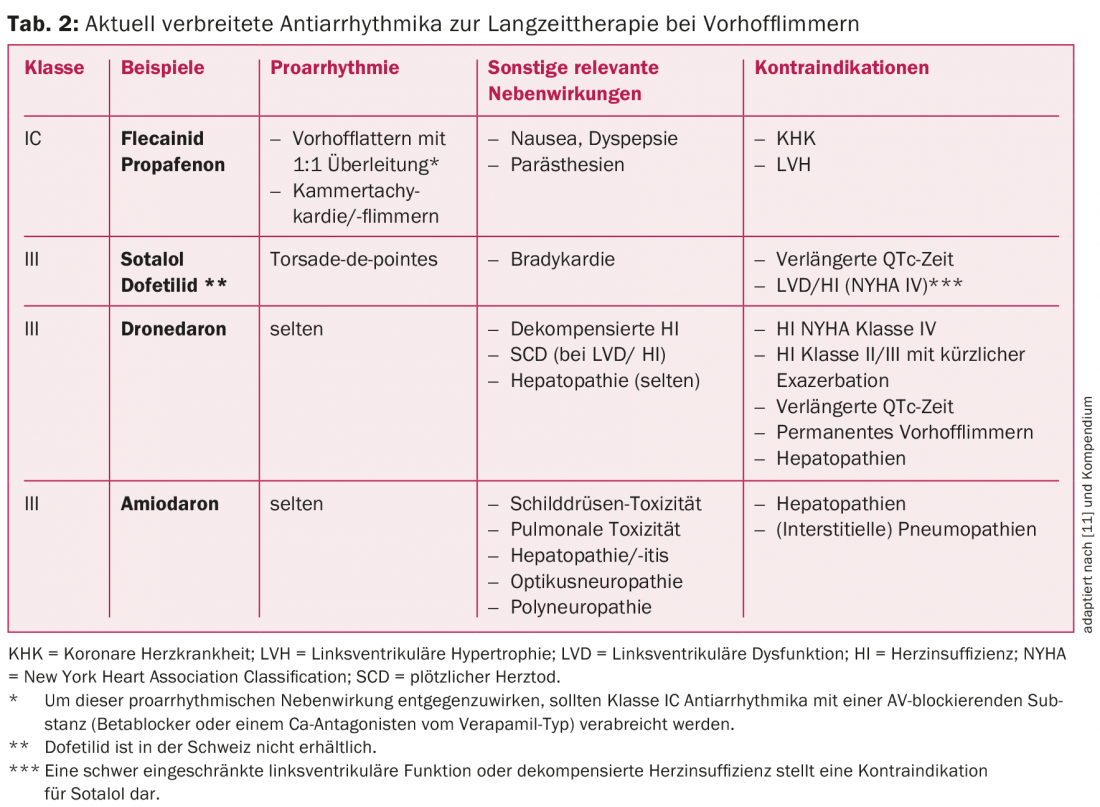
Los fármacos antiarrítmicos más comunes en la actualidad para el control del ritmo a largo plazo y sus indicaciones en la fibrilación auricular se enumeran en la tabla 2 y en la figura 2. En pacientes sin cardiopatía estructural, los fármacos antiarrítmicos de clase IC (por ejemplo, flecainida o propafenona) en combinación con un β-bloqueante cardioselectivo son la primera elección [1]. La amiodarona y la dofetilida (esta última no disponible en Suiza) son los agentes terapéuticos de elección, sobre todo en pacientes con cardiopatía estructural o deterioro de la función de bomba (fig. 2) [1,3]. La amiodarona es el fármaco antiarrítmico más potente disponible y debe administrarse de forma limitada en el tiempo si es posible debido a su considerable perfil de efectos secundarios e interacciones [2,3,11]. Los fármacos antiarrítmicos más recientes, como el vernakalant (sólo disponible i.v.) y la dronedarona, no han podido establecerse a largo plazo debido a su eficacia limitada y también a estudios desfavorables. La dronedarona, en particular, sólo debe utilizarse con precaución debido a los resultados de los ensayos PALLAS y ANDROMEDA [2,3,11]. Por ejemplo, la dronedarona no se recomienda en pacientes con fibrilación auricular permanente o fibrilación auricular. la insuficiencia cardíaca está incluso contraindicada [2,3,11]. Sin embargo, como los fármacos antiarrítmicos de clase IC y III establecidos también tienen sólo un efecto limitado y la fibrilación auricular es una enfermedad dinámica, la medicación a largo plazo para mantener el ritmo no suele tener mucho éxito [2,3,11].
Control del ritmo – Opciones electrofisiológicas
Con la creciente comprensión fisiopatológica del desarrollo de la fibrilación auricular, surgen constantemente nuevas dianas terapéuticas. Desde que se realizaron los primeros procedimientos ritmoquirúrgicos (procedimientos MAZE) para preservar el ritmo sinusal, mucho ha llovido en el campo del tratamiento intervencionista de la fibrilación auricular. Hoy en día, el objetivo es aislar eléctricamente las venas pulmonares en pacientes con fibrilación auricular paroxística y también persistente mediante procedimientos de ablación con catéter y la colocación de líneas de escleroterapia, ya que se considera que los focos eléctricamente activos en ellas son desencadenantes importantes de la arritmia (Fig. 3) [1,2,11].
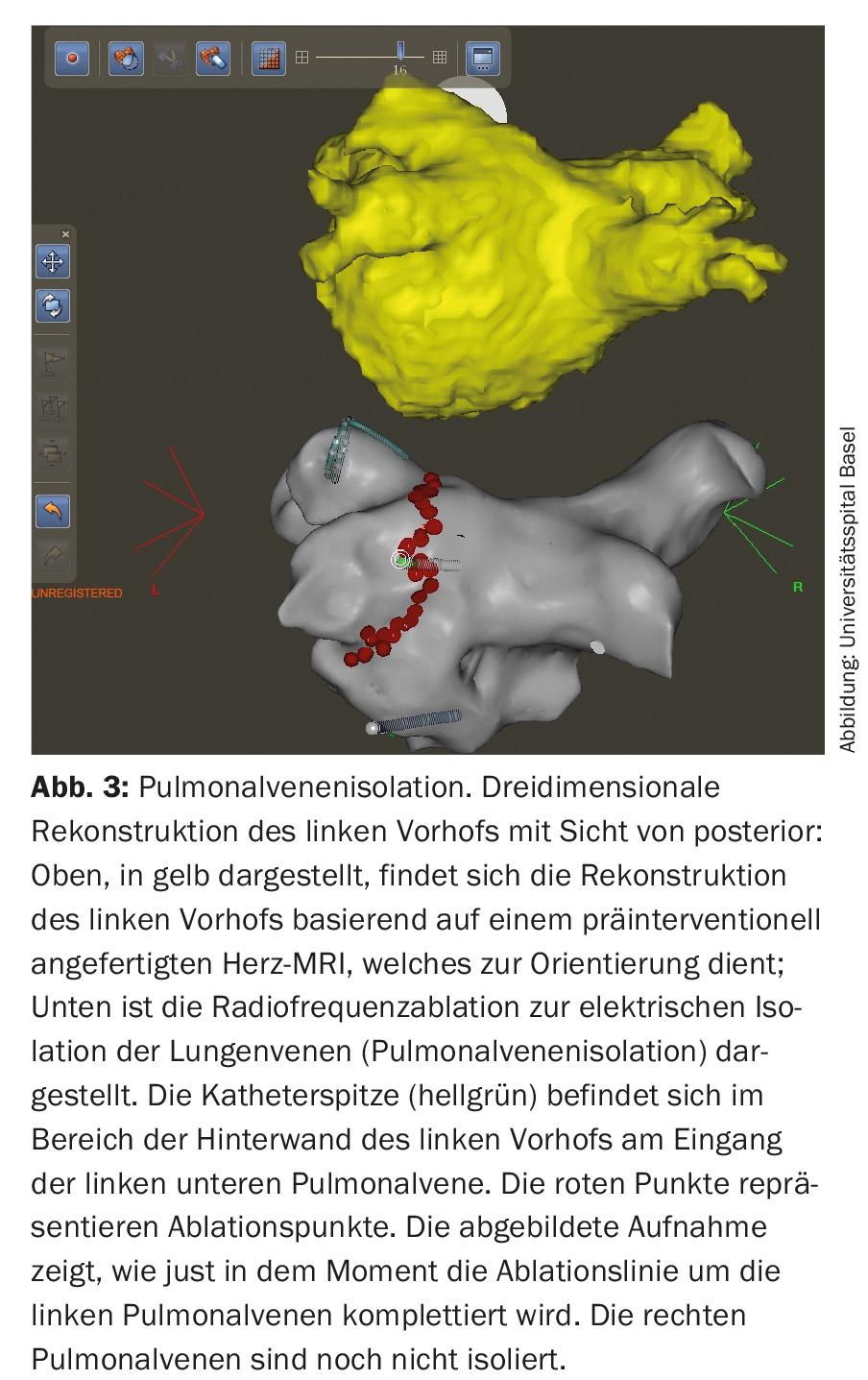
El aislamiento de la vena pulmonar se realiza mediante radiofrecuencia o crioablación y se ha convertido en un procedimiento cardiaco rutinario. El riesgo de complicaciones es ahora muy bajo en los centros con un elevado número de procedimientos. Además de las complicaciones en el lugar de la punción inguinal (aprox. 2%), en raras ocasiones puede producirse un taponamiento pericárdico que requiera drenaje (<1%). El AIT o el ictus también son poco frecuentes (<1%), y la complicación más temida, la fístula atrioesofágica, es muy rara (0,01-0,2%) [2,10,11]. Cada vez más, la terapia de ablación es el tratamiento primario para muchos pacientes sintomáticos con FA [1–3,11]. No obstante, la indicación de una terapia intervencionista sólo debe hacerse tras una cuidadosa evaluación de riesgos y beneficios. En general, además de la preferencia del paciente, deben evaluarse los siguientes factores: tipo y duración de la fibrilación auricular, tamaño de la aurícula y cardiopatías subyacentes [1,2,11].
Las tasas de éxito de la ablación de la fibrilación auricular han mejorado significativamente en los últimos años. Un metaanálisis publicado recientemente demostró que la ablación con catéter hacía que el 77% de todos los pacientes estuvieran libres de FA sintomática al cabo de un año, en comparación con el 52% con tratamiento farmacológico antiarrítmico [2]. Sin embargo, la experiencia demuestra que entre una cuarta y una tercera parte de todos los pacientes necesitan una segunda intervención (la llamada redoablación) para lograr un control sostenido de los síntomas [3,11].
Control de frecuencia
En pacientes asintomáticos y especialmente ancianos y polimórbidos con fibrilación auricular, la atención suele centrarse en controlar la frecuencia cardiaca. Este planteamiento se basa en los datos de varios ensayos aleatorios (por ejemplo, los ensayos AFFIRM y RACE), que no pudieron demostrar un beneficio discernible en la mortalidad de una terapia de control del ritmo frente a una de control de la frecuencia en las respectivas poblaciones de pacientes [2,3,11]. Si se acepta la fibrilación auricular porque el paciente está asintomático, sólo se controla entonces la frecuencia ventricular con un betabloqueante o un antagonista del calcio [2,3,11]. La digoxina se sigue utilizando, por ejemplo, cuando es necesario controlar la frecuencia en el contexto de una insuficiencia cardiaca descompensada, pero los autores sólo la emplean en casos muy seleccionados. El recientemente publicado estudio TREAT-AF, un análisis retrospectivo de más de 120.000 pacientes, apunta en la misma dirección al demostrar que la digoxina se asocia a una mayor mortalidad en la FA [12].
Si no se consigue un control adecuado de la frecuencia con medicación, debe buscarse un control intervencionista de la frecuencia [2]. También se utiliza la ablación con catéter para cortar el nodo AV, lo que da lugar a un control de la frecuencia ventricular pero también a la dependencia del marcapasos [2]. Esta opción terapéutica está volviendo a cobrar importancia, ya que tiene una elevada tasa de éxito (>99%) y el efecto secundario positivo para el paciente de que los fármacos bloqueadores de la frecuencia (y sus efectos secundarios) también pueden suspenderse.
Tratamiento de los factores de riesgo y concomitantes
Un gran número de estudios han demostrado que el tratamiento óptimo de los factores de riesgo cardiovascular clásicos (hipertensión arterial, diabetes, dislipidemia y consumo de nicotina), así como de enfermedades concomitantes comunes como la obesidad, el síndrome de apnea obstructiva del sueño y la insuficiencia renal, influye positivamente en la incidencia y el curso de la FA [2,3,11,13].
En un trabajo publicado recientemente, se demostró de forma impresionante que una reducción rigurosa del peso en combinación con un tratamiento óptimo de los factores de riesgo cardiometabólicos conlleva una reducción de la fibrilación auricular sintomática y una influencia positiva en el remodelado cardiaco [13]. El término “terapia ascendente” se ha puesto de moda en relación con el tratamiento integral de la fibrilación auricular [2,3,11]. Esto incluye el tratamiento farmacológico de factores como la inflamación y la fibrosis que favorecen la fibrilación auricular. A este respecto, diversos estudios han demostrado que los inhibidores de la ECA/antagonistas de la AT-2 y las estatinas en particular pueden tener un efecto positivo a largo plazo y contrarrestar la evolución de la fibrilación auricular.
Conflictos de intereses
- Matthias Bossard no tiene ningún conflicto de intereses en relación con este artículo.
- Stefan Osswald: Honorarios por consultoría/conferencias: Boehringer-Ingelheim
- Michael Kühne: Honorarios por consultoría/conferencias: Boehringer-Ingelheim, Bayer, Daiichi-Sankyo
Literatura:
- Camm AJ, et al: 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: actualización de las directrices de la ESC de 2010 para el tratamiento de la fibrilación auricular. Desarrollado con la contribución especial de la Asociación Europea del Ritmo Cardiaco. Eur Heart J 2012 Nov; 33(21): 2719-2747.
- European Heart Rhythm A, European Association for Cardio-Thoracic S, Camm AJ, et al: Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J 2010 Oct; 31(19): 2369-2429.
- Trulock KM, Narayan SM, Piccini JP: Control del ritmo en pacientes con insuficiencia cardiaca y fibrilación auricular: retos contemporáneos, incluido el papel de la ablación. J Am Coll Cardiol 2014 Ago 19; 64(7): 710-721.
- Lip GY: Evaluación del riesgo de ictus y hemorragia en la fibrilación auricular: ¿cuándo, cómo y por qué? Eur Heart J 2013 abr; 34(14): 1041-1049.
- Heidbuchel H, et al: Guía práctica de la EHRA sobre el uso de nuevos anticoagulantes orales en pacientes con fibrilación auricular no valvular: resumen ejecutivo. Eur Heart J 2013 Jul; 34(27): 2094-2106.
- Granger CB, et al: Apixaban frente a warfarina en pacientes con fibrilación auricular. N Engl J Med 2011 Sep 15; 365(11): 981-992.
- Giugliano RP, et al: Edoxaban frente a warfarina en pacientes con fibrilación auricular. N Engl J Med 2013 Nov 28; 369(22): 2093-2104.
- Hart RG, et al: Anticoagulantes en pacientes con fibrilación auricular y enfermedad renal crónica. Nat Rev Nephrol 2012 Oct; 8(10): 569-578.
- Reddy VY, et al: Cierre percutáneo de la orejuela auricular izquierda frente a warfarina para la fibrilación auricular: un ensayo clínico aleatorizado. JAMA 2014 Nov 19; 312(19): 1988-1998.
- John Camm A, et al: Cierre del apéndice auricular izquierdo: una nueva técnica para la práctica clínica. Ritmo cardiaco 2014 mar; 11(3): 514-521.
- Woods CE, Olgin J: Terapia de la fibrilación auricular ahora y en el futuro: fármacos, productos biológicos y ablación. Circ Res 2014 abr 25; 114(9): 1532-1546.
- Turakhia MP, et al: Mayor mortalidad asociada a la digoxina en pacientes contemporáneos con fibrilación auricular: resultados del estudio TREAT-AF. J Am Coll Cardiol 2014 Ago 19; 64(7): 660-668.
- Abed HS, et al: Efecto de la reducción de peso y el control de los factores de riesgo cardiometabólico sobre la carga y la gravedad de los síntomas en pacientes con fibrilación auricular: un ensayo clínico aleatorizado. JAMA 2013 Nov 20; 310(19): 2050-2060.
CARDIOVASC 2015











