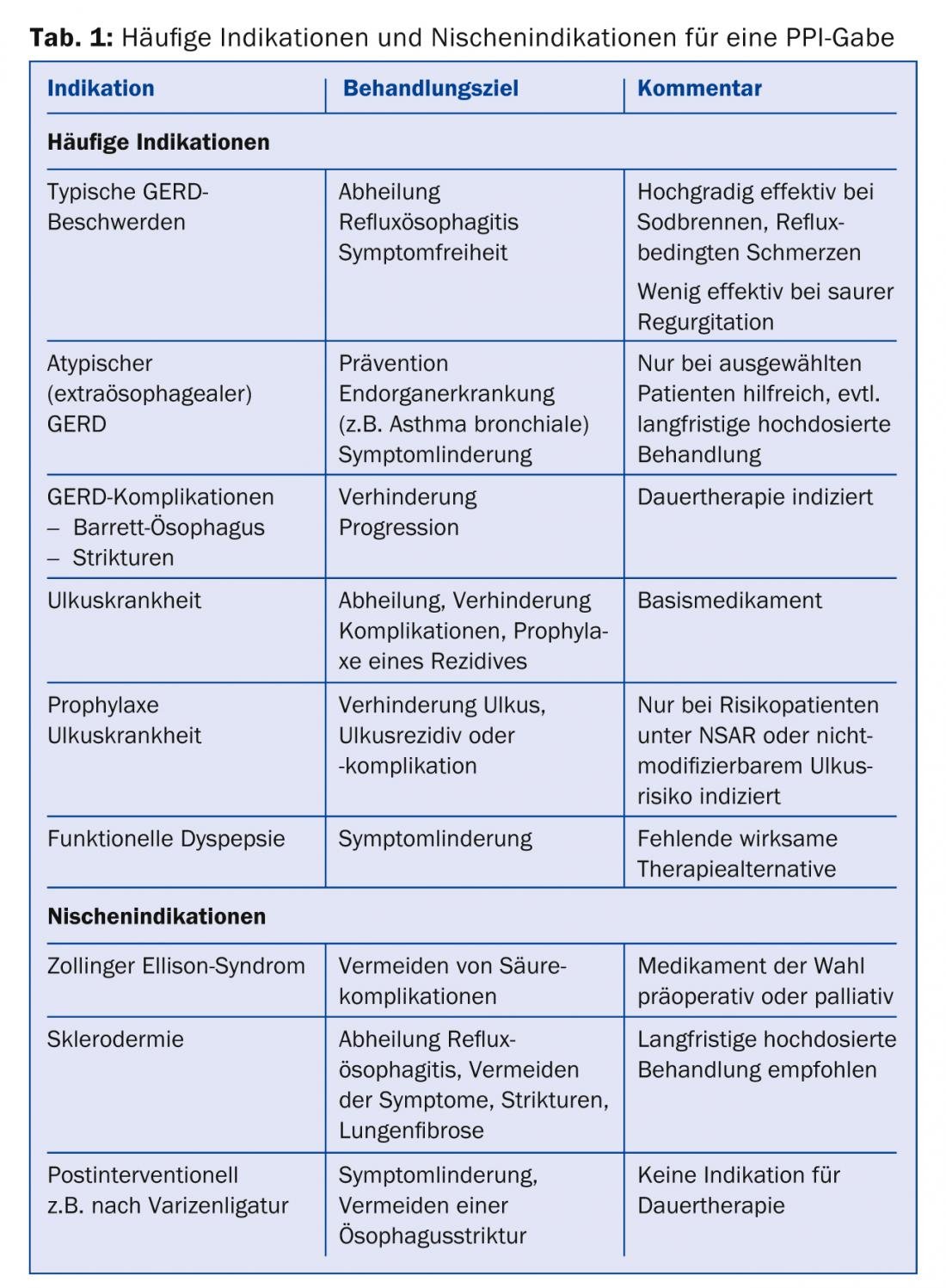
Los inhibidores de la bomba de protones (IBP) son la tercera clase de fármacos más utilizados en la práctica clínica actual en todo el mundo, después de los antibióticos y las estatinas (Tab. 1). Estos inhibidores de la acidez altamente potentes curan y mejoran eficazmente los síntomas de la enfermedad por reflujo gastroesofágico y otras enfermedades causadas por la acidez estomacal. Sin embargo, con el uso generalizado y a menudo a largo plazo de los IBP, incluso los pequeños riesgos para la salud son relevantes. La tarea del médico de cabecera es evitar el uso innecesario de IBP sin privar de este fármaco eficaz a los pacientes con buenas indicaciones. El siguiente artículo ofrece una visión general de las indicaciones y los riesgos de su uso.
¿Cuál es el papel de los IBP en el tratamiento de la enfermedad por reflujo gastroesofágico (ERGE)? Los IBP son la clase de medicación más eficaz para la ERGE. Gracias a la disponibilidad de los IBP, la mayoría de los pacientes con síntomas típicos de reflujo (por ejemplo, ardor de estómago, regurgitaciones ácidas) pueden ser tratados bien por el médico de cabecera o incluso automedicándose con IBP [1,2]. La aclaración o derivación a un gastroenterólogo sólo es necesaria para el tratamiento de los síntomas de reflujo refractarios. También es importante comprobar siempre la indicación de una terapia a largo plazo con IBP en pacientes sin síntomas. A menudo puede reducirse la dosis y hasta un 40% de los pacientes permanecen sin síntomas durante meses incluso después de suspender los IBP [3]. Esta proporción puede incrementarse aún más administrando medicación a demanda (por ejemplo, antiácidos, alginatos como Gaviscon®) [2].
Con los IBP, la esofagitis por reflujo y las estenosis pépticas como complicaciones de la ERGE pueden curarse o prevenirse [4]. El esófago de Barrett es otra consecuencia clínicamente importante de la ERGE y puede desembocar en un adenocarcinoma de esófago en aproximadamente un 0,2% al año [5]. Los estudios de casos y controles sugieren que los IBP pueden prevenir aquí la progresión a carcinoma [6]. Los resultados del gran estudio prospectivo y aleatorizado ASPECT estarán pronto disponibles para aclarar definitivamente esta cuestión [7]. En nuestra opinión, la terapia a largo plazo con un IBP ya está indicada para el esófago de Barrett.
Las manifestaciones extraesofágicas de la ERGE incluyen tos crónica, ronquera y sensación de globo. En estos pacientes, la relación entre el reflujo y los síntomas es menos clara y las dolencias ORL (sinusitis crónica, “goteo post-nasal”) así como las enfermedades neumológicas pueden contribuir a la patogénesis [1]. Las tasas de éxito del tratamiento con IBP son correspondientemente más modestas [8].
Si los síntomas persisten, el médico generalista tiene dos opciones: el tratamiento empírico con IBP al doble de la dosis estándar durante ocho a doce semanas, y la medición objetiva del pH para determinar la gravedad de la exposición ácida esofágica y la relación entre el reflujo y los síntomas extraesofágicos [8]. El paciente debe participar en esta decisión. Es importante que en caso de que el tratamiento con IBP no tenga éxito o la medición del pH sea negativa, se interrumpa el IBP.
Indicación úlcera péptica
Los IBP son la medicación básica para el tratamiento de la úlcera péptica y sus complicaciones. Así, en la situación de hemorragia, la neutralización del pH gástrico puede activar la coagulación de la sangre y limitar la hemorragia [9]. Además, la mayoría de las úlceras gástricas o duodenales se curan a las pocas semanas del tratamiento con IBP [10]. Los IBP también forman parte de la terapia de erradicación del H. pylori. También en este caso debe suspenderse el IBP una vez que la úlcera haya cicatrizado y se haya eliminado el factor de riesgo. El tratamiento continuo con IBP para la profilaxis del desarrollo o la reaparición de úlceras está indicado en pacientes de alto riesgo que toman AINE y en pacientes que ya han tenido una úlcera y presentan factores de riesgo no modificables [11].
Indicación dispepsia funcional
Los IBP son eficaces en el tratamiento de la dispepsia funcional (DF) en algunos casos y también pueden administrarse empíricamente en ausencia de síntomas de alarma y tras descartar la infección por H. pylori. Por desgracia, la tasa de éxito de los IBP para esta indicación es baja (“número necesario a tratar”, NNT: 10, frente a NNT 2-3 para los síntomas típicos del reflujo) [12].
Falta de respuesta a la administración de IBP
No todos los síntomas de la ERGE responden al tratamiento con IBP. Por ejemplo, los síntomas del reflujo de volumen pueden reducirse con medicación en el mejor de los casos. Incluso para los pacientes con síntomas típicos de ERGE (Fig. 1), el efecto de los IBP no es perfecto.

Aunque hasta el 90% de todos los pacientes responden al tratamiento, aproximadamente un tercio de todos los pacientes que siguen una terapia IBP a largo plazo no llegan a estar completamente libres de síntomas [1,2]. Además, un gran número de pacientes con ERGE toman medicamentos sin receta además de los IBP [13]. Sugerimos un enfoque secuencial en caso de respuesta insatisfactoria a la IBP (Fig. 2) .

Si los síntomas son típicos bajo IBP, debe probarse un preparado de alginato (por ejemplo, Gaviscon®). Los alginatos forman una capa viscosa delante de la entrada del esófago y pueden evitar así el reflujo ácido y no ácido [14]. Además, se podría cambiar el IBP y/o aumentar la dosis.
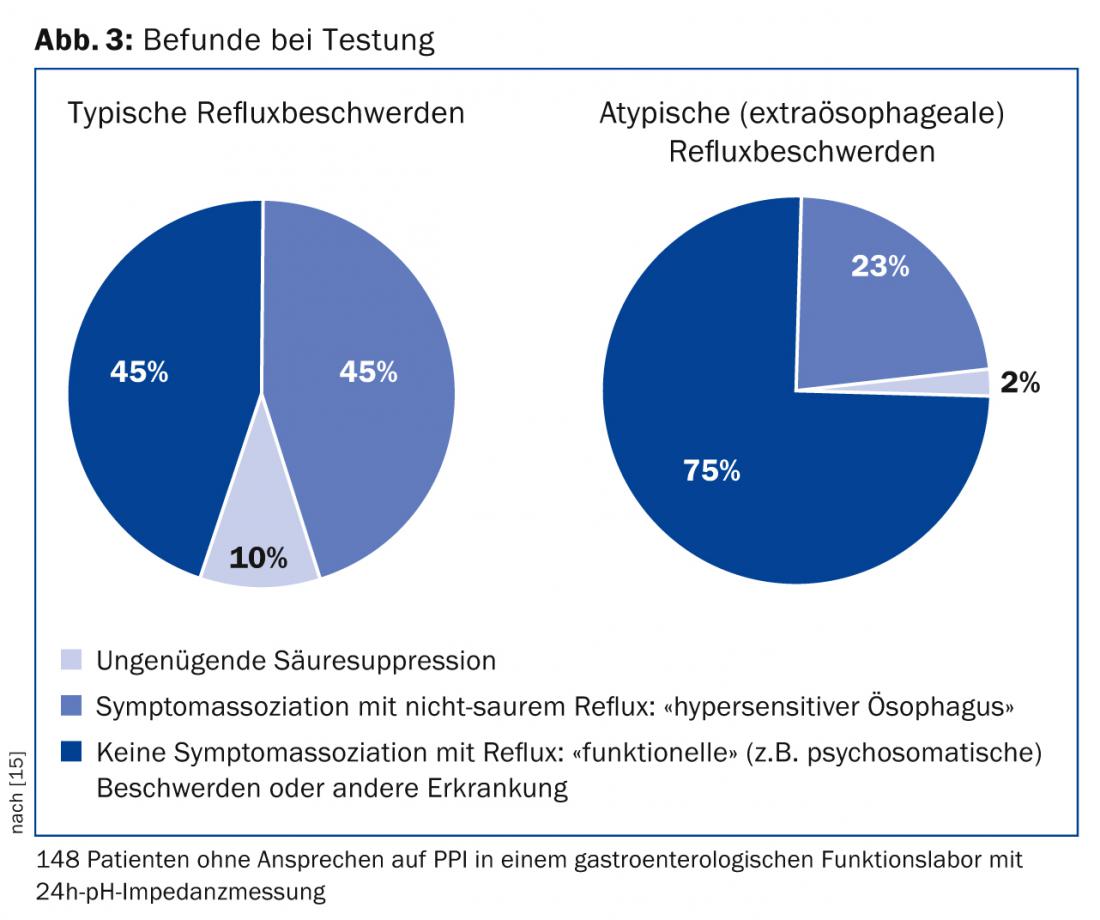
En caso de síntomas atípicos o de falta de respuesta a los IBP a pesar de las medidas mencionadas, deberán realizarse otros diagnósticos gastroenterológicos. La primera indicación es una gastroscopia para excluir una úlcera péptica o una neoplasia. Si los hallazgos son normales, debe realizarse entonces una manometría y una impedanciometría del pH para identificar la causa de las molestias [1,2]. Así, sólo aproximadamente la mitad de todos los pacientes con “quejas de reflujo” que son remitidos a un laboratorio funcional gastroenterológico tienen una enfermedad por reflujo objetivable (Fig. 3) [15]. Por ejemplo, los pacientes que padecen acalasia son diagnosticados inicialmente de forma errónea como pacientes con ERGE en cerca del 40% de los casos y tratados con IBP [16].
Un diagnóstico exacto de las dolencias refractarias permite entonces un tratamiento específico (figs. 2 y 3 ). Si se confirma que el reflujo ácido es la causa de la dolencia, deberá optimizarse aún más la supresión de ácido. En ausencia de reflujo patológico, pero en presencia de asociación sintomática entre reflujo y ardor de estómago o dolor torácico (el llamado “esófago sensible”), pueden administrarse alginatos además de IBP. Además, la sensibilidad visceral puede modularse con dosis bajas de antidepresivos (por ejemplo, amitriptilina 25 mg nocté). En ausencia de enfermedad por reflujo y asociación de síntomas, el IBP puede interrumpirse. En su lugar, debe tratarse, si es necesario, un trastorno de la motilidad o un trastorno psicosomático, o bien realizar un diagnóstico más exhaustivo.
Riesgo de rebote ácido
Según la experiencia clínica, la acidez suele empeorar brevemente tras dejar de tomar un IBP. Los síntomas de reflujo pueden desencadenarse tras la administración de IBP a corto plazo, incluso en sujetos previamente libres de síntomas [17]. Este efecto rebote puede dificultar a los pacientes la interrupción de los IBP y contribuir a la administración innecesaria de IBP [18]. Si se producen síntomas de rebote tras la interrupción, el IBP debe reducirse gradualmente (por ejemplo, una semana la dosis estándar única, una semana la mitad de la dosis estándar). Además, recomendamos antiácidos o alginatos según sea necesario durante el destete.
Otros riesgos de un PPI
Contrariamente a los temores iniciales, los IBP no aumentan el riesgo de cáncer gástrico [19]. Muchos estudios de casos y controles han encontrado una asociación del riesgo de cáncer con la indicación del tratamiento con IBP (ERGE, úlceras gástricas, etc.) pero no con el uso de IBP [20]. Por otro lado, un IBP puede enmascarar los síntomas del cáncer gástrico. Por lo tanto, la gastroscopia es obligatoria en caso de síntomas de alarma antes del tratamiento empírico con IBP y debe considerarse siempre de nuevo si el efecto de los IBP es insuficiente.
La pérdida del efecto antibacteriano del ácido gástrico aumenta el riesgo de enteritis infecciosa con shigella y salmonella, entre otras [21]. Especialmente en el caso de los pacientes hospitalizados o necesitados de cuidados, es probable que el aumento del riesgo en relación con las infecciones por Clostridium difficile (HR 2,5) o la neumonía (HR 1,4) sea relevante [22]. En pacientes con cirrosis hepática, los IBP no pueden detener la hemorragia por varices esofágicas, pero pueden aumentar el riesgo de peritonitis bacteriana espontánea, por lo que en general no deben administrarse en este grupo de pacientes [23].
Las consideraciones fisiológicas también sugieren una menor absorción de vitamina B12, calcio, magnesio y hierro con el uso de IBP [24]. Con la abundancia actual de alimentos con cantidades suficientes de vitaminas y minerales, este riesgo rara vez es relevante [24]. No obstante, en caso de quejas compatibles con malnutrición de estas sustancias mencionadas, la vigilancia debe ser generosa. Los estudios de asociación también han identificado la osteoporosis como una posible complicación del uso prolongado de IBP (HR para el riesgo de fractura 1,25) [25]. Es importante señalar que todos estos riesgos se han encontrado en estudios de casos y controles, pero no en grandes ensayos prospectivos aleatorios, por lo que no están libres de la influencia de posibles factores de confusión.
Las interacciones farmacológicas de los IBP y otros riesgos se resumen en la tabla 2. Una interacción farmacológica inicialmente temida entre los IBP y el clopidogrel fue refutada en estudios recientes. Los IBP, por ejemplo, conllevan el riesgo teórico de bloqueo del clopidogrel, ya que pueden bloquear el citocromo CYP2C19, que es importante para la activación del clopidogrel. No obstante, en un amplio estudio en el que los pacientes recibieron clopidogrel solo o junto con un IBP tras la inserción de un stent coronario, el riesgo de acontecimientos adversos cardiacos fue exactamente el mismo en ambos brazos del estudio, con menos acontecimientos adversos gastrointestinales con el IBP [26]. Así pues, la interacción farmacológica de IBP y clopidogrel no es relevante en la práctica. Este discurso muestra cómo las consideraciones fisiológicas pueden inducir ocasionalmente a error y hasta qué punto el factor de confusión “morbilidad” puede fingir interacciones relevantes en los estudios de casos y controles.

Una indicación adecuada es crucial
A pesar de todas las ventajas, es importante advertir contra el uso acrítico de estos fármacos: Las estimaciones sugieren que entre el 25 y el 75% de todos los pacientes tratados con IBP no tienen una indicación adecuada. En series de casos típicas de pacientes hospitalizados, el 20% toma IBP al ingreso, el 40% comienza a tomar un IBP durante la hospitalización y el 50% se encuentra tomando un IBP en la medicación al alta [27]. Esto ocurre casi siempre sin una indicación adecuada y sin que en la carta de alta se sugiera una hora para la revisión de la medicación. Por tanto, es probable que los pacientes hospitalizados con frecuencia también sean tratados frecuentemente con IBP en el ámbito ambulatorio [28]. Es precisamente este grupo de pacientes el más vulnerable a los problemas mencionados.
CONCLUSIÓN PARA LA PRÁCTICA
- La introducción de los IBP como inhibidores seguros y eficaces de la secreción ácida ha tenido un gran impacto positivo en el tratamiento de muchas enfermedades gastroesofágicas.
- No obstante, hay que estar prevenido contra un uso acrítico de estos medicamentos.
- Sigue siendo tarea responsable del médico de cabecera suspender el IBP “innecesario”, continuar con el IBP “necesario”, útil, a la dosis eficaz más baja y, sobre todo, distinguir entre ambas situaciones con certeza.
A RETENIR
- La puesta en el mercado de los PPI como inhibidores seguros y eficaces de la secreción de ácido ha tenido un importante efecto positivo en el tratamiento de muchas enfermedades del estómago y del esófago.
- Toutefois une mise en garde contre une utilisation irrationnelle de ces médicaments est nécessaire.
- Existe un alto nivel de responsabilidad por parte del médico de familia para detener los PPI “inútiles”, continuar con los PPI “necesarios” a las dosis más eficaces y, sobre todo, diferenciar entre ambas situaciones con precisión.
Prof. Dr. med. Mark Fox
PD Dr. med. Benjamin Misselwitz
Dr. Daniel Pohl
Literatura:
- Fox M, Forgacs I: Enfermedad por reflujo gastroesofágico. BMJ 2006; 332: 88-93.
- Tytgat GN, et al: Nuevo algoritmo para el tratamiento de la enfermedad por reflujo gastroesofágico. Aliment Pharmacol Ther 2008 Feb 1; 27(3): 249-256.
- Schwizer W, et al: El efecto de la infección por Helicobacter pylori y su erradicación en pacientes con enfermedad por reflujo gastroesofágico: un estudio multicéntrico de grupos paralelos, doble ciego y controlado con placebo. Revista Europea Unida de Gastroenterología 2013; 1(4): 226-235.
- Castell DO, et al: Esomeprazol (40 mg) comparado con lansoprazol (30 mg) en el tratamiento de la esofagitis erosiva. Am J Gastroenterol 2002; 97(3): 575-583.
- de Jonge PJ, et al: Esófago de Barrett: epidemiología, riesgo de cáncer e implicaciones para el tratamiento. Gut 2014 Jan; 63(1): 191-202.
- Singh S, et al: Medicamentos supresores de ácido y riesgo de adenocarcinoma esofágico en pacientes con esófago de Barrett: revisión sistemática y metaanálisis. Gut 2013 nov 12.
- Jankowski J, Sharma P: Artículo de revisión: enfoques para el tratamiento del esófago de Barrett: el papel de los inhibidores de la bomba de protones y otras intervenciones. Aliment Pharmacol Ther 2004 Feb; 19 Suppl 1: 54-59.
- Sifrim D, Barnes N: Tos crónica relacionada con la ERGE: ¿cómo identificar a los pacientes que responderán a la terapia antirreflujo? J Clin Gastroenterol. 2010 Abr; 44(4): 234-236.
- Sung JJ, et al: Esomeprazol intravenoso para la prevención de la hemorragia recurrente por úlcera péptica: un ensayo aleatorizado. Ann Intern Med 2009 abr 7; 150(7): 455-464.
- Leodolter A, et al: Un metaanálisis que compara las tasas de erradicación, curación y recaída en pacientes con úlcera gástrica o duodenal asociada a Helicobacter pylori. Aliment Pharmacol Ther 2001 Dic; 15(12): 1949-1958.
- Chan FK, Sung JJ: Papel de los supresores ácidos en la profilaxis de los daños causados por los AINE. Best Pract Res Clin Gastroenterol 2001 Jun; 15(3): 433-445. PubMed PMID: 11403537.
- Wang WH, et al: Efectos de los inhibidores de la bomba de protones en la dispepsia funcional: un metaanálisis de ensayos aleatorizados controlados con placebo. Clin Gastroenterol Hepatol. 2007 Feb; 5(2): 178-185; quiz 40.
- Hungin AP, et al: Revisión sistemática: Patrones de uso de inhibidores de la bomba de protones y adherencia en la enfermedad por reflujo gastroesofágico. Clin Gastroenterol Hepatol 2012 Feb; 10(2): 109-116.
- Sweis R, et al: Supresión del reflujo postprandial mediante un alginato formador de balsas (Gaviscon Advance) en comparación con un antiácido simple documentada mediante resonancia magnética y monitorización de la impedancia del pH: evaluación mecanicista en voluntarios sanos y estudio aleatorizado, controlado y a doble ciego en pacientes con reflujo. Aliment Pharmacol Ther 2013 Jun; 37(11): 1093-1102.
- Mainie I, et al: Reflujo ácido y no ácido en pacientes con síntomas persistentes a pesar de la terapia supresora de ácido: un estudio multicéntrico mediante monitorización combinada ambulatoria de impedancia-pH. Gut. 2006 Oct; 55(10): 1398-1402.
- Kessing BF, Bredenoord AJ, Smout AJ: Diagnóstico erróneo de la enfermedad por reflujo gastroesofágico en la acalasia. Clin Gastroenterol Hepatol. 2011 dic; 9(12): 1020-1024.
- Reimer C, et al.: La terapia con inhibidores de la bomba de protones induce síntomas relacionados con la acidez en voluntarios sanos tras la retirada del tratamiento. Gastroenterología 2009; 137(1): 80-87.
- Howden CW, Kahrilas PJ: Editorial: ¿hasta qué punto es “difícil” retirar el tratamiento con IBP? Am J Gastroenterol 2010 Jul; 105(7): 1538-1540.
- Klinkenberg-Knol EC, et al: Tratamiento a largo plazo con omeprazol en la enfermedad por reflujo gastroesofágico resistente: eficacia, seguridad e influencia en la mucosa gástrica. Gastroenterología 2000 abr; 118(4): 661-669.
- Tamim H, et al.: Asociación entre el uso de fármacos supresores de la acidez y el riesgo de cáncer gástrico. Un estudio anidado de casos y controles. Drug Saf 2008; 31(8): 675-684.
- Leonard J, Marshall JK, Moayyedi P: Revisión sistemática del riesgo de infección entérica en pacientes que toman supresión ácida. Am J Gastroenterol 2007 Sep; 102(9): 2047-2056; quiz 57.
- Howell MD, et al: Supresión iatrogénica de la acidez gástrica y riesgo de infección nosocomial por Clostridium difficile. Arch Intern Med. 10 de mayo de 2010; 170(9): 784-790.
- Goel GA, et al: Aumento de la tasa de peritonitis bacteriana espontánea entre los pacientes cirróticos que reciben supresión ácida farmacológica. Clin Gastroenterol Hepatol 2012 abr; 10(4): 422-427.
- Pohl D, et al.: ¿Necesitamos ácido gástrico? Digestión 2008; 77(3-4): 184-197.
- Gray SL, et al: Uso de inhibidores de la bomba de protones, fractura de cadera y cambio en la densidad mineral ósea en mujeres posmenopáusicas: resultados de la Iniciativa de Salud de la Mujer. Arch Intern Med 2010 mayo 10; 170(9): 765-771.
- Bhatt DL, et al: Clopidogrel con o sin omeprazol en la enfermedad arterial coronaria. N Engl J Med 2010 Nov 11; 363(20): 1909-1917.
- Yachimski PS, et al: Inhibidores de la bomba de protones para la profilaxis de la hemorragia nosocomial del tracto gastrointestinal superior: efecto de las directrices estandarizadas en la práctica de prescripción. Arch Intern Med. 10 de mayo de 2010; 170(9): 779-783.
- Arasaradnam RP, et al: Auditoría de la prescripción de inhibidores de la bomba de protones (IBP): ¿se siguen las directrices del NICE? Clin Med 2003 Jul-Ago; 3(4): 387-388.
PRÁCTICA GP 2014; 9(6): 26-31