La hipertensión pulmonar en la cardiopatía izquierda se debe con mayor frecuencia a una elevación pasiva de la presión debida al aumento de las presiones de llenado del lado izquierdo. Aunque la hipertensión pulmonar poscapilar aislada es frecuente, sólo un pequeño grupo de pacientes se ve afectado por una enfermedad vascular pulmonar grave.
Mientras que la hipertensión arterial pulmonar idiopática sigue siendo una cebra en el amplio campo de la hipertensión pulmonar (HP), entre el 65 y el 80% de todos los pacientes con HP tienen una cardiopatía izquierda como causa del aumento de la presión en los vasos pequeños (en lo sucesivo, abreviada como PH-LHD por Left Heart Disease) [20]. Los principales clínicos e investigadores en el campo de la HP diferencian entre HP-HL con fenotipo ventricular izquierdo y HP-HL con fenotipo ventricular derecho, refiriéndose el tipo ventricular izquierdo a la presencia de HP poscapilar aislada (HPpc) y el tipo ventricular derecho a la presencia de HP poscapilar y precapilar combinada (HPpc). Mientras que la IpcPH es frecuente, sólo un pequeño grupo de pacientes (<10%) está afectado por una enfermedad vascular pulmonar grave (CpcPH). Se cree que la transición de los fenotipos ventriculares izquierdo a derecho es suave y está causada por lo que se conoce como remodelación de las pequeñas arterias pulmonares del lecho vascular pulmonar. Esta revisión examinará más de cerca los criterios diagnósticos, sus limitaciones e imprecisiones, así como las posibles opciones terapéuticas para la PH-LHD.
Definición, fisiopatología y diagnóstico
La HP es un problema común y relevante desde el punto de vista pronóstico en pacientes con cardiopatía izquierda y se asocia a una reducción de la capacidad de ejercicio y a un aumento de la morbilidad y la mortalidad [15]. Según las directrices actuales, la HP-LHD se asigna al grupo 2 de la OMS de un total de 5 grupos de HP (grupo 1: hipertensión arterial pulmonar (HAP), 2: HP en cardiopatía izquierda, 3: HP en enfermedad pulmonar o hipoxia, 4: HP tromboembólica crónica, 5: HP con asignación poco clara o mecanismos multifactoriales) [7]. Inicialmente, la PH-LHD está causada por una contrapresión pasiva, denominada postcapilar, de las presiones de llenado del lado izquierdo, especialmente de la aurícula izquierda. Este remanso se asocia a un aumento de la permeabilidad de la membrana alveolocapilar y puede provocar un edema pulmonar intersticial y alveolar. La PH-LHD puede darse en pacientes con insuficiencia cardiaca izquierda reducida (HFrEF), así como con función de bomba preservada (HFpEF) o defectos valvulares. La prevalencia de la HP en la IC-FEr se sitúa entre el 40-75% [8,17] y en la IC-FEp entre el 36-83% [13,22].
Se sospecha que en algunos pacientes -en términos de una secuencia fisiopatológica temporal- el aumento permanente y pasivo de la presión en la circulación pulmonar puede conducir a una remodelación (irreversible) de los vasos arteriales pulmonares y, por tanto, a una enfermedad vascular pulmonar y, en última instancia, a una insuficiencia cardiaca derecha. Sin embargo, no está claro en qué pacientes ocurre esto y en cuáles no. Como ocurre con muchas enfermedades, se sospecha que existe una predisposición genética además de las influencias ambientales, pero aún no se ha demostrado.
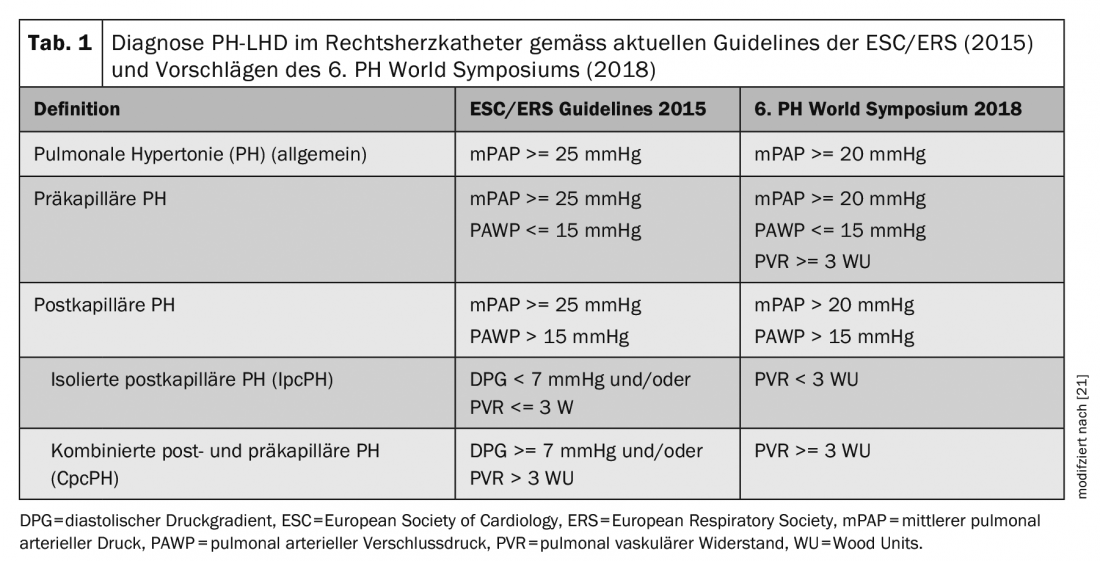
Según las directrices actuales [7], la HP poscapilar se diagnostica cuando se mide una presión arterial pulmonar media (PAPm) >= 25 mmHg y una presión de oclusión arterial pulmonar (PAWP) >15 mmHg en el catéter cardiaco derecho. Para diferenciar aún más entre la IpcPH y la CpcPH, se determinan también el gradiente de presión diastólica (PAP diastólica – PAWP) y la resistencia vascular pulmonar (PVR = (mPAP-PAWP)/Salida cardiaca). Véase la tabla 1, donde también se enumeran los nuevos criterios diagnósticos según las propuestas del 6º Simposio Mundial de HP [25] . Estudios realizados en más de 20 000 sujetos han demostrado que una PAPm entre 21-24 mmHg se asocia a una mayor mortalidad independientemente del grupo de HP – incluso en pacientes con insuficiencia cardiaca izquierda [3,5,16]. El valor normal de la mPAP es (media +/- desviación estándar) 14 +/- 3 mmHg. En conjunto, por tanto, estos estudios demostraron que por encima del umbral de la media +2 desviaciones estándar existe valor de enfermedad, razón por la cual las recomendaciones actuales para diagnosticar la hipertensión pulmonar se ajustaron durante el Simposio Mundial sobre la Hipertensión Pulmonar, de mPAP >= 25 mmHg a >20 mmHg.
No todos los pacientes necesitan un catéter cardiaco derecho
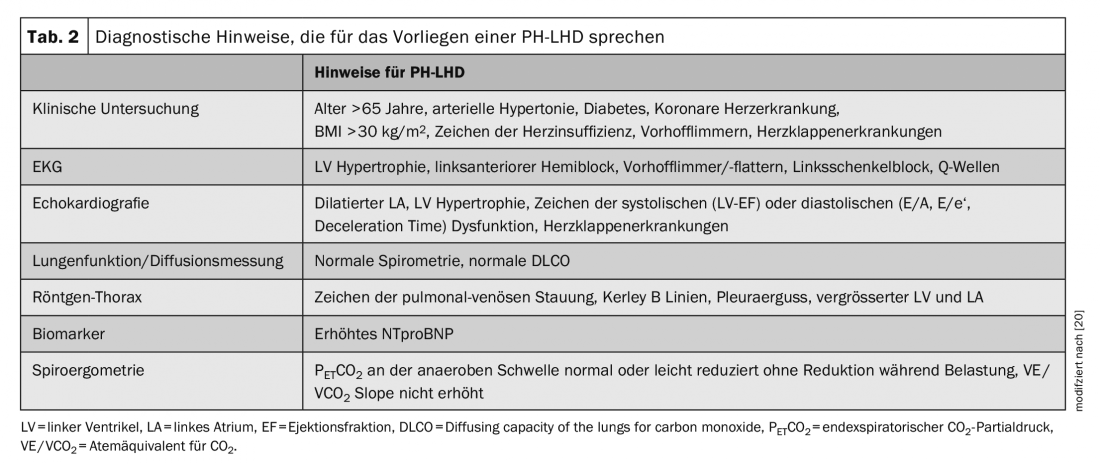
Si se sospecha que un paciente tiene hipertensión pulmonar, se recomienda realizar primero investigaciones no invasivas para acotar la causa con mayor precisión y establecer una hipótesis de trabajo. Debido a la complejidad del tema, aquí sólo se tratará la diferenciación entre HAP y PH-LHD y se descuidarán los otros grupos de PH (grupos 2, 4 y 5), aunque estos importantes diagnósticos diferenciales no deben olvidarse en el esclarecimiento de la PH. Las pruebas recomendadas y los resultados que indican PH-LHD se enumeran en la tabla 2.
Si existen pruebas ecocardiográficas de enfermedad vascular pulmonar, a saber, una relación VD/VL elevada >= 1,0, índice de centricidad del VI >1,2, formación del ápex a través del ventrículo derecho, diámetro de la vena cava > 2 cm sin colapso y una PAP sistólica estimada >50 mmHg, debe realizarse un cateterismo cardíaco derecho para una mayor diferenciación, incluso si están presentes los signos de PH-LHD enumerados en la tabla 2. Si sólo hay una HP leve o ninguno de los signos ecocardiográficos de enfermedad vascular pulmonar, lo más probable es que se trate de una HP poscapilar y no está indicada una evaluación invasiva adicional.
Limitaciones y dificultades del cateterismo cardíaco derecho
Tanto para el diagnóstico de la PH-LHD per se como para la diferenciación de un posible componente precapilar, la medición correcta de la PAWP es esencial. Existen aquí limitaciones e imprecisiones que el examinador debe conocer y tener en cuenta a la hora de interpretar los resultados.
La medición de la PAWP no es factible en todos los pacientes (la “posición en cuña” no puede lograrse si, por ejemplo, hay arterias pulmonares dilatadas). En estos casos, sobre todo si existe una alta sospecha de PH-LHD, se recomienda la medición directa de la LVEDP (presión diastólica final del ventrículo izquierdo) en el catéter cardiaco izquierdo.
La determinación incorrecta del punto cero también puede provocar errores de medición. El punto cero debe estar en la parte media del tórax a la altura de la aurícula izquierda [11]. En presencia de una deformidad torácica, determinar el punto cero puede resultar extremadamente difícil.
Existe desacuerdo entre los expertos sobre cómo medir la PAWP. Aunque muchos cardiólogos prefieren el tiempo al final de la espiración normal para la medición en reposo, los expertos en HP son más de la opinión de que las curvas de la PAWP también deben promediarse a lo largo de varios ciclos respiratorios, sobre todo también para poder comparar los valores en reposo con los valores en situación de estrés [12]. La contención de la respiración o la respiración forzada conducen a la falsificación de los valores (presión intratorácica, Valsalva, etc.). Para pacientes con enfermedades pulmonares, por ejemplo EPOC, las curvas de presión muestran fluctuaciones respiratorias prominentes. En estos casos, se recomienda promediar las curvas de presión a lo largo de varios ciclos respiratorios.
Incluso en presencia de fibrilación auricular o de una onda v elevada como indicación de regurgitación mitral, existe el riesgo de una medición errónea de la PAWP. La obesidad abdominal también puede falsear las lecturas al aumentar la presión intraabdominal e intratorácica.
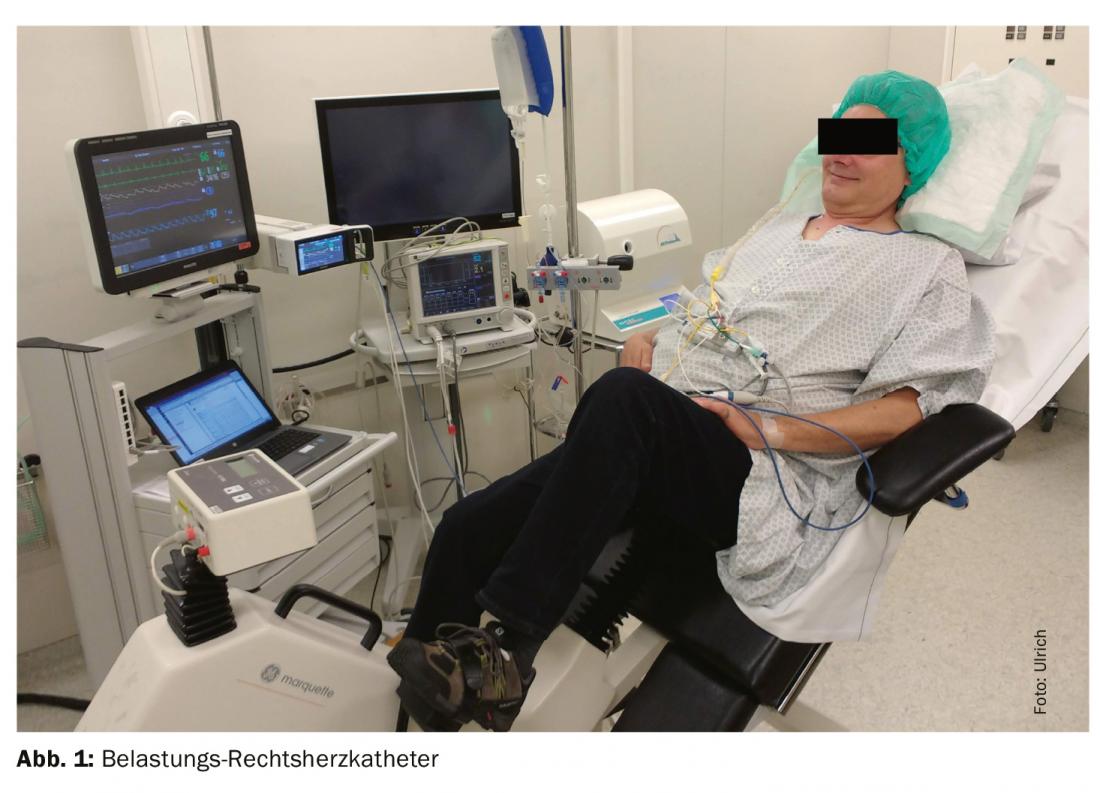
Por último, el cateterismo cardiaco derecho sólo debe realizarse en estado de enfermedad compensada, es decir, en ausencia de retención de agua cardiaca. En el paciente bien controlado en normovolemia, la presión hidrostática en el pequeño circuito debe ser normal y no debe producirse HP en reposo. No obstante, un paciente demasiado “seco” también puede tener presiones de PAWP falsamente profundas y, por tanto, la HP poscapilar puede clasificarse erróneamente como precapilar. Para desenmascarar la PH-LHD oculta, se recomienda realizar pruebas de esfuerzo suplementarias mediante la administración de volumen o pruebas de ejercicio (ergometría en bicicleta, fig. 1), especialmente en el caso de presiones de PAWP limítrofes (13-15 mmHg). Sin embargo, aún no se dispone de métodos de medición normalizados y validados [25]. Dado que estas investigaciones y la interpretación del resultado pueden ser muy complejas, se recomienda la derivación a un centro terciario con experiencia en HP.
Terapia
Dado que la mayoría de los casos de PH-LHD son PH pasiva, postcapilar, el objetivo terapéutico principal de toda PH-LHD es ajustar de forma óptima el tratamiento de la insuficiencia cardiaca y normalizar las presiones de llenado. Entre ellos se incluyen la terapia diurética intensiva, la terapia farmacológica para la insuficiencia cardiaca y los procedimientos intervencionistas (TRC, DAI, DAVI, MitraClip, etc.).
HFrEF: Según las directrices actuales [19], se recomienda un tratamiento farmacológico con inhibidores de la ECA/antagonistas de los receptores de la angiotensina II, inhibidores de la neprilisina, betabloqueantes y antagonistas de los receptores coricoides minerales. Sobre todo, es crucial conseguir las dosis objetivo previstas y una buena adherencia a la terapia. Los resultados de los estudios iniciales con el inhibidor de SGLT2 dapagilfozin [27] son prometedores. Además, se hace hincapié en un control adecuado de la frecuencia cardiaca, que puede complementarse con ivabradina si los betabloqueantes no son eficaces. Si el tratamiento farmacológico no es suficiente, puede estar indicada la terapia de resincronización cardiaca.
FANEF: La terapia de la FANEF sigue siendo un reto. Hasta el momento, no existen buenas terapias basadas en pruebas para las que se pueda demostrar un éxito terapéutico. El reciente ensayo PARAGON-HF (valsartán frente a Entresto) tampoco logró un criterio de valoración primario significativo [23]. Básicamente, con el estado actual de los conocimientos para la terapia de la rigidez ventricular izquierda y la disfunción diastólica, se recomienda la optimización del control de la presión arterial y una terapia diurética intensiva para controlar el equilibrio de volumen. La amiloidosis cardiaca también debe descartarse en presencia de IC-FEM.
Regurgitación mitral funcional: Si la regurgitación mitral funcional está presente debido a la dilatación de las cavidades cardiacas izquierdas, no sólo se asocia a un aumento de la mortalidad [4], sino que también debe considerarse como una posible causa de HP. Se ha demostrado una mejora significativa de la hemodinámica en pacientes con IC-FEr tras la reparación de la válvula mitral [6]. No obstante, es importante señalar que los pacientes con hipertensión pulmonar presentan mayores tasas de mortalidad con las intervenciones de clip mitral [24].
Dispositivo de asistencia ventricular izquierda (DAVI): El DAVI también debe mencionarse brevemente aquí, ya que es una opción de tratamiento en la IC-FEr avanzada. Al aumentar la eyección ventricular izquierda, se descarga el VI, con el objetivo de normalizar la hemodinámica. En el 30% de todos los pacientes con HP fija (es decir, componente vascular pulmonar), el uso de DAVI e inotrópicos antes del trasplante de corazón dio lugar a la normalización de la hemodinámica pulmonar [2].
Sensor de presión implantable – CardioMEMS: Mediante el uso de sensores de presión implantables se ha podido demostrar que la descompensación “hemodinámica” se produce unas 2-3 semanas antes de la descompensación clínica. La monitorización selectiva de la presión pulmonar mediante CardioMEMS consiguió reducir significativamente la tasa de hospitalizaciones en pacientes con IC-FEp y FC-FEr mediante intervenciones farmacológicas tempranas (diuréticos) [1].
Terapia específica de la HP: Las terapias existentes para la HP (antagonistas de los receptores de endotelina (ARE), prostanoides, inhibidores de la fosfodiesterasa-5 (inhibidores de la PDE-5), estimuladores de la guanilato ciclasa soluble (sGC)) no están aprobadas para la HP-LHD. Incluso en las directrices actuales, el tratamiento dirigido de la HP no suele recomendarse para los pacientes con HP-LHD (III-C) [7].
No obstante, en casos seleccionados, si existe un componente vascular pulmonar significativo con un aumento marcado de la RVP, puede intentarse un ensayo terapéutico con medicación específica para la HP (recomendación IIa-C). Estas consideraciones se basan principalmente en pequeñas series de casos y datos de registros sobre el inhibidor de la PDE-5 sildenafilo, que ha demostrado reducir la RVP y mejorar la función ventricular derecha en pacientes con CpcPH [9,10,14,26] y en los resultados del registro europeo Compera [18]. El motivo es que la IPAH rara concomitante (cebra) puede estar presente junto con la insuficiencia cardiaca común (caballo).
Por el contrario, existen varios ensayos aleatorizados de gran tamaño que han mostrado resultados neutros o incluso un empeoramiento de los resultados con terapias dirigidas para la HAP en pacientes no seleccionados con insuficiencia ventricular izquierda sin un componente significativo de HP. Puede encontrar un resumen de los estudios recientemente finalizados y en curso en los comentarios del reciente simposio mundial de PH [25]. La mayor crítica a los estudios realizados hasta ahora es la falta de una diferenciación hemodinámica clara, ya que se ha incluido sobre todo a pacientes con IpcPH y en parte también a pacientes con IC-FE sin HP. Se cree que un efecto deletéreo de la medicación para la HP en pacientes con HP postcapilar aislada se debe al intento de vasodilatación pulmonar por efecto del fármaco con el consiguiente aumento del flujo sanguíneo pulmonar, que puede provocar edema pulmonar y descompensación cardiaca en pacientes con presiones de llenado elevadas en el lado izquierdo preexistentes.
En resumen, en los pacientes con HP poscapilar aislada (HPpc), la terapia dirigida de la HP no debe utilizarse e incluso puede ser perjudicial. Los pacientes con CpcPH que puedan beneficiarse de una terapia deben ser remitidos a un centro de HP donde puedan ser evaluados por expertos y tratados, idealmente en ensayos.
Mensajes para llevarse a casa
- La hipertensión pulmonar en la cardiopatía izquierda (HP-LHD) es frecuente y en la mayoría de los casos se debe a una elevación pasiva de la presión causada por el aumento de las presiones de llenado del lado izquierdo.
- Si se sospecha un componente precapilar/enfermedad vascular pulmonar, debe realizarse una evaluación adicional mediante cateterismo cardíaco derecho.
- La terapia específica de la hipertensión pulmonar puede ser considerada por el experto del centro de hipertensión pulmonar en pacientes con componentes precapilares significativos, ya que la diferenciación de la hipertensión arterial pulmonar idiopática rara puede ser difícil en este caso.
Literatura:
- Abraham WT, Stevenson LW, Bourge RC, et al: Eficacia sostenida de la presión arterial pulmonar para guiar el ajuste del tratamiento de la insuficiencia cardiaca crónica: resultados del seguimiento completo del ensayo aleatorizado CHAMPION. Lancet 387: 453-461, 2016.
- Al-Kindi SG, Farhoud M, Zacharias M, et al: Dispositivos de asistencia ventricular izquierda o inotrópicos para disminuir la resistencia vascular pulmonar en pacientes con hipertensión pulmonar incluidos en la lista para un trasplante de corazón. Revista de insuficiencia cardiaca 23: 209-215, 2017.
- Assad TR, Maron BA, Robbins IM, et al: Efecto pronóstico y evaluación hemodinámica longitudinal de la hipertensión pulmonar limítrofe. JAMA Cardiology 2: 1361-1368, 2017.
- Bursi F, Barbieri A, Grigioni F, et al: Implicaciones pronósticas de la regurgitación mitral funcional según la gravedad de la insuficiencia cardiaca crónica subyacente: un estudio de resultados a largo plazo. 12: 382-388, 2010.
- Douschan P, Kovacs G, Avian A, et al: Elevación leve de la presión arterial pulmonar como predictor de mortalidad. 197: 509-516, 2018.
- Gaemperli O, Moccetti M, Surder D, et al: Cambios hemodinámicos agudos tras la reparación percutánea de la válvula mitral: relación con los resultados a medio plazo. 98: 126-132, 2012.
- Galie N, Humbert M, Vachiery JL, et al: 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension: The Joint Task Force for the Diagnosis and Treatment of Pulmonary Hypertension of the European Society of Cardiology (ESC) and the European Respiratory Society (ERS): Avalado por: Asociación Europea de Cardiología Pediátrica y Congénita (AEPC), Sociedad Internacional de Trasplante de Corazón y Pulmón (ISHLT). Revista europea del corazón 37: 67-119, 2016.
- Ghio S, Gavazzi A, Campana C, et al: Valor pronóstico independiente y aditivo de la función sistólica ventricular derecha y la presión arterial pulmonar en pacientes con insuficiencia cardiaca crónica. Revista del Colegio Americano de Cardiología 37: 183-188, 2001.
- Guazzi M, Vicenzi M, Arena R, Guazzi MD: Hipertensión pulmonar en la insuficiencia cardiaca con fracción de eyección preservada: objetivo de la inhibición de la fosfodiesterasa-5 en un estudio de 1 año. Circulation 124: 164-174, 2011.
- Hoendermis ES, Liu LC, Hummel YM, et al: Efectos del sildenafilo sobre la hemodinámica invasiva y la capacidad de ejercicio en pacientes con insuficiencia cardiaca con fracción de eyección preservada e hipertensión pulmonar: un ensayo controlado aleatorizado. Revista europea del corazón 36: 2565-2573, 2015.
- Kovacs G, Avian A, Pienn M, et al: Lectura de los trazados de presión vascular pulmonar. Cómo manejar los problemas de la nivelación cero y las oscilaciones respiratorias. Revista americana de medicina respiratoria y de cuidados críticos 190: 252-257, 2014.
- Kovacs G, Herve P, Barbera JA, et al: Una declaración oficial de la Sociedad Respiratoria Europea: hemodinámica pulmonar durante el ejercicio. La revista respiratoria europea 50: 2017.
- Lam CS, Roger VL, Rodeheffer RJ, et al: Hipertensión pulmonar en la insuficiencia cardiaca con fracción de eyección preservada: un estudio comunitario. Revista del Colegio Americano de Cardiología 53: 1119-1126, 2009.
- Lewis GD, Shah R, Shahzad K, et al: El sildenafilo mejora la capacidad de ejercicio y la calidad de vida en pacientes con insuficiencia cardiaca sistólica e hipertensión pulmonar secundaria. Circulation 116: 1555-1562, 2007.
- Luscher TF: Embolia pulmonar e hipertensión pulmonar: dos cuestiones a menudo olvidadas en cardiología. Revista europea del corazón 36: 581-583, 2015.
- Maron BA, Hess E, Maddox TM, et al: Association of Borderline Pulmonary Hypertension With Mortality and Hospitalization in a Large Patient Cohort: Insights From the Veterans Affairs Clinical Assessment, Reporting, and Tracking Program. Circulation 133: 1240-1248, 2016.
- Miller WL, Grill DE, Borlaug BA: Características clínicas, hemodinámica y resultados de la hipertensión pulmonar debida a insuficiencia cardiaca crónica con fracción de eyección reducida: hipertensión pulmonar e insuficiencia cardiaca. JACC Insuficiencia cardiaca 1: 290-299, 2013.
- Opitz CF, Hoeper MM, Gibbs JS, et al: Hipertensión pulmonar precapilar, combinada y poscapilar: un continuo fisiopatológico. Revista del Colegio Americano de Cardiología 68: 368-378, 2016.
- Ponikowski P, Voors AA, Anker SD, et al.: 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Desarrollado con la contribución especial de la Asociación de Insuficiencia Cardiaca (HFA) de la ESC. Eur J Heart Fail 18: 891-975, 2016.
- Rosenkranz S, Gibbs JS, Wachter R, et al: Insuficiencia cardiaca ventricular izquierda e hipertensión pulmonar. Revista europea del corazón 37: 942-954, 2016.
- Rosenkranz S, Kramer T, Gerhardt F, et al: Pulmonary hypertension in HFpEF and HFrEF: Pathophysiology, diagnosis, treatment approaches. Corazón 2019.
- Shah AM, Shah SJ, Anand IS, et al: Estructura y función cardiaca en la insuficiencia cardiaca con fracción de eyección preservada: resultados basales del estudio ecocardiográfico del ensayo Tratamiento de la insuficiencia cardiaca con función cardiaca preservada con un antagonista de la aldosterona. Circulation Heart failure 7: 104-115, 2014.
- Solomon SD, McMurray JJV, Anand IS, et al: Inhibición de la angiotensina-neprilisina en la insuficiencia cardiaca con fracción de eyección preservada. The New England journal of medicine 2019.
- Tigges E, Blankenberg S, von Bardeleben RS, et al: Implicación de la hipertensión pulmonar en pacientes sometidos a terapia MitraClip: resultados del registro alemán de intervenciones transcatéter sobre la válvula mitral (TRAMI). 20: 585-594, 2018.
- Vachiery JL, Tedford RJ, Rosenkranz S, et al: Hipertensión pulmonar debida a cardiopatía izquierda. Revista respiratoria europea 53: 2019.
- Wu X, Yang T, Zhou Q, Li S, Huang L: Uso adicional de un inhibidor de la fosfodiesterasa 5 en pacientes con hipertensión pulmonar secundaria a insuficiencia cardiaca sistólica crónica: un metaanálisis. Eur J Heart Fail 16: 444-453, 2014.
- www.escardio.org/The-ESC/Press-Office/Press-releases/dapagliflozin-reduces-death-and-hospitalisation-in-patients-with-heart-failure, consultado por última vez el 03/09/2019).
CARDIOVASC 2019; 18(6): 11-15











