En Suiza, alrededor del 32% de todas las mujeres embarazadas padecen una carencia de hierro que, junto con la anemia resultante, puede provocar complicaciones para la madre y el niño. Existen preparados de hierro orales e intravenosos para el tratamiento. El objetivo es evitar posibles transfusiones con los correspondientes riesgos para la madre y el niño con una terapia oportuna y adecuada de la carencia de hierro.
Como oligoelemento esencial, es necesario suministrar hierro al cuerpo humano desde el exterior en cualquier momento de la vida. Sin embargo, la necesidad varía según el sexo y la etapa de la vida, informa el Prof. Olav Lapaire, MD, Jefe Adjunto del Departamento. Jefe de obstetricia en la clínica ginecológica del Hospital Universitario de Basilea. El embarazo y el puerperio aumentan la necesidad de hierro, por lo que la ingesta de hierro recomendada de 30 y 20 mg/d es significativamente superior a los 15 mg/d recomendados para las mujeres en edad fértil [2]. Estas mayores necesidades se deben a la demanda adicional de hierro por parte del feto, la placenta y la expansión del volumen eritrocitario durante el embarazo. Si no se trata, la carencia de hierro desemboca con el tiempo en una anemia ferropénica, que sigue afectando al 7% de las mujeres embarazadas en Suiza. Tras el parto, cerca del 33% de las parturientas padecen anemia [1].
Diagnóstico
El primer paso en el diagnóstico es una historia clínica y un examen físico detallados. A continuación se toma una muestra de sangre. En este sentido, la Sociedad Suiza de Ginecología y Obstetricia (SGGG) ha definido los criterios de diagnóstico en el embarazo en su carta de expertos nº 48 del siguiente modo [1]: Existe una carencia de hierro a partir de un valor de ferritina de <30 μg/l. En lo que respecta a la anemia ferropénica, la Sociedad sigue los valores fijados por la Organización Mundial de la Salud (OMS): ferritina <30 μg/l y hemoglobina (Hb) de <110 g/l o refiriéndose a las recomendaciones del Centro de Control de Enfermedades (CDC), la anemia se presenta en el segundo trimestre a partir de un valor de Hb de <105 g/l. Es difícil establecer comparaciones internacionales o aplicar los resultados de estudios internacionales a la práctica suiza en este ámbito, ya que el valor de corte de la ferritina en el embarazo no está definido de manera uniforme a escala internacional. El valor límite de ferritina en otros países ya es <15 μg/l. Esta falta de homogeneidad en el diagnóstico dificulta la extracción de conclusiones sobre la prevalencia global o la interpretación de las intervenciones, afirma el Dr. Lapaire.
En Suiza, se recomienda el cribado de la carencia de hierro como parte de la atención prenatal regular. El mejor momento para dicho examen es cuando la mujer embarazada se presenta regularmente a la prueba del primer trimestre entre las 11 0⁄7 y las 13 6⁄7 semanas de embarazo (SSW), dijo el ponente. En esta presentación, normalmente ya se extrae sangre para la determinación de los diversos parámetros serológicos que se comprueban rutinariamente en el embarazo, por lo que la determinación de la ferritina y la Hb pueden añadirse sin más. Dado que la ferritina es también una proteína de fase aguda, se recomienda la determinación simultánea de la proteína C reactiva (PCR) para excluir en la medida de lo posible valores falsamente elevados.
Se aplican otros valores de referencia para el diagnóstico de la anemia posparto. Aquí se habla ya de anemia a partir de un valor de Hb <120 g/l. Suele formarse sobre la base de una carencia de hierro preexistente a la que se añade una pérdida de sangre periparto. No se recomienda una determinación del valor de ferritina directamente después del parto. En cuanto a su función como proteína de fase aguda, la ferritina puede ser falsamente demasiado alta o falsamente normal hasta seis semanas después del nacimiento.
Además de la anemia asociada a la infección, existen otras consideraciones de diagnóstico diferencial en el estudio de la anemia. La carta de expertos de la SGGG menciona como ejemplos la deficiencia de sustratos como la vitamina B12 o la deficiencia de ácido fólico y las hemoglobinopatías. La combinación de anemia, ferritina normal a elevada e índices eritrocitarios alterados puede proporcionar indicaciones iniciales de posibles diagnósticos diferenciales. En caso de sospecha de los diagnósticos mencionados, se requiere una mayor clarificación y, si es necesario, un régimen terapéutico adaptado. Sin embargo, la anemia ferropénica representa la mayor proporción de anemias en el embarazo.
Síntomas y riesgos
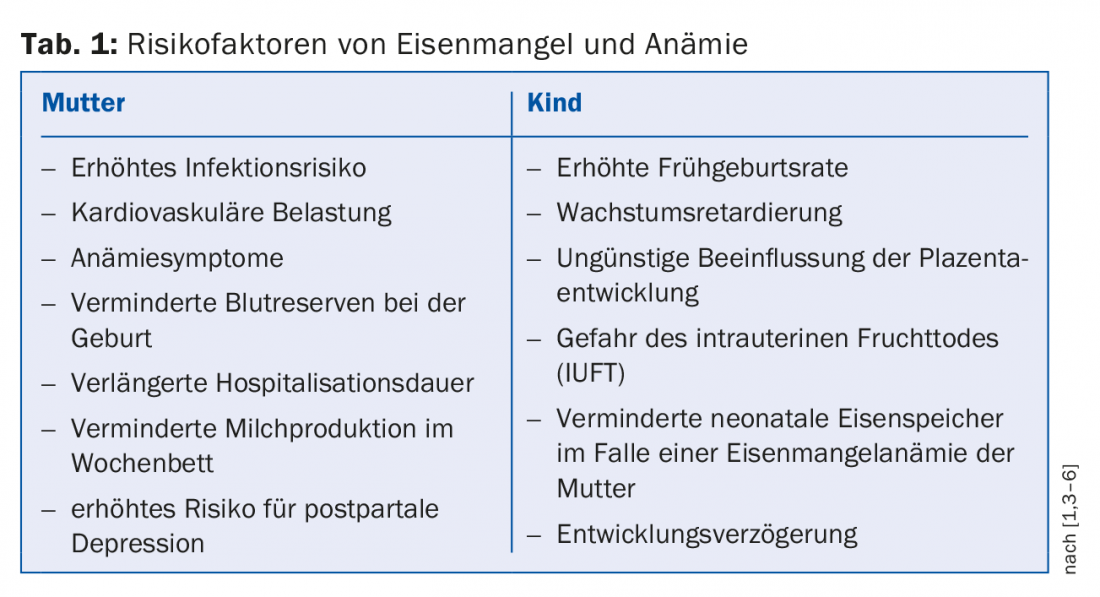
La carencia de hierro puede manifestarse a través de diversos síntomas inespecíficos. A veces estas molestias también se describen sin anemia acompañante. A saber: menor rendimiento, dolores de cabeza, fatiga, agotamiento, sensibilidad al frío y un mayor riesgo de desarrollar depresión. Si se añade anemia, pueden intensificarse los síntomas mencionados o aparecer disnea, mareos, palidez, uñas quebradizas o rágades en las comisuras de los labios, angina de pecho, palpitaciones o parestesia en las piernas, etc. ocurrir. Para aliviar estos síntomas, que los pacientes suelen encontrar angustiosos, está indicada la administración de suplementos de hierro una vez confirmado el diagnóstico. Además de los síntomas clínicos, también es importante minimizar los posibles riesgos de carencia de hierro y anemia ferropénica en el embarazo y el posparto. Aquí se hace una distinción entre los factores maternos y los infantiles, que se enumeran en la tabla 1 .
Terapia
Como opción terapéutica para remediar la carencia de hierro, se dispone básicamente de la administración oral o la administración intravenosa (i.v.) de un preparado de hierro. La SGGG recomienda la sustitución oral con sales de hierro II o polimaltosas de hierro III en una dosis de 160-200 mg/día en casos de anemia leve durante el embarazo (valor de Hb 90-110 g/l o 90-105 g/l en el 2º trimestre ) o con un valor de ferritina de <30 μg/l sin anemia al inicio del embarazo. El éxito de la terapia debe comprobarse al cabo de dos a cuatro semanas. Si el valor de Hb no ha aumentado al menos 10 g/l después de 14 días, si el preparado oral no se toleró debido a efectos secundarios gastrointestinales frecuentes o si no se tomó, existe una anemia avanzada con una Hb < 90 g/l o si hay presión de tiempo debido al avance del embarazo o a riesgos de hemorragia, se recomienda cambiar a terapia intravenosa. La terapia intravenosa también se aconseja más comúnmente para ciertas comorbilidades, como la enfermedad inflamatoria intestinal, que impiden la absorción enteral del hierro.
En el puerperio, la anemia leve se define como niveles de Hb entre 95-120 g/l, para los que se recomienda la administración peroral de hierro (80-200 mg de sales de hierro II o polimaltosa de hierro III). Si el valor de hemoglobina desciende por debajo de 95 g/l, si no se tolera bien la administración oral o si existen otras contraindicaciones para la sustitución oral, en este caso también está indicado pasar a la administración i.v.
Terapia intravenosa
Existen varios preparados para la terapia con hierro intravenoso. Desde el lanzamiento de los primeros productos que contenían dextrano, las nuevas soluciones de infusión sin dextrano han mejorado la tolerabilidad y reducido significativamente el riesgo de reacciones anafilácticas [7]. Del mismo modo, la derivación de la absorción enteral reduce los efectos secundarios gastrointestinales [8] y permite la posibilidad de ampliar la terapia a poblaciones de pacientes con comorbilidades que son una contraindicación para la terapia oral. El Dr. Lapaire sigue las recomendaciones de la SGGG y nombra la carboximaltosa de hierro (Ferinject) como preparado de primera elección para la sustitución intravenosa de hierro tanto en el embarazo como en el posparto. Esta recomendación se basa en los resultados de estudios clínicos. Breymann et al. pudieron demostrar que, en comparación con la terapia de primera línea de hierro administrado por vía oral, la carboximaltosa de hierro conducía a la corrección de la anemia en un número significativamente mayor de mujeres embarazadas en un tiempo más corto y con una mejor calidad de vida [8]. En comparación con el también disponible sacarato de hierro (Venofer), se ha podido demostrar que su perfil de efectos secundarios es comparativamente bajo [9,10]. Otros estudios demostraron que la administración del preparado también es segura para el recién nacido durante la lactancia [11] y que la carboximaltosa férrica no puede atravesar la barrera placentaria [12]. Una ventaja adicional de la carboximaltosa férrica es también que puede administrarse en dosis de hasta 1000 mg, mientras que la dosis única máxima de sacarato ferroso es de 200 mg. Con Ferinject, pueden evitarse las costosas dosis individuales múltiples. El preparado está aprobado a partir del segundo trimestre y debe ajustarse al peso previo al embarazo. Como sigue existiendo un riesgo residual de reacción anafiláctica incluso con carboximaltosa férrica, el fabricante recomienda que el preparado sólo se administre en instalaciones en las que se pueda tener a punto todo el equipo de reanimación. Debido a la posible decoloración de la piel a largo plazo, debe tenerse especial cuidado para evitar la extravasación. La administración de sustitutivos de hierro debe cuestionarse críticamente o rechazarse, por ejemplo, en presencia de inflamación aguda, indicios de daño hepático o riesgos de sobrecarga de hierro. En resumen, al igual que con todos los fármacos administrados durante el embarazo, debe realizarse una evaluación detallada de los riesgos y beneficios antes de iniciar la terapia con hierro intravenoso.
Si la madre ha perdido más sangre en torno al parto, por ejemplo en el contexto de una hemorragia periparto (HPP), además de la administración de preparados de hierro se puede recurrir a la administración adicional de eritropoyetina (rhEPO) o, en caso de anemia sintomática, a la administración de sangre ajena. Sin embargo, el objetivo de una terapia oportuna y adecuada de la ferropenia es evitar posibles transfusiones y los riesgos asociados.
Fuente:10ª Academia del Hierro, 1 de junio de 2017, Zúrich
Literatura:
- Sociedad Suiza de Ginecología y Obstetricia: Diagnóstico y terapia de la anemia ferropénica en el embarazo y el posparto. Carta de Expertos nº 48 (sustituye al nº 22) 2017.
- Deutsche Gesellschaft für Ernährung e.V.: Eisen. 2017. www.dge.de/wissenschaft/referenzwerte/eisen/
- Allen LH: Anemia y deficiencia de hierro: efectos sobre el resultado del embarazo. Am J Clin Nutr 2000; 71(5 Suppl): 1280S-1284S.
- Lelic M, et al: Influencia de la anemia materna durante el embarazo en la placenta y los recién nacidos. Med Arch 2014; 68(3): 184-187.
- Akhter S, et al: Efecto de la anemia materna en el resultado fetal. Mymensingh Med J 2010; 19(3): 391-398.
- Radlowski EC, Johnson RW: Deficiencia perinatal de hierro y desarrollo neurocognitivo. Front Hum Neurosci 2013; 7: 585.
- Cançado RD, Muñoz M: Terapia con hierro intravenoso: ¿hasta dónde hemos llegado? Rev Bras Hematol Hemoter 2011; 33(6): 461-469.
- Breymann C, et al.: Ferric carboxymaltose vs. oral iron in the treatment of pregnant women with iron deficiency anemia: an international, open-label, randomized controlled trial (FER-ASAP). J Perinat Med 2016; pii: /j/jpme.ahead-of-print/jpm-2016-0050/jpm-2016-0050.xml.
- Christoph P, et al: Tratamiento con hierro intravenoso en el embarazo: comparación de altas dosis de carboximaltosa férrica frente a sacarosa de hierro. J Perinat Med 2012; 40(5): 469-474.
- Pfenniger A, et al.: Seguridad y eficacia de altas dosis intravenosas de hierro carboximaltosa frente a hierro sacarosa para el tratamiento de la anemia posparto. J Perinat Med 2012; 40(4): 397-402.
- Bailie GR: Eficacia y seguridad de la carboximaltosa férrica en la corrección de la anemia ferropénica: una revisión de ensayos controlados aleatorizados en diferentes indicaciones. Investigación sobre fármacos 2010; 60(6a): 386-398.
- Malek A: Estudios in vitro de la carboximaltosa férrica sobre la permeabilidad placentaria utilizando el modelo de perfusión dual de la placenta humana. Investigación sobre fármacos 2010; 60(6a): 354-361.
PRÁCTICA GP 2017; 12(7): 36-38











