La tercera causa más común de muerte por enfermedad cardiovascular es la embolia pulmonar aguda. La determinación de los dímeros D es muy sensible en la exclusión de la embolia pulmonar aguda. Hoy en día se utiliza la angiografía por TC para realizar el diagnóstico. Tras la estratificación del riesgo, se elige la estrategia de tratamiento. Los pacientes de alto riesgo requieren una terapia agresiva, mientras que los de bajo riesgo pueden ser tratados como pacientes ambulatorios. La duración de la anticoagulación depende de la presencia de factores provocadores, del riesgo de hemorragia y de cualquier indicio de coagulación persistentemente activada tras la interrupción de la anticoagulación. De los nuevos anticoagulantes, el rivaroxaban está aprobado en Suiza como profilaxis de la recaída.
Las embolias pulmonares son la tercera causa más frecuente de muerte por enfermedades cardiovasculares, después del infarto de miocardio y la lesión cerebrovascular. En los estudios de registro, la mortalidad a los 90 días se sitúa entre el 8,6-17% [1, 2]. Los factores de riesgo de una mortalidad elevada son la edad >70 años, la enfermedad tumoral, la insuficiencia cardiaca, la enfermedad pulmonar obstructiva crónica (EPOC), la hipertensión arterial, la taquipnea y la hipocinesia ventricular derecha en la ecocardiografía.
La hipertensión pulmonar tromboembólica crónica se encuentra en el 2-4% de los pacientes tras una embolia pulmonar aguda. Esta afección se define como una presión arterial pulmonar media superior a 25 mmHg que persiste más de 6 meses después del diagnóstico de embolia pulmonar aguda [3].
Diagnóstico
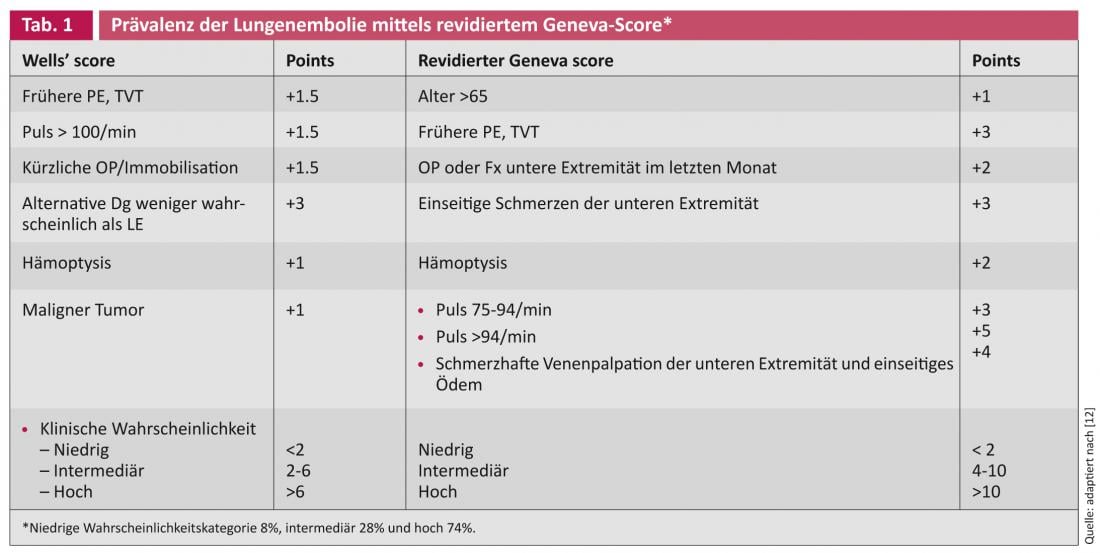
Los pacientes con sospecha de embolia pulmonar aguda deben clasificarse en niveles de sospecha alto (60-80%), intermedio (20-30%) o bajo (5-10%) en función de la situación clínica. Si la probabilidad es baja, una prueba de dímero D normal es suficiente para descartarlo. Los pacientes con probabilidad media y alta requieren anticoagulación hasta que se disponga de los resultados. El historial, los síntomas, la saturación de oxígeno y el ECG son necesarios para evaluar la probabilidad. Puede hacerse de forma empírica o mediante puntuaciones de puntos: la puntuación de Wells y la puntuación de Ginebra revisada son bien conocidas [4].
Dímero D
El dímero D es un producto de degradación de la fibrina reticulada y se eleva en los episodios tromboembólicos venosos agudos. Analizada mediante ELISA cuantitativo o pruebas turbidimétricas automatizadas, la determinación del dímero D es muy sensible (>95%) para descartar una embolia pulmonar aguda. En pacientes con baja probabilidad clínica y dímeros D negativos, el riesgo a los 3 meses de un acontecimiento tromboembólico es muy bajo, en torno al 0,1%. Sin embargo, la especificidad de los dímeros D no es muy alta, especialmente en pacientes con alta probabilidad clínica, pacientes asignados por otras razones, >personas de 65 años y mujeres embarazadas. Los umbrales de dímero D ajustados a la edad podrían aumentar la significación, pero siguen siendo necesarias validaciones prospectivas.
Por ejemplo, un estudio internacional demostró una mejor discriminación por D-dímeros en pacientes mayores de 50 años y con baja probabilidad clínica con un valor de corte de (edad del paciente x10) µg/l frente al fijo de 500 µg/l [5].
Angiografía por TC
La angiografía por TC multidetector es más sensible que la angiografía por TC monodetector y ha sustituido en gran medida a la gammagrafía pulmonar de ventilación y perfusión. Debe tenerse en cuenta el riesgo de radiación, especialmente en mujeres embarazadas; en estas pacientes, las ventajas de la angio-TC sobre la gammagrafía pulmonar siguen siendo controvertidas.
Angiografía convencional
La angiografía pulmonar convencional sigue siendo el patrón oro para el diagnóstico de la embolia pulmonar. Debido a su carácter invasivo, este método sólo debe utilizarse en pacientes en los que no pueda confirmarse una sospecha de alto grado o en los que se planifique una terapia endovascular.
Tratamiento
Debe evaluarse el pronóstico de los pacientes con embolia pulmonar aguda; para ello puede utilizarse el índice de gravedad de la embolia pulmonar o su versión simplificada según la clínica [6].
Para la terapia de las embolias pulmonares agudas, deben observarse los siguientes puntos:
– Pacientes de alto riesgo:
- aprox. 5% de todos los pacientes sintomáticos
- Mortalidad en la fase aguda del 15%
- debe tratarse de forma agresiva mediante trombólisis, quirúrgicamente o cateterismo [7].
– Pacientes de bajo riesgo:
- La mayoría de los pacientes
- Mortalidad en la fase aguda de aproximadamente el 1%.
- Puede tratarse como paciente hospitalizado de corta estancia o incluso como paciente ambulatorio
– Riesgo intermediario:
- Afecta a cerca del 30% de los pacientes sintomáticos
- Tratamiento hospitalario
- Beneficio poco claro con respecto a la trombolisis
La ecocardiografía, las mediciones de troponina o el péptido natriurético pro-cerebro (pro-BNP) pueden afinar la estratificación del riesgo, pero la rentabilidad aún no está clara.
Un estudio multicéntrico realizado en Suiza, Francia, Bélgica y EE.UU. no mostró diferencias significativas en las tasas de recurrencia y hemorragia en comparación con el tratamiento hospitalario en pacientes con embolia pulmonar sintomática aguda, bajo riesgo de mortalidad (clase de riesgo I o II del índice de gravedad de la embolia pulmonar) y tratamiento ambulatorio con enoxaparina subcutánea durante al menos 5 días seguida de antagonistas de la vitamina K [8].

En la fase aguda, se dispone de heparina no fraccionada, heparinas de bajo peso molecular (HBPM), fondaparinux y, más recientemente, rivaroxaban.
Las heparinas actúan uniéndose al anticoagulante natural antitrombina, lo que provoca una inactivación masiva y acelerada de la trombina por la antitrombina. Debido a las grandes diferencias individuales en la unión de la heparina a las proteínas plasmáticas, la dosis debe controlarse y ajustarse mediante pruebas de coagulación. Esto puede hacerse utilizando aPTT, tiempo de trombina, actividad anti-FXa.
La principal ventaja de la administración subcutánea de HNM es la dosis fija adaptada al peso, en la mayoría de los casos sin necesidad de monitorización. El mecanismo de acción es el mismo que el de la heparina no fraccionada, pero con un efecto más fuerte también sobre el FXa. La equivalencia clínica de la heparina no fraccionada y la NMH se demostró en un estudio [9]. El fondaparinux, un pentasacárido sintético, a una dosis de 7,5 mg/día es equivalente a la heparina no fraccionada y al NMH en pacientes con embolia pulmonar.
El NMH y el fondaparinux se excretan predominantemente por el riñón, por lo que se recomienda precaución en caso de insuficiencia renal con un aclaramiento <30 ml/min. En tal situación, existen como alternativas la reducción de la dosis, intervalos más largos, la medición de la actividad anti-FXa o el uso de heparina no fraccionada . Los pacientes con enfermedad tumoral maligna deben ser tratados con NMH durante al menos 3 meses. Al cambiar a un antagonista de la vitamina K, el solapamiento con NMH o heparina no fraccionada debe durar al menos 5 días y suspenderse tras alcanzar un INR de 2,0.
Todos los anticoagulantes pueden provocar hemorragias. Las hemorragias graves asociadas a los antagonistas de la vitamina K aumentan con la edad. Hoy en día, existen puntuaciones clínicas validadas para evaluar el riesgo de hemorragia (puntuación RIETE, puntuación HEMORR2HAGES).
Al elegir la duración de la anticoagulación, debe sopesarse el riesgo de recurrencia tromboembólica frente al riesgo de hemorragia bajo anticoagulación. Las 8ª directrices de consenso de la ACCP recomiendan en general una terapia de al menos 3 meses. Esto es especialmente cierto para los pacientes con un acontecimiento provocado en los que el factor provocador se ha eliminado entretanto. En pacientes con eventos idiopáticos, se puede hablar de terapia prolongada si la evaluación beneficio-riesgo es positiva. En los tumores malignos, la anticoagulación debe continuar hasta que el tumor esté controlado o curado. En los últimos años se ha buscado un enfoque individualizado. Por ejemplo, un estudio con medición de los dímeros D 4 semanas después de interrumpir la anticoagulación mostró que es posible la estratificación del riesgo; bajo riesgo con dímeros D normales, sin necesidad de más terapia, o alto riesgo (15% de recurrencias después de 18 meses) con dímeros D elevados con la recomendación de continuar la anticoagulación durante otros 12 meses [10].
Hay varios anticoagulantes nuevos en desarrollo o ya aprobados. Estos inhibidores directos, independientes de la antitrombina, del FXa (rivaroxaban, apixaban) o de la trombina (dabigatran) pueden sustituir a las heparinas y a los antagonistas de la vitamina K en muchos pacientes. Estos fármacos se administran en una dosis fija y normalmente no requieren un control de la coagulación. El ensayo Einstein PE demostró que el rivaroxaban a la dosis estándar (2×15 mg durante 3 semanas seguido de 20 mg 1x/d) no era inferior a la enoxaparina seguida de antagonistas de la vitamina K durante 3, 6 ó 12 meses. Se produjeron hemorragias significativamente menos graves con la misma tasa de recurrencia [11]. Sin embargo, hasta ahora sólo se ha aprobado en Suiza el rivaroxaban, y únicamente para la prevención de la embolia pulmonar recurrente.
Conclusión para la práctica
- Si se sospecha que se trata de una embolia pulmonar aguda, se procede a un esclarecimiento ulterior sobre la base de una evaluación de la probabilidad clínica.
- Los dímeros D tienen una sensibilidad y un valor predictivo negativo elevados y pueden excluir la embolia pulmonar aguda con una probabilidad clínica baja.
- Para el tratamiento, los pacientes se dividen en grupos de riesgo; los pacientes de alto riesgo necesitan un tratamiento agresivo rápidamente, los pacientes de bajo riesgo pueden ser tratados como pacientes ambulatorios.
- El tratamiento es con heparinas (no fraccionadas o NMH) seguidas de antagonistas de la vitamina K; ninguna de las nuevas sustancias está aprobada actualmente en Suiza para el tratamiento agudo de la embolia pulmonar, pero puede administrarse profilaxis de la recurrencia con rivaroxaban.
Dr. Thomas Lehmann
Prof. Dr. med. Wolfgang Korte
Literatura:
- Goldhaber SZ, et al: Embolia pulmonar aguda: resultados clínicos en el Registro Cooperativo Internacional de Embolia Pulmonar (ICOPER). Lancet 1999;353:1386-1389.
- Laporte S, et al: Predictores clínicos de embolia pulmonar mortal en 15 520 pacientes con tromboembolia venosa: resultados del Registro Informatizado de la Enfermedad Tromboembólica venosa (RIETE). Circulation 2008;117:1711–1716.
- Piazza G, Goldhaber SZ: Hipertensión pulmonar tromboembólica crónica. N Engl J Med 2011;364:351-360.
- Ceriani E, et al: Reglas de predicción clínica de la embolia pulmonar: revisión sistemática y metaanálisis. J Thromb Haemost 2010;8:957-970.
- Douma RA, et al: Potencial de un valor de corte del dímero D ajustado a la edad para mejorar la exclusión de la embolia pulmonar en pacientes de edad avanzada: un análisis retrospectivo de tres grandes cohortes. BMJ 2010;340:c1475.
- Torbicki A, et al: Guidelines on the diagnosis and management of acute pulmonary embolism: the Task Force for the Diagnosis and Management of Acute Pulmonary Embolism of the European Society of Cardiology (ESC). Eur Heart J 2008;29:2276-2315.
- Kucher N, et al: Embolia pulmonar masiva. Circulation 2006;113:577-582.
- Aujesky D, et al: Tratamiento ambulatorio frente al hospitalario para pacientes con embolia pulmonar aguda: un ensayo internacional, abierto, aleatorizado y de no inferioridad. The Lancet 2011;378:41-48.
- Simonneau G, et al: Comparación de la heparina de bajo peso molecular con la heparina no fraccionada para la embolia pulmonar aguda. N Engl J Med 1997;337:663-669.
- Palareti G, et al: Prueba del dímero D para determinar la duración del tratamiento anticoagulante. N Engl J Med 2006;355:1780-1789.
- Büller HR, et al: Rivaroxaban oral para el tratamiento de la embolia pulmonar sintomática. N Engl J Med 2012;366:1287-97.
- Le Gal G, et al: Predicción de la embolia pulmonar en urgencias: la puntuación de Ginebra revisada. Ann Intern Med. 2006;144:165-171.