La hipertensión pulmonar tromboembólica crónica (HPTEC) es un subtipo de hipertensión pulmonar (HP). El diagnóstico es muy poco frecuente en general, aunque la HPTEC también suele no reconocerse y, por tanto, infradiagnosticarse, por lo que el número de casos no declarados es probablemente mayor.
La hipertensión pulmonar tromboembólica crónica (HPTEC) es un subtipo de hipertensión pulmonar (HP), de clase 4 según la clasificación ESC/ERC [1]. El diagnóstico de HPTEC puede realizarse cuando se presenta HP sintomática precapilar (mPAP mínima de 20-25 mmHg y presión de oclusión capilar pulmonar ≤15 mmHg) combinada con alteraciones de la perfusión en los pulmones tras un mínimo de 3 meses de anticoagulación fiable [2] para diferenciarla de la embolia pulmonar aguda (EP). El diagnóstico es muy poco frecuente en general, aunque la HPTEC a menudo no se reconoce y, por tanto, se infradiagnostica, y el número de casos no declarados es probablemente mayor.
Este artículo presenta el diagnóstico y el tratamiento de la HPTEC con el objetivo de sensibilizar a los médicos generalistas y también a los colegas especialistas sobre esta afección, ya que existe una terapia curativa para estos pacientes, todo lo contrario que para las demás formas de HP.
Incidencia, factores de riesgo y patogénesis
La incidencia anual de la HPTEC en EE.UU., Europa y Japón es de aproximadamente 3 a 5 casos por cada 100.000 habitantes [2]. La incidencia acumulada de HPTEC en los 2 primeros años tras un LE agudo oscila entre el 0,1 y el 9,1% [2–10], un amplio rango; en el caso de Suiza, incluso un estudio informó de sólo un 0,79% [11]. Para empeorar las cosas, más del 25% de los casos recién diagnosticados no tienen antecedentes de LE agudo [12]. Existen otros factores de riesgo conocidos, además de los acontecimientos tromboembólicos, como los trastornos autoinmunes y hematológicos [13], la presencia de una derivación ventriculoauricular o de electrodos de estimulación infectados, antecedentes de esplenectomía, grupo sanguíneo no 0, presencia de anticuerpos anticoagulantes/antifosfolípidos lúpicos, terapia de sustitución de hormonas tiroideas y antecedentes de tumores [14], que también son desfavorables desde el punto de vista pronóstico.
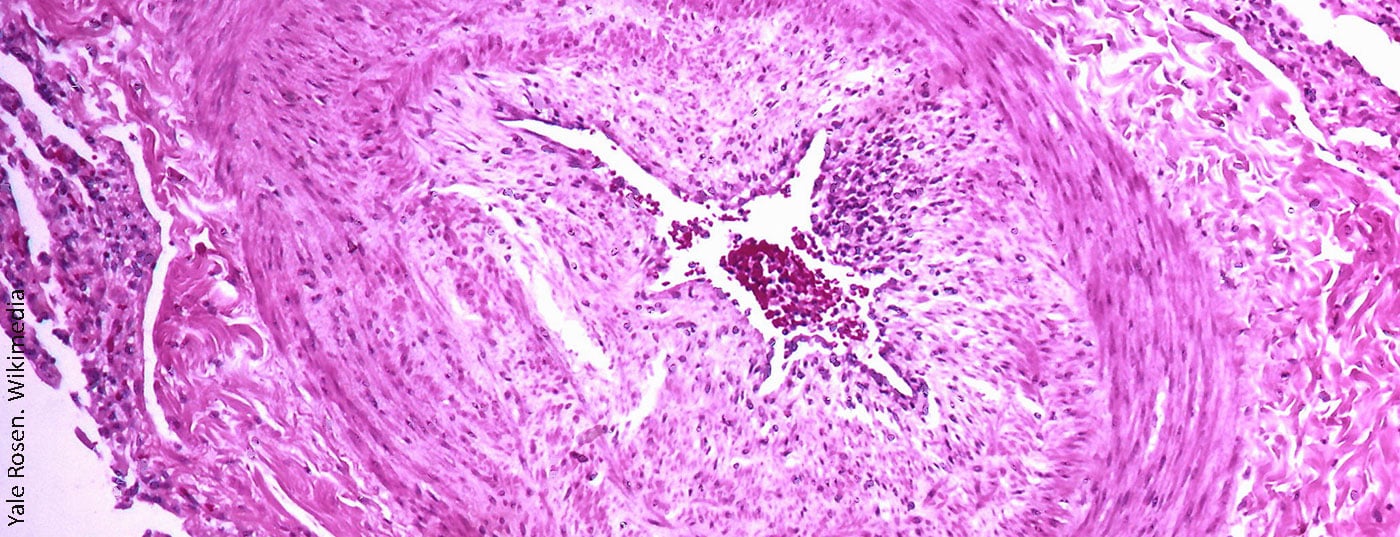
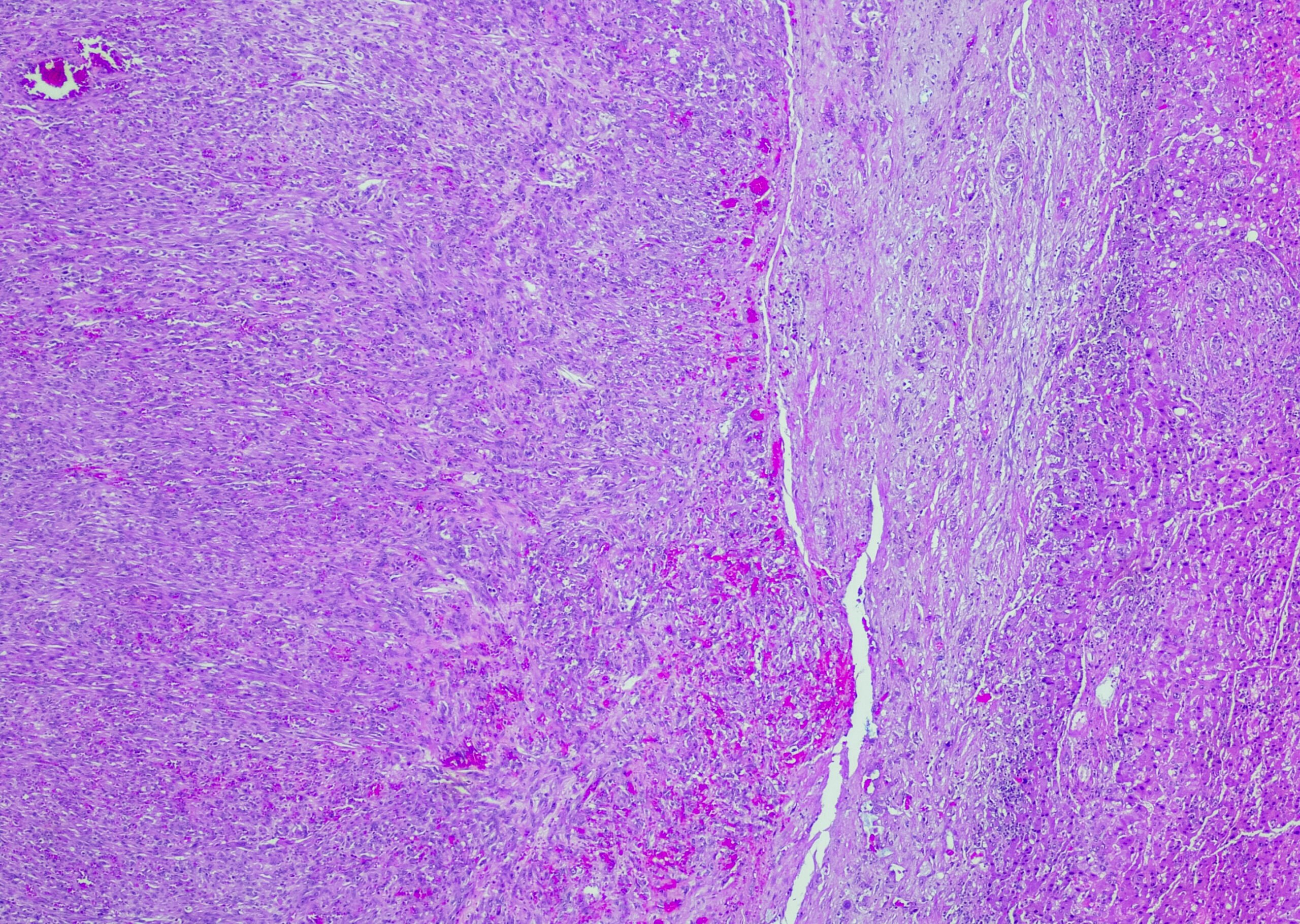
La fisiopatología exacta de la HPTEC es compleja, sigue sin estar clara y es probable que existan múltiples mecanismos causales, como trombos organizados persistentes y cicatrices en las arterias pulmonares proximales (principales, lobulares y segmentarias) y/o microangiopatía [15]. Se han asociado diversos procesos a la resolución incompleta del trombo [16]: inflamatorios [17–19], factores genéticos [20–22], anomalías de la fibrinólisis [23–27] y muchos otros [28].
Cuadro clínico y descripción del caso
El cuadro clínico siempre incluye disnea de esfuerzo, el síntoma principal [29,30]. Otros síntomas incluyen fatiga en cerca del 30% de los casos, dolor torácico en el 15%, un episodio de síncope en cerca del 14% y hemoptisis en el 5% [12,31,32]. Todos estos síntomas no son infrecuentes, especialmente en pacientes de edad avanzada con comorbilidades adicionales como la enfermedad pulmonar obstructiva crónica, el desacondicionamiento y, a menudo, la obesidad asociada [33,34]. Para empeorar las cosas, aproximadamente la mitad de los pacientes con LE agudo declaran una disnea persistente, incluso años después del episodio, lo que se denomina “síndrome post-PE”. No obstante, estos pacientes deben someterse a un trabajo diagnóstico adicional para excluir la HPTEC.
El examen clínico revela un edema progresivo de las extremidades inferiores y otros signos de congestión (venas del cuello, agrandamiento del hígado) [33]. Además, en la auscultación puede detectarse una acentuación del componente pulmonar del segundo ruido cardiaco.
Diagnóstico
Desgraciadamente, hasta la fecha no existe ningún biomarcador que diferencie claramente la HPTEC de otras formas de HP, se han estudiado algunos marcadores inflamatorios circulantes (por ejemplo la PCR, las interleucinas -6, -8 y -10) [17,18,35], pero ninguna de estas pruebas tiene un uso rutinario hasta la fecha. El ECG muestra signos de distensión ventricular derecha, como bloqueo de rama derecha (in)completo o negatividades de la onda T en las derivaciones anteriores V1-V4 (“patrón de distensión ventricular derecha”). En la radiografía de tórax sólo hay signos inespecíficos de sobrecarga cardiaca derecha, con un ventrículo y una aurícula derechos agrandados, por ejemplo.
En los diagnósticos posteriores, suele utilizarse en primer lugar la ecocardiografía transtorácica (ETT), que también figura en la conferencia de consenso de 2016 como la primera medida diagnóstica del algoritmo diagnóstico (Fig. 1). También es una buena primera prueba de detección cuando se distingue del síndrome post-PE. La hipertensión pulmonar se define en la ETT por la expresión de la velocidad de regurgitación tricuspídea [36], a partir de la cual puede medirse la sPAP. A partir de la medición asistida por Doppler de la velocidad de regurgitación (Vmax) a través de la válvula tricúspide, se estima el gradiente de presión entre el ventrículo derecho y la aurícula derecha mediante la ecuación simplificada de Bernoulli (∆P=4×Vmax2). La presión de la aurícula derecha suele aproximarse por la anchura y la variabilidad respiratoria de la vena cava inferior. Otros signos son el tamaño y la dilatación del ventrículo derecho y las aurículas, una “forma en D” del tabique y el movimiento del plano tricúspide (“excursión sistólica del plano anular tricúspide”, TAPSE). Sin embargo, una eco normal no descarta la HPTEC.
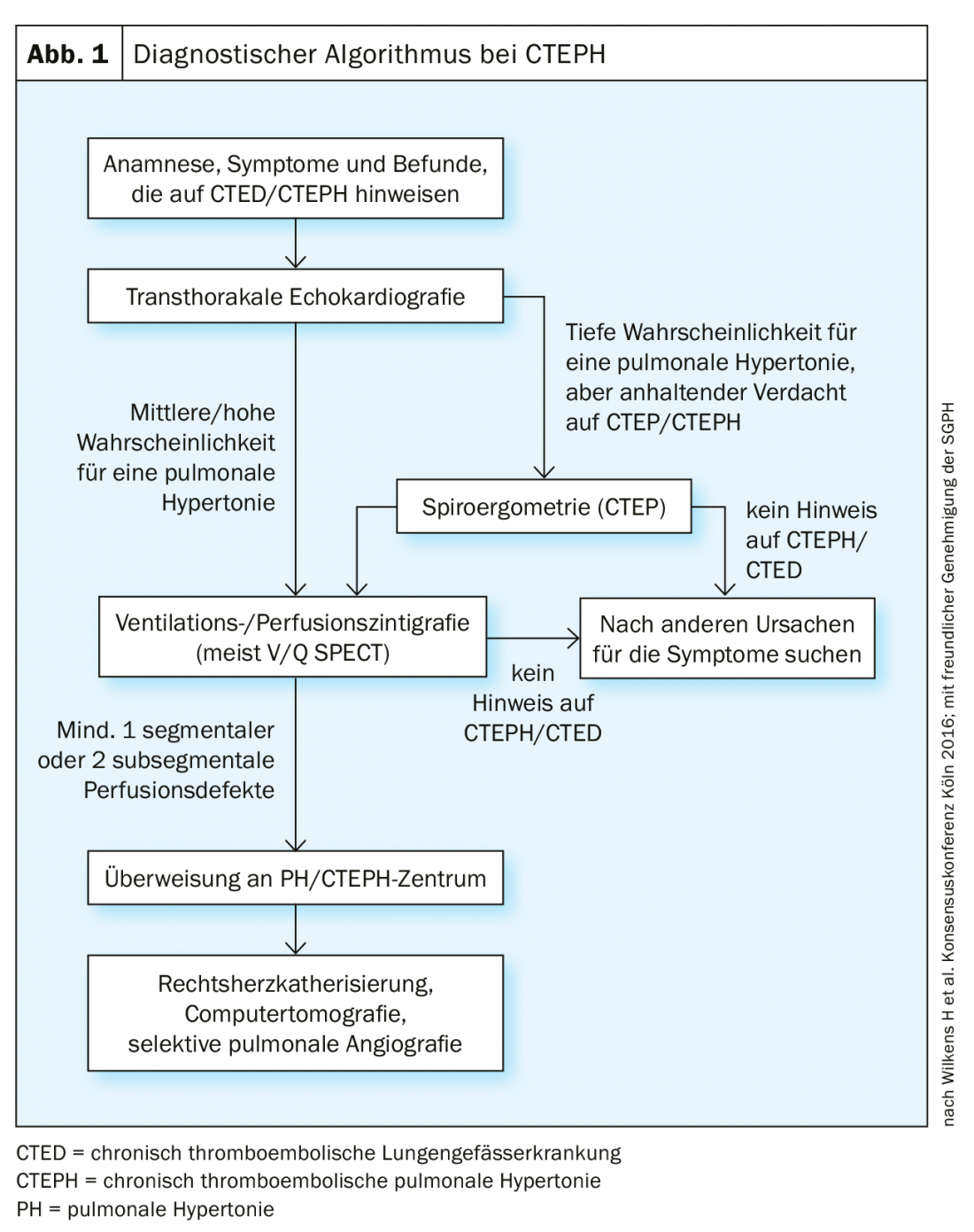
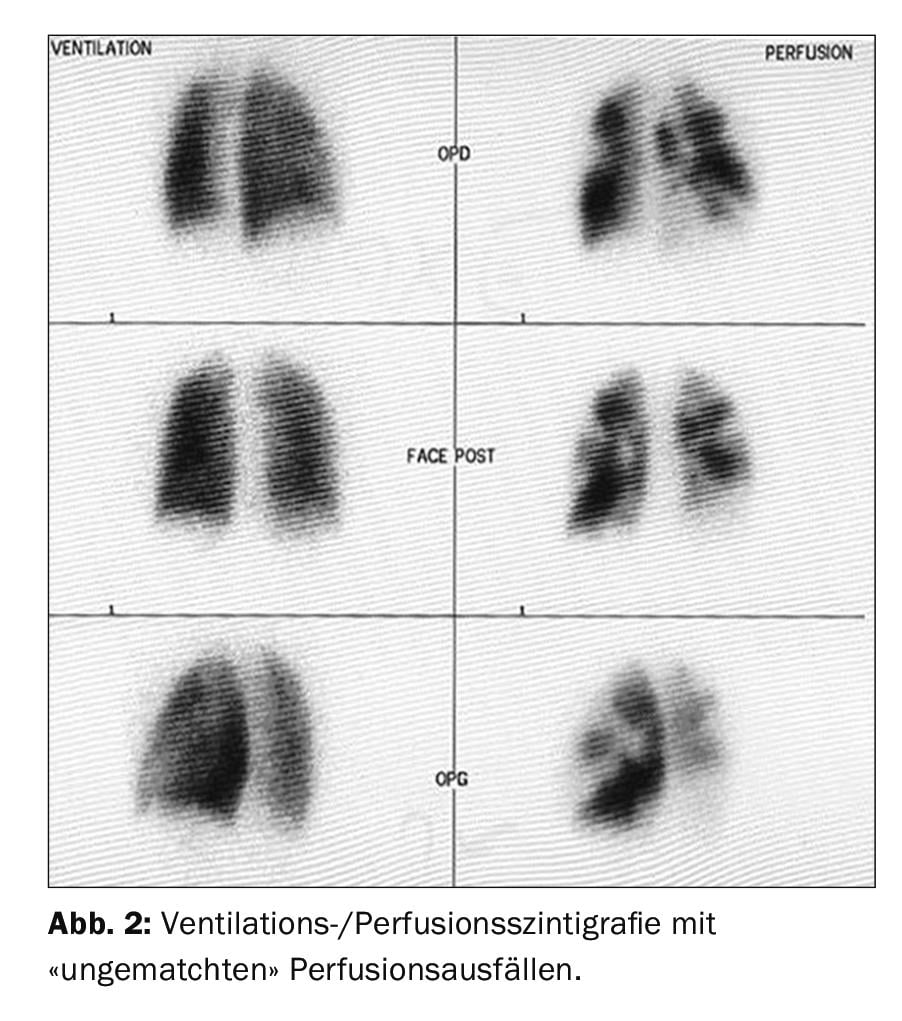
El primer método de cribado por imagen es la gammagrafía de ventilación/perfusión (Fig. 2), que, si es normal (es decir, sin déficits de perfusión “no coincidentes”), puede utilizarse para descartar la HPTEC con una sensibilidad del 90-100% y una especificidad del 94-100% [37,38]. Las nuevas técnicas de “doble energía” con una combinación híbrida de SPECT y TC tienen la ventaja de obtener imágenes simultáneas del parénquima pulmonar además de los déficits de perfusión [39,40], pero no están disponibles en todos los hospitales.
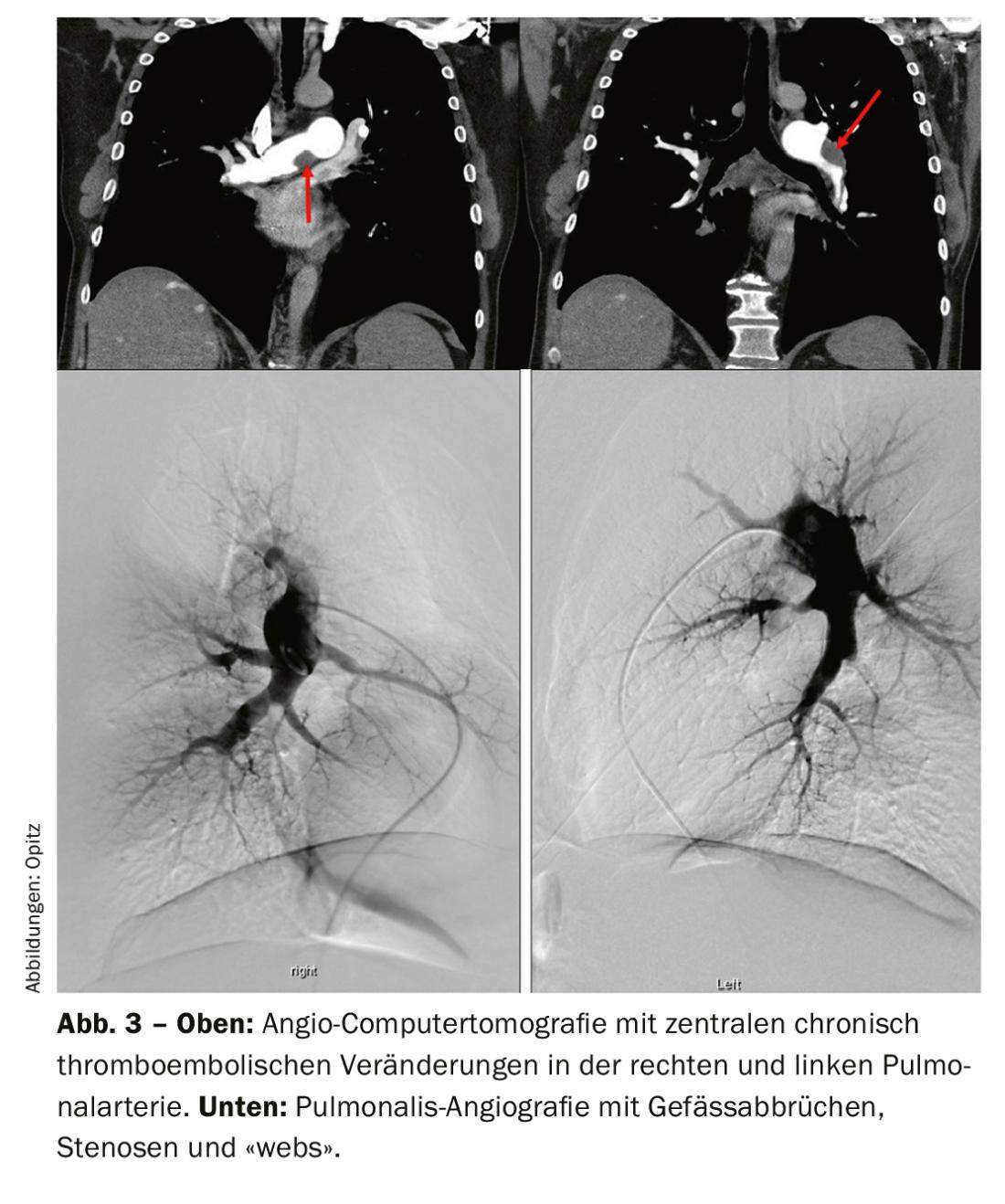
La angiografía pulmonar por tomografía computarizada (APTC) tiene muchas ventajas en el diagnóstico y también en la evaluación de la operabilidad de la HPTEC. En concreto, tiene sensibilidad y especificidad para detectar cambios tromboembólicos a nivel lobar (97-100% y 95-100%, respectivamente), y algo menor a nivel segmentario más periférico (86-100 y 93-99%, respectivamente) [33,41–43]. Los signos clásicos son los trombos excéntricos (Fig. 3 más arriba), las llamadas “telarañas” y las “lesiones en bolsa” oclusivas, así como las colaterales pronunciadas de las arterias intercostales, por ejemplo. Todos estos signos pueden observarse también en la angiografía pulmonar (Fig. 3 abajo), que también tiene la ventaja de la medición invasiva de la presión de la AP. Sin embargo, en la TC pueden detectarse otros diagnósticos diferenciales (DD), así como signos de “perfusión en mosaico” y posiblemente infartos en el parénquima pulmonar. Otra ventaja es la representación de la accesibilidad de los cambios tromboembólicos crónicos a la hora de identificar lo proximal que se presenta una capa de disección y si es accesible para la endarterectomía pulmonar. Para poder interpretarlas, se necesitan reconstrucciones en el plano sagital y también coronario, además del corte axial, y el TAC debería haberse realizado con un grosor de corte de 1 mm. La resonancia magnética (RM) aún no ha desempeñado un papel en el diagnóstico de la HPTEC en una aplicación estandarizada; sin embargo, el registro simultáneo de la función ventricular derecha es una ventaja y en el futuro se espera que la RM desempeñe un papel cada vez mayor para el cribado, pero también, si es necesario, para el seguimiento de los pacientes con HPTEC tras la cirugía u otro tratamiento.
La confirmación hemodinámica de la HPTEC se realiza mediante un cateterismo cardíaco derecho: La presión arterial pulmonar media (PAPm) debe ser ≥20-25 mmgHg [1] y la presión precapilar (“presión en cuña”/presión de oclusión capilar pulmonar ≤15 mmHg). La obtención del gasto cardiaco mediante termodilución o el método directo de Fick es un requisito previo para el cálculo correcto de la resistencia vascular pulmonar (RVP), un factor importante en relación con el pronóstico y el riesgo quirúrgico [44].
La espiroergometría representa un examen funcional más en la delimitación de la HPTEC: Aquí se revelan los signos típicos del desajuste ventilación-perfusión con un aumento de los equivalentes respiratorios en el umbral anaeróbico, un aumento del gradiente alveo-arterial de pO2, un gradiente capilar positivo de CO2 al final de la marea, una hipoxemia inducida por el ejercicio y una capacidad de ejercicio claramente reducida [45–48].
Es especialmente importante que, si se sospecha de HPTEC, se remita al paciente a un centro especializado para un diagnóstico interdisciplinar y la asignación de la terapia.
A continuación se describe un caso clásico con toda la historia de la paciente:
Un paciente de 50 años con antecedentes de múltiples émbolos pulmonares y eventos tromboembólicos se presenta con dificultad respiratoria NYHA III-IV. En la prueba de marcha de 6 minutos, la paciente alcanzó los 270 metros en el Borg 2 (tab. 1).
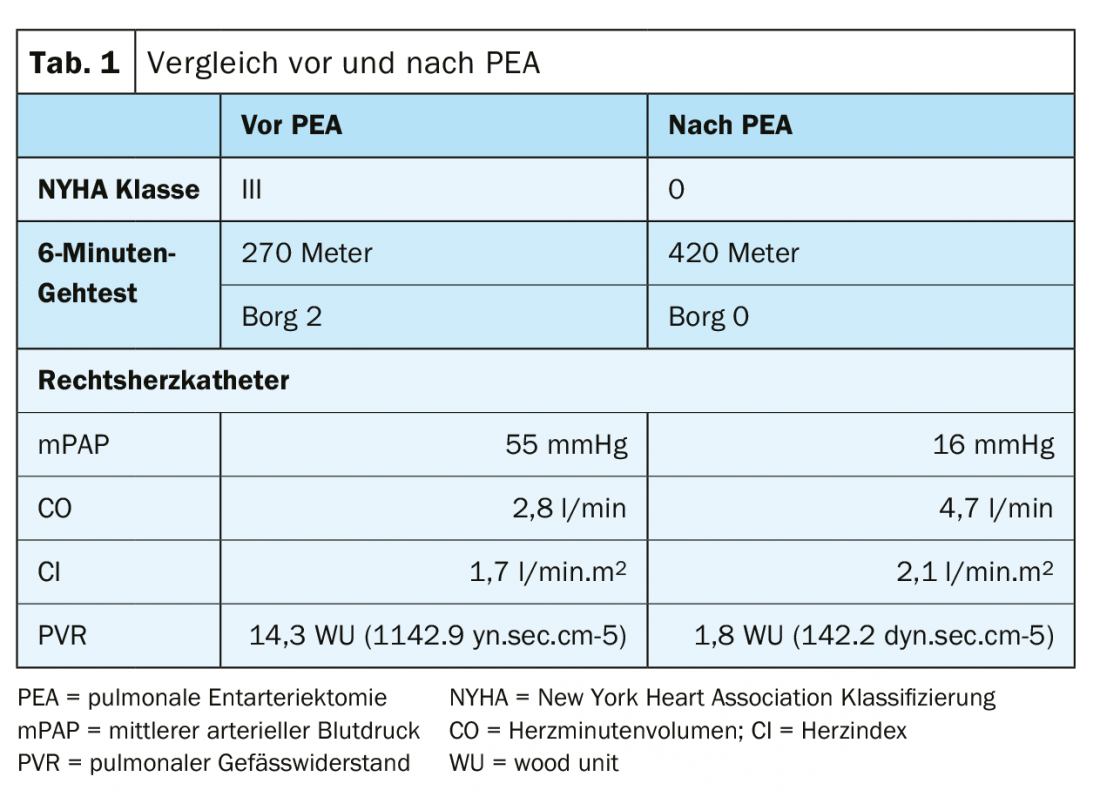
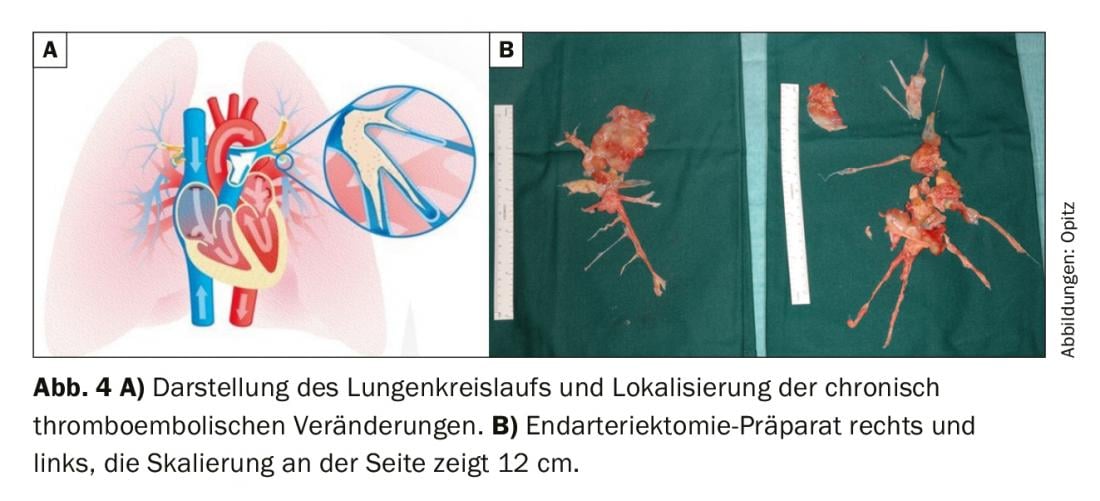
La gammagrafía de ventilación/perfusión mostró defectos de perfusión bilaterales “no coincidentes” (fig. 2) . La ecocardiografía transtorácica muestra una presión arterial pulmonar sistólica (PAPs) elevada y un ventrículo derecho dilatado. El TAC muestra lesiones centrales (Fig. 3 arriba), que se extirparon a la periferia en la entarterectomía pulmonar (Fig. 4B) . En el postoperatorio, la paciente se recuperó rápidamente y presentó una hemodinámica normal y una NYHA 0 en el seguimiento de 1 año (tab. 1).
Previsión
Una vez diagnosticada, el tratamiento debe plantearse de inmediato, ya que sin tratamiento, una mPAP de >50 mmgHg tiene una mortalidad a los 2 años de >80% y una mPAP de >30 mmgHg se asocia a una mortalidad a los 3 años del 90% [49].
Desde 2015, en el Hospital Universitario de Zúrich (USZ) se ofrece un programa interdisciplinar de HPTEC que ofrece todo el espectro de tratamiento, desde la cirugía hasta la angioplastia y la terapia farmacológica. Una o dos veces al mes, se ofrece una junta nacional de HPTEC a través de la Sociedad Suiza de Hipertensión Pulmonar para que los médicos remitentes se pongan en contacto para la presentación y discusión de casos (CTEPH@usz.ch, CTEPH@sgph.ch).
Terapia
Terapia quirúrgica: Según las directrices actuales de la ERS/ESC, se recomienda la endarterectomía pulmonar (EAP) como terapia de primera línea en pacientes con HPTEC accesible quirúrgicamente [1]. (Fig. 4A). En la EEP, las arterias pulmonares se abren secuencialmente (siempre en ambos lados) en el sistema de circulación extracorpórea y en hipotermia profunda (20°C) y el material tromboembólico crónico se extrae en paradas circulatorias de 20 minutos; esto es técnicamente posible hasta bien entrada la periferia (Fig. 4B). La decisión de la intervención quirúrgica y la selección de los pacientes deben ser tomadas siempre por un equipo interdisciplinar de especialistas, formado por especialistas en PH, radiólogos y cirujanos de PEA. [50]. Los factores determinantes de la EAP son: la gravedad de los síntomas, la extensión de la HP, la función del ventrículo derecho, el perfil de comorbilidad del paciente y el material quirúrgicamente accesible. Este último punto en particular es una evaluación difícil, ya que es bien sabido que las imágenes casi siempre subestiman la extensión del material tromboembólico crónico. Los pacientes con enfermedad segmentaria y subsegmentaria también pueden beneficiarse de la EEP con excelentes resultados a corto y largo plazo en centros experimentados [51,52]. Las recomendaciones realizadas durante el Simposio Mundial sobre la HP establecen que debe obtenerse una “segunda opinión” de un centro quirúrgico experto en HPTEC si un paciente ha sido considerado inoperable en un centro no especializado en HPTEC [50]. Asimismo, la gravedad de la HP y la limitación de la disfunción cardiaca derecha no son contraindicaciones per se para la EAP y a los pacientes sintomáticos debe ofrecérseles tratamiento quirúrgico [53]. La edad tampoco es una contraindicación absoluta, ya que los datos muestran que los pacientes >de 70 años se benefician tanto como los más jóvenes [54]. Sin embargo, la mortalidad del procedimiento no es del todo insignificante y en la bibliografía se señala que es del 2,4-13,2%, siendo esta última de periodos anteriores [55].
Una cirugía exitosa puede mejorar significativamente la calidad de vida y la esperanza de los pacientes (tasas de supervivencia del >90% después de 1 año >70%, después de 6 a 10 años [31,55,56]): La disnea, la prueba de la marcha de 6 minutos, así como un aumento de la captación de oxígeno, una mejora del equivalente respiratorio para elCO2 y una menor necesidad de oxígeno pudieron demostrarse [57,58]. Se ha registrado un aumento de la esperanza de vida a medio y largo plazo.
Angioplastia pulmonar con balón (BPA)
Si la cirugía no es una opción, la BPA intervencionista puede tratar los cambios crónicos segmentarios o subsegmentarios periféricos en varias sesiones. Pueden lograrse mejoras convincentes en la hemodinámica, la prueba de la marcha de 6 minutos y la clase NYHA/OMS. Aún faltan datos a largo plazo [59].
Tratamiento farmacológico: Los pacientes con HPTEC distal, no accesible quirúrgicamente e hipertensión pulmonar residual tras la EEP pueden ser tratados con fármacos [50,60]. Se utilizan fármacos similares a los empleados para la HAP [61–64]. Independientemente de la terapia reductora de la presión, que actúa sobre todo en el componente distal de la HPTEC, todo paciente con HPTEC debe ser anticoagulado de por vida, independientemente de otras terapias. Las decisiones terapéuticas sólo deben tomarse tras al menos 3 meses de ACO [1,65]. Actualmente, los pacientes siguen siendo tratados con antagonistas de la vitamina K. Debido a su eficacia comparable y a su buen perfil de seguridad, los NOAK (nuevos anticoagulantes orales) también se utilizan cada vez más, especialmente también en casos de problemas para encontrar la dosis y en los casos en los que el INR (cociente internacional normalizado) suele estar fuera del intervalo objetivo de 2,5-3,5 [65,66].
Mensajes para llevarse a casa
- La hipertensión pulmonar tromboembólica crónica (HPTEC) se define como hipertensión pulmonar sintomática con defectos de perfusión pulmonar persistentes a pesar de una anticoagulación adecuada durante al menos 3 meses.
- Los pacientes con HPTEC deben ser remitidos a un centro especializado en HPTEC para la confirmación del diagnóstico mediante cateterismo cardíaco derecho y la terapia posterior.
- La Sociedad Suiza de Hipertensión Pulmonar ofrece una junta nacional de HPTEC a la que pueden dirigirse los médicos remitentes para la presentación y discusión de casos (CTEPH@usz.ch, CTEPH@sgph.ch).
- La capacidad funcional, la resistencia física y también la esperanza de vida de los pacientes pueden aumentar con la endarterectomía pulmonar. Por esta razón, debe evaluarse una PEA en cualquier caso.
- El tratamiento farmacológico y/o la angioplastia con balón pueden ayudar a los pacientes con HPTEC inoperable o hipertensión pulmonar residual postoperatoria.
- La HPTEC requiere anticoagulación oral obligatoria de por vida.
|
Equipo de CTEPH del Hospital Universitario de Zúrich: |
Literatura:
- Galie N, Humbert M, Vachiery JL, et al: 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension: The Joint Task Force for the Diagnosis and Treatment of Pulmonary Hypertension of the European Society of Cardiology (ESC) and the European Respiratory Society (ERS): Avalado por: Asociación Europea de Cardiología Pediátrica y Congénita (AEPC), Sociedad Internacional de Trasplante de Corazón y Pulmón (ISHLT). La revista respiratoria europea. 2015;46(4): 903-975.
- Gall H, Hoeper MM, Richter MJ, et al: Un análisis epidemiológico de la carga de la hipertensión pulmonar tromboembólica crónica en EE.UU., Europa y Japón. European respiratory review : revista oficial de la Sociedad Respiratoria Europea. 2017;26(143).
- Korkmaz A, Ozlu T, Ozsu S, et al: Resultados a largo plazo en el tromboembolismo pulmonar agudo: incidencia de la hipertensión pulmonar tromboembólica crónica y factores de riesgo asociados. Clin Appl Thromb Hemost. 2012;18(3): 281-288.
- Otero R, Oribe M, Ballaz A, et al: Evaluación ecocardiográfica de la presión arterial pulmonar en el seguimiento de pacientes con embolia pulmonar. Investigación de la trombosis. 2011;127(4): 303-308.
- Poli D, Grifoni E, Antonucci E, et al: Incidencia de tromboembolismo venoso recurrente y de hipertensión pulmonar tromboembólica crónica en pacientes tras un primer episodio de embolia pulmonar. J Thromb Thrombolysis. 2010;30(3): 294-299.
- Surie S, Gibson NS, Gerdes VE, et al: La búsqueda activa de hipertensión pulmonar tromboembólica crónica no parece indicada tras una embolia pulmonar aguda. Investigación de la trombosis. 2010;125(5): e202-205.
- Dentali F, Donadini M, Gianni M, et al: Incidencia de la hipertensión pulmonar crónica en pacientes con embolia pulmonar previa. Investigación de la trombosis. 2009;124(3): 256-258.
- Martí D, Gómez V, Escobar C, et al: Incidencia de la hipertensión pulmonar tromboembólica crónica sintomática y asintomática. Arch Bronconeumol. 2010;46(12): 628-633.
- Klok FA, van Kralingen KW, van Dijk AP, et al: Programa prospectivo de cribado cardiopulmonar para detectar la hipertensión pulmonar tromboembólica crónica en pacientes tras una embolia pulmonar aguda. Haematologica. 2010;95(6): 970-975.
- Noble S, Pasi J: Epidemiología y fisiopatología de la trombosis asociada al cáncer. Br J Cancer. 2010;102 Suppl 1: S2-9.
- Coquoz N, Weilenmann D, Stolz D, et al: Encuesta de cribado observacional multicéntrica para la detección de la HPTEC tras una embolia pulmonar. La revista respiratoria europea. 2018;51(4).
- Pepke-Zaba J, Delcroix M, Lang I, et al: Hipertensión pulmonar tromboembólica crónica (HPTEC): resultados de un registro prospectivo internacional. Circulación. 2011;124(18): 1973-1981.
- Blauwet LA, Edwards WD, Tazelaar HD, McGregor CG: Patología quirúrgica de la tromboendarterectomía pulmonar: estudio de 54 casos entre 1990 y 2001. Hum Pathol. 2003;34(12): 1290-1298.
- Bonderman D, Wilkens H, Wakounig S, et al: Factores de riesgo de la hipertensión pulmonar tromboembólica crónica. La revista respiratoria europea. 2009;33(2): 325-331.
- Kim NH: Grupo 4 Hipertensión pulmonar: Hipertensión pulmonar tromboembólica crónica: Epidemiología, fisiopatología y tratamiento. Cardiol Clin. 2016;34(3): 435-441.
- Simonneau G, Torbicki A, Dorfmuller P, Kim N: La fisiopatología de la hipertensión pulmonar tromboembólica crónica. European respiratory review: revista oficial de la Sociedad Respiratoria Europea. 2017; 26 (143).
- Quarck R, Nawrot T, Meyns B, Delcroix M: Proteína C reactiva: un nuevo predictor de resultados adversos en la hipertensión arterial pulmonar. Revista del Colegio Americano de Cardiología. 2009;53(14): 1211-1218.
- Zabini D, Heinemann A, Foris V, et al: Análisis exhaustivo de los marcadores inflamatorios en pacientes con hipertensión pulmonar tromboembólica crónica. La revista respiratoria europea. 2014;44(4): 951-962.
- Reesink HJ, Meijer RC, Lutter R, et al: Correlatos hemodinámicos y clínicos de la endotelina-1 en la hipertensión pulmonar tromboembólica crónica. Circ J. 2006;70(8): 1058-1063.
- Wolf M, Boyer-Neumann C, Parent F, et al: Factores de riesgo trombótico en la hipertensión pulmonar. La revista respiratoria europea. 2000;15(2): 395-399.
- Bonderman D, Turecek PL, Jakowitsch J, et al: Alta prevalencia de factor VIII de coagulación elevado en la hipertensión pulmonar tromboembólica crónica. Thromb Haemost. 2003;90(3): 372-376.
- Gu S, Su P, Yan J, et al.: Comparación de los perfiles de expresión génica y las vías relacionadas en la hipertensión pulmonar tromboembólica crónica. Int J Mol Med. 2014;33(2): 277-300.
- Lang IM, Dorfmuller P, Vonk Noordegraaf A: La patobiología de la hipertensión pulmonar tromboembólica crónica. Ann Am Thorac Soc. 2016;13 Suppl 3: S215-221.
- Le Gal G, Delahousse B, Lacut K, et al: Fibrinogen Aalpha-Thr312Ala and factor XIII-A Val34Leu polymorphisms in idiopathic venous thromboembolism. Investigación de la trombosis. 2007;121(3): 333-338.
- Suntharalingam J, Goldsmith K, van Marion V, et al: El polimorfismo del fibrinógeno Aalpha Thr312Ala se asocia a la hipertensión pulmonar tromboembólica crónica. La revista respiratoria europea. 2008;31(4): 736-741.
- Marsh JJ, Chiles PG, Liang NC, Morris TA: Las disfibrinogenemias tromboembólicas crónicas asociadas a la hipertensión pulmonar presentan una estructura de fibrina desorganizada. Investigación de la trombosis. 2013;132(6): 729-734.
- Morris TA, Marsh JJ, Chiles PG, et al: Alta prevalencia de disfibrinogenemia entre los pacientes con hipertensión pulmonar tromboembólica crónica. Sangre. 2009;114(9): 1929-1936.
- Opitz I, Kirschner MB: Investigación molecular en hipertensión pulmonar tromboembólica crónica. Int J Mol Sci. 2019;20(3).
- Mayer E, Jenkins D, Lindner J, et al: Tratamiento quirúrgico y resultados de los pacientes con hipertensión pulmonar tromboembólica crónica: resultados de un registro prospectivo internacional. J Thorac Cardiovasc Surg. 2011;141(3): 702-710.
- Held M, Grun M, Holl R, et al.: Hipertensión pulmonar tromboembólica crónica: tiempo transcurrido desde el inicio de los síntomas hasta el diagnóstico y estado clínico en el momento del diagnóstico. Dtsch Med Wochenschr. 2014;139(33): 1647-1652.
- Hoeper MM, Madani MM, Nakanishi N, et al: Hipertensión pulmonar tromboembólica crónica. Lancet Respir Med. 2014;2(7): 573-582.
- Lang IM, Simonneau G, Pepke-Zaba JW, et al: Factores asociados al diagnóstico y la operabilidad de la hipertensión pulmonar tromboembólica crónica. Un estudio de casos y controles. Thromb Haemost. 2013;110(1): 83-91.
- Gopalan D, Delcroix M, Held M. Diagnóstico de la hipertensión pulmonar tromboembólica crónica. European respiratory review: revista oficial de la Sociedad Respiratoria Europea. 2017; 26 (143).
- Fedullo P, Kerr KM, Kim NH, Auger WR: Hipertensión pulmonar tromboembólica crónica. Revista americana de medicina respiratoria y de cuidados críticos. 2011;183(12):1605–1613.
- Quarck R, Wynants M, Verbeken E, et al: Contribución de la inflamación y la angiogénesis alterada a la patobiología de la hipertensión pulmonar tromboembólica crónica. La revista respiratoria europea. 2015;46(2): 431-443.
- Rehman MB, Garcia R, Christiaens L, et al: Potencia de las mediciones ecocardiográficas en reposo para clasificar a los pacientes con hipertensión pulmonar según los puntos de corte de estratificación del riesgo de las pruebas de ejercicio de la Sociedad Europea de Cardiología. Revista internacional de cardiología. 2018;257: 291-297.
- Leblanc M, Leveillee F, Turcotte E: Evaluación prospectiva del valor predictivo negativo de la SPECT V/Q utilizando 99mTc-technegas. Nucl Med Commun. 2007;28(8): 667-672.
- Gruning T, Drake BE, Farrell SL, Nokes T. Experiencia clínica de tres años con VQ SPECT para el diagnóstico de la embolia pulmonar: rendimiento diagnóstico. Clin Imaging. 2014;38(6): 831-835.
- Gutte H, Mortensen J, Jensen CV, et al: Detección de la embolia pulmonar con SPECT de ventilación-perfusión combinada y TC de dosis baja: comparación directa con la angiografía por TC multidetector. J Nucl Med. 2009;50(12): 1987-1992.
- Simanek M, Koranda P: El beneficio de la imagen pulmonar híbrida SPECT/TC personalizada. Am J Nucl Med Mol Imaging. 2016;6(4): 215-222.
- Ley S, Ley-Zaporozhan J, Pitton MB, et al: Rendimiento diagnóstico de las técnicas de imagen más avanzadas para la evaluación morfológica de las anomalías vasculares en pacientes con hipertensión pulmonar tromboembólica crónica (HPTEC). Eur Radiol. 2012;22(3): 607-616.
- Reichelt A, Hoeper MM, Galanski M, Keberle M: Hipertensión pulmonar tromboembólica crónica: evaluación con TC en hilera de 64 detectores frente a angiografía por sustracción digital. Eur J Radiol. 2009;71(1): 49-54.
- Sugiura T, Tanabe N, Matsuura Y, et al: Papel de la TC de 320 cortes en la evaluación diagnóstica de pacientes con hipertensión pulmonar tromboembólica crónica. Pecho. 2013;143(4): 1070-1077.
- Jenkins D, Mayer E, Screaton N, Madani M: Diagnóstico y tratamiento de la hipertensión pulmonar tromboembólica crónica de última generación. European respiratory review: revista oficial de la Sociedad Respiratoria Europea. 2012;21(123): 32-39.
- Scheidl SJ, Englisch C, Kovacs G, et al: Diagnosis of CTEPH versus IPAH using capillary to end-tidal carbon dioxide gradients. La revista respiratoria europea. 2012;39(1): 119-124.
- Held M, Meintz S, Baron S, et al: ¿Curación quirúrgica de la apnea central del sueño? Revista americana de medicina respiratoria y de cuidados críticos. 2013;188(3): 395-396.
- Held M, Grun M, Holl R, et al: Prueba de ejercicio cardiopulmonar para detectar la hipertensión pulmonar tromboembólica crónica en pacientes con ecocardiografía normal. Respiración. 2014;87(5): 379-387.
- Held M, Linke M, Jany B: Ecocardiografía y cateterismo cardíaco derecho en la hipertensión pulmonar. Dtsch Med Wochenschr. 2014;139(30): 1511-1517.
- Lewczuk J, Piszko P, Jagas J, et al: Factores pronósticos en pacientes con embolia pulmonar crónica tratados médicamente. Pecho. 2001;119(3): 818-823.
- Kim NH, Delcroix M, Jenkins DP, et al: Hipertensión pulmonar tromboembólica crónica. Revista del Colegio Americano de Cardiología. 2013;62(25 Suppl): D92-99.
- Madani MM, Auger WR, Pretorius V, et al: Endarterectomía pulmonar: cambios recientes en la experiencia de una única institución con más de 2.700 pacientes. Anales de cirugía torácica. 2012;94(1): 97-103; discusión
- D’Armini AM, Morsolini M, Mattiucci G, et al: Endarterectomía pulmonar para la hipertensión pulmonar tromboembólica crónica distal. J Thorac Cardiovasc Surg. 2014;148(3): 1005-1011; 12 e1-2; discusión 11-2.
- Madani MM: Tratamiento quirúrgico de la hipertensión pulmonar tromboembólica crónica: tromboendarterectomía pulmonar. Methodist Debakey Cardiovasc J. 2016;12(4): 213-218.
- Berman M, Hardman G, Sharples L, et al: Endarterectomía pulmonar: resultados en pacientes de >70. Revista europea de cirugía cardiotorácica : revista oficial de la Asociación Europea de Cirugía Cardiotorácica. 2012;41(6): e154-160.
- Cannon JE, Su L, Kiely DG, et al: Estratificación dinámica del riesgo de los resultados a largo plazo de los pacientes tras una endarterectomía pulmonar: resultados de la cohorte nacional del Reino Unido. Circulación. 2016;133(18): 1761-1771.
- Archibald CJ, Auger WR, Fedullo PF, et al: Resultados a largo plazo tras la tromboendarterectomía pulmonar. Revista americana de medicina respiratoria y de cuidados críticos. 1999;160(2): 523-528.
- Rahnavardi M, Yan TD, Cao C, et al: Tromboendarterectomía pulmonar para la hipertensión pulmonar tromboembólica crónica: una revisión sistemática. Anales de cirugía torácica y cardiovascular: revista oficial de la Asociación de Cirujanos Torácicos y Cardiovasculares de Asia. 2011;17(5): 435-445.
- Condliffe R, Kiely DG, Gibbs JS, et al: Mejora de los resultados en la hipertensión pulmonar tromboembólica crónica tratada médica y quirúrgicamente. Revista americana de medicina respiratoria y de cuidados críticos. 2008;177(10): 1122-1127.
- Mahmud E, Behnamfar O, Ang L, et al: Angioplastia pulmonar con balón para la hipertensión pulmonar tromboembólica crónica. Interv Cardiol Clin. 2018;7(1): 103-117.
- Mayer E: Tratamiento quirúrgico y postoperatorio de la hipertensión pulmonar tromboembólica crónica. European respiratory review: revista oficial de la Sociedad Respiratoria Europea. 2010;19(115): 64-67.
- Moser KM, Bloor CM: Lesiones vasculares pulmonares que se producen en pacientes con hipertensión pulmonar tromboembólica crónica de grandes vasos. Pecho. 1993;103(3): 685-692.
- Ghofrani HA, D’Armini AM, Grimminger F, et al: Riociguat para el tratamiento de la hipertensión pulmonar tromboembólica crónica. The New England journal of medicine. 2013;369(4): 319-329.
- Simonneau G, D’Armini AM, Ghofrani HA, et al: Predictores de resultados a largo plazo en pacientes tratados con riociguat para la hipertensión pulmonar tromboembólica crónica: datos del ensayo CHEST-2 de extensión a largo plazo, aleatorizado y abierto. Lancet Respir Med. 2016;4(5): 372-380.
- Ghofrani HA, Simonneau G, D’Armini AM, et al: Macitentan for the treatment of inoperable chronic thromboembolic pulmonary hypertension (MERIT-1): results from the multicentre, phase 2, randomised, double-blind, placebo-controlled study. Lancet Respir Med. 2017;5(10): 785-794.
- Konstantinides SV, Torbicki A, Agnelli G, et al: Directrices de la ESC de 2014 sobre el diagnóstico y el tratamiento de la embolia pulmonar aguda. Eur Heart J. 2014;35(43): 3033-3069, 69a-69k.
- Konstantinides SV, Torbicki A, Agnelli G, et al: Corrección de errores de: Directrices de la ESC de 2014 sobre el diagnóstico y el tratamiento de la embolia pulmonar aguda. Eur Heart J. 2015;36(39): 2642.
InFo NEUMOLOGÍA Y ALERGOLOGÍA 2020; 2(2): 12-15.