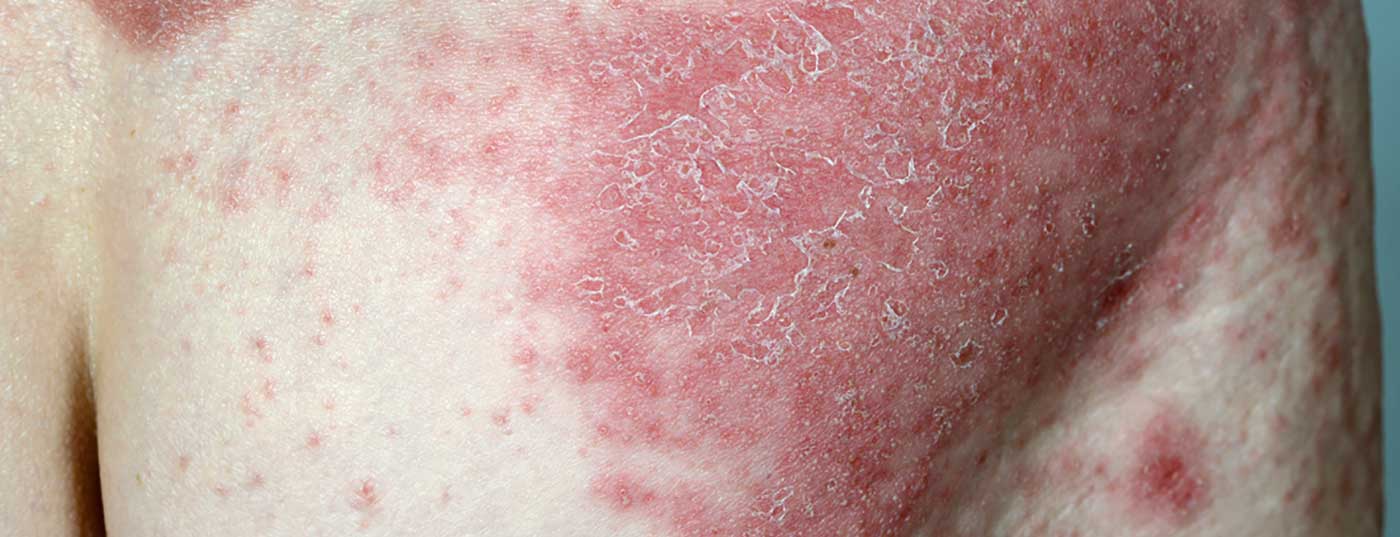
Los datos recientemente publicados del estudio multicéntrico LIBERATE confirman el favorable perfil beneficio-riesgo del apremilast en su uso a largo plazo. Se trata de un avance significativo para las opciones de tratamiento de esta población de pacientes. Esto se debe a que una terapia eficaz y bien tolerada a largo plazo es esencial, especialmente para los cursos moderados y graves de la enfermedad.
Los efectos positivos a largo plazo pudieron reproducirse en varios estudios de evaluación publicados en 2017 y 2018. El inhibidor de la fosfodiesterasa 4 (PDE4), aprobado desde 2015, es por tanto una opción terapéutica muy interesante para los pacientes que requieren un uso prolongado, entre otros.
Perfil beneficio-riesgo favorable
Crowley et al. [1] informó en 2017 de un resultado positivo con el uso del inhibidor oral de la PDE4 apremilast durante un periodo de hasta tres años. Se trata de una réplica y ampliación de los resultados de los estudios multicéntricos de fase III ESTEEM 1 y ESTEEM 2, que demostraron la eficacia y seguridad del apremilast durante un periodo de 52 semanas [2,3].
En 2018, se produjo una nueva réplica de los efectos positivos a largo plazo. El estudio LIBERATE [4] demostró la eficacia y seguridad del apremilast en pacientes sin tratamiento biológico con psoriasis de moderada a grave durante un periodo de 104 semanas (n=226).
Hubo mejoras en la piel, el cuero cabelludo, las uñas, el prurito y la calidad de vida. Apremilast también fue eficaz y seguro 104 semanas después del inicio en pacientes que cambiaron de etanercept a apremilast. El 50,0-59%–59,2% de todos los participantes en el estudio alcanzaron una ScPGA (Scalp Psoriasis Physician’s Global Assessment) de 0 (libre de lesiones) o 1 (casi libre de lesiones). La reducción media del prurito según la EVA (escala analógica visual) fue de -24,4 a -32,3. El cambio medio en el NAPSI (índice de gravedad de la psoriasis ungueal) desde el inicio fue de -48,1% a -51,1%. El 66,0-72,5% de los participantes obtuvieron una puntuación ≤5 en el Índice de Calidad de Vida Dermatológica (DLQI).
La mejora de la calidad de vida influye positivamente en el cumplimiento terapéutico, lo que repercute favorablemente en la evolución de la enfermedad. La frecuencia de acontecimientos adversos (diarrea, náuseas, nasofaringitis, enfermedad respiratoria, dolor de cabeza) no aumentó con el incremento de la duración del tratamiento con apremilast [4].
Beneficio para esta población de pacientes
La psoriasis es una de las enfermedades inflamatorias crónicas más comunes de la piel. En las últimas décadas se han realizado grandes progresos en el campo de la investigación de nuevas opciones terapéuticas. Además de las terapias sistémicas (metotrexato, ciclosporina A, acitretina), la introducción de los anticuerpos monoclonales permitió alcanzar el PASI75 (75% de mejora de los síntomas de la enfermedad). La investigación de otros objetivos condujo a la identificación de nuevas sustancias activas. En 2015, se aprobó el secukinumab, un anticuerpo monoclonal contra la IL-17, para la psoriasis de moderada a grave, que mostró una respuesta PASI puntual y un buen perfil de eficacia en términos de PASI90 y PASI100 (completamente libre de síntomas) para la psoriasis de moderada a grave.
El inhibidor de la fosfodiesterasa 4 (PDE4) apremilast (Otezla®) también está aprobado en Suiza desde 2015 para adultos con psoriasis en placas de moderada a grave si otra terapia sistémica está contraindicada, es intolerable o refractaria. Los inhibidores de la PDE-4 reducen los procesos inflamatorios al regular la concentración de monofosfato de adenosina cíclico (AMPc), un importante modulador de la respuesta inmunitaria. Un aumento de la concentración de AMPc de las células inflamatorias por el inhibidor de la PDE-4 apremilast (Otezla®) provoca una reducción de la liberación de TNF-α, IL-17 e IL-23 y un aumento de la IL-10 antiinflamatoria [5].
En general, la conclusión sobre los objetivos del tratamiento y la adherencia es positiva.
Literatura:
- Crowley J, et al: Seguridad y tolerabilidad a largo plazo del apremilast en pacientes con psoriasis: Análisis conjunto de la seguridad durante ≥156 semanas de 2 ensayos de fase 3, aleatorizados y controlados (ESTEEM 1 y 2). J Am Acad Dermatol 2017; 77(2):310-317.e1. doi: 10.1016/j.jaad.2017.01.052. Epub 2017 abr 14.
- Papp K, et al.: Apremilast, un inhibidor oral de la fosfodiesterasa 4 (PDE4), en pacientes con psoriasis en placas de moderada a grave: resultados de un ensayo de fase III, aleatorizado y controlado (Efficacy and Safety Trial Evaluating the Effects of Apremilast in Psoriasis [ESTEEM 1]). J Am Acad Dermatol 2015; 73: 37-49.
- Paul C, et al: Eficacia y seguridad del apremilast, un inhibidor oral de la fosfodiesterasa 4, en pacientes con psoriasis en placas de moderada a grave durante 52 semanas: un ensayo de fase III, aleatorizado y controlado (ESTEEM 2). Br J Dermatol.2015; 173: 1387-1399.
- Reich K, et al: Seguridad y eficacia del apremilast durante 104 semanas en pacientes con psoriasis moderada a grave que continuaron con apremilast o cambiaron del tratamiento con etanercept: resultados del estudio LIBERATE. J Eur Acad Dermatol Venereol. 2018 Mar;32(3):397-402. doi: 10.1111/jdv.14738.
- Wick-Urban B: Antipsoriásicos. Una comparación de las nuevas terapias. Periódico farmacéutico. Edición 09/2017, 27.02.2017, www.pharmazeutische-zeitung.de/ausgabe-092017/neue-therapien-im-vergleich/, último acceso 09.05.2019.
- Kavanaugh A et al: 5-Year Efficacy and Safety of Apremilast Treatment in Subjects With Psoriatic Arthritis: Pooled Analysis of the PALACE Studies. Póster THU0294 presentado en la EULAR; del 13 al 16 de junio de 2018 en Ámsterdam, Países Bajos.
PRÁCTICA DERMATOLÓGICA 2019; 29(4): 48