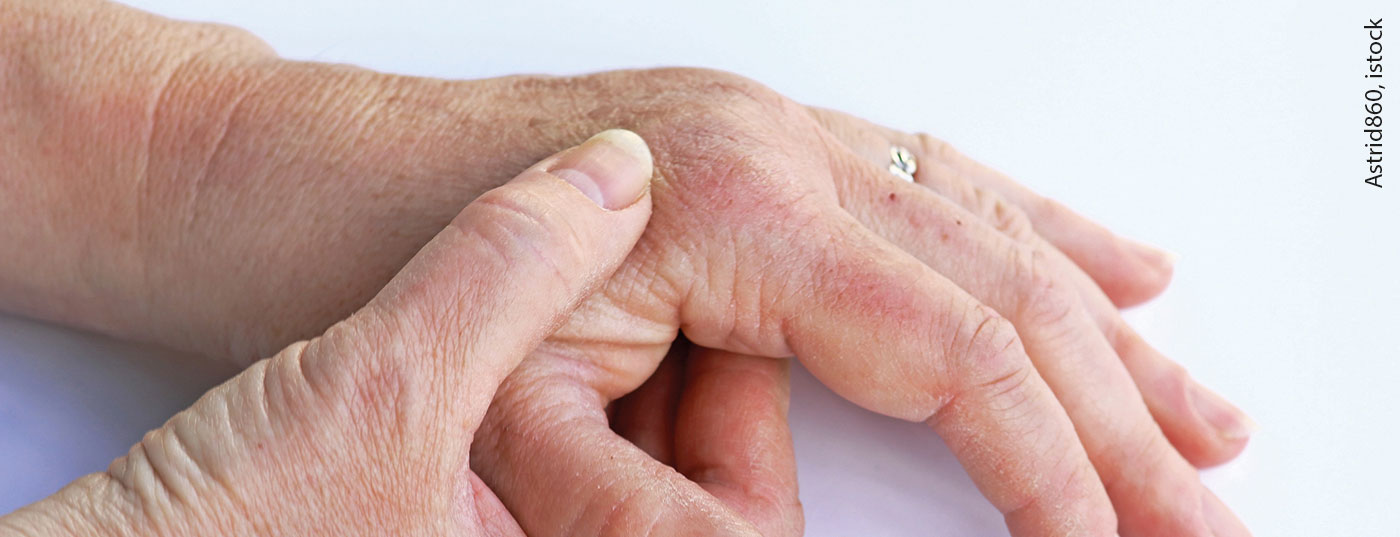
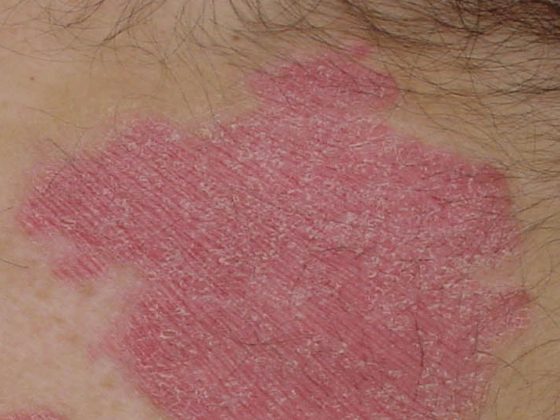
El anticuerpo monoclonal anti-IL-17A ixekizumab ya está aprobado para el tratamiento de la psoriasis en placas de moderada a grave y la artritis psoriásica desde 2016. En 2020, se añadió la espondiloartritis axial (axSpA) como indicación adicional para la que el ixekizumab es una opción terapéutica. Basándose en el programa del estudio COAST, se ha demostrado la eficacia y la tolerabilidad del ixekizumab en la axSpA tanto no radiográfica como radiográfica en pacientes con o sin tratamiento previo con inhibidores del TNF-α.
El anticuerpo monoclonal anti-IL-17A ixekizumab ya está aprobado para el tratamiento de la psoriasis en placas de moderada a grave y la artritis psoriásica desde 2016. En 2020, se añadió la espondiloartritis axial (axSpA) como indicación adicional para la que el ixekizumab es una opción terapéutica. Basándose en el programa de ensayos COAST, se ha demostrado la eficacia y tolerabilidad del ixekizumab en la axSpA tanto no radiográfica como radiográfica en pacientes con o sin tratamiento previo con inhibidores del TNF-α [1–4].
Artritis psoriásica
Las estrategias terapéuticas aprobadas para la artritis psoriásica (PsA) incluyen el uso de AINE, csDMARD, biológicos (inhibidores del TNF, inhibidores de la IL-12/23 y la IL-17, moduladores de las células T) y tsDMARD (inhibidores de la PDE4, inhibidores de la JAK). Qué agentes se utilizan en qué pacientes se determina individualmente según el patrón de manifestación y otros factores (por ejemplo, comorbilidades, factores sociales, modo de aplicación y enfermedades concomitantes).
Con el Colegio Americano de Reumatología (ACR), la Liga Europea contra el Reumatismo (EULAR) y el Grupo de Investigación y Evaluación de la Psoriasis y la Artritis Psoriásica (GRAPPA), se dispone de recomendaciones terapéuticas de tres instituciones internacionales que proporcionan orientación para la prescripción [5]. Como estrategia de primera línea en el tratamiento de la APs, se sigue recomendando aquí el uso de antiinflamatorios no esteroideos (AINE), que pueden utilizarse al inicio de los síntomas, pero también antes de que se confirme el diagnóstico. En los cuidados cotidianos, debe prestarse atención a los riesgos gastrointestinales, cardiovasculares y renales específicos de cada sustancia. Por otro lado, los glucocorticoides sistémicos (GC) sólo desempeñan un papel menor en la APs. Sin embargo, la inyección intraarticular puede considerarse para el tratamiento de patrones de afectación mono u oligoarticular o como complemento de la terapia existente con terapias antirreumáticas modificadoras de la enfermedad (DMARD). Los DMARD se utilizan una vez confirmado el diagnóstico y si los síntomas persisten.
Mejora significativa ya después de 6 semanas
El ixekizumab está indicado en el tratamiento de la APs en adultos que han tenido una respuesta inadecuada o son intolerantes a uno o más fármacos antirreumáticos modificadores de la enfermedad (FAME), solos o en combinación con metotrexato. Esto puede conducir a una mejora significativa de las florescencias cutáneas con una casi normalización de la estructura de la piel tras sólo 6 semanas de terapia. Además, se describió una rápida reducción del picor y una mejora de la calidad de vida gracias a la sustancia activa.
Actualmente, se ha notificado una mejoría del dolor con ixekizumab en pacientes con y sin inflamación medible en la artritis psoriásica [6]. Habiendo demostrado previamente la eficacia del ixekizumab (IXE) y el adalimumab (ADA) en pacientes con APs con referencia a las tasas de respuesta en ACR50 y PASI(Psoriasis Area and Severity Index)-100 [7,8]El estudio investigó la eficacia de la monoterapia con IXE o ADA en la reducción del dolor más allá de la inflamación medible en pacientes con APs activa y proteína C reactiva (PCR, <5 mg/l) baja al inicio del estudio.
El estudio SPIRIT-H2H incluyó a 95 pacientes en monoterapia. Las características basales fueron similares entre los dos brazos de tratamiento. En los pacientes con inflamación baja persistente (medida por la PCR), no hubo diferencias en la mejora del dolor articular entre los pacientes tratados con IXE y los tratados con ADA. Sin embargo, en los pacientes con inflamación fluctuante, los pacientes tratados con IXE mostraron una mejora media numéricamente mayor del dolor articular (EAV) frente a los pacientes tratados con ADA en la semana 16 (IXE: -31,64, ADA: -25,33). Esto continuó hasta la semana 52 (IXE: -47,69, ADA: -20,67). La significación a favor de IXE se midió en las semanas 32 (p=0,0045) y 52 (p=0,0288). Del mismo modo, los pacientes con una mejoría sostenida de la inflamación articular, así como con una mejoría fluctuante (evaluada por el SJC), presentaron mejoras medias numéricamente mayores del dolor articular en el brazo IXE en comparación con los pacientes tratados con ADA a partir de la semana 4 y 16, respectivamente, que se mantuvieron hasta la semana 52.
Este análisis sugiere patrones diferenciales de mejora del dolor en pacientes con PCR basal baja tratados con IXE o monoterapia con ADA, con un resultado de reducción del dolor más favorable para los pacientes tratados con IXE. Esto es evidente incluso cuando la inflamación, medida por la PCR o la mejora del SJC, fluctúa. Así pues, el estudio respalda la hipótesis de que la IXE mejora el dolor articular en pacientes con APs con y sin inflamación medible.
Espondiloartritis axial
La espondiloartritis axial (axSpA) es una enfermedad inflamatoria crónica compuesta por la axSpA no radiológica y la axSpA radiológica (r-axSpA). Esta última, también conocida como espondilitis anquilosante (EA), se caracteriza por dolor de espalda inflamatorio y pruebas radiológicas de daños en la articulación sacroilíaca [9]. Estas manifestaciones, así como los signos y síntomas musculoesqueléticos y extraarticulares periféricos, pueden contribuir a la limitación de la movilidad, la discapacidad progresiva y la reducción de la calidad de vida (CdV). Los fármacos antirreumáticos modificadores de la enfermedad biológicos (bDMARD), entre los que se incluyen los inhibidores del factor de necrosis tumoral (TNFi) y un antagonista de la interleucina (IL)-17A, se recomiendan para el tratamiento de pacientes con AxSpA que no responden o no pueden tolerar los antiinflamatorios no esteroideos (AINE). Sin embargo, hasta un 40% de los pacientes no logran un control satisfactorio de la enfermedad con los inhibidores del TNF [10], y el tratamiento con TNFi puede estar contraindicado en determinados pacientes.
La vía de señalización de la IL-17 desempeña un papel clave en la patogénesis de la axAspA. Dos ensayos clínicos aleatorizados y controlados de fase 3 (COAST-V y COAST-W) evaluaron la eficacia y la seguridad del ixekizumab como anticuerpo monoclonal de alta afinidad dirigido selectivamente contra la IL-17A durante un periodo de hasta 52 semanas en pacientes con espondiloartritis axial radiográfica activa (r-axSpA). Los participantes del COAST-V no habían recibido bDMARD y los del COAST-W tenían experiencia con inhibidores del TNF.
En COAST-V, 341 pacientes con AxSpAr activa fueron aleatorizados 1:1:1 a 80 mg de ixekizumab (IXE) cada 2 ó 4 semanas, placebo o 40 mg de adalimumab (ADA) quincenalmente. En el COAST-W, 316 pacientes recibieron ixekizumab 1:1:1 cada 2 ó 4 semanas o placebo. En la semana 16, los pacientes que recibían ixekizumab continuaron con el tratamiento asignado, los pacientes con placebo o ADA fueron cambiados 1:1 a IXE Q2W o IXE Q4W hasta la semana 52.
Buena eficacia y seguridad
Ambas terapias con ixekizumab demostraron mejorar la actividad de la enfermedad, la función física, los marcadores objetivos de inflamación, la calidad de vida, el estado de salud y la función general durante un periodo de hasta 52 semanas.
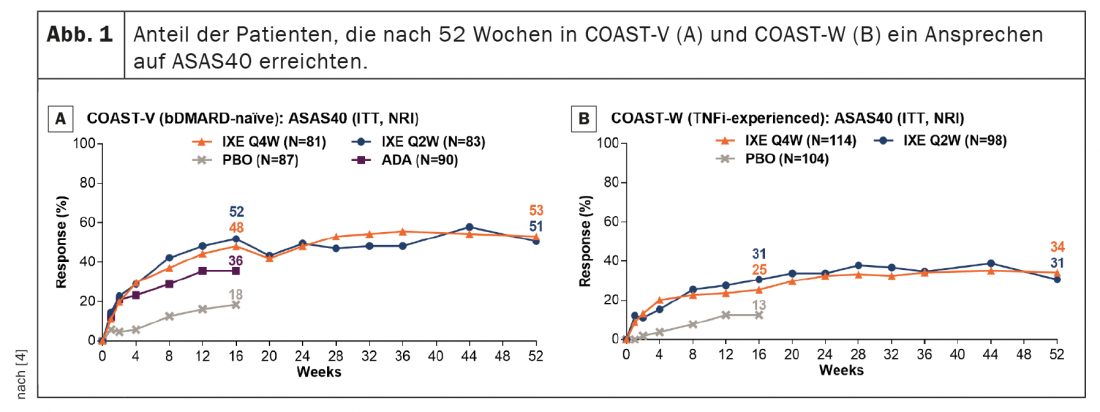
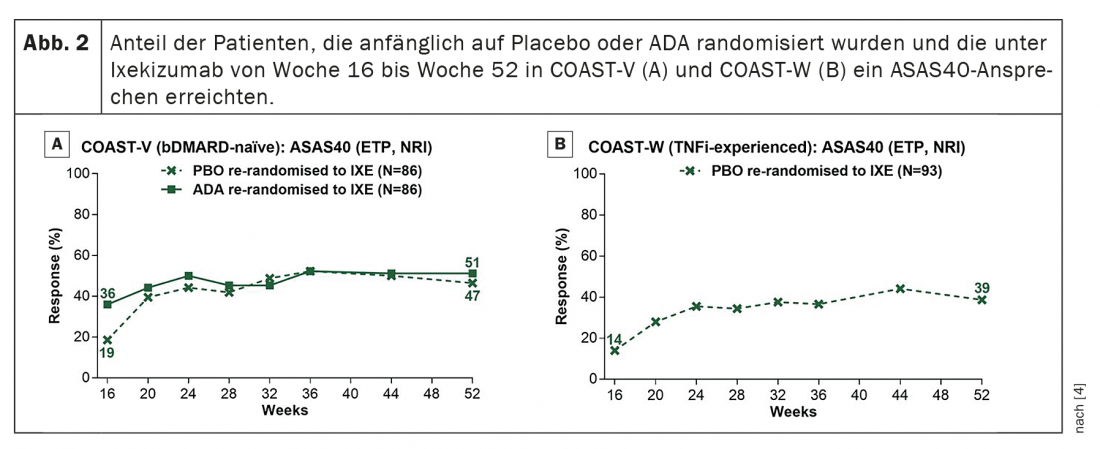
En los pacientes tratados de forma continuada con ixekizumab, las tasas de respuesta al ASAS40 persistieron desde la semana 16 hasta la 52 (Fig. 1 ). Las tasas de respuesta al ASAS40 en la semana 52 fueron del 53,1% (IXE Q4W) y del 50,6% (IXE Q2W) en COAST-V y del 34,2% (IXE Q4W) y del 30,6% (IXE Q2W) en COAST-W. Los pacientes aleatorizados a placebo y realeatorizados a ixekizumab en la semana 16 mostraron una rápida mejora en las tasas de respuesta al ASAS40 tras cambiar a ixekizumab (Fig. 2); Las tasas de respuesta en la semana 52 (46,5% en COAST-V, 38,7% en COAST-W) fueron numéricamente similares a las de los pacientes aleatorizados inicialmente a ixekizumab. En COAST-V, los pacientes aleatorizados a ADA mostraron nuevas mejoras numéricas en las tasas de respuesta al ASAS40 (36,0% en la semana 16, 51,2% en la semana 52) tras cambiar a ixekizumab (figura 2A); las tasas de respuesta en la semana 52 fueron numéricamente similares a las de los pacientes aleatorizados inicialmente a ixekizumab.
El EAIR agrupado para la psoriasis fue de 1,0. Un paciente sufrió un acontecimiento adverso cerebrocardiovascular grave (infarto agudo de miocardio) y se notificaron dos neoplasias malignas (leucemia promielocítica aguda y cáncer de vejiga). Se notificaron menos reacciones en el lugar de la inyección (RSI) con IXE Q4W (9,2%) que con IXE Q2W (17,2%). El número de pacientes que informaron de ISR disminuyó con el tiempo. En concreto, el 6,4%, el 3,8% y el 3,4% de los pacientes con IXE Q4W y el 14,3%, el 8,6% y el 5,2% de los pacientes con IXE Q2W notificaron ISR en las semanas 0-12, 12-24 y 24-36, respectivamente. Sólo unos pocos pacientes (IXE Q4W ≤1%; IXE Q2W aprox. 3%) informaron de ISR más allá de la semana 36.
En general, las respuestas al tratamiento fueron numéricamente inferiores en los pacientes con experiencia con TNFi en comparación con los pacientes sin tratamiento con bDMARD, lo que refleja una población más difícil de tratar, con un fracaso previo del tratamiento y una enfermedad más duradera [4]. Las terapias biológicas aprobadas actualmente para la axSpA incluyen varias TNFi y un antagonista de la IL-17A. Aunque sólo los estudios comparativos directos pueden evaluar plenamente la eficacia y la seguridad relativas de los distintos tratamientos, los resultados del ASAS40 comunicados aquí en la semana 52 son coherentes con los comunicados para el TNFi en pacientes que no habían recibido bDMARD y para el secukinumab en subgrupos de pacientes que no habían recibido bDMARD o que habían fracasado previamente en el tratamiento con TNFi.
La tasa de interrupción debida a acontecimientos adversos (AA) fue <4% en ambos estudios, y los acontecimientos adversos graves (AAG) fueron notificados por <6% de los pacientes. La mayoría de las infecciones e ISR fueron de leves a moderadas. Los ISR fueron más frecuentes en IXE Q2W que en IXE Q4W. Además, las ISR se notificaron con mayor frecuencia durante las primeras 4 semanas de tratamiento y su frecuencia disminuyó con el tiempo. Durante los periodos de estudio de 52 semanas de COAST-V y COAST-W (n=641), la tasa de incidencia conjunta ajustada a la exposición por 100 pacientes-año (EAIR) de infecciones graves fue de 2,0 en pacientes tratados con ixekizumab. Los EAIR agrupados de infección por Candida y neutropenia de grado 3/4 fueron de 1,0 y 0,2, respectivamente. Los EAIR correspondientes a la enfermedad de Crohn, la colitis ulcerosa y la enfermedad inflamatoria intestinal (EII) (NOS) fueron de 0,8, 0,4 y 0,4 respectivamente (EAIR total de la EII: 1,6). El EAIR para la uveítis anterior (UA) fue de 3,9; 15 de 20 pacientes (75%) tenían antecedentes de UA y 14 de 20 pacientes (70%) procedían de COAST-W. Se notificaron menos acontecimientos CED en IXE Q2W que en IXE Q4W, y no hubo una asociación aparente entre la duración de la exposición al ixekizumab y los CED. Informes anteriores han demostrado que el EAIR para la UA en pacientes con espondilitis anquilosante (EA) oscila entre 2,6 y 3,5 para los pacientes tratados con TNFi [11].
En resumen, los datos del COAST-V y el COAST-W demuestran que el ixekizumab logró una mejora sostenida y clínicamente significativa de los signos y síntomas de la AxSpAr activa durante un máximo de 52 semanas. Los resultados de seguridad fueron coherentes con el perfil de seguridad conocido del ixekizumab. Estos resultados sugieren que el ixekizumab puede ser una opción de tratamiento para la axAspA en pacientes que no hayan recibido bDMARD o que hayan tenido previamente una respuesta inadecuada o intolerancia a los inhibidores del TNF.
Estudio sobre el efecto tras la remisión
Los resultados de los ensayos aleatorios sobre la interrupción del inhibidor del factor de necrosis tumoral (TNF) en pacientes con espondiloartritis axial sugieren que la interrupción del TNFi provoca una recaída en la mayoría de los pacientes y que la continuación del tratamiento puede ser importante para mantener el control de la enfermedad. Sin embargo, aún no se han realizado estudios centrados en los efectos de la continuación frente a la interrupción de un antagonista de la interleucina (IL)-17A en pacientes con axSpA. COAST-Y es un estudio de seguimiento de COAST-V y COAST-W. El objetivo de este estudio [12], publicado en 2021, era llenar este vacío e investigar la continuación frente a la interrupción del tratamiento con ixekizumab en pacientes con espondiloartritis axial que habían alcanzado la remisión.
En el estudio de extensión de fase 3, doble ciego, controlado con placebo y aleatorizado, los pacientes que habían completado los ensayos originales COAST-V, COAST-W o COAST-X de 52 semanas entraron en una fase introductoria de 24 semanas y continuaron con 80 mg de IXE cada 2 semanas (Q2W) o 4 semanas (Q4W). Los pacientes que alcanzaron la remisión (es decir, una puntuación de la actividad de la enfermedad de la espondilitis anquilosante (ASDAS) <1,3 al menos una vez en la semana 16 o en la semana 20 y <2,1 en ambas visitas) fueron asignados aleatoriamente por igual en la semana 24 a continuar con IXE Q4W, IXE Q2W o suspender el placebo de forma ciega. El criterio de valoración primario fue la proporción de pacientes sin recaída (ASDAS ≥2,1 en dos visitas consecutivas o ASDAS >3,5 en cada visita) tras el RWRP (periodo aleatorio de retirada-retratamiento) de 40 semanas, siendo el tiempo hasta la recaída un criterio de valoración secundario importante.
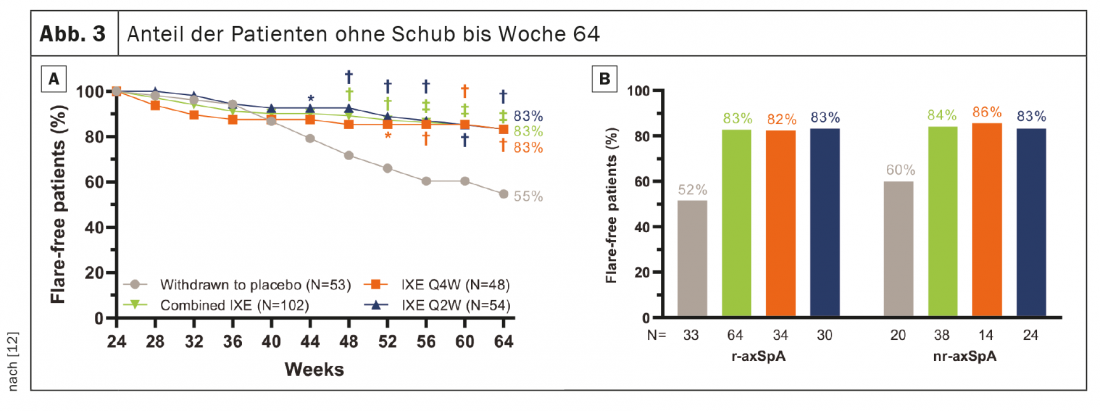
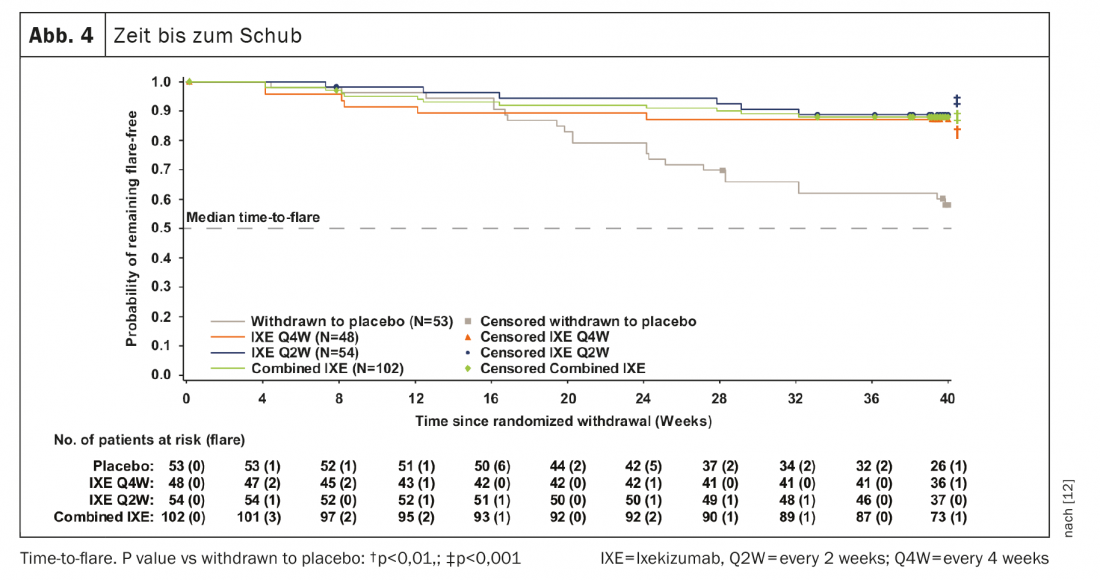
741 pacientes completaron la fase introductoria de 24 semanas y 155 entraron en el PRTR. El objetivo principal y todos los objetivos secundarios importantes se alcanzaron en la semana 64. Cuarenta semanas después de la retirada aleatoria, el 83,3% de los pacientes de los grupos combinados seguían siendo IXE (85/102, p<0,001), IXE Q4W (40/48, p=0,003) e IXE Q2W (45/54, p=0,001) libres de recaída frente al 54,7% del grupo placebo (29/53). (Fig. 3A). La proporción de pacientes sin recaída fue similar entre los subgrupos de pacientes con r-axSpA y nr-axSpA (Fig. 3B). La continuación de IXE retrasó significativamente el tiempo hasta la recaída en comparación con el placebo, y la mayoría de los pacientes permanecieron libres de recaída hasta 20 semanas después de interrumpir IXE (Fig. 4). El hecho de que el 54,7% de los pacientes que interrumpieron el placebo permanecieran libres de recaídas durante la PRTR fue un valor superior al de estudios comparables de interrupción de adalimumab (47%) y certolizumab pegol (20,2%). [13–16].
Predictores y seguridad
Los análisis post hoc identificaron varias características de los pacientes asociadas a la recaída, incluida el área bajo la curva ASDAS, lo que sugiere que los pacientes con una enfermedad menos controlada tenían más probabilidades de haber recaído con el tiempo que aquellos cuyo control de la enfermedad era estable. Además, la interrupción de la IXE, una PCR basal más elevada y un IMC no normal (que era ≥25kg/m2 en la mayoría de los casos) se identificaron como factores asociados a la recaída. Una puntuación de dolor BASDAI más alta en la semana 24 también se asoció con una recaída en los pacientes que continuaron el tratamiento con IXE, pero no en los pacientes que lo dejaron con placebo.
El RWRP del COAST-Y incluyó a pacientes de todo el espectro de la axAspA con y sin fracaso previo del TNFi y con una duración de los síntomas que oscilaba entre 1,9 y 44,7 años (media de 12,7 años) [17]. No hubo problemas de seguridad nuevos o inesperados durante el RWRP. Se notificaron acontecimientos adversos emergentes del tratamiento (AAET) en el 42,6% (IXE Q4W), el 44,4% (IXE Q2W) y el 52,8% (destete a placebo) de los pacientes y, en general, fueron de gravedad leve a moderada. Dos pacientes (IXE Q2W) interrumpieron el estudio debido a UE. Se observaron SUE en dos (4,3%) pacientes del grupo IXE Q4W (teratoma benigno de células germinales ováricas y fractura por compresión), dos (3,7%) pacientes del grupo IXE Q2W (amigdalitis crónica y mielopatía en un paciente y colitis por Clostridium difficile en otro) y un (1,9%) paciente que había interrumpido el placebo (inflamación de tejidos blandos). Sólo un SUE (colitis por C. difficile) llevó a la interrupción. No hubo muertes ni informes de reactivación de la tuberculosis, enfermedad inflamatoria intestinal, acontecimientos adversos cardiovasculares graves (MACE) o neoplasias.
En general, estos resultados sugieren que el tratamiento continuado con IXE es importante para que la mayoría de los pacientes mantengan el control de la enfermedad a largo plazo [12]. Sin embargo, la larga duración de la respuesta al tratamiento tras la interrupción de IXE sugiere que es poco probable que la interrupción temporal del tratamiento, por ejemplo durante una infección o antes de una intervención quirúrgica, provoque una recaída en la mayoría de los pacientes. Estos resultados son importantes para los clínicos a la hora de tomar decisiones sobre la interrupción del tratamiento y la optimización del tratamiento a largo plazo de la axSpA.

Mensajes para llevarse a casa
- El ixekizumab está aprobado para el tratamiento de la psoriasis en placas de moderada a grave, la artritis psoriásica y la espondiloartritis axial.
- En la APs, el ixekizumab puede producir una mejora significativa de las florescencias cutáneas tras sólo 6 semanas de tratamiento. Además, se ha informado de una mejoría del dolor en pacientes con y sin inflamación medible.
- En pacientes con AxSpAr activo que no han recibido bDMARD o que tienen experiencia con TNFi, el ixekizumab es un tratamiento eficaz.
- El ixekizumab puede mejorar la actividad de la enfermedad, la función física, los marcadores objetivos de inflamación, la calidad de vida, el estado de salud y la función general en pacientes con EAxr durante un máximo de 52 semanas.
- En pacientes con axSpA en remisión, el tratamiento continuo con IXE se asocia a una mayor probabilidad de mantener un control óptimo de la enfermedad en comparación con la retirada de IXE.
Literatura:
- Deodhar A, et al: Ixekizumab para pacientes con espondiloartritis axial no radiográfica (COAST-X): un ensayo aleatorizado controlado con placebo. Lancet 2020 Ene 4; 395 (10217): 53-64.
- van der Heijde D, et al: Ixekizumab, un antagonista de la interleucina-17A en el tratamiento de la espondilitis anquilosante o espondiloartritis axial radiográfica en pacientes no tratados previamente con fármacos antirreumáticos modificadores de la enfermedad biológicos (COAST-V): resultados a las 16 semanas de un ensayo de fase 3 aleatorizado, doble ciego, con control activo y placebo. Lancet 2018 dic 8; 392 (10163): 2441-2451.
- Deodhar A, et al: Eficacia y seguridad del ixekizumab en el tratamiento de la espondiloartritis axial radiográfica: resultados de dieciséis semanas de un ensayo de fase III aleatorizado, doble ciego y controlado con placebo en pacientes con respuesta previa inadecuada o intolerancia a los inhibidores del factor de necrosis tumoral. Arthritis Rheumatol 2019; 71 (4): 599-611.
- Dougados M, Wei JCC, Landewé R, et al: Eficacia y seguridad del ixekizumab durante 52 semanas en dos ensayos clínicos de fase 3, aleatorizados y controlados en pacientes con espondiloartritis axial radiográfica activa (COAST-V y COAST-W). Ann Rheum Dis 2020; 79: 176-185; doi: 10.1136/annrheumdis-2019-216118.
- Köhm M, Burkhardt H, Behrens F: Estrategias terapéuticas de la artritis psoriásica. DMW – Deutsche Medizinische Wochenschrift 2020; 145(11): 773-780; doi: 10.1055/a-0964-0231.
- de Vlam K, Gallo G, Mease P, et al: El ixekizumab muestra un patrón de mejora del dolor en pacientes con y sin inflamación medible en la artritis psoriásica. Artritis Reumatol 2021; 73 (suplemento 10).
- Mease PJ, Smolen JS, Behrens F, The SPIRIT H2H study group et al: A head-to-head comparison of the efficacy and safety of ixekizumab and adalimumab in biological-naïve patients with active psoriatic arthritis: 24-week results of a randomised, open-label, blinded-assessor trial. Ann Rheum Dis 2020; 79: 123-131; doi: 10.1136/annrheumdis-2019-215386.
- Smolen JS, Sebba A, Ruderman EM, et al: Eficacia y seguridad del ixekizumab con o sin metotrexato en pacientes sin tratamiento biológico con artritis psoriásica: resultados a las 52 semanas del estudio SPIRIT-H2H. Reumatol Ther 2020; 7: 1021-1035; doi: 10.1007/s40744-020-00250-3.
- Sieper J, Poddubnyy D: Espondiloartritis axial. Lancet 2017; 390: 73-84; doi: 10.1016/S0140-6736(16)31591-4.
- Sepriano A, Regel A, van der Heijde D, et al: Efficacy and safety of biological and targeted-synthetic DMARDs: a systematic literature review informing the 2016 update of the ASAS/EULAR recommendations for the management of axial spondyloarthritis. RMD Open 2017; 3: e000396; doi: 10.1136/rmdopen-2016-000396.
- Deodhar A, Miceli-Richard C, Baraliakos X, et al: Baja incidencia tanto de uveítis de nueva aparición como de brotes en pacientes con espondilitis anquilosante tratados con secukinumab: ensayo clínico y análisis de seguridad posterior a la comercialización. Ann Rheum Dis 2018; 77(Suppl 2): 999; doi: 10.1136/annrheumdis-2018-eular.4474.
- Landewé RBM, Gensler LS, Poddubnyy D, et al: Continuación frente a retirada del tratamiento con ixekizumab en pacientes con espondiloartritis axial que alcanzaron la remisión: resultados de eficacia y seguridad de un estudio de retirada aleatorizado y controlado con placebo (COAST-Y). Ann Rheum Dis 2021; 80: 1022-1030; doi: 10.1136/annrheumdis-2020-219717.
- Landewé RB, van der Heijde D, Dougados M, et al: Mantenimiento de la remisión clínica en la espondiloartritis axial temprana tras la reducción de la dosis de certolizumab pegol. Ann Rheum Dis 2020; 79: 920-928; doi: 10.1136/annrheumdis-2019-216839.
- Landewé R, Sieper J, Mease P, et al: Eficacia y seguridad de continuar frente a retirar el tratamiento con adalimumab para mantener la remisión en pacientes con espondiloartritis axial no radiográfica (ABILITY-3): un estudio multicéntrico, aleatorizado y doble ciego. Lancet 2018; 392: 134-144; doi: 10.1016/S0140-6736(18)31362-X.
- Haibel H, Heldmann F, Braun J, et al: Eficacia a largo plazo del adalimumab tras la retirada del fármaco y el retratamiento en pacientes con espondiloartritis axial activa no evidente radiográficamente que experimentan una reagudización. Arthritis Rheum 2013; 65: 2211-2213; doi: 10.1002/art.38014.
- Song IH, Althoff CE, Haibel H, et al: Frecuencia y duración de la remisión libre de fármacos tras 1 año de tratamiento con etanercept frente a sulfasalazina en la espondiloartritis axial temprana: datos de 2 años del ensayo ESTHER. Ann Rheum Dis 2012; 71: 1212-1215; doi: 10.1136/annrheumdis-2011-201010.
- Smolen JS, Schöls M, Braun J, et al: Treating axial spondyloarthritis and peripheral spondyloarthritis, especially psoriatic arthritis, to target: 2017 update of recommendations by an international task force. Ann Rheum Dis 2018; 77: 3-17; doi: 10.1136/annrheumdis-2017-211734.
InFo DOLOR Y GERIATURA 2021; 3(2): 14-18