Las recomendaciones de las directrices para el tratamiento quirúrgico de la fibrilación auricular (FA) varían y a menudo el éxito del tratamiento está estrechamente ligado a la experiencia del hospital tratante, las comorbilidades del paciente y el intenso intercambio interdisciplinar entre electrofisiólogos y cirujanos cardiacos. Además, no parece haber consenso entre los cirujanos cardiacos en cuanto a la indicación, la técnica quirúrgica y los cuidados postoperatorios. Desde 2009, el Inselspital ha introducido un nuevo algoritmo para el tratamiento quirúrgico de la FVC en colaboración interdisciplinar, que incluye un concepto uniforme para la indicación, la técnica intraoperatoria, los cuidados postoperatorios y el seguimiento.
La fibrilación auricular (FA) es la arritmia cardiaca más común. Sólo en el mundo occidental, alrededor del 1% de la población padece FVC. La incidencia aumenta con la edad [1, 2]. El riesgo de FVC aumenta considerablemente con la gravedad de la cardiopatía existente. Por ejemplo, se encontró una prevalencia del 4% en el estadio de insuficiencia cardiaca NYHA I, una prevalencia de alrededor del 25% en los estadios NYHA II y III, y de hasta el 50% en el estadio NYHA IV.
La mortalidad es aproximadamente el doble en la HFV que en los compañeros con ritmo sinusal, pero esto se debe principal o exclusivamente a las cardiopatías más frecuentes. De media, alrededor del 6% de los pacientes con FVC sufren un ictus cada año, y entre el 15 y el 20% de todos los ictus están asociados a la FVC. El Euro Heart Survey para la FVC ha identificado el creciente número de hospitalizaciones y la tasa cada vez mayor de procedimientos intervencionistas como los principales impulsores del coste económico de la FVC. Por lo tanto, está justificado el interés por desarrollar enfoques exitosos para el tratamiento de la FVC que promuevan la prevención primaria o secundaria [3].
Tanto el ensayo AFFIRM como el RACE han demostrado que, en pacientes ancianos y poco sintomáticos, una terapia farmacológica puramente de control de ritmo combinada con anticoagulación oral es equivalente a una terapia de control de ritmo farmacológico en términos de mortalidad. Sin embargo, menos del 30% de los pacientes son tratables con medicación o terapia eléctrica. Además, los fármacos antiarrítmicos suelen tener un éxito moderado a largo plazo en el mejor de los casos y suelen tener efectos secundarios indeseables. En cambio, la ablación por radiofrecuencia intervencionista o con catéter ha demostrado ser una terapia eficaz para la FVC sintomática recurrente y refractaria a los fármacos [5]. No obstante, con el procedimiento del catéter, las tasas de éxito de la FVC paroxística se sitúan en torno al 60-80% cuando se utiliza por primera vez; el 30-40% de los pacientes necesitan al menos una segunda intervención [6–8]. Sin embargo, las tasas de éxito a largo plazo siguen disminuyendo con los años: la supervivencia sin arritmia sólo se registra en el 29-53% de los pacientes [9–11]. Para los pacientes con FVC persistente, el péndulo no se inclina a favor de la ablación intervencionista, ya que suelen ser necesarias ablaciones repetidas y extensas [12–14]. Dadas las limitaciones de las terapias farmacológicas e intervencionistas, la ablación quirúrgica de la FVC es cada vez más importante.
FVC: Desarrollo del tratamiento quirúrgico
En 1980, Williams et al. [15]cinco años después Guiraudon et al. [16] los primeros tratamientos quirúrgicos para la FVC. Estos métodos intentaban canalizar las vías eléctricas mediante incisiones en la aurícula izquierda para poder garantizar una conducción regular en los ventrículos. Ambos métodos fracasaron porque grandes porciones de las aurículas siguieron mostrando FVC y, por tanto, no se pudo garantizar el transporte auricular y el riesgo de tromboembolia permaneció inalterado.
En 1991, Cox [17] presentó la primera operación denominada laberinto (Cox-Maze I). El concepto se basa en dos supuestos:
- El fraccionamiento del tejido auricular en pequeños segmentos evita múltiples “reentradas”.
- Sin embargo, estos pequeños segmentos deben seguir conectados para permitir la despolarización de suficiente tejido miocárdico.
Ferguson y Cox [18] definieron cinco objetivos del tratamiento quirúrgico de la FVC: eliminación de la FVC, restablecimiento del ritmo sinusal, sincronía aurículo-ventricular, preservación de la función de transporte auricular y prevención del ictus.
Con la operación Cox-MAZE III, más avanzada, se consigue el ritmo sinusal en el 75-98% de los casos y se restablece la función de transporte en el 81-86%. El seguimiento a 10 años muestra una incidencia de ictus de <1%. El efecto sobre la tasa de supervivencia aún no está claro. Sin embargo, el proceso lleva tiempo y requiere práctica. Ahora es posible imitar la fragmentación auricular compleja original de la cirugía Cox-Maze III con menos esfuerzo utilizando diversas fuentes de energía hipertérmica o hipotérmica (especialmente la ablación por radiofrecuencia). Las tasas de éxito de este método -denominado ablación quirúrgica o Cox-Maze-IV- muestran unos resultados comparativamente buenos: Sin embargo, en el 70-98% de los casos, el ritmo sinusal se produce con un único procedimiento [19–29], dependiendo del resultado a corto o largo plazo.
Directrices
Las recomendaciones para el tratamiento quirúrgico de la FVC varían. El único ensayo aleatorizado que comparó la ablación quirúrgica con la intervencionista con catéter mostró una mayor libertad de arritmias auriculares un año después de la intervención quirúrgica, pero una mayor tasa de complicaciones en comparación con el método basado en catéter [30]. La experiencia del hospital tratante, las comorbilidades y los deseos del paciente y un intenso intercambio interdisciplinar entre electrofisiólogos y cirujanos cardiacos forman parte de la decisión terapéutica.
Las directrices de la Sociedad Europea de Cardiología (ESC) de 2010 para el tratamiento de la FVC recomiendan la ablación quirúrgica para:
- Pacientes sintomáticos con FVC que tendrán que someterse a cirugía cardiaca de todos modos (IIA-A).
- Los pacientes asintomáticos que vayan a someterse a una intervención quirúrgica cardiaca de todos modos también deberían considerarse para la ablación quirúrgica si el procedimiento conlleva poco riesgo adicional y una buena probabilidad de éxito, y si el procedimiento lo realiza un cirujano experimentado (IIB-C).
- Pacientes con FVC que no tienen ninguna otra indicación de cirugía cardiaca, o en los que la ablación por catéter no tuvo éxito y es posible una ablación quirúrgica mínimamente invasiva (IIB-C).
Se aplican las recomendaciones de expertos EHRS-EHRA-ECAS de 2012 para la ablación quirúrgica:
- Para pacientes con FVC sintomática paroxística o persistente que tengan cualquier otra indicación de cirugía cardiaca (IIa-C).
- Pacientes con FVC farmacorresistente (antiarrítmicos de clase 1 ó 3), paroxística o persistente, sin ninguna otra indicación de cirugía cardiaca y tras una ablación con catéter sin éxito, o pacientes que prefieren la ablación quirúrgica por sí mismos (IIb-C).
Ablación quirúrgica de la VHF como operación concomitante
La prevalencia de la FVC en pacientes sometidos a cirugía cardiaca varía entre aproximadamente el 2% (para la cirugía de bypass aortocoronario) y el 60% para la cirugía de la válvula mitral [31, 32]. Dado que es muy poco probable que una FVC persistente de larga duración no tratada se convierta espontáneamente a ritmo sinusal y que la FVC por sí sola también puede influir en la supervivencia a largo plazo, tiene sentido realizar una ablación adicional si de todos modos está indicada la cirugía cardiaca [33, 34]. Incluso en la FVC inducida por válvulas, la corrección de la patología valvular por sí sola no basta para tratar la arritmia. Parece que el aislamiento eléctrico de los orificios de las venas pulmonares por sí solo es suficientemente eficaz para tratar la FVC paroxística [35]. Aún no está claro si la ablación biauricular es mejor que la ablación de la aurícula izquierda sola en todos los casos [36].
Eficacia de la ablación quirúrgica y seguimiento de los pacientes
El consenso publicado en 2007 entre la Sociedad del Ritmo Cardíaco, la Sociedad de Cirujanos Torácicos, la Asociación Europea del Ritmo Cardíaco y la Sociedad Europea de Arritmia Cardíaca [37] contiene una recomendación para revisar el éxito de la terapia y el tratamiento posterior del paciente tras la ablación quirúrgica o intervencionista. Sin embargo, la realidad en la práctica clínica y en la mayoría de las publicaciones, especialmente tras la ablación quirúrgica, es diferente: Muy pocos médicos adoptan las recomendaciones anteriores. Además, no parece haber consenso ni siquiera entre los cirujanos cardiacos en cuanto a la indicación, la técnica quirúrgica y los cuidados postoperatorios. Así pues, ni los propios cirujanos ni los electrofisiólogos pueden demostrar la eficacia de la terapia quirúrgica o de los cambios introducidos. Para sortear este obstáculo, a partir de febrero de 2009 se introdujo en el Inselspital un nuevo algoritmo para el tratamiento quirúrgico de la FVC en un enfoque interdisciplinar en el que participan electrofisiólogos e internistas. Esto incluye un concepto uniforme para la indicación, la técnica intraoperatoria, los cuidados postoperatorios y el seguimiento.
Nuevo algoritmo de ablación quirúrgica de la fibrilación auricular
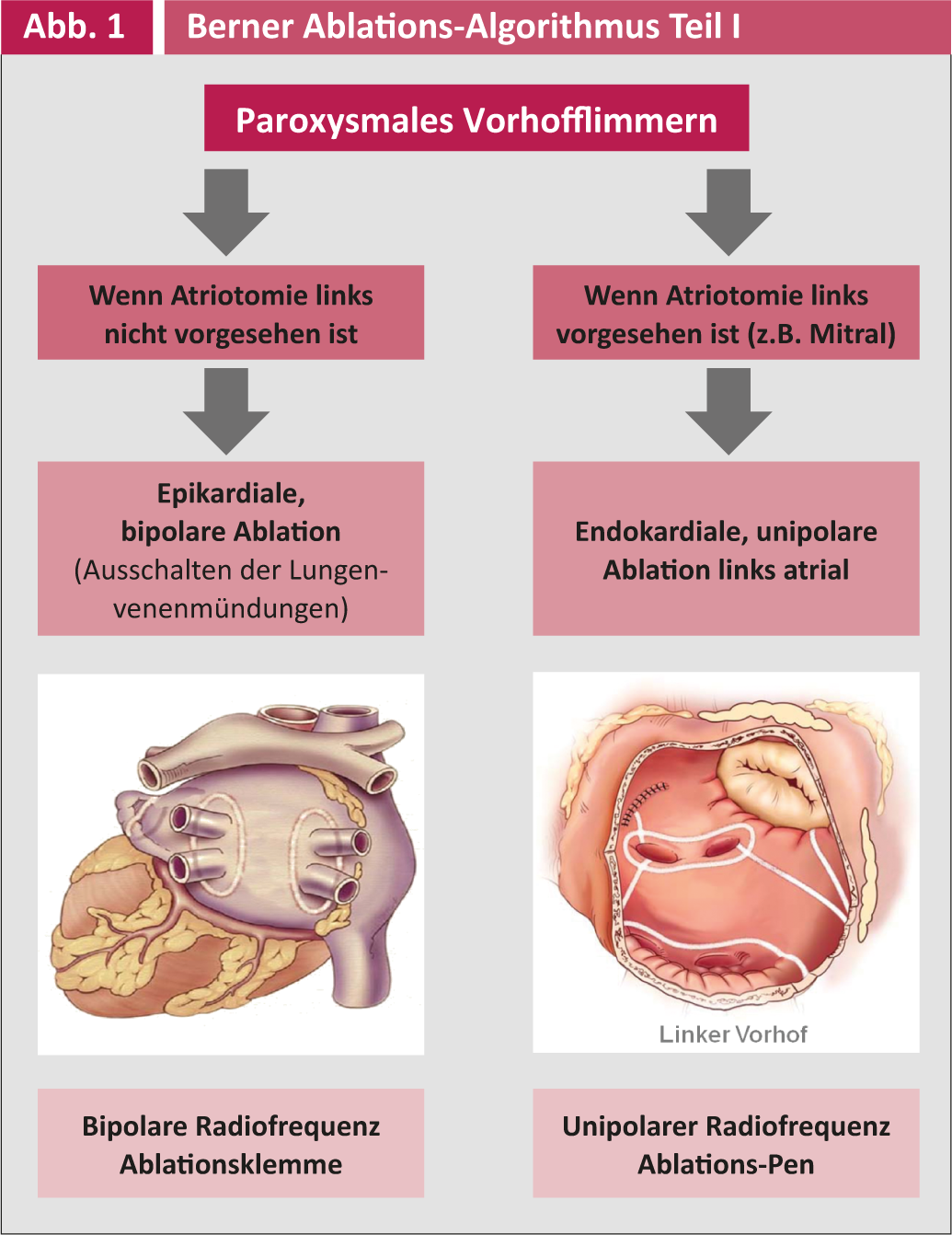
Las indicaciones para la ablación quirúrgica como operación concomitante en otra cirugía cardiaca y la técnica quirúrgica correspondiente se resumen en las figuras 1 y 2.
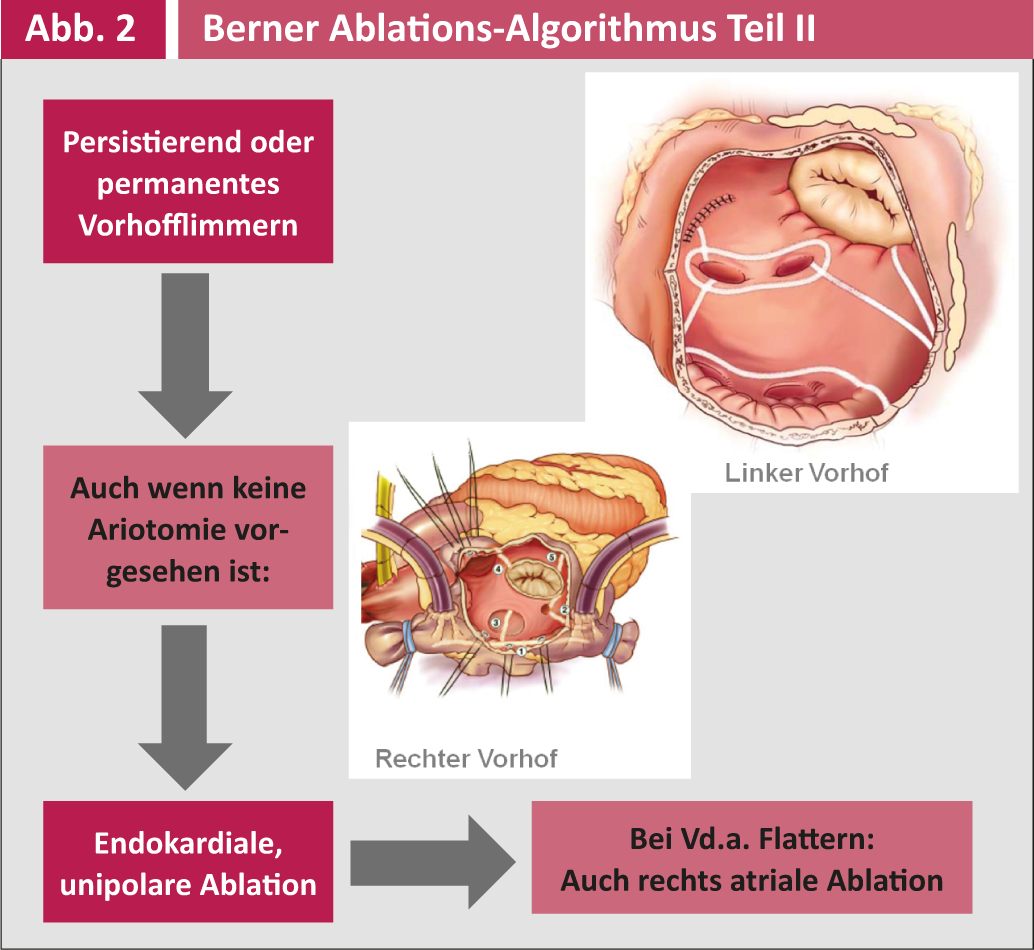
La terapia antiarrítmica postoperatoria la gestionan los cardiólogos/internistas e incluye principalmente metroprolol y secundariamente amiodarona. El seguimiento postoperatorio se lleva a cabo tres veces al mes durante el primer año y después anualmente por los electrofisiólogos del Inselspital o los cardiólogos de la práctica privada. Todos los controles incluyen un ECG a largo plazo con registrador de eventos de 7 días (prueba R) para detectar episodios asintomáticos de FVC y ajustar el tratamiento antiarrítmico o anticoagulante en consecuencia. Sólo se puede hablar de éxito eléctrico si no aparece ninguna arritmia VHF o auricular >30 segundos en un periodo de siete días. Un éxito clínico, por otro lado, es la ausencia de síntomas en el paciente, aunque sigan produciéndose recidivas asintomáticas.
La resección o eliminación intraoperatoria de la orejuela auricular izquierda para la profilaxis de tromboembolias se realiza si la puntuación CHADS-VASC es ≥2, el paciente tiene antecedentes de AIT y/o si se localiza fibrina o un trombo en la orejuela auricular izquierda mediante inspección o ecocardiografía. Se ha demostrado que una orejuela auricular intacta contribuye significativamente al transporte auricular izquierdo. Además, el equilibrio hídrico del organismo desempeña un papel importante [38–44].
El criterio de valoración principal de este análisis continuo es la ausencia de episodios de fibrilación auricular en la prueba R. Los criterios de valoración secundarios son la ausencia de anticoagulación oral, la ausencia de medicación antiarrítmica, la tasa de ictus cerebrales y la identificación de posibles factores predictivos del ritmo sinusal estable. Un seguimiento completo es obligatorio.
Resultados provisionales y análisis parcial
Desde la introducción de un nuevo algoritmo de ablación en 2009, 144 pacientes que presentaban FVC además de sus respectivas cardiopatías fueron tratados intraoperatoriamente mediante ablación quirúrgica utilizando el nuevo algoritmo. El 64% de los pacientes fueron ablacionados con radiofrecuencia unipolar, el 29% con radiofrecuencia bipolar y el 7% con otra fuente de energía (criotermia).
Un análisis parcial de los primeros 42 pacientes muestra: antes de la intervención quirúrgica, 21 (50%) pacientes sufrían de FVC paroxística, 21 (50%) de FVC persistente. La duración media de la enfermedad fue de 26 meses (DE 40,5). La edad media en el momento de la intervención era de 69 años (DE 7,8). 34 (81%) pacientes eran varones, ocho (19%) mujeres. Los diferentes perfiles preoperatorios de los pacientes se resumen en las tablas 1 y 2.
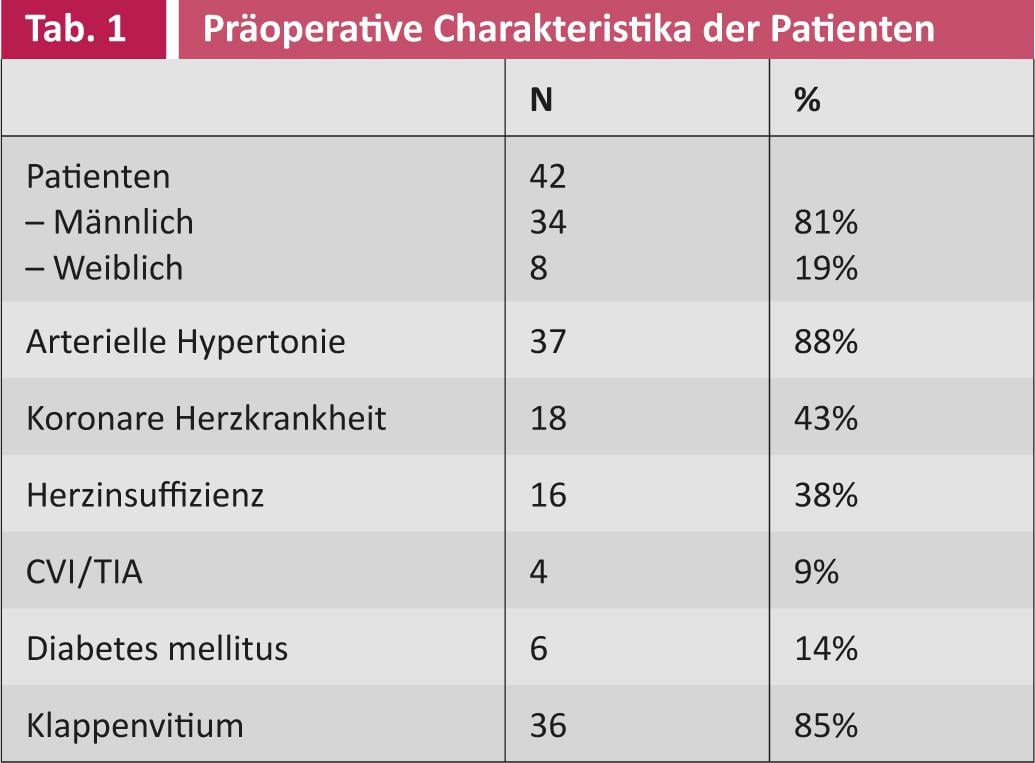
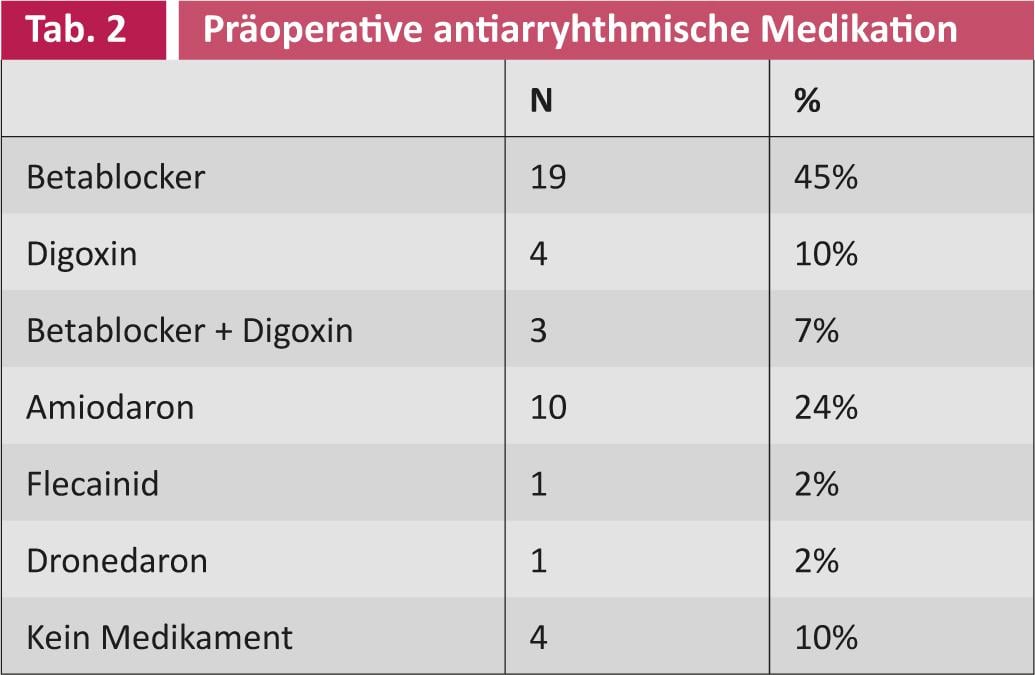
30 (71%) pacientes fueron anticoagulados por vía oral antes de la ablación quirúrgica. La puntuación media CHADS2 y CHA2DS2-VASc fue de 2 y 2, respectivamente. 3 (DE 1 resp. 1,5). Debido al riesgo de tromboembolia, la orejuela auricular izquierda se ligó en 18 (43%) de los pacientes y se extirpó por completo en dos (5%). Así que en la mayoría de los pacientes la orejuela auricular se dejó intacta. Como ya se ha mencionado, la ablación quirúrgica se realizó con otro procedimiento en el corazón. El tiempo de funcionamiento sólo se prolonga ligeramente, el tiempo adicional necesario es de unos 15-20 minutos.
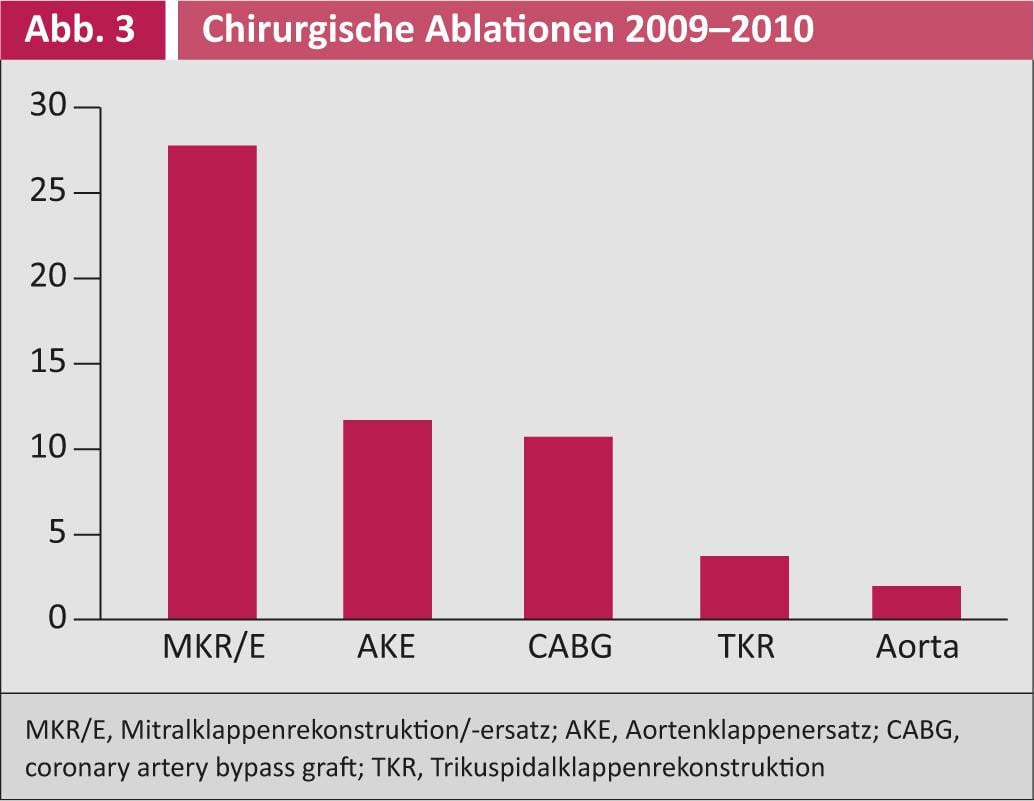
La figura 3 muestra las operaciones que se combinaron con ablación quirúrgica entre 2009 y 2010. La ablación quirúrgica se utilizó junto con la cirugía de la válvula mitral en más del 25% de los casos, seguida de la cirugía de la válvula aórtica y del bypass.
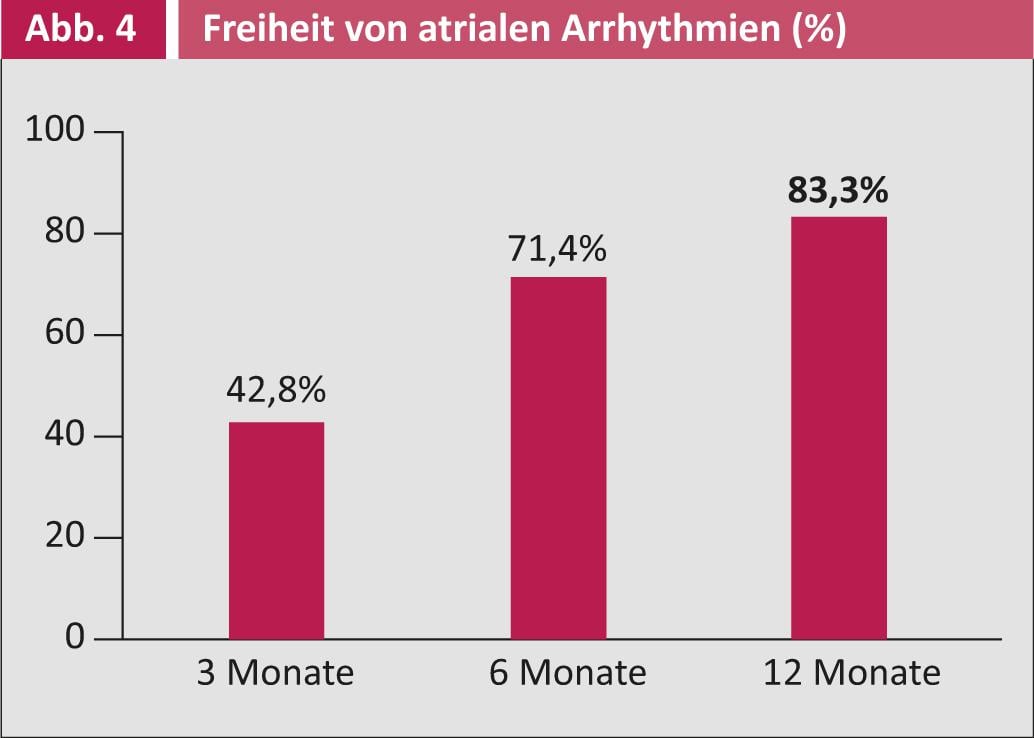
La figura 4 muestra los respectivos porcentajes de éxito de la ablación quirúrgica: a los tres meses, el 43% de los pacientes estaban libres de FVC, a los seis meses el porcentaje de éxito se eleva incluso al 71%. Al cabo de doce meses, el 83% de los pacientes estaban completamente libres de FVC.
El éxito de la ablación también se manifestó en el hecho de que la ingesta de fármacos antiarrítmicos, así como de anticoagulantes, se redujo o incluso se eliminó por completo tras la operación. En este subanálisis, el 85% de los pacientes dejaron de tomar anticoagulantes orales al cabo de un año y el 69% pudieron suspender los fármacos antiarrítmicos de clase I y III.
Complicaciones: Se produjeron complicaciones postoperatorias en 5 (12%) pacientes: Dos pacientes sufrieron una lesión cerebrovascular. Uno de ellos tenía una orejuela auricular izquierda apagada, el otro paciente tenía una orejuela auricular intacta. Ambas estaban anticoaguladas antes y después de la operación.
Un paciente anticoagulado desarrolló un taponamiento pericárdico en el curso del tratamiento, pero fue tratado quirúrgicamente con éxito. Además, un paciente sufrió una taquicardia ventricular con parada cardiaca, tras lo cual se realizó con éxito una cardioversión eléctrica y se le insertó un DAI. Otro paciente necesitó un marcapasos definitivo en el postoperatorio (total de implantes de marcapasos en el postoperatorio: 4,7%).
El ritmo sinusal o el ritmo estimulado auricular al final de la cirugía (p=0,001) y la corta duración de la cirugía (p=0,02) se han identificado previamente como predictores positivos de ausencia de FVC un año después de la operación.
Discusión: Se plantea la cuestión de si una grabadora de ECG “en bucle” continua e implantable (Reveal) ofrecería una monitorización aún más precisa y continua del ritmo cardiaco. Los dispositivos disponibles en la actualidad ofrecen una resistencia limitada, una alta sensibilidad pero una especificidad reducida y siguen siendo muy caros. Además, no está claro cómo afecta al cumplimiento del paciente este registro continuo con un dispositivo implantado.
Conclusión
La ablación quirúrgica por radiofrecuencia para el tratamiento de la FVC como intervención combinada durante otras operaciones cardiacas ofrece un procedimiento exitoso y seguro. La monitorización repetida y prolongada (al menos 7 días de ECG con registro de eventos) de los pacientes en el postoperatorio permite detectar hasta un 13% de casos que sufren episodios postoperatorios aún asintomáticos de fibrilación auricular. A menudo se pasan por alto con una instantánea como la que proporciona un ECG simple o incluso un ECG Holter de 24 horas. Esto tiene una implicación significativa para el manejo postoperatorio de los pacientes en términos de anticoagulación y ajustes de la medicación antiarrítmica. Sin duda, resulta útil para los centros que deseen ofrecer una terapia quirúrgica para la FVC diseñar un algoritmo longitudinal similar. Desempeña un papel importante en la evaluación de los resultados, pero también estimula la inmensamente importante colaboración interdisciplinar entre cirujanos y electrofisiólogos. En última instancia, son los pacientes los que se benefician.
Bibliografía del editor
PD Dr. med. Alberto Weber
PD Dra. Hildegard Tanner
Prof. Dr. med. Thierry Carrel