En la actualidad, el furoato de fluticasona es el corticosteroide inhalado (CSI) más potente y con mayor índice terapéutico disponible hasta la fecha [2,3]. Es un componente de Relvar Ellipta junto con el vilanterol. Daley-Yates et al. demostró que el furoato de fluticasona proporciona una protección 3,4 veces mayor con menos efectos sistémicos que otros CSI [2,3]. Del mismo modo, el Estudio Pulmonar de Salford confirmó que un 25% más de pacientes lograban un control relevante del asma en la práctica diaria con Relvar Ellipta que con otros controladores [1]. Hablamos de ello con el profesor Dr. Laurent Nicod, de la Clínica Privada Hirslanden de Lausana, y el Dr. Jean-Luc Kurzen, médico jefe de Neumología del Hospital de Männedorf.
El término “control del asma” se utiliza hoy en día con tanta naturalidad como si todo el mundo quisiera decir lo mismo, nada más lejos de la realidad. No todos los médicos y pacientes entienden lo mismo por control del asma [4]. Muchos médicos incluso sobrestiman el grado de control del asma de sus pacientes, como demostró un estudio [5]. Esto no fue así para aproximadamente la mitad de los asmáticos clasificados como controlados [5]. Los pacientes también suelen pensar que tienen su asma bajo control ajustando su estilo de vida a la carga de síntomas [4]. Evitan la actividad física, sufren síntomas diurnos y despertares nocturnos debido a la disnea y/o la tos, y son dependientes de su medicación de urgencia [4]. De hecho, hasta el 71% de los pacientes no consiguen controlar el asma a pesar del tratamiento [1]. Esto subraya la importancia de un control proactivo del asma que evite los síntomas y mejore así la calidad de vida [6].
Proactivo en lugar de orientado a los síntomas
Si la terapia se basa únicamente en los síntomas actuales, se perderá el objetivo de un buen control del asma [7]. En el MART
*
– esquemas, el control de los síntomas se basa en la percepción del paciente, y esto a menudo deja mucho que desear [4,7]. A diferencia del MART, el proactivo La terapia con Relvar Ellipta trata tanto los síntomas como la inflamación crónica, el remodelado de las vías respiratorias y la hiperreactividad bronquial [8].
Relvar Ellipta aumenta el número de días y noches sin síntomas en comparación con el furoato de fluticasona o el propionato de fluticasona, entre otros [9]. Los pacientes pueden beneficiarse de este tratamiento proactivo del asma al poder reanudar sus actividades cotidianas, algo que el Prof. Nicod también señala en la entrevista [9].
El Estudio Pulmonar de Salford es un estudio que ha marcado un hito [1].
El Salford Lung Study, un estudio en un entorno real, reclutó a 4.233 pacientes con asma insuficientemente controlada y los aleatorizó para recibir Relvar Ellipta o la terapia anterior (CSI o CSI/LABA) durante 52 semanas, que podían optimizarse según las necesidades [1]. Criterio de valoración primario: consecución de una puntuación ACT (Prueba de Control del Asma) >20 o mejora de la puntuación en ≥3 puntos tras 24 semanas [1].
Resultados
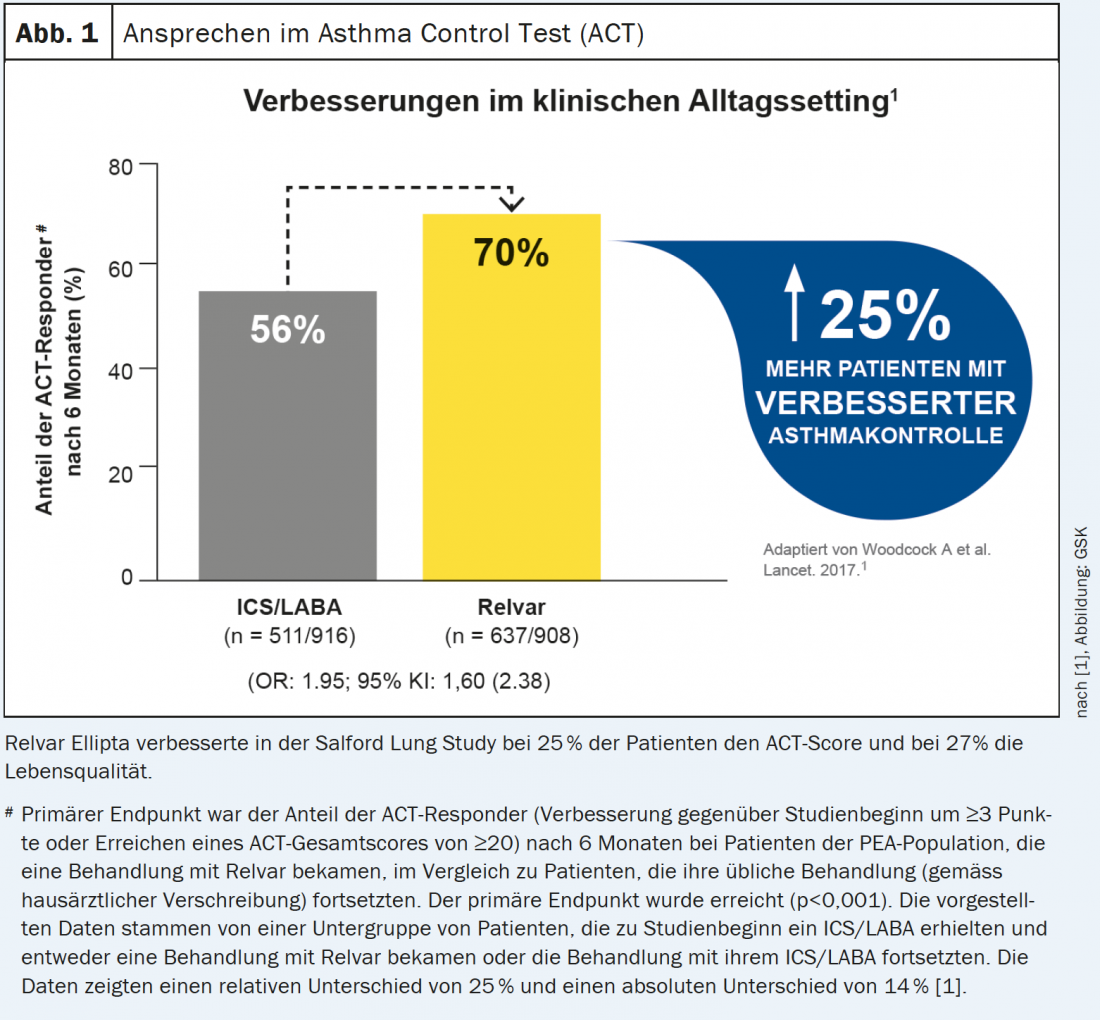
- El control proactivo del asma permitió mejorar el control en un 25% más de pacientes (56% en el grupo de control frente al 70% con Relvar Ellipta) en la práctica diaria [1] (Fig. 1).
- Además de los síntomas, la calidad de vida también mejoró en un 27% más de pacientes [1,10].
- El perfil de efectos secundarios en ambos brazos del estudio fue comparable, y la neumonía sólo se produjo en raras ocasiones [1].
Alto índice terapéutico como hito
El furoato de fluticasona en Relvar tiene un índice terapéutico significativamente superior al de otros ICS y, por tanto, puede conseguirse un efecto antiinflamatorio más potente con una menor exposición sistémica [2,3]. Así, a la dosis más baja, muestra un efecto antiinflamatorio 3,4 veces superior al de la budesonida [2,3]. Relvar en el dispositivo Ellipta, cuando se utiliza una vez al día, ofrece un valor añadido que los pacientes sienten inmediatamente, a saber, disminuye la inflamación de las vías respiratorias [8], disminuye la hiperreactividad bronquial [8] y se ralentiza el remodelado de las vías respiratorias [8].
Mejora de la calidad de vida
El efecto notable, que se manifiesta en una mejora de todos los componentes del TCA, sólo se ve compensado por efectos sistémicos indeseables muy leves [10]. En particular, los pacientes se beneficiaron de una mejora relevante de su calidad de vida [10].



Pie de imprenta
Texto:
Dra. Renate Weber
Primera publicación:
Tribuna Médica 40/2021. Los interlocutores están de acuerdo con la segunda publicación. ©Tribuna Médica
Este artículo ha sido elaborado con el amable apoyo de GlaxoSmithKline AG, Talstrasse 3-5, 3053 Münchenbuchsee, Suiza.
PM-CH-FFV-ADVR-210003-11/2021
© Prime Public Media AG, Zúrich 2021
Literatura:
Woodcock A, et al: Eficacia del furoato de fluticasona más vilanterol en el control del asma en la práctica clínica: un ensayo controlado aleatorizado, abierto y de grupos paralelos. Lancet 2017; 390: 2247-2255.
Daley-Yates P: Corticosteroides inhalados: potencia, equivalencia de dosis e índice terapéutico. BJCP 2015; 80(3): 372-380.
Daley-Yates P, et al: Índice terapéutico de los corticosteroides inhalados en el asma: Una comparación dosis-respuesta sobre la hiperreactividad de las vías respiratorias y la supresión del eje suprarrenal. BJCP 2021; 87: 483-493.
Fletcher M, Hiles D: Discrepancia continua entre la percepción de los pacientes sobre el control del asma y los síntomas en el mundo real: una encuesta cuantitativa en línea de 1.083 adultos con asma del Reino Unido. Prim Care Respir J 2013; 22: 431-438.
Greenblatt M, et al: Comparación de la evaluación del control del asma por el médico y el paciente. Medicina respiratoria 2010; 104(3); 356-361.
Correira de Sousa J, et al: Asthma control, quality of life, and the role of patient enablement: a cross-sectional observational study. Prim Care Respir J 2013; 22(2): 181-187.
Chapman KR, et al: Tratamiento único de mantenimiento y alivio (SMART) del asma: una valoración crítica. Tórax 2021; 65: 47-52.
Ishmael FT: La respuesta inflamatoria en la patogénesis del asma. Revista de la Asociación Americana de Osteopatía 2011; 111: S11-S17.
Kerwin E, et al: Fluticasone furoate/vilanterol once daily improves nighttime awakenings in asthma patients with night symptoms: post-hoc analysis of three randomized controlled trials. J Asthma 2018; 55: 890-897.
10 Svedsater H, et al: Patient-reported outcomes with initiation of flutucasone furoate/vilanterol versus continuing usual care in the Salford Lung Study. Respir Med 2018; 141: 198-206.
11 Katsaounou P, et al: Omalizumab como alternativa al uso crónico de corticosteroides orales en el asma grave. Respir. Med. 2019; 150: 51-62.
12 Wells KE, et al: Real-world effects of once vs. greater daily inhaled corticosteroid dosing on medication adherence. Ann. Alergia, Asma Inmunol. 2013; 111: 216-220.
13 Molimard M, et al: Agudización de la enfermedad pulmonar obstructiva crónica y manejo del dispositivo inhalador: evaluación real de 2935 pacientes. Eur Respir J 2017; 49(2): 1601794.
Relvar Ellipta (polvo monodosis para inhalación). W: Furoato de fluticasona 92 ó 184 μg, vilanterol 22 μg. I: Asma bronquial: Tratamiento regular en adultos y adolescentes a partir de 12 años si son sintomáticos con CSI y broncodilatador de acción corta. EPOC: Tratamiento sintomático en pacientes con FEV
1
<70% y ≥2 exacerbaciones en los últimos 12 meses. D: Asma bronquial: Adultos y adolescentes a partir de 12 años: 1× diario. 1 inhalación de Relvar Ellipta 92/22 ó 184/22. EPOC: Adultos mayores de 40 años: 1× diario. 1 inhalación Relvar Ellipta 92/22. Relvar Ellipta 184/22 no está aprobado para la EPOC.
AI:
Hipersensibilidad a cualquier ingrediente, alergia grave a la proteína de la leche. W/V: No para el tratamiento de síntomas agudos de asma o exacerbaciones agudas de EPOC. Si se produce un broncoespasmo paradójico, trátelo inmediatamente con un broncodilatador de acción corta, interrumpa Relvar Ellipta y considere otras terapias. Posibles efectos cardiovasculares como arritmias; antes de la terapia, aclaración de enfermedades cardiovasculares concomitantes (por ejemplo, se recomienda un ECG para aclarar la prolongación del QTc). Precaución en diabetes, tuberculosis pulmonar, infecciones crónicas/no tratadas. Relvar Ellipta 184/22 no debe utilizarse en caso de deterioro moderado o grave de la función hepática. Pueden producirse efectos adversos sistémicos a dosis elevadas durante un largo periodo de tiempo. Pueden producirse alteraciones visuales con el uso sistémico y tópico de corticosteroides, y debe considerarse la derivación del paciente a un oftalmólogo para la evaluación de las posibles causas. Los pacientes con EPOC que tomaron Relvar Ellipta tuvieron una mayor incidencia de neumonía. En los pacientes asmáticos, la neumonía se produjo con más frecuencia con Relvar Ellipta 184/22 que con Relvar Ellipta 92/22 o placebo. IA: Precaución con la administración concomitante de β-bloqueantes, así como de fármacos que prolonguen el intervalo QTc, tengan efectos simpaticomiméticos o afecten a los niveles de potasio. Debe evitarse la administración concomitante de inhibidores potentes del CYP3A4 (por ejemplo, ketoconazol, itraconazol, claritromicina, ritonavir o productos que contengan cobicistat) a menos que el beneficio supere el aumento del riesgo de efectos secundarios de los corticosteroides sistémicos; en ese caso, debe vigilarse a los pacientes para detectar efectos secundarios de los corticosteroides sistémicos. S/S: Embarazo: Relvar Ellipta no debe utilizarse durante el embarazo a menos que sea claramente necesario. Lactancia: Interrumpa la lactancia o el tratamiento con Relvar Ellipta. UW: Muy frecuentes: dolor de cabeza, nasofaringitis. Frecuentes: Neumonía, infecciones de las vías respiratorias superiores, bronquitis, síntomas de gripe, dolor o candidiasis en la boca y la garganta, sinusitis, faringitis, rinitis, tos, ronquera, dolores abdominales, articulares, de espalda, fracturas, pirexia. Ocasionalmente: extrasístoles. Experiencias posteriores a la comercialización: comunes: espasmos musculares; ocasionales: palpitaciones, taquicardia, hiperglucemia; raras/desconocidas : Reacciones de hipersensibilidad (incluyendo anafilaxia, angioedema, urticaria, erupción cutánea), temblor, ansiedad, broncoespasmo paradójico. AK: B, aprobado en efectivo. Estado de la información: Enero de 2019. GlaxoSmithKline AG, 3053 Münchenbuchsee. Encontrará información detallada en www.swissmedicinfo. ch. Por favor, notifique las reacciones adversas a los medicamentos en pv.swiss@gsk.com. Los profesionales pueden solicitar las referencias mencionadas a GlaxoSmithKline AG.