La inmunoterapia también está adquiriendo cada vez más importancia en el tratamiento del carcinoma urotelial. Especialmente en los tumores avanzados, los inhibidores de los puntos de control ya se utilizan con éxito en la actualidad. Ahora, ya están surgiendo áreas potenciales de aplicación para el avelumab, el atezolizumab y compañía en estadios más tempranos de la enfermedad y líneas de terapia.
En Suiza, la terapia con inhibidores de puntos de control para el carcinoma urotelial está actualmente aprobada exclusivamente para el tratamiento de segunda línea de tumores localmente avanzados o metastásicos [1]. Sin embargo, es probable que las recientes ampliaciones de las indicaciones del avelumab y el pembrolizumab por parte de la EMA ( Agencia Europea del Medicamento ) y la FDA (Administración de Alimentos y Medicamentos de EE.UU.) anuncien un uso más amplio de estos agentes en el futuro. Arlene O. Siefker-Radtke, catedrática de Oncología Urogenital de la Universidad de Texas, examinó más de cerca el papel de los inhibidores de puntos de control en el carcinoma urotelial en la Reunión Anual de la NCCN de este año y presentó en su charla una visión general de las cuestiones de investigación más candentes en este campo.
Norma establecida para tumores avanzados
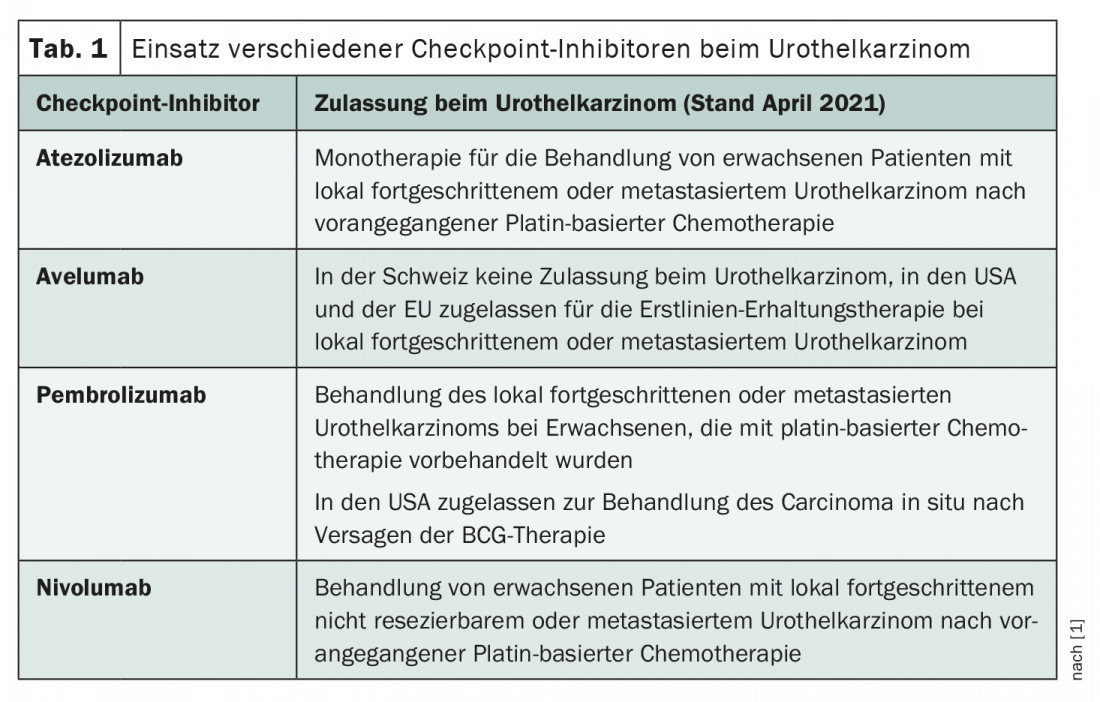
A lo largo de los años, las quimioterapias basadas en el platino en particular han demostrado su eficacia en el tratamiento del carcinoma urotelial avanzado. Así, la gemcitabina/cisplatino y el MVAC (metotrexato, vinblastina, doxorrubicina y cisplatino) siguen siendo los tratamientos de primera línea más comunes en la actualidad [2]. Sin embargo, a principios del milenio ya se realizaban esfuerzos para explorar opciones inmunoterapéuticas. Por ejemplo, se ha intentado utilizar interferón-α2b [3]. Sin embargo, éstas siguieron sin tener un éxito significativo, hasta que aparecieron los inhibidores de los puntos de control. En la segunda línea, la inmunoterapia ganó aceptación rápidamente, de modo que Swissmedic aprobó el atezolizumab, el nivolumab y el pembrolizumab para esta indicación. Actualmente se están investigando intensamente otras áreas de aplicación, y la introducción de los inhibidores de los puntos de control en la terapia de primera línea no sólo es posible, sino probable en un futuro próximo. De hecho, no fue hasta enero de este año cuando el avelumab recibió la aprobación en Europa para el tratamiento de mantenimiento de primera línea del carcinoma urotelial avanzado, menos de un año después de que la FDA le diera luz verde (tab. 1) .
En el carcinoma urotelial avanzado, según Siefker-Radtke, hay básicamente tres enfoques de tratamiento que implican inhibidores de puntos de control que están actualmente en el punto de mira. En su presentación, distinguió entre terapias combinadas, terapias de mantenimiento y uso secuencial.
Inhibidor de puntos de control sí – ¿pero cómo?
Además de las combinaciones de quimioterapia e inhibidores de los puntos de control, los inmunoterápicos también se están probando actualmente en terapia de mantenimiento tras una respuesta a la quimioterapia y en uso secuencial, es decir, en caso de progresión de la enfermedad tras una terapia de primera línea. Según Siefker-Radtke, aún no está claro el momento óptimo de uso en particular. Los datos más convincentes existen sobre los beneficios en la segunda línea. Por ejemplo, el pembrolizumab prolonga la mediana de supervivencia global tras la progresión de la enfermedad en unos tres meses en comparación con la quimioterapia basada en taxanos [4]. El inhibidor de los puntos de control también presenta tasas de respuesta más elevadas y un perfil de toxicidad más favorable. Por ello, no es de extrañar que los inhibidores de los puntos de control ya estén aprobados para esta indicación en Suiza.
Los datos sobre el beneficio de la terapia de mantenimiento tras una respuesta a la quimioterapia de primera línea son algo más escasos. El avelumab, en particular, se encuentra actualmente en el punto de mira de esta cuestión. La sustancia fue aprobada por la FDA en 2020 y por la EMA en enero de este año para terapia de mantenimiento. Los últimos datos se presentaron en el Congreso de la ASCO (Sociedad Americana de Oncología Clínica) de 2020 y hacen albergar esperanzas de que el avelumab pueda desempeñar pronto un papel importante como fármaco de primera línea también en Suiza, con al menos una ligera mejora del pronóstico en el carcinoma urotelial avanzado. Así, la mediana de supervivencia global en el estudio se prolongó con la terapia de mantenimiento de 14,3 a 21,4 meses. Sin embargo, subrayó Siefker-Radtke, también se dispone de datos menos claros. Por ejemplo, el pembrolizumab no ha resultado convincente en la terapia de mantenimiento hasta ahora. Se observó una mejora de la supervivencia libre de progresión (SLP), pero no una prolongación de la supervivencia global [5]. El experto lo atribuyó, entre otras cosas, a que el estudio sobre pembrolizumab permitía un cross-over, es decir, el uso del inmunoterápico en caso de progresión, mientras que el de avelumab excluía esta opción. Siefker-Radtke concluyó que el momento de la aplicación no es potencialmente tan crucial y que el uso de inhibidores del punto de control per se podría ser el factor decisivo. O dicho de otro modo: “Es una cuestión de SIEMPRE inmunoterapia frente a NUNCA inmunoterapia”. En este sentido, puede tener sentido abstenerse de una aplicación precoz y esperar a la progresión de la enfermedad o a una recaída antes de administrar la inmunoterapia. Por último, no hay que olvidar los efectos secundarios. Por lo tanto, queda por ver si la terapia de mantenimiento con inhibidores de los puntos de control llegará a establecerse.
Otro foco de atención de diversos estudios es la investigación sobre el uso paralelo de quimioterapia e inmunoterapia en primera línea. En el Congreso de la Sociedad Europea de Oncología Médica (ESMO) 2018 se presentaron datos prometedores sobre la administración neoadyuvante de una terapia combinada de gemcitabina y pembrolizumab, y el ensayo IMvigor130 investiga la adición de atezolizumab a la quimioterapia en el carcinoma urotelial avanzado, por citar dos ejemplos. Hasta ahora, este enfoque no ha sido aprobado en ninguna parte, pero con los resultados de ensayos más amplios, los cambios en el tratamiento están potencialmente en el horizonte en los próximos años. En su presentación, Siefker-Radtke expuso las razones a favor y en contra de la terapia combinada.
Tensión entre sinergismo y antagonismo
El efecto de la administración simultánea de quimioterapia e inmunoterapia no es fácil de evaluar por varias razones. Las múltiples influencias sobre el sistema inmunitario y las diversas interacciones conducen a una situación extremadamente compleja. Por ejemplo, aunque la quimioterapia provoca un aumento de la presentación de antígenos y, por tanto, podría potenciar el efecto de los inhibidores de los puntos de control, también causa inmunosupresión.
Siefker-Radtke destacó dos razones en particular para la terapia simultánea. Además del aumento de la presentación de antígenos a través de la quimioterapia, que podría ser beneficioso para la inmunoterapia, el bloqueo de los puntos de control también es potencialmente beneficioso para la eficacia de la quimioterapia. Por ejemplo, el aumento de la expresión de PD-L1 tras la quimioterapia es un factor de pronóstico desfavorable y posiblemente podría reducirse mediante un ataque dirigido. Por tanto, el bloqueo adicional PD1/PD-L1 podría ayudar a prevenir la resistencia a la quimioterapia [6,7]. Los estudios realizados hasta la fecha sugieren que la terapia combinada puede ser especialmente útil para las personas con metástasis hepáticas. Este subgrupo con enfermedad mayoritariamente rápidamente progresiva tiene una respuesta significativamente peor a la monoterapia con inhibidores de puntos de control, como se ha demostrado en estudios de pacientes sin tratamiento previo con cisplatino [8,9].
Sin embargo, también hay consideraciones que hablan en contra del uso conjunto de la quimioterapia y la inmunoterapia. Así, el efecto de los inhibidores de los puntos de control podría verse atenuado por la neutropenia inducida por la quimioterapia [10]. Según Siefker-Radtke, la quimioterapia también da lugar a otros mecanismos que favorecen la tolerancia del sistema inmunitario y contrarrestan así la inmunoterapia. Por ejemplo, el número de células dendríticas disminuye con la quimioterapia, mientras que el número de células T reguladoras aumenta. En esta área de conflicto entre efectos sinérgicos y antagónicos, quedan por ver los resultados de estudios más amplios antes de poder evaluar de forma concluyente el beneficio real de la terapia combinada.
Inhibidores de los puntos de control en fases más tempranas de la enfermedad
Cada vez hay más datos que apoyan el uso de inhibidores de los puntos de control en fases más tempranas de la enfermedad. En este caso, el experto presentó dos indicaciones en las que pronto podría utilizarse la inmunoterapia: Carcinoma superficial in situ de la vejiga urinaria y como terapia adyuvante tras la cirugía radical. Si fracasa el tratamiento con BCG, el pembrolizumab ya está aprobado en EE.UU. para el tratamiento del carcinoma in situ. En el ensayo Keynote 057, cuyos últimos resultados se presentaron en el Congreso ASCO 2020, el 40% de los pacientes experimentaron una respuesta completa al pembrolizumab al cabo de tres meses, que duró una media de 16,2 meses.
Especialmente en los casos de expresión de PD-L1, la administración adyuvante de inhibidores de puntos de control también suscita esperanzas. Por ejemplo, la administración postoperatoria de nivolumab durante un año se investigó en el ensayo de fase III Checkmate 274 en pacientes de alto riesgo. Los datos publicados recientemente muestran una prolongación de la mediana de supervivencia libre de enfermedad en la población general de 10,9 meses con placebo a 21 meses. Este efecto fue aún más impresionante con una expresión de PD-L1 ≥1%. En particular, surgió una meseta en el subgrupo con expresión de PD-L1 – según Siefker-Radtke, un indicio de control de la enfermedad a más largo plazo.
Así que la conclusión es que en el carcinoma urotelial ocurren muchas cosas. En los próximos años, los inhibidores de los puntos de control también podrían utilizarse cada vez más en fases más tempranas de la enfermedad, especialmente de forma adyuvante y en el carcinoma in situ. Queda por ver si puede establecerse su uso como terapia de mantenimiento para el carcinoma urotelial avanzado. En la actualidad, las combinaciones de quimioterapia e inmunoterapia están todavía en pañales, pero no son en absoluto impensables.
Fuente: Presentación “New Settings for Immune Checkpoint Inhibitors in Urothelial Bladder Cancer”, Arlene O. Siefker-Radtke, MD, en la reunión anual de la NCCN, Virtual Conduct 18-20 March 2021.
Congreso: Conferencia anual de la NCCN
Literatura:
- Información sobre medicamentos de swissmedic. www.swissmedicinfo.ch (última consulta: 28.03.2021)
- de Wit M, et al: Carcinoma vesical (carcinoma urotelial) – Onkopedia. Estado marzo 2019. www.onkopedia.com/de/onkopedia/guidelines/blasenkarzinom-urothelkarzinom (último acceso 28.03.2021).
- Siefker-Radtke AO, et al: Ensayo de fase III de fluorouracilo, interferón alfa-2b y cisplatino frente a metotrexato, vinblastina, doxorrubicina y cisplatino en cáncer urotelial metastásico o irresecable. J Clin Oncol. 2002; 20(5): 1361-1367.
- Bellmunt J, et al: Pembrolizumab como terapia de segunda línea para el carcinoma urotelial avanzado. N Engl J Med. 2017; 376(11): 1015-1026.
- Galsky MD, et al: Randomized Double-Blind Phase II Study of Maintenance Pembrolizumab Versus Placebo After First-Line Chemotherapy in Patients With Metastatic Urothelial Cancer. J Clin Oncol. 2020; 38(16): 1797-1806.
- Shin J, et al: Efecto de la quimioterapia basada en platino sobre la expresión de PD-L1 en las células tumorales del cáncer de pulmón no microcítico. Cancer Res Treat. 2019; 51(3): 1086-1097.
- Jiang Q, et al: CD19. Cancer Immunol Immunother. 2019; 68(1): 45-56.
- Balar AV, et al: Atezolizumab como tratamiento de primera línea en pacientes elegibles para cisplatino con carcinoma urotelial localmente avanzado y metastásico: un ensayo de fase 2, multicéntrico y de un solo brazo. Lancet. 2017; 389(10064): 67-76.
- Balar AV, et al: Pembrolizumab de primera línea en pacientes elegibles para cisplatino con cáncer urotelial localmente avanzado e irresecable o metastásico (KEYNOTE-052): un estudio multicéntrico, de un solo brazo, de fase 2. Lancet Oncol. 2017; 18(11): 1483-1492.
- Galsky MD, et al: Ensayo de fase 2 de gemcitabina, cisplatino más ipilimumab en pacientes con cáncer urotelial metastásico e impacto de las mutaciones genéticas de respuesta al daño del ADN en los resultados. Eur Urol. 2018; 73(5): 751-759.
InFo ONCOLOGY & HEMATOLOGY 2021; 9(2): 28-29 (publicado el 11.4.21, antes de impresión).











