El éxito del tratamiento del ictus depende esencialmente del tiempo que transcurre entre el inicio de los síntomas y la recanalización del vaso ocluido. Para ello, es importante que se reconozcan rápidamente los síntomas sospechosos de ictus y que se les remita inmediatamente a un centro especializado. El tratamiento estándar para el ictus agudo es la trombólisis sistémica con activador del plasminógeno recombinante (rtPA) en las 4,5 horas siguientes al inicio de los síntomas, aunque la revascularización endovascular es un complemento recomendado de la trombólisis sistémica, especialmente para las oclusiones de vasos proximales.
El ictus es una emergencia médica que se manifiesta mediante la aparición de un déficit neurológico focal agudo, como la aparición repentina de trastornos del habla, hemiplejia o discapacidad visual. Es una de las principales causas de mortalidad y morbilidad en todo el mundo. El 85% de los ictus son isquémicos y, por tanto, el resultado de un trastorno circulatorio circunscrito del cerebro. La diferenciación clínica fiable entre éstas y el 15% restante causado por hemorragias intracraneales no es posible sin un diagnóstico por aparatos. Dado que los conceptos terapéuticos del ictus isquémico son fundamentalmente diferentes de los del ictus hemorrágico, y que el concepto de “el tiempo es cerebro” se aplica esencialmente al primero, sólo hablaremos del ictus isquémico en el curso posterior de este artículo.
Concepto de penumbra
Teoría: El concepto de “tiempo es cerebro” en el ictus isquémico se basa en gran medida en el concepto de penumbra isquémica, descrito, por ejemplo, por Astrup et al. Se ha descrito 1981. La penumbra isquémica se define como una zona cerebral funcionalmente alterada pero estructuralmente intacta, que suele rodear al núcleo del infarto. En la penumbra isquémica es posible un suministro aún rudimentario de oxígeno y nutrientes a las células, por ejemplo a través de vasos colaterales, de modo que la muerte celular se retrasa al menos. Lo crucial de la penumbra isquémica es que puede pasar a un estado de daño permanente e irreversible en un tiempo relativamente corto. Esta ventana temporal permite recanalizar un vaso ocluido y salvar así la zona cerebral correspondiente (penumbra).
En un experimento con animales se pudo demostrar que las alteraciones de las funciones neuronales se producen después de que el flujo sanguíneo regional caiga por debajo de un valor aproximado de 20 ml/100 g/min de sangre y son reversibles después de que se recupere la perfusión. Si el flujo sanguíneo sigue disminuyendo o si persiste este estado de flujo sanguíneo reducido, se producen daños irreversibles en la zona afectada del cerebro [1]. Esta cascada isquémica consiste en la despolarización y la eliminación de aminoácidos tóxicos. La afluencia de iones de calcio y sodio provoca un edema citotóxico. Esto activa las enzimas proteolíticas y libera radicales libres, lo que provoca un mayor daño celular. Este proceso puede extenderse a la penumbra, dando lugar al agrandamiento del infarto [2].
El concepto “el tiempo es cerebro”, basado en estas observaciones, se ve respaldado además por las estimaciones de que cada minuto que se deja sin tratar un ictus se pierden potencialmente 1,9 millones de neuronas y 14 mil millones de sinapsis [3].
Hoy en día, la imagen multimodal puede utilizarse en pacientes con ictus en cuestión de minutos para hacer una declaración sobre el tejido isquémico, es decir, el llamado “tejido isquémico”. núcleo del infarto y la penumbra, pueden realizarse (Fig. 1a-d, Fig. 2a-d) . Esto es posible mediante tomografía computarizada (TC) y resonancia magnética (RM). Otras técnicas de diagnóstico por imagen como la PET y la SPECT también lo harían posible, pero no están disponibles con la suficiente rapidez en una situación de emergencia.
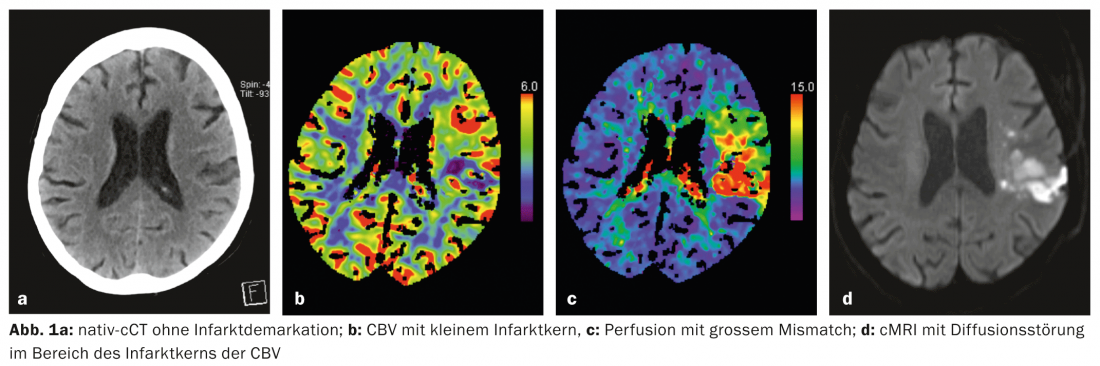
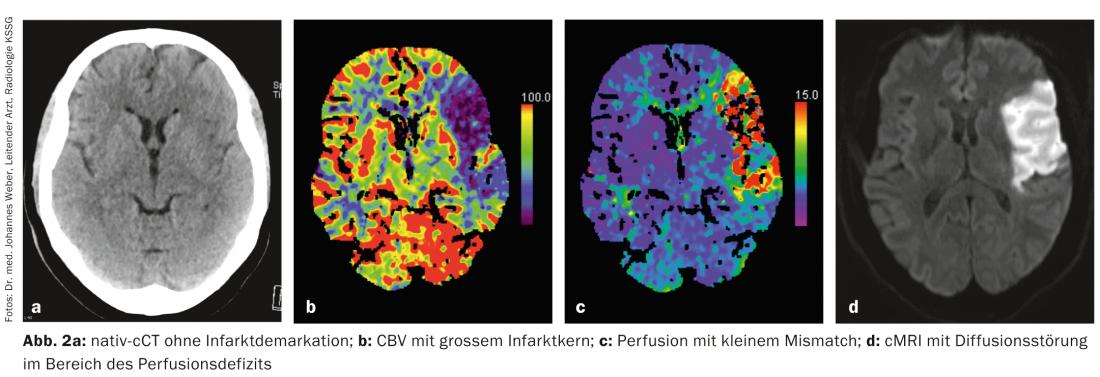
Práctica: En medicina del ictus, es importante hacer todo lo posible para evitar la expansión del infarto cerebral en el sentido de un infarto de la penumbra. Una parte esencial de la terapia del ictus es la recanalización lo más rápida posible del vaso ocluido. La única terapia aprobada para este fin es la trombólisis sistémica con activador del plasminógeno recombinante (alteplasa; rtPA) en las 4,5 horas siguientes al inicio de los síntomas. En casos seleccionados, también puede realizarse una trombectomía mecánica mediante angiografía intervencionista.
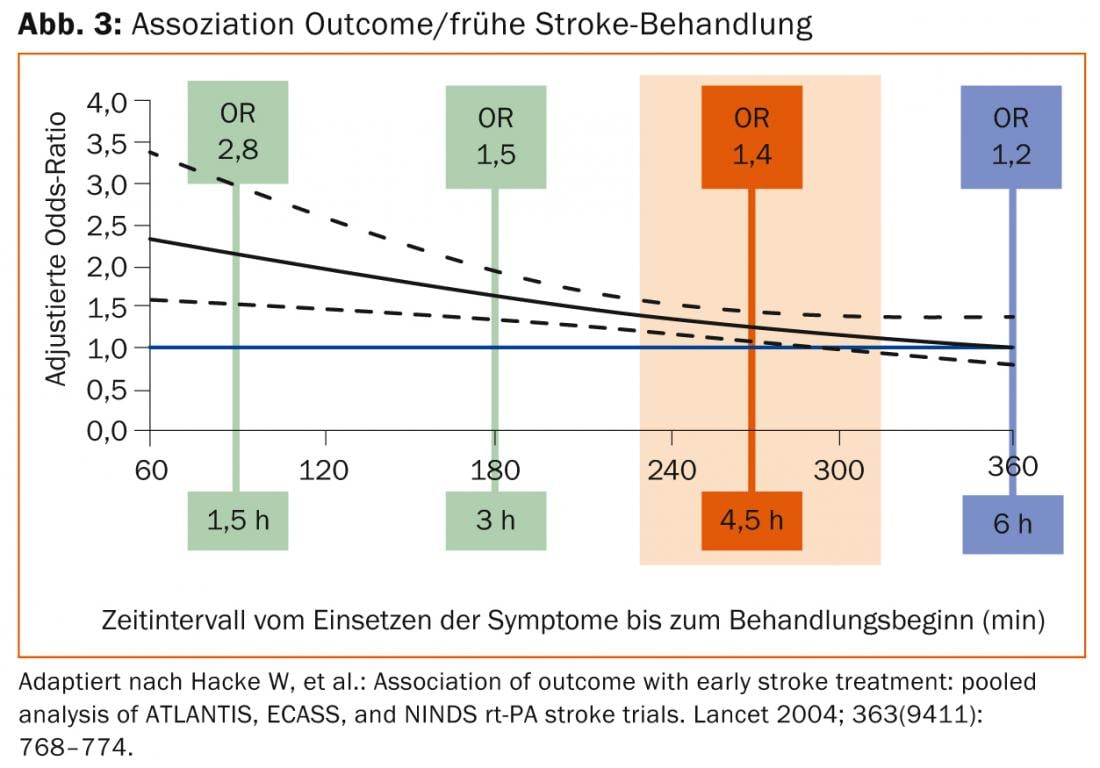
Según la fisiopatología presentada, existe una clara dependencia temporal del éxito de esta terapia. El número necesario a tratar (NNT) para un buen resultado es de 4,5 si la terapia de lisis se inicia en los primeros 90 minutos. Esto aumenta a 9 para el inicio entre 90 y 180 minutos y a 14,1 para el inicio entre 180 y 270 minutos (Fig. 3).
Otras medidas que reducen la propagación del infarto son la profilaxis intensiva de las infecciones y la reducción agresiva de las temperaturas corporales elevadas, el control óptimo de los niveles de glucosa en sangre, el equilibrio de líquidos y electrolitos y el control óptimo de la presión arterial y la respiración.
Pérdida de tiempo en la vía de tratamiento del ictus agudo
La cadena de tratamiento del ictus se divide en la fase de prehospitalización (inicio de los síntomas hasta el ingreso en el hospital) y la fase de hospitalización (ingreso en el hospital hasta el inicio de la terapia). Sin duda, el mayor tiempo se pierde en la fase de prehospitalización [4]. El tiempo perdido desde la aparición de los síntomas hasta la alerta a los servicios de emergencia depende del nivel de conocimiento de la población sobre los síntomas sospechosos de ictus y sobre la necesidad de alertar inmediatamente a los servicios de emergencia. El siguiente eslabón importante es el servicio de ambulancias, donde el reconocimiento de síntomas sospechosos de ictus debería activar un algoritmo de derivación predefinido con remisión inmediata a un hospital que pueda ofrecer terapia de ictus agudo (unidades de ictus). Como han demostrado diversos estudios, un traslado directo a un centro especializado con una información previa lo más precisa posible conduce a un inicio más rápido del tratamiento y, por tanto, a un mejor resultado [5].
Escalas como la Escala prehospitalaria de ictus de Cincinnati se utilizan para identificar síntomas sospechosos de ictus. Esta escala mide tres parámetros clínicos simples (paresia facial, paresia unilateral del brazo, afasia) y tiene una sensibilidad del 90% y una especificidad del 66% para la presencia de un ictus de la circulación anterior [6].
Fase de hospitalización
A su llegada al hospital de destino, debe realizarse un diagnóstico rápido mediante pruebas de laboratorio básicas (especialmente hemograma y coagulación), constantes vitales, una anamnesis orientada a los síntomas y exámenes clínicos estandarizados (“Escala de ictus de los Institutos Nacionales de Salud” [NIHSS]), ECG y, lo más importante, diagnóstico cerebral por imagen. Los procesos en la clínica de destino deben estar estructurados de forma tan eficiente que
- El diagnóstico por imagen (TAC o RMN) puede realizarse no más tarde de 25 minutos después de la llegada (tiempo “de puerta a TAC”).
- La trombólisis sistémica puede realizarse como muy tarde 60 minutos después de la llegada (tiempo “puerta-aguja”).
- A continuación, el paciente puede seguir siendo controlado y tratado en una unidad de ictus [7].
Las oclusiones de vasos proximales muestran bajas tasas de recanalización con trombólisis sistémica, por lo que en estos casos debe evaluarse la posibilidad de un tratamiento endovascular (con catéter). En el caso de una isquemia asociada a una trombosis de la arteria basilar, esta terapia es posible incluso hasta doce horas después de la aparición de los síntomas. La decisión sobre qué pacientes pueden recibir estas terapias debe ser tomada caso por caso por especialistas experimentados en ictus.
Ahorro de tiempo en la fase de prehospitalización
Relaciones públicas: Para lograr una derivación más rápida de los pacientes con ictus a una unidad de ictus, las campañas de educación pública, que deben llevarse a cabo a intervalos regulares, han demostrado su eficacia, ya que de lo contrario el efecto no dura más de cinco meses. La experiencia demuestra que las futuras campañas deberían centrarse más en grupos objetivo específicos como las personas mayores, las minorías, los vecinos de los supervivientes de un ictus, los estudiantes de medicina e incluso los niños como posibles futuros pacientes, familiares o futuros médicos [8].
Información previa: Tanto la Sociedad Alemana de Neurología como las sociedades profesionales internacionales recomiendan informar con antelación al hospital de destino sobre la llegada del paciente. Esto permite la activación temprana del equipo de ictus y el suministro de TC, lo que puede reducir significativamente el tiempo hasta la terapia y aumentar la tasa de trombolisis.
Ahorro de tiempo en la fase de hospitalización
Para permitir un proceso fluido y una coordinación óptima entre las disciplinas implicadas, es indispensable definir algoritmos de actuación. Estos incluyen, entre otros:
- Activación de una “lysecall” por el neurólogo de guardia inmediatamente después de recibir el registro para notificarlo a todas las partes implicadas
- Tenga preparada la sala de shock, el equipo de ictus (neurólogo experimentado y enfermeras cualificadas), el TAC y el radiólogo.
Telemedicina: Para posibilitar la trombolisis más rápida posible de un paciente en hospitales geográficamente remotos sin la experiencia y los recursos de personal correspondientes, se desarrolló el concepto de conexión telemédica a un centro de ictus con la posibilidad de interacción en directo y transmisión de los hallazgos.
Literatura:
- Heiss WD, et al: Penumbra isquémica: pruebas de imagen funcional en el hombre. J Cereb Blood Flow Metab. 2000; 20(9): 1276-1293.
- Sitzer M, Steinmetz H: Libro de texto de neurología. Urban&Fischer 2011; 121-122.
- Saver JL, et al: El tiempo es cerebro – cuantificado. Ictus 2006; 37: 263-266.
- Puolakka T, et al: Análisis secuencial de los retrasos previos al tratamiento en la trombólisis del ictus. Acad Emerg Med. 2010; 17(9): 965-969.
- Pe’rez de la Ossa N, et al: Influencia del ingreso directo en centros integrales de ictus en el resultado de los pacientes con ictus agudo tratados con trombolisis intravenosa. J Neurolog 2009; 256(8): 1270-1276.
- Kothari RU, et al: Escala prehospitalaria de ictus de Cincinnati: reproducibilidad y validez. Ann Emerg Med 1999; 33: 373-378.
- Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares. Actas de un Simposio Nacional sobre Identificación Rápida y Tratamiento del Ictus Agudo 1996.
- Haass A, et al: El tiempo es cerebro. Nervenarzt 2013; Nov 27. [Epub ahead of print].
InFo Neurología y Psiquiatría 2014; 12(2): 4-6