La proctitis venérea no es infrecuente. El 34% de los hombres seropositivos tienen problemas anorrectales [1]. En pacientes con síntomas de proctitis y/o relaciones anales receptivas en cualquiera de sus formas, siempre hay que pensar en una enfermedad infecciosa de transmisión sexual (ETS). La proctitis suele ser asintomática (>85%) con gonorrea y Chlamydia trachomatis, serovares D-K [2]. La detección directa de patógenos (cultivo bacteriano, PCR dirigida) a partir de un frotis tomado anoscópicamente es adecuada para el esclarecimiento. Sólo para el diagnóstico de la sífilis es útil e indicado un examen serológico. La transmisión del VIH se ve facilitada en la proctitis [3]. También deben tenerse en cuenta las coinfecciones con otras ITS (incluidas las pruebas del VIH, la hepatitis B, C). En el caso del linfogranuloma venéreo (LGV), se aplica lo siguiente: “Una vieja enfermedad con un vestido nuevo”, también en Suiza [4].
La proctitis se define como la inflamación de las partes distales del recto. La proctitis infecciosa puede transmitirse por vía sexual durante los contactos genito-anal y oro-genital y también como infección por frotis con dedos e instrumentos desde un orificio corporal hasta el ano. Los patógenos anorrectales de transmisión más común son N. gonnorhoeae, C. trachomatis (incluido el linfogranuloma venéreo), el virus del herpes simple y el Treponema pallidum [5]. El uso del preservativo no garantiza la protección contra las ITS (“infecciones de transmisión sexual”), ya que a menudo intervienen vías de transmisión distintas a la penetración del pene [6].
Síntomas
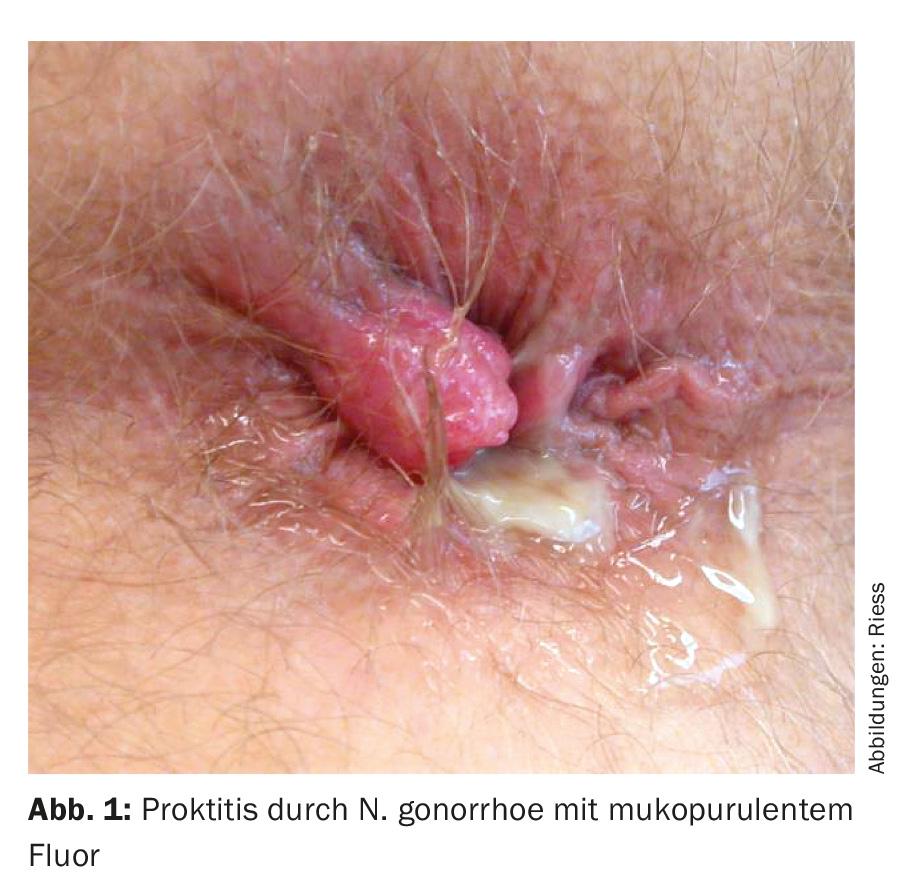
Los posibles síntomas de proctitis son fluorosis mucopurulenta, hemorragia anorrectal, estreñimiento, ganas de defecar, tenesmo, dolor sordo, plenitud rectal o defecación incompleta (Fig. 1) . Sin embargo, la proctitis también suele ser asintomática (gonorrea y clamidia).
Los síntomas de la proctocolitis incluyen diarrea de pequeño volumen, sangre en las heces, dolor abdominal bajo, sensibilidad abdominal y sensación de defecación incompleta. La transmisión puede producirse a través de prácticas sexuales oro-anales. En los viajes, las amebas y, en los pacientes seropositivos, la shigella pueden ser a menudo la causa de la proctocolitis, por lo que se recomienda un examen de las heces para detectar estos síntomas.
La enteritis se presenta con diarrea acuosa de gran volumen, sangre en las heces, dolor abdominal medio, náuseas, vómitos, malestar general, fiebre y pérdida de peso. La mucosa rectal no suele verse afectada. La shigelosis puede transmitirse por contacto oro-anal y provocar estos síntomas (Tab. 1).
Examen de proctitis
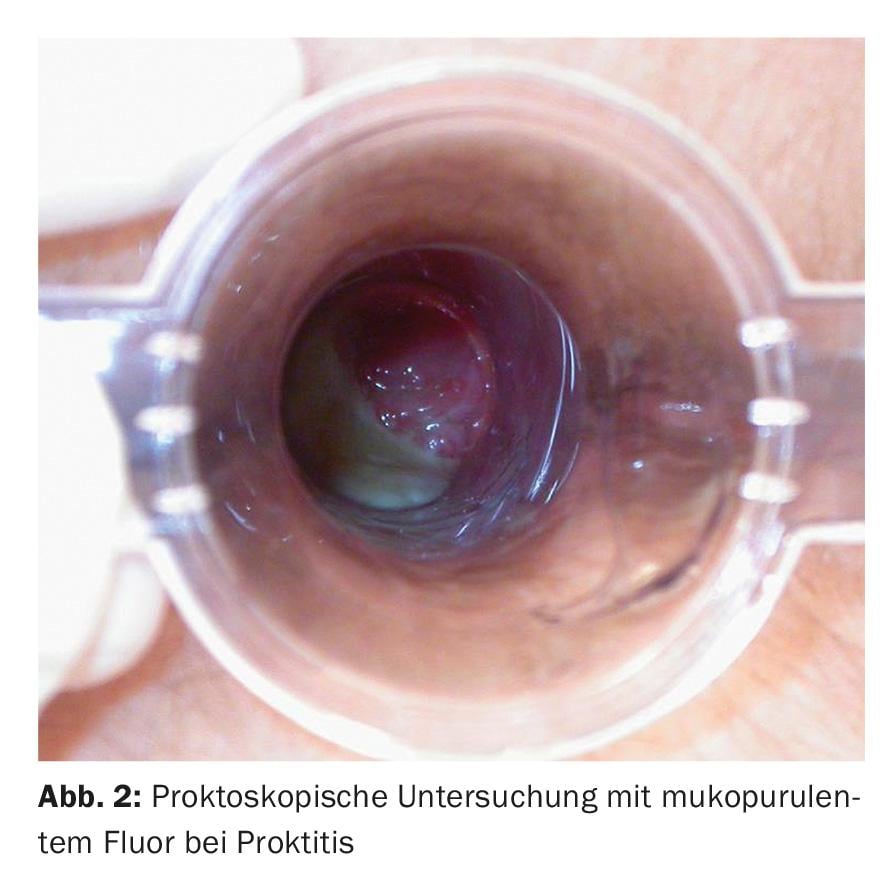
La proctoscopia es el examen de elección. Se evalúa la presencia de moco o fluor purulento en el recto, la pérdida de dibujo vascular, el edema de la mucosa, la hemorragia de contacto y la ulceración. Además, se puede tomar una preparación directa para la detección de diplococos (gonococos) y muestras para el examen PCR específicamente a través del proctoscopio. Dado que la proctitis venérea suele ser asintomática, se recomienda realizar exámenes y frotis periódicos si existen antecedentes de relaciones anales receptivas (especialmente sin protección) para descartar esta enfermedad (Fig. 2).
Neisseria gonorrhoeae
Según estimaciones de la OMS, la gonorrea es una de las ITS más comunes, con 106 millones de nuevos casos cada año. La gonorrea anal se da predominantemente en HSH (“hombres que tienen relaciones sexuales con hombres”) con coito anal receptivo. También puede transferirse al canal anal mediante la inserción de dedos o instrumentos. A menudo es asintomática, pero en las proctitis floridas puede haber abundantes secreciones pútridas. La gonorrea se diagnostica mediante PCR (reacción en cadena de la polimerasa). Sin embargo, debido a la frecuente resistencia, debe realizarse un cultivo bacteriano para cada PCR positivo para gonococos. Con el creciente desarrollo de resistencias en todo el mundo, actualmente se recomienda la terapia dual con 500 mg de ceftriaxona i.m. y 2 g de azitromicina p.o. [7].
Chlamydia trachomatis, serovares D-K
Los serovares A-C de Chlamydia trachomatis conducen al tracoma (enfermedad ocular), los serovares D-K causan uretritis, cervicitis, endometritis y proctitis. En Europa, las infecciones causadas por Chlamydia trachomatis, serogrupo D-K, son las infecciones de transmisión sexual más frecuentes [2,8,9]. Aún más frecuente que la gonococia anal, la infección anal por clamidias (serovares D-K) es casi siempre asintomática. Clínicamente, sin embargo, suele haber hallazgos de proctitis. La detección se realiza por PCR a partir de un frotis. La terapia estándar es 100 mg de doxiciclina 2×/d durante siete a diez días, alternativamente azatioprina 1 g una vez.
Chlamydia trachomatis, serovares L1-3 o linfogranuloma venéreo (LGV)
Los serovares L1-3 causan el linfogranuloma venéreo, que es invasivo, linfotrópico y normalmente sintomático. Sin embargo, también se describen cursos asintomáticos [2,8]. Antes de 2004, esta enfermedad se encontraba predominantemente en la región ecuatorial. Desde entonces, se ha observado una aparición endémica del LGV en los HSH seropositivos en el mundo occidental. También se observó un conglomerado de infecciones por LGV en Zúrich. Al igual que en los demás centros europeos, se vieron afectados predominantemente HSH seropositivos [4]. El tipo de serovar más común es el L2b [10].
El periodo de incubación es de una a cuatro semanas. El curso trifásico comienza con una úlcera o erosión genital (estadio I), seguida de linfadenopatía inguinal (Bubo, estadio II) y finalmente un síndrome ano-genito-rectal con fibrosis y complicaciones irreversibles (estadio III). Las complicaciones pueden incluir fístulas, obstrucción linfática, elefantiasis, estenosis o estomas (enfermedades ulcerosas de los genitales femeninos). En las infecciones rectales primarias, normalmente sólo se encuentran síntomas de proctitis. A diferencia de las infecciones anales por Chlamydia trachomatis, serovares D-K, la LGV suele provocar una proctitis grave, que no pocas veces se interpreta erróneamente como enfermedad intestinal inflamatoria crónica. A nivel mundial, la LGV representa sólo entre el 2 y el 10% de las enfermedades genitoulcerativas, pero está en aumento [4,9]. El LGV es la tercera causa más común de proctitis en HSH después del VHS y la gonorrea [11].
La PCR se considera el patrón oro para detectar el serovar. El cultivo está obsoleto y la serología es inespecífica. Según la recomendación de consenso europea, la terapia consiste en doxiciclina 2×100 mg/día durante 21 días. Existen muy pocas pruebas de la eficacia de una dosis única de azitromicina. Otra posibilidad es la eritromicina 4×500 mg/día durante 21 días.
Treponema pallidum
Desde el cambio de milenio, la sífilis ha experimentado un verdadero renacimiento. Se da predominantemente en hombres, especialmente en HSH [7]. Como todas las demás enfermedades de transmisión sexual, también favorece la transmisión del VIH [3]. El efecto primario es extragenital en más del 20%. Las lesiones anales primarias suelen ser asintomáticas; a menudo sólo se descubren como hallazgos incidentales durante los exámenes proctológicos. Clínicamente, se encuentran cambios ulcerosos indoloros en la mucosa o ulceraciones perianales. En el estadio II de la sífilis se producen, entre otros, condilomas lata, que son muy contagiosos.
La detección del primer estadio de la sífilis se realiza mediante microscopía de campo oscuro, aunque en la actualidad suele sustituirse por el examen PCR, más sensible y mucho más sencillo. Tras unas cinco semanas, la infección puede detectarse de forma fiable serológicamente (TPPA, VDRL, IgM). La terapia es y sigue siendo una inyección de depósito con bencilpenicilina benzatina una vez 2,4 millones de unidades por vía intramuscular. Actualmente, no se encuentran resistencias.
Virus del herpes simple
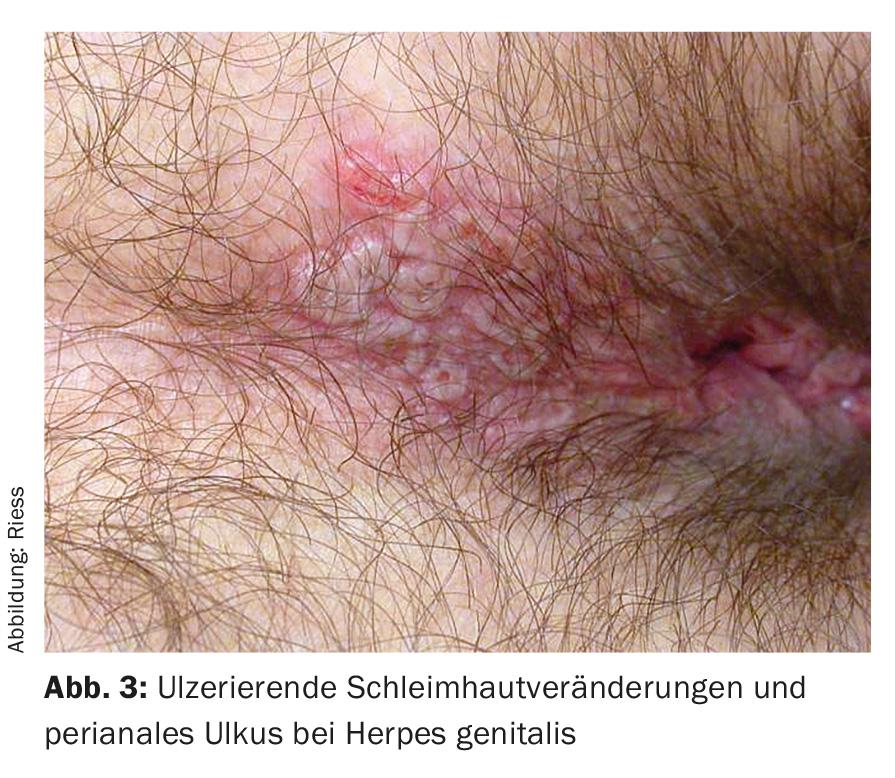
Las infecciones por herpes genital están causadas por el herpes simple tipo 2 en más del 80%, con cursos crónicos recurrentes en cerca del 20% de los casos. La clínica característica de vesículas agrupadas suele estar ausente en la localización perianal; se observan enrojecimiento extenso atípico, lesiones ulcerativas de la mucosa y úlceras perianales (Fig. 3). La infestación suele ir asociada a picores y dolor. Las formas necrotizantes y ulcerosas se observan en la inmunodeficiencia. La detección se realiza mediante PCR. La terapia consiste en valaciclovir 2×500 mg p.o. durante cinco días.
Diagnósticos diferenciales
El diagnóstico diferencial de la proctitis debe incluir también causas no venéreas de proctocolitis o enteritis con los patógenos correspondientes (Shigella spp, Salmonella spp, Campylobacter spp, citomegalovirus, amebiasis, giardiasis), infección estafilocócica rectal y enfermedad inflamatoria intestinal crónica.
En el caso de cambios cutáneos perianales inflamatorios o ulcerosos, también deben excluirse como causas un carcinoma anal, un tumor epitelial como el carcinoma basocelular, una génesis irritativa-tóxica, los condilomas acuminados, así como la enfermedad de Crohn.
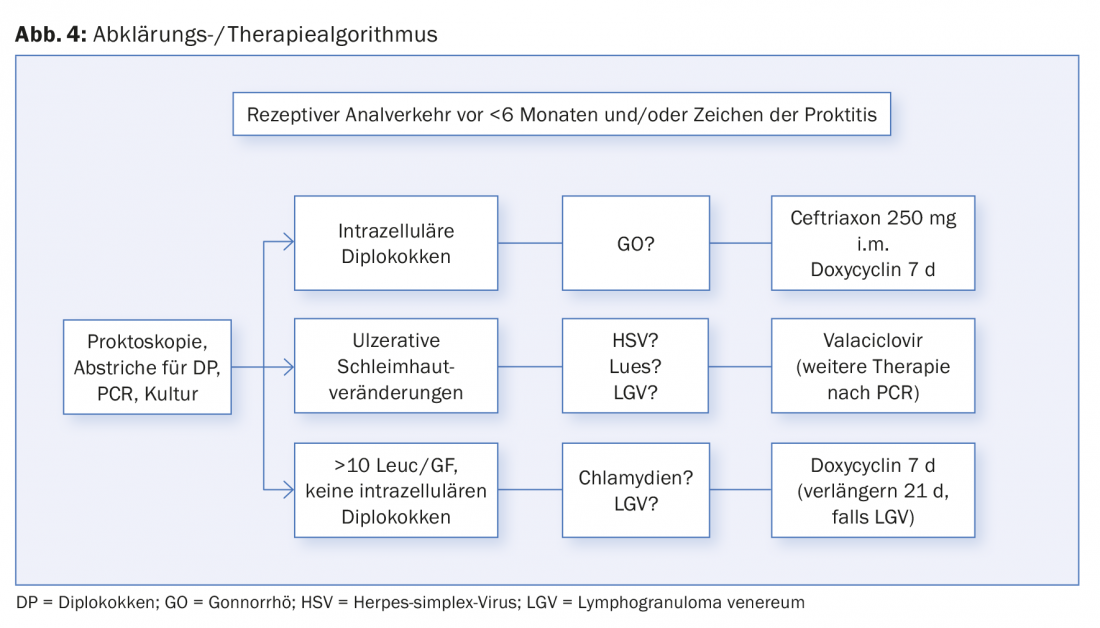
La figura 4 muestra un algoritmo de evaluación y tratamiento del coito anal receptivo y/o síntomas de proctitis.
Conclusión
Y lo que es más importante, si los síntomas anorrectales no están claros, también debe considerarse una génesis venérea, especialmente en los HSH con los correspondientes antecedentes sexuales. En pacientes con relaciones anales receptivas sin protección, también debe buscarse la proctitis asintomática mediante frotis regulares.
Agradecimientos: Muchas gracias al Dr. Christoph Riess, que nos ha facilitado todas las fotos.
Literatura:
- Yuhan R, et al: Enfermedad anorrectal en pacientes infectados por el VIH. Dis Colon Rectum 1998 Nov; 41(11): 1367-1370.
- Spornraft-Ragaller P, Boashie U, Esser S: Infecciones de transmisión sexual de la región anorrectal. Dermatólogo 2015; 66: 430-438.
- Cohen MS, et al: Reducción de la concentración de VIH-1 en el semen tras el tratamiento de la uretritis: implicaciones para la prevención de la transmisión sexual del VIH-1. Grupo de investigación AIDSCAP Malawi. Lancet 1997 Jun 28; 349(9069): 1868-1873.
- Kamarashev J, et al: Linfogranuloma venéreo en Zúrich, Suiza: proctitis por Chlamydia trachomatis serovar L2 entre hombres que tienen relaciones sexuales con hombres. Swiss Med Wkly 2010; 140: 209-212.
- Kreuter A: Proctología – Enfermedades de la región anal. JDDG 2016; 14(4): 352-375.
- de Vries HJC, et al: Directriz europea 2013 sobre el tratamiento de la proctitis, la proctocolitis y la eneteritis causadas por patógenos sexualmente transmisibles. Int Journal of STC & AIDS 2014; 25(7): 465-474.
- Schöpfer H, et al: S2k Guideline diagnosis an and thereapy of syphilis- short version. J Dtsch Dermatol Ges 2015; 13: 472-480.
- Fuchs W, Brockmeyer NH: Infecciones de transmisión sexual. J Dtsch Dermatol Ges 2014; 12: 45-63.
- Lanjouw E, et al: Directriz europea 2015 sobre el tratamiento de las infecciones por Chlamydia trachomatis. Int J ETS SIDA 2016 abr; 27(5): 333-348.
- de Vries HJC, et al: Directriz europea 2013 sobre el tratamiento del linfogranuloma venéreo. JEADV 2015; 29: 1-6.
- Halse TA, Musser KA, Limberger RJ: A multiplexed real-time PCR assay for rapid detection of Chlamydia trachomatis and identification of serovar L-2, the major cause of lymphogranuloma venereum in New York. Mol Cell Probes 2006 Oct; 20(5): 290-297.
PRÁCTICA DERMATOLÓGICA 2016; 26(3): 16-19