En el pasado, un diagnóstico de fibrosis quística (FQ) era sinónimo de muerte prematura, normalmente antes de los 30 años. Esta enfermedad hereditaria sigue acortando la vida, pero gracias a los avances en la investigación y a las nuevas terapias, la esperanza media de vida en Europa Central ya ha aumentado a más de 50 años. Para los afectados en la edad adulta, existen ahora varias opciones para controlar la fibrosis quística.
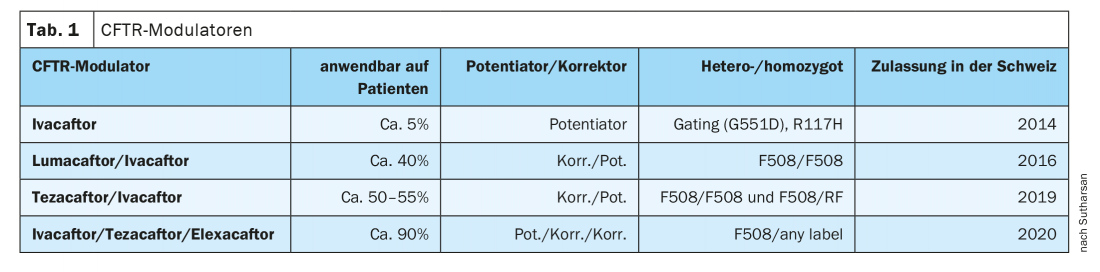
La introducción de las enzimas pancreáticas supuso un gran avance terapéutico, pero la creación de centros en los que los pacientes con FQ reciben un tratamiento específico también ha contribuido a aumentar la probabilidad de supervivencia, afirmó a modo de introducción el Dr. Sivagurunathan Sutharsan, médico jefe de la Clínica de Neumología de la Ruhrlandklinik, Medicina Universitaria de Essen (D). En 1989, se descubrió el gen CFTR. Aunque todavía no existe terapia génica, la medicina personalizada también ha llegado a la fibrosis quística, afirma el experto: en 2014, se aprobó en Suiza el ivacaftor (IVA) como primer principio activo para un pequeño grupo de pacientes (5-6%); entretanto, hay otros tres moduladores que están disponibles como combinaciones y, desde agosto de 2020, también como triple (Tab.1).
Complicaciones crecientes con la edad
Las primeras complicaciones se manifiestan ya en la infancia: los niños presentan con frecuencia (hasta un 25%) íleo meconial como indicador más precoz, generalmente (>85%), la insuficiencia pancreática ya está presente y a menudo se producen infecciones pulmonares (sin embargo, sólo <25% Pseudomonas aeruginosa). En el transcurso de la infancia y la adolescencia, la proporción de P. aeruginosa aumenta hasta aproximadamente el 45%, pero también entran en juego otros órganos, como las enfermedades hepáticas y los pólipos nasales (25%). En la edad adulta, aparece finalmente la enfermedad completa, que incluye graves enfermedades pulmonares y óseas (resumen 1).
Durante la primera década de vida, Staphylococcus aureus y Haemophilus influenzae son las bacterias más comunes aisladas del esputo en la FQ; en la segunda y tercera décadas de vida, Pseudomonas aerugiosa es mucho más común.

Las exacerbaciones aumentan el riesgo
Un aspecto central del tratamiento de la fibrosis quística es evitar las exacerbaciones. “Los pacientes que sufren más de dos exacerbaciones pulmonares al año tienen un mayor riesgo de muerte o de trasplante de pulmón”, explicó el Dr. Sutharsan. Reducir el número de exacerbaciones y la consiguiente pérdida de función pulmonar debería ser, por tanto, uno de los principales objetivos del tratamiento de la FQ.
En cuanto al tratamiento, suele prescribirse fisioterapia para sacar las secreciones de los pulmones, la terapia antibiótica está indicada para las infecciones crónicas por Pseudomonas o estafilococos, y los macrólidos como la azitromicina se utilizan a menudo como terapia a largo plazo para la colonización crónica por Pseudomonas. Si los pacientes sangran, se tiene la opción de realizar una oclusión de la arteria bronquial. La terapia con moduladores de CFTR es nueva (resumen 2).

Moduladores CFTR
En la mutación más común, F508del, la proteína se produce pero suele degradarse en la célula. Pero con los nuevos moduladores, los correctores de CFTR elexacaftor (ELX) y tezacaftor (TEZ), el canal de cloruro se estabiliza en diferentes sitios de unión, evitando así su degradación. A esto le sigue un transporte dirigido a la superficie celular, donde el potenciador CFTR ivacaftor puede aumentar la probabilidad de apertura del canal de cloruro. En la actualidad existen 4 moduladores CFTR aprobados. Mientras que el ivacaftor puede utilizarse en cerca del 5% de la población con FQ, la nueva combinación triple de ivacaftor/tezacaftor/elexacaftor puede tratar a cerca del 90% de los pacientes en todo el mundo. Como requisito previo para el tratamiento, se debe tener al menos una mutación 508 en un alelo. “La segunda mutación no suele tener importancia”, afirma el Dr. Sutharsan. Los principales efectos secundarios descritos son erupciones cutáneas y picor, que suelen controlarse bien con antihistamínicos orales o esteroides. Sin embargo, se describe un buen efecto no sólo en los pulmones, sino también en los senos paranasales.
En su clínica de Essen, el Dr. Sutharsan y sus colegas han ajustado a 133 pacientes con FQ a la nueva triple ELX/TEZ/IVA (80 homocigotos, 32 + 21 (caso de dificultad) heterocigotos). En el grupo homocigoto, hubo 96 hospitalizaciones con terapia i.v. debido a exacerbaciones en los 12 meses anteriores. En 6 meses con el triple, este número se redujo a sólo 5 terapias i.v. La situación era similar en los heterocigotos: 29 + 74 (privaciones) tratamientos i.v. antes de la iniciación durante un periodo de 12 meses se convirtieron en sólo 2 + 7 (privaciones) tratamientos i.v. en los primeros 6 meses con ELX/TEZ/IVA. Aún está por ver la evolución posterior, pero las cifras “ya muestran el enorme progreso en la terapia que traen consigo los nuevos moduladores”, concluyó el Dr. Sutharsan.
Fuente: 128. Congreso de la Sociedad Alemana de Medicina Interna (DGIM)
InFo NEUMOLOGÍA Y ALERGOLOGÍA 2022; 4(2): 30-31