La enfermedad de Parkinson se define clínicamente por los principales síntomas motores derivados de la degeneración nigroestriatal. Sin embargo, en la actualidad se reconoce que la enfermedad suele constar de varias patologías. ¿De qué nuevos descubrimientos se dispone en relación con la fisiopatología y cómo puede tratarse actualmente el Parkinson de forma eficaz?
La prevalencia de la enfermedad de Parkinson ha aumentado rápidamente en los últimos diez años en el contexto del envejecimiento de la población. Los estudios histopatológicos han demostrado una pérdida neuronal progresiva.
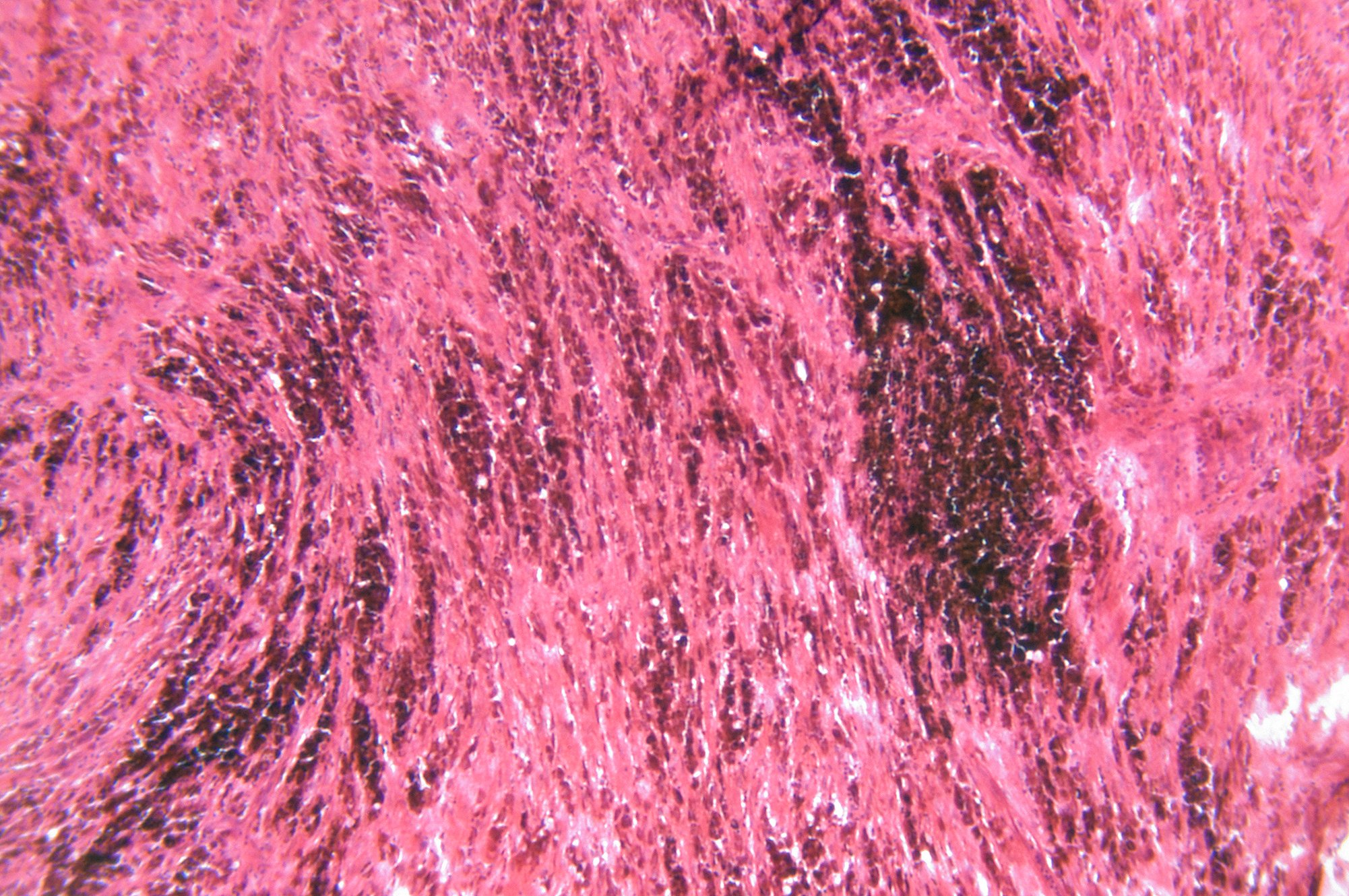
[LB] [LN] En la mayoría de los pacientes, existe una acumulación progresiva de inclusiones intraneuronales proteináceas (cuerpos de Lewy y neuritas de Lewy ) en estructuras subcorticales y corticales. El principal componente de los LB y LN es una forma agregada de α-sinucleína, una proteína implicada en la regulación de la fusión de las vesículas sinápticas con la membrana plasmática. Los monómeros de α-sinucleína mal plegados se agregan para formar oligómeros y después fibrillas. Éstas se consideran especies tóxicas que no sólo provocan daños neuronales directos, sino que también se propagan de forma priónica entre las neuronas. Aún se desconocen las causas y los mecanismos que provocan el mal plegamiento y la agregación de la α-sinucleína.
Según la estadificación de Braak, el depósito de LB sigue una secuencia predecible que progresa en un patrón estereotipado que comienza caudalmente desde el tronco cerebral inferior y se desplaza rostralmente implicando a la sustancia negra en el estadio 3 de Braak. Alternativamente, la patología puede originarse en el bulbo olfatorio. Sin embargo, los estadios 1 y 2 de la EP de Braak se producen antes de que se observe la patología de los cuerpos de Lewy en la sustancia negra, y en estos estadios ya existe una densidad neuronal reducida de neuronas positivas para la tirosina hidroxilasa (TH) y un mayor porcentaje de neuronas inmunonegativas para la TH cargadas de melanina. Esto sugiere que la neurodegeneración y la disfunción neuronal preceden a la patología de Lewy α-syn-positiva en la sustancia negra.
Variedad de síntomas y su base
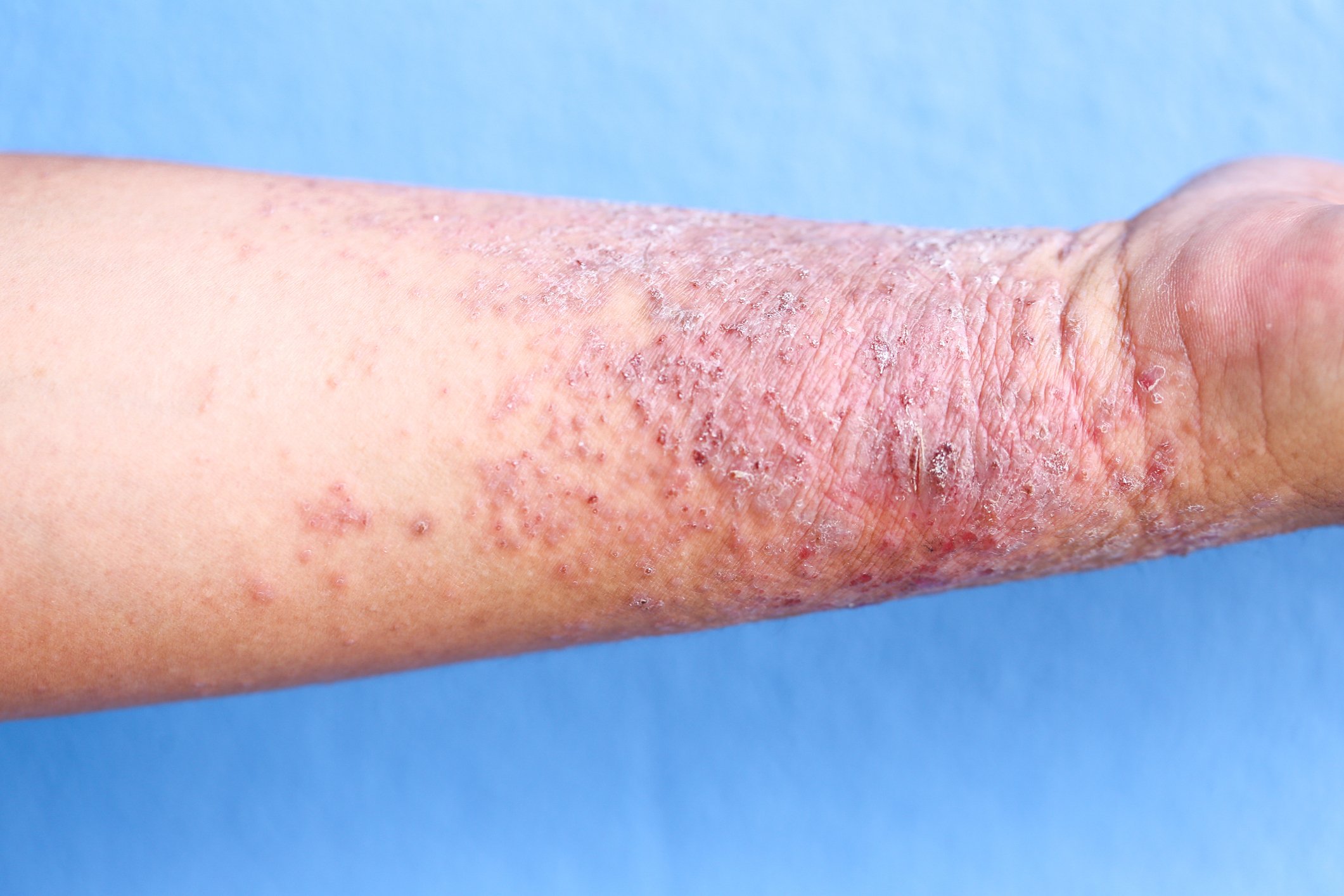
Las personas con enfermedad de Parkinson experimentan una combinación de síntomas motores y no motores (SNM), que pueden variar de un paciente a otro. Los síntomas motores clásicos incluyen temblor en reposo, lentitud de movimientos (bradicinesia) y aumento del tono muscular (rigidez). Se cree que los pacientes que presentan un fenotipo de temblor dominante, caracterizado por temblor en reposo dominante o asimétrico aislado, tienen mejor pronóstico que el grupo más raro de pacientes que presentan alteraciones del equilibrio y la marcha. Los síntomas no motores, como la disfunción autonómica, la hiposmia y los trastornos del estado de ánimo, pueden aparecer en cualquier fase de la enfermedad. Un estudio descubrió que el 90,3% de los pacientes experimentaban NMS antes del diagnóstico de la enfermedad de Parkinson. La hiposmia y el trastorno aislado del comportamiento del sueño REM (iRBD, por sus siglas en inglés), en particular, se consideran fuertes factores de riesgo para la enfermedad de Parkinson. Muchos pacientes con estos dos síntomas ya presentan patología de α-sinucleína.
Sin embargo, la agregación de tau en la sustancia negra también se da por supuesta, sobre todo en el caso de los trastornos de la marcha. En algunos estudios, el 50% de los cerebros de pacientes con Parkinson mostraban inclusiones de tau. La tau es una proteína de origen normal que sufre amplias modificaciones postraduccionales como la hiperfosforilación, el acortamiento y la desglicosilación. Esto da lugar a isoformas proteicas insolubles, mal plegadas y agregadas. Puede producirse una alteración de la red de microtúbulos y un deterioro del transporte axonal, lo que en última instancia conduce a la degeneración sináptica y neuronal. Inicialmente, el Parkinson no se consideraba una tauopatía típica. Sin embargo, varios estudios han aportado cada vez más pruebas de la existencia de patología tau en los cerebros de los pacientes de Parkinson. Si la patología tau precede a la patología Lewy y qué papel desempeña en la degeneración nigroestriatal es una cuestión importante que aún no ha sido respondida.
Neurodegeneración y disfunción celular
Observaciones recientes en pacientes con déficits motores leves (MMD) han demostrado ahora que la tau patológica forma parte de un proceso presinuclear temprano de degeneración nigroestriatal en la enfermedad de Parkinson premotora. Sin embargo, este mecanismo propuesto está sujeto al supuesto de que los casos de MMD sean realmente precursores de la enfermedad de Parkinson. Los casos de MMD son intermedios entre la NMD y la EP en cuanto al deterioro motor, la pérdida de células nigrales TH-ir y la pérdida de inervación putamenal TH-ir, y la regulación a la baja de TH fenotípica nigral y putamenal. Todos estos acontecimientos patológicos están asociados a la patología tau, pero no siempre a la α-Syn, ya que se dan por igual en los casos de MMD con y sin patología Lewy.
Gestión del tratamiento de una enfermedad compleja
La monoterapia con L-DOPA tenía el potencial de convertirse en el patrón oro del tratamiento del Parkinson, ya que suministra al cerebro la dopamina que le falta. Sin embargo, como fármaco oral, la L-DOPA presentaba algunas desventajas para su uso clínico regular: debido a su vida media muy corta, debe administrarse con mucha frecuencia (lo que conlleva un cumplimiento deficiente), mientras que su biodisponibilidad bastante variable requiere una titulación individualizada basada en los efectos secundarios derivados de su estrechísimo margen terapéutico. Además, se producen fluctuaciones motoras durante el tratamiento a largo plazo. Por tanto, por razones farmacocinéticas, es importante minimizar la dosis diaria de L-DOPA. Un método para conseguirlo fue la adición de un inhibidor de la descarboxilasa. En 1957, Julius Axelrod aisló una nueva enzima que cataliza la metilación de la adrenalina, la noradrenalina y otras catecolaminas, la catecol-o-metiltransferasa (COMT). Tiene una semivida terminal de unas 12 horas y compite muy eficazmente con la L-DOPA en el transportador de aminoácidos neutros de la barrera hematoencefálica, sobre todo cuando se administra también un inhibidor periférico de la descarboxilasa. Por ello, los pacientes tratados con dosis muy altas de L-DOPA necesitan siempre un inhibidor de la COMT. Éste también está disponible ahora para administración una vez al día.
Para saber más:
- Chu Y, Hirst WD, Federoff HJ, et al: Patología tau nigroestriatal en el parkinsonismo y la enfermedad de Parkinson. Brain. 2024 Feb; 147(2):444-457.
- Pavese N, Ledingham D: Parkinson, ¿hacia dónde nos dirigimos? Br J Hosp Med (Lond). 30 de julio de 2024;85(7): 1-5.
- Riederer P, Horowski R: Terapia con L-DOPA en la enfermedad de Parkinson: algunas reflexiones personales sobre la terapia con L-DOPA desde Viena y Berlín. J Neural Transm (Viena). 2023; 130(11): 1323-1335.
InFo NEUROLOGÍA Y PSIQUIATRÍA 2024; 22(5): 27