“Es más importante saber qué persona tiene una enfermedad que saber qué enfermedad tiene una persona” – esta frase se atribuye a Hipócrates, lo que significa que el antiguo griego ya conocía la utilidad de la terapia personalizada hace unos 2400 años. La medida en que este enfoque puede ayudar también en reumatología a identificar a los pacientes con riesgo de padecer AR en una fase temprana y a tratarlos de forma selectiva es objeto de estudios actuales.
El concepto de medicina de “talla única”, es decir, el curso estandarizado de la terapia independientemente de las peculiaridades del paciente respectivo, naturalmente también conlleva siempre una proporción relativamente alta de efectos secundarios (graves) y de no respondedores. Los efectos de la medicina personalizada, basada en diagnósticos moleculares (análisis de biomarcadores) y en la estratificación de los pacientes basada en biomarcadores, pretenden reducirlos y aumentar la tasa de respondedores.
La lista de medicamentos para los que es obligatorio un test genético en Alemania se extiende a lo largo de 29 páginas en la página web de la Asociación Alemana de Empresas Farmacéuticas Basadas en la Investigación (vfa). Las enfermedades reumáticas aún no figuran en esta lista. Para la Prof. Dra. Andrea Rubbert-Roth, de la Clínica de Reumatología del Hospital Cantonal de St. Gallen, se trata de una prueba evidente de que el tema de la medicina personalizada aún no ha podido establecerse en el campo de la reumatología.
Se sabe que, además de factores ambientales como el tabaco, el polvo y las fibras textiles, también existe una susceptibilidad genética a la artritis reumatoide (AR). Ya en 2007, un gran análisis de datos con 14.000 pacientes y 3.000 sujetos de control en 7 enfermedades demostró que en el caso de la AR con HLA y PTPN22 destacan dos genes. El Prof. Rubbert-Roth recordó la hipótesis denominada Epítopo Compartido (SE), según la cual los alelos HLA-DRB1 asociados a la AR codifican una secuencia común de aminoácidos en la 3ª región hipervariable de la cadena DRβ1.
Los pacientes seropositivos se benefician más
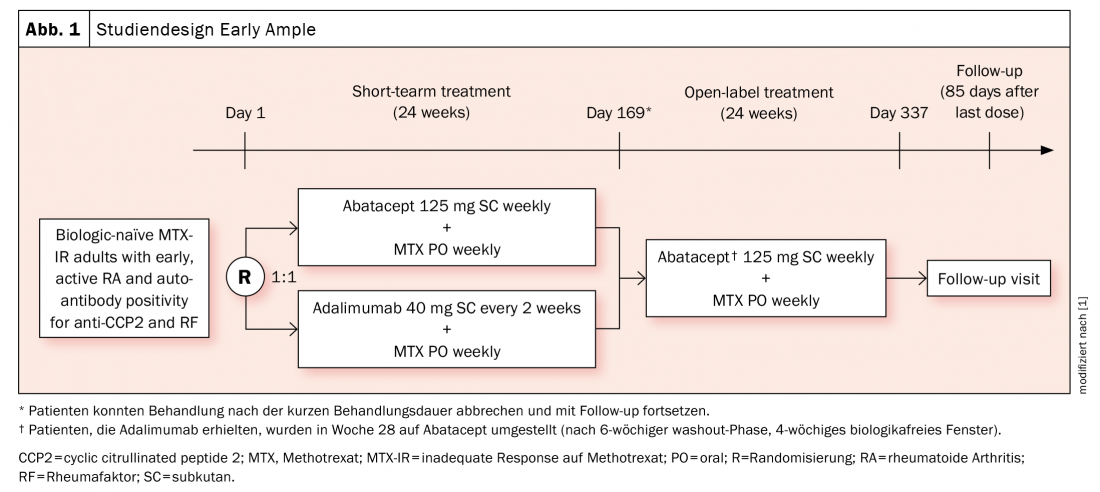
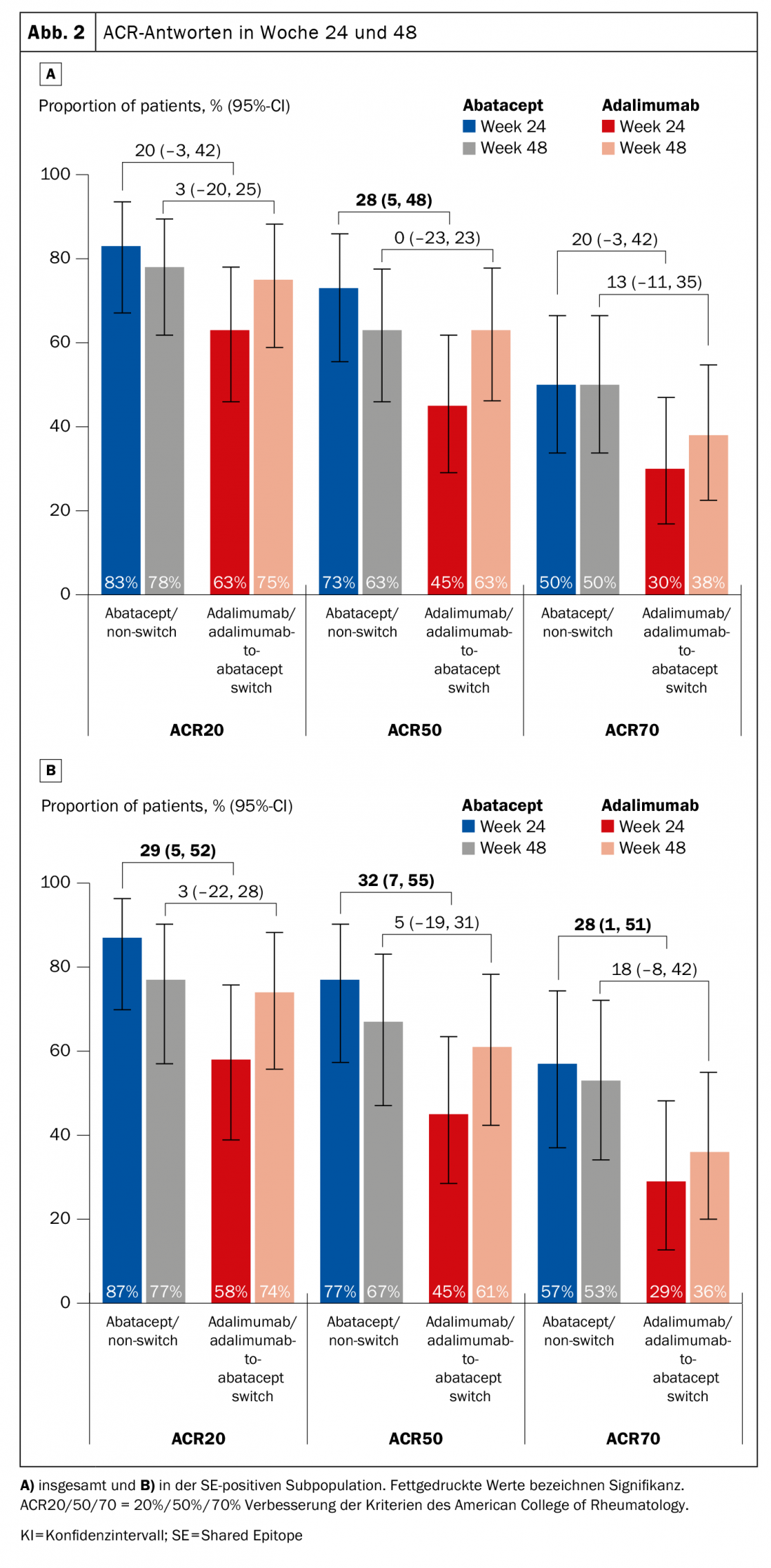
Las evaluaciones anteriores han dado indicios de que los pacientes HLA-DRB1 positivos responden mejor a Abatacept (lo que no significa que esto no pueda aplicarse también a otros agentes, como señaló el experto). El estudio de fase 4 Early Ample [1], publicado en 2021, se basa en esto y dividió a los pacientes con AR temprana sin tratamiento biológico que no habían respondido adecuadamente al metotrexato (MTX) en un brazo de abatacept (n=39, de los cuales 30 eran SE positivos) y otro de adalimumab (n=40, de los cuales 31 eran SE positivos) (Fig. 1) . Los afectados debían ser CCP2 y factor reumatoide positivos. Los sujetos fueron asignados aleatoriamente a ABA o ADA durante 24 semanas y después todos cambiaron a ABA. Se demostró que los pacientes HLA-DRB1 positivos ya tenían significativamente más posibilidades de alcanzar un ACR20, -50 y -70 con abatacept tras 24 y 48 semanas (Fig. 2A). El resultado fue aún más contundente a favor de la subpoblación SE+ (Fig. 2B).
¿Puede prevenirse la AR en pacientes de riesgo?
Se sabe que los pacientes que aún no presentan una sinovitis clínicamente reconocible, pero que ya tienen anticuerpos CCP detectables, tienen un mayor riesgo de desarrollar AR. Si es posible prevenir el desarrollo de la AR en este grupo en una fase temprana y cómo hacerlo es el tema del estudio ARIAA, que se presentó en el Congreso 2021 del ACR [2]. Los criterios de inclusión para este estudio de fase 2 fueron positividad para ACPA (+/- RF), artralgias durante al menos 6 semanas, signos de inflamación de la mano dominante (sinovitis, tenosinovitis u osteítis) en la IRM pero sin inflamación clínica, y ningún tratamiento previo con esteroides o DMARD. 49 pacientes identificados de esta forma fueron tratados con abatacept durante un periodo de 6 meses frente a placebo (n=49). A esto le siguió un periodo de seguimiento de 12 meses sin tratamiento.
El criterio de valoración primario, la mejora en al menos un parámetro de la IRM (puntuación RAMRIS), se cumplió: hubo una mejora significativa en el 61,2% de los pacientes del brazo de abatacept (frente al 30,6% con placebo; p=0,0043). El grupo verum también obtuvo resultados significativamente mejores en los criterios de valoración secundarios de interrupción prematura del estudio y progresión a AR clínica (interrupción 14,3% frente a 42,9%; p=0,0032; progresión 8,2% frente a 34,7%; p=0,0025). Por tanto, el beneficio de Abatacept en comparación con el placebo es claramente visible y el Prof. Rubbert-Roth espera que los resultados adicionales del seguimiento a largo plazo se presenten en la próxima EULAR. “Si los resultados se confirmaran durante el periodo de seguimiento, sería realmente espectacular”, concluye.
Mensajes para llevarse a casa
- La aplicación de nuevos conceptos de estudio que incluyan una estrategia personalizada también puede contribuir a optimizar la eficacia y la seguridad del tratamiento con DMARD en reumatología.
- Prueba de principio: Lo ideal sería que los biomarcadores fueran fácilmente accesibles y fáciles de determinar en el futuro.
- ¿Puede aplicarse este concepto también a otras enfermedades reumatológicas? (por ejemplo, la firma del interferón en el LES)
Literatura:
- Rigby W, Buckner JH, Louis Bridges S, et al: Los alelos de riesgo HLA-DRB1 para la AR se asocian con una capacidad de respuesta clínica diferencial al abatacept y al adalimumab: datos de un estudio individualizado, aleatorizado y comparativo en AR temprana con autoanticuerpos positivos. Arthritis Res Ther 2021; 23: 245; doi: 10.1186/s13075-021-02607-7.
- Rech J, et al: ACR 2021 [#0455].
InFo DOLOR Y GERIATURA 2022; 4(1-2): 20-21