La afectación pulmonar en el contexto de una enfermedad sistémica reumática inflamatoria es una manifestación relativamente frecuente, que requiere un conocimiento adecuado tanto por parte de los neumólogos como de los reumatólogos y, en el mejor de los casos, una atención interdisciplinar de estos casos. Pueden encontrarse diversas patologías parenquimatosas pulmonares, entre las que los cambios granulomatosos deben entenderse como un subgrupo.
La afectación pulmonar en el contexto de una enfermedad sistémica reumática inflamatoria es una manifestación relativamente frecuente, que requiere un conocimiento adecuado tanto por parte de los neumólogos como de los reumatólogos y, en el mejor de los casos, una atención interdisciplinar de estos casos. Pueden encontrarse diversas patologías parenquimatosas pulmonares, entre las que los cambios granulomatosos deben entenderse como un subgrupo. Granuloma se refiere a una acumulación nodular circunscrita de células inflamatorias en el tejido, clásicamente de macrófagos, pero también de granulocitos o linfocitos. Cuando se encuentran pruebas histológicas de enfermedad pulmonar granulomatosa, hay que trabajar con varios diagnósticos diferenciales reumatológicos. El objetivo de este artículo es ofrecer una visión general de las enfermedades pulmonares granulomatosas desde el ámbito reumatológico, con la excepción de la sarcoidosis. La atención se centra en el diagnóstico y, sobre todo, en la terapia.
Vasculitis asociadas a ANCA
Las vasculitis asociadas a ANCA son las primeras que deben tenerse en cuenta. Este grupo de vasculitis de pequeños vasos incluye tres entidades: Granulomatosis con poliangeítis (GPA), poliangeítis microscópica (MPA) y granulomatosis eosinofílica con poliangeítis (EGPA), sin formación de granulomas histológicamente en la MPA.
Granulomatosis con poliangitis (GPA), cuadro clínico
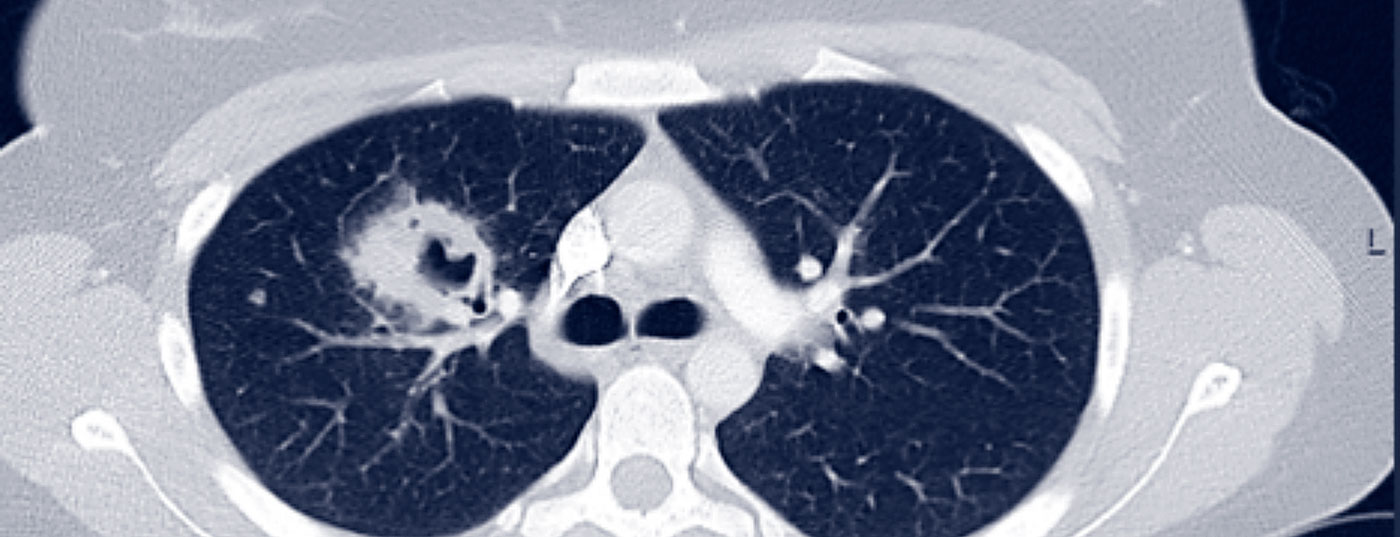
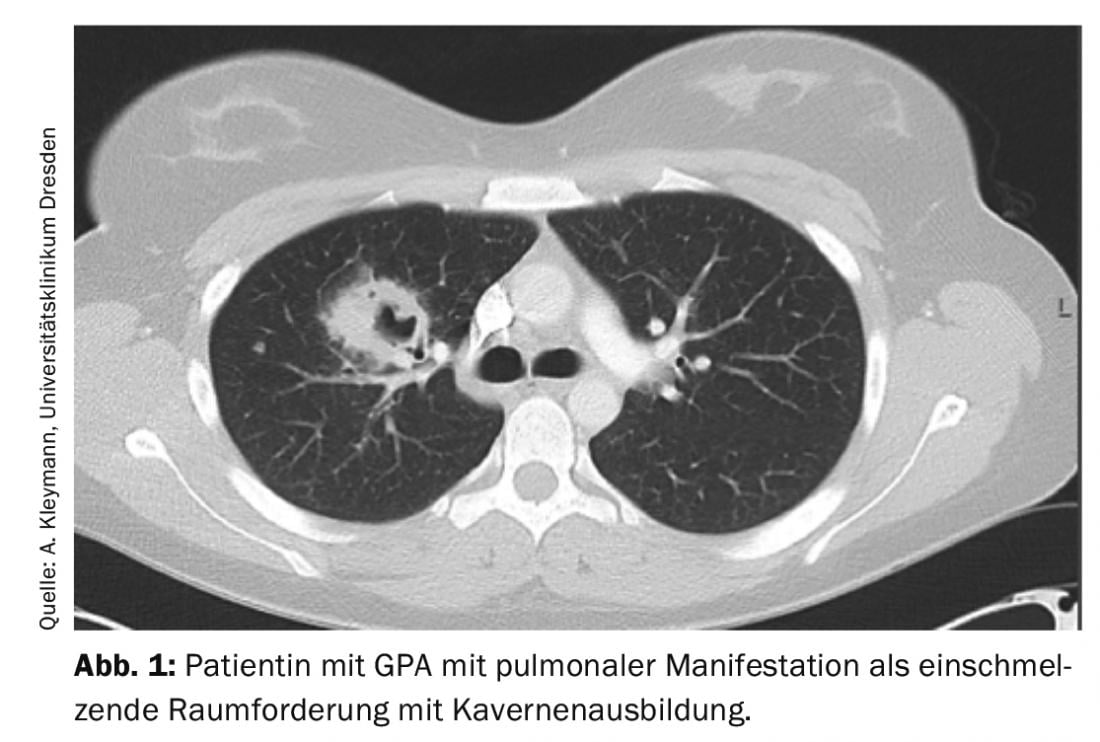
La GPA puede ser inicialmente oligosintomática (fase localizada de la enfermedad). La afectación de la nasofaringe en el sentido de sinusitis crónica o rinitis es típica al principio. Con la afectación pulmonar, la GPA ya se clasifica como enfermedad generalizada, por lo que cabe esperar síntomas clínicos acompañantes (síntomas B, mialgias, artralgias, erupciones cutáneas, artritis) y síntomas paraclínicos (elevación de la PCR y la VSG, anemia, leucocitosis, trombocitosis). La afectación pulmonar es posible en forma de nódulos pulmonares, infiltrados, fibrosis pulmonar, cavernas o incluso hemorragia alveolar (Fig. 1).
Diagnóstico ANCA
Una parte importante del diagnóstico es la determinación de ANCA (anticuerpos citoplasmáticos antineutrófilos) con autoanticuerpos dirigidos contra la proteinasa-3 y la mieloperoxidasa. Los ANCA se describieron por primera vez en 1982 en la glomerulonefritis e inicialmente se evaluaron como asociados a virus. No fue hasta 1985 cuando se describió en pacientes con GPA. Inicialmente, se recomienda la inmunofluorescencia indirecta como patrón oro. Los resultados se clasificarán según el patrón de fluorescencia y el título. pANCA es un patrón de fluorescencia perinuclear, cANCA es un patrón citoplasmático (Fig. 2). En ocasiones, el patrón de fluorescencia se notifica como xANCA, pero se supone que se trata de ANCA inespecíficos, por ejemplo, en el contexto de la colitis ulcerosa.
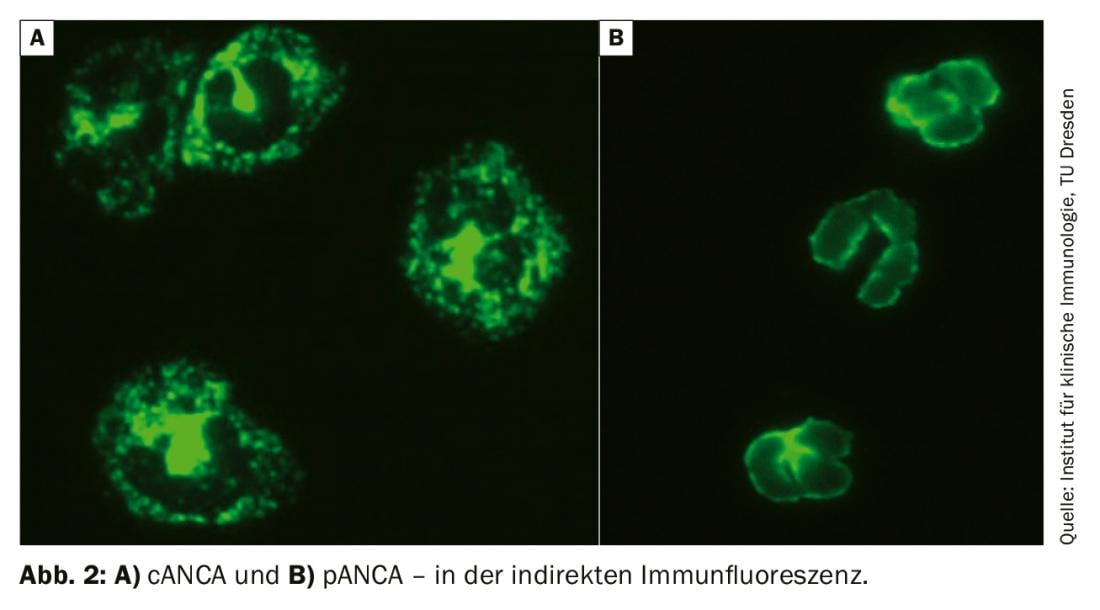
La especificidad de los resultados ANCA positivos sólo aumenta con la detección de autoanticuerpos contra los antígenos diana correspondientes, en el caso de pANCA contra la mieloperoxidasa y en el caso de cANCA contra la proteinasa-3. Su determinación suele realizarse mediante ELISA (ensayo inmunoenzimático). Si se sospecha una vasculitis asociada a ANCA, debe iniciarse un cribado estructurado de otras posibles manifestaciones orgánicas. En particular, debe considerarse la afectación renal en forma de glomerulonefritis inmune de Pauci. Por lo tanto, además de los parámetros de retención (creatinina, volumen urinario, TFG), debe solicitarse sin excepción un sedimento urinario. En caso de eritrocituria, proteinuria o evidencia de cilindros hialinos, debe disponerse la microscopia de orina con interrogatorio de eritrocitos dismórficos en el sentido de un sedimento nefrítico activo y cuantificación de proteínas. Si se sospecha una manifestación renal, es necesaria una biopsia de riñón. A menudo, esto no sólo confirma el diagnóstico, sino que también determina el pronóstico con respecto a la función renal. En pacientes obesos o con mayor riesgo de hemorragia, la biopsia renal transyugular es una alternativa razonable a la biopsia transcutánea.
Terapia
Tras el diagnóstico, en el caso de una manifestación pulmonar de vasculitis, suele indicarse una terapia de inducción con ciclofosfamida o rituximab de forma concomitante con corticosteroides, por lo que los corticosteroides deben reducirse con relativa rapidez para que la dosis sea de 7,5-10 mg/d equivalente de prednisolona al cabo de 3 meses. La excepción es una manifestación aislada con nódulos pulmonares pequeños, no disgregables y sin limitación funcional, en la que también es posible una terapia básica con metotrexato, siempre que no haya insuficiencia renal, o azatioprina sin terapia de inducción previa.
Basándose en los datos del estudio CYCLOPS, la inducción con ciclofosfamida como administración i.v. en bolo debe favorecerse frente a la administración oral debido a las bajas tasas de efectos secundarios [1]. La dosis estándar es de 15 mg/kg de peso corporal, las primeras 3 dosis se administran cada 2 semanas, después cada 3 semanas. La dosis debe ajustarse según la edad y la función renal (reducción a 12,5 mg/kgKG en personas de 60-70 años si la creatinina es de hasta 300 µmol/l, a 10 mg/kgKG en creatinina >300 µmol/l y en >personas de 70 años si creatinina hasta 300 µmol/l, y a 7,5 mg/kgKG en >personas de 70 años si creatinina >300 µmol/l). Por lo general, 6 bolos de son suficientes. En el tratamiento con ciclofosfamida, además de la toxicidad gonadal y para la vejiga urinaria (por lo que también se recomienda la administración de 2-mercaptoetanosulfonatsodio (MESNA)), hay que destacar el riesgo de leucopenia relevante. El nadir se produce 10 -12 días después de la administración, por lo que debe realizarse un control adecuado del recuento sanguíneo en torno a este momento y, si es necesario, un nuevo ajuste de la dosis para la siguiente administración (si los leucocitos <4 GPT/l reducción de la dosis de ciclofosfamida en un 25% y la siguiente administración sólo cuando el recuento de leucocitos >4 GPT/l). Una alternativa a la ciclofosfamida es la inducción con el anticuerpo anti-CD20 rituximab. La eficacia del rituximab quedó demostrada en 2 estudios (RAVE y RITUXVAS). Aquí tanto el régimen con administración 4× semanal de 375 mg/m2 de superficie corporal como 2× 1 g de dosis absoluta a intervalos de 14 días son práctica habitual. Antes de iniciar la terapia con rituximab, debe realizarse un cribado de la hepatitis (riesgo de reactivación de la hepatitis B crónica) e, idealmente, una actualización del estado de vacunación, ya que puede suponerse una respuesta de vacunación reducida/insuficiente durante la terapia.
El aumento del riesgo de infección por patógenos atípicos no debe subestimarse con ambos fármacos, por lo que la profilaxis de Pneumocystis jirovecii es necesaria para todos los pacientes durante la terapia de inducción, independientemente de la sustancia elegida (por ejemplo, Cotrim [Trimethoprim/Sulfamethoxazol] 480 mg 1× diario). La profilaxis puede interrumpirse una vez finalizada la inducción y a la dosis de prednisolona <10-15 mg/d. El papel de la plasmaféresis en cursos graves como la hemorragia alveolar difusa (DAH) sigue considerándose controvertido. La Sociedad Europea de Reumatología (EULAR) recomienda tenerla en cuenta en su última recomendación de 2016; sin embargo, el estudio PEXIVAS publicado en NEJM en febrero de 2020, que incluyó a 31 pacientes de con DAH grave en el brazo de intercambio de plasma y a 30 pacientes en el brazo de estudio sin plasmaféresis, no mostró ningún beneficio para la supervivencia [2].
Una vez completada la inducción, la terapia de mantenimiento debe realizarse normalmente con rituximab (2 dosis de 500 mg i.v. a intervalos de 14 días, seguidas de 500 mg cada 6 meses) o alternativamente con azatioprina (2 mg/kg de peso corporal) durante al menos 2 años. Cuando se inicia la medicación con azatioprina, se requieren inicialmente controles regulares de laboratorio (hemograma y transaminasas) y está contraindicada la medicación conjunta con inhibidores de la xantina oxidasa (alopurinol y febuxostat). Además, en algunos centros se recomienda la determinación de la tiopurina S-metiltransferasa (TPMT) para evitar una supresión grave de la médula ósea en pacientes con la correspondiente deficiencia enzimática.
Las alternativas en caso de contraindicación/intolerancia son el metotrexato (pero no en caso de afectación renal con insuficiencia renal) o el micofenolato mofetilo. Sin embargo, cabe destacar que el micofenolato mofetilo no está aprobado para este fin y, por lo tanto, es un “uso fuera de etiqueta” y también menos eficaz que la azatioprina según los datos del estudio IMPROVE (cociente de riesgos de recaída con micofenolato mofetilo frente a azatioprina 1,69) [3]. Un nuevo e interesante enfoque terapéutico es el bloqueo del receptor del complemento C5a con avacopan [4]. En el estudio presentado en línea en el Congreso Europeo de Reumatismo EULAR de este año, esta sustancia administrada por vía oral mostró un efecto comparable al del grupo de control con esteroides cuando se utilizó de forma concomitante con la terapia estándar con ciclofosfamida o rituximab, pero sin esteroides. Así, en el futuro, se podría prescindir por completo de los esteroides en este grupo de enfermedades utilizando Avacopan.
Granulomatosis eosinofílica con poliangitis (EGPA)
La EGPA supone un reto en el grupo de las vasculitis asociadas a ANCA. Es difícil confirmar el diagnóstico porque la histología a menudo no detecta la vasculitis, los ANCA suelen ser negativos y debe excluirse un síndrome hipereosinofílico primario como expresión de una enfermedad clonal.
Una manifestación pulmonar típica es la aparición de infiltrados volátiles. Histológicamente, a menudo puede detectarse eosinofilia tisular en la biopsia pulmonar. La decisión sobre la terapia tampoco es siempre fácil debido a la insuficiencia de estudios. En ausencia de parámetros pronósticos desfavorables, como la afectación renal o cardiaca, es concebible la monoterapia con corticosteroides; de lo contrario, se dispone de ciclofosfamida para las manifestaciones que ponen en peligro los órganos o de metotrexato y azatioprina para los cursos más leves. El rituximab tiene una importancia secundaria en la EGPA debido a la insuficiencia de datos. Por otro lado, es interesante el uso del antagonista de la IL-5 mepolizumab, que mostró eficacia en un estudio de fase 3 con 136 pacientes con EGPA refractaria o recidivante.
Más pacientes lograron la remisión con la administración de mepolizumab s.c. cada 4 semanas. 300 mg de mepolizumab durante 52 semanas, más pacientes alcanzaron la remisión (32% frente a 3%) y también redujeron la dosis de prednisolona por debajo de 4 mg/d (44% frente a 7%). Sin embargo, incluso en el grupo de mepolizumab no se alcanzó la remisión en el 47% de los casos [5]. El mepolizumab también cuenta ahora con la aprobación de la FDA para la EGPA.
Nódulos reumáticos
Los nódulos reumatoides muestran otra formación de granulomas. Es más probable que se produzcan en pacientes con artritis reumatoide seropositiva de larga duración (factor reumatoide y/o anticuerpos anti-CCP positivos) y nódulos reumatoides cutáneos. La diferenciación de la malignidad es difícil sin histología, ya que, por un lado, puede haber varios nódulos reumatoides que progresan de tamaño durante el curso de la enfermedad y, por otro, los pacientes con artritis reumatoide per se tienen un mayor riesgo de malignidad. Normalmente, los nódulos reumáticos pulmonares se localizan subpleurales o en la zona de los septos interlobulares y suelen ser asintomáticos (Fig. 3).
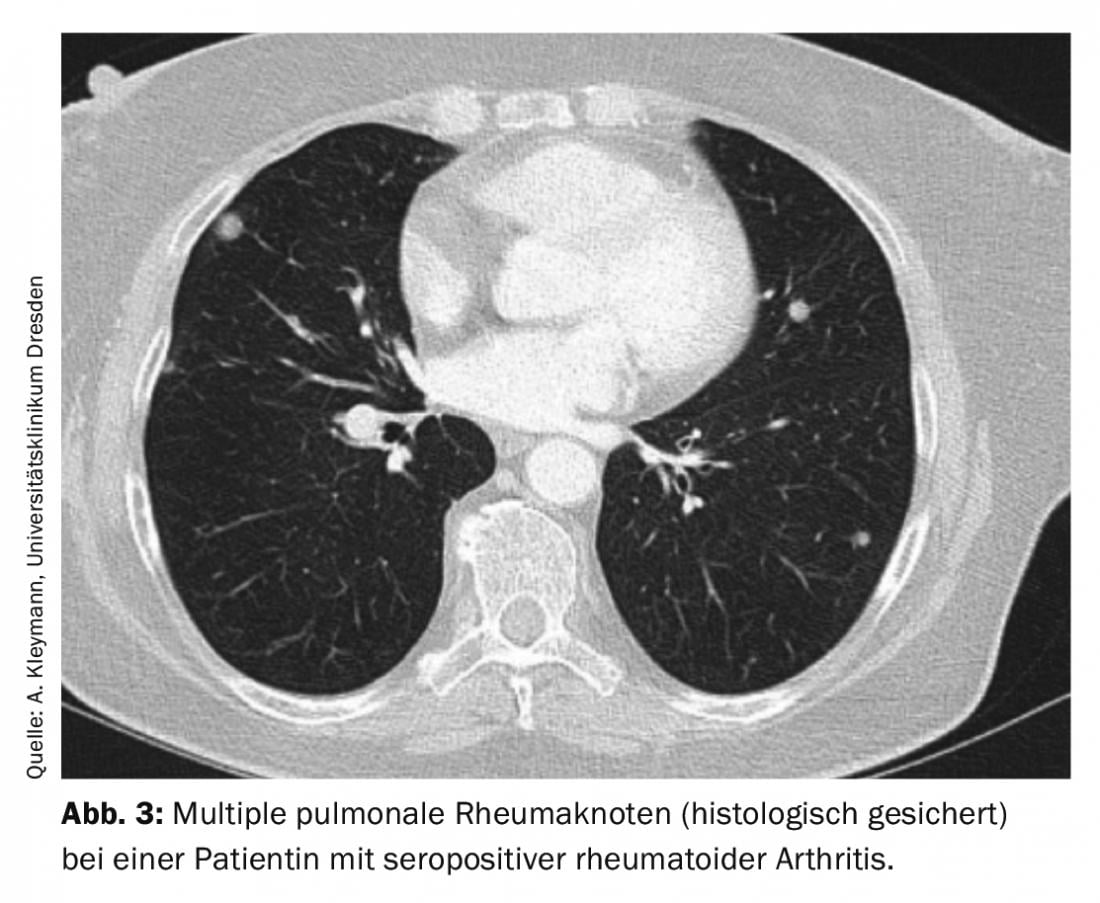
Sin embargo, también pueden provocar derrame pleural, neumotórax, hemoptisis o incluso fístulas broncopulmonares. Si se detectan nódulos reumatoides, puede que haya que ajustar la terapia básica, ya que a menudo se observa un aumento del tamaño de los nódulos reumatoides con el metotrexato. También se han descrito casos con desarrollo de nódulos reumatoides pulmonares con leflunomida [6,7].
Infecciones atípicas
En el caso de una reacción inflamatoria granulomatosa, también deben considerarse las infecciones atípicas bajo la terapia básica más inmunosupresora. Infecciosamente, las infecciones fúngicas como la histoplasmosis y la esporotricosis deben considerarse además de la tuberculosis. El riesgo de infección en pacientes con enfermedades sistémicas reumáticas inflamatorias aumenta tanto por la enfermedad subyacente como por la terapéutica básica inmunosupresora utilizada.
Sobre todo, los bloqueantes del TNF parecen tener una influencia relevante en el riesgo de infecciones pulmonares granulomatosas. Esto se entiende bien por la importancia fisiopatológica del TNF-alfa en la defensa y la formación de granulomas contra patógenos bacterianos y fúngicos.
Histoplasmosis
La histoplasmosis pulmonar está causada por el Histoplasma capsulatum. Este patógeno ubicuo se encuentra principalmente en América del Norte y Central. La diferenciación clínica entre sarcoidosis y neoplasia suele ser difícil porque las manifestaciones pulmonares son diversas (infiltrados pulmonares o focos redondos, cavernas, linfadenopatía medistínica o lesiones que ocupan espacio) (Fig. 4).
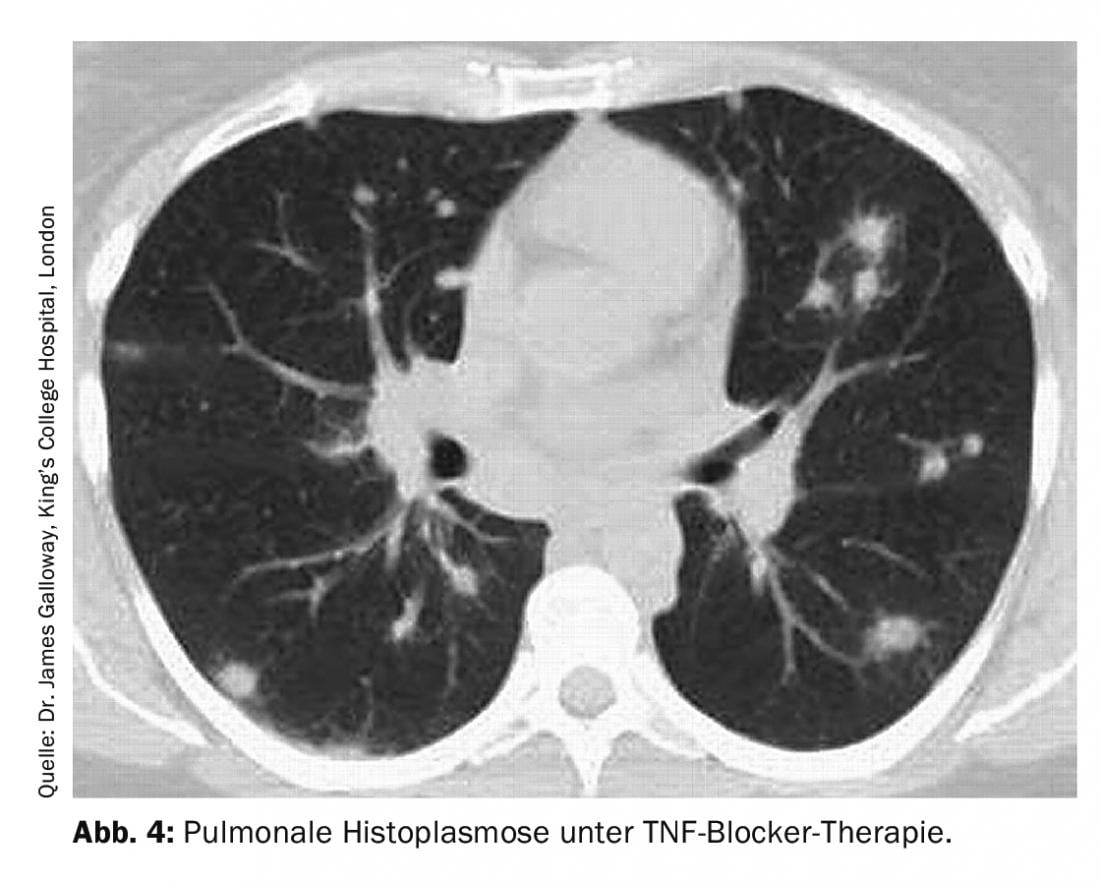
Además de la serología (anticuerpos específicos contra el histoplasma y determinación de antígenos), se utilizan con fines diagnósticos el lavado broncoalveolar con tinción fúngica y cultivo, pero también el correspondiente examen histológico del biopéptido en busca de hongos. Desde el punto de vista terapéutico, no se utiliza ninguna terapia o se emplean diversos antimicóticos, en función de la gravedad de la enfermedad.
Esporotricosis
La esporotricosis está causada por el Sporothrix schenckii y tiene clásicamente una manifestación cutánea. En las manifestaciones pulmonares, la enfermedad se parece a la tuberculosis (Fig. 5) . El patrón oro del diagnóstico es la detección cultural de patógenos, ya que la histopatología puede ser falsamente negativa por un recuento bajo de patógenos incluso con una tinción adecuada, y las pruebas serológicas y de PCR aún no están disponibles de forma rutinaria.
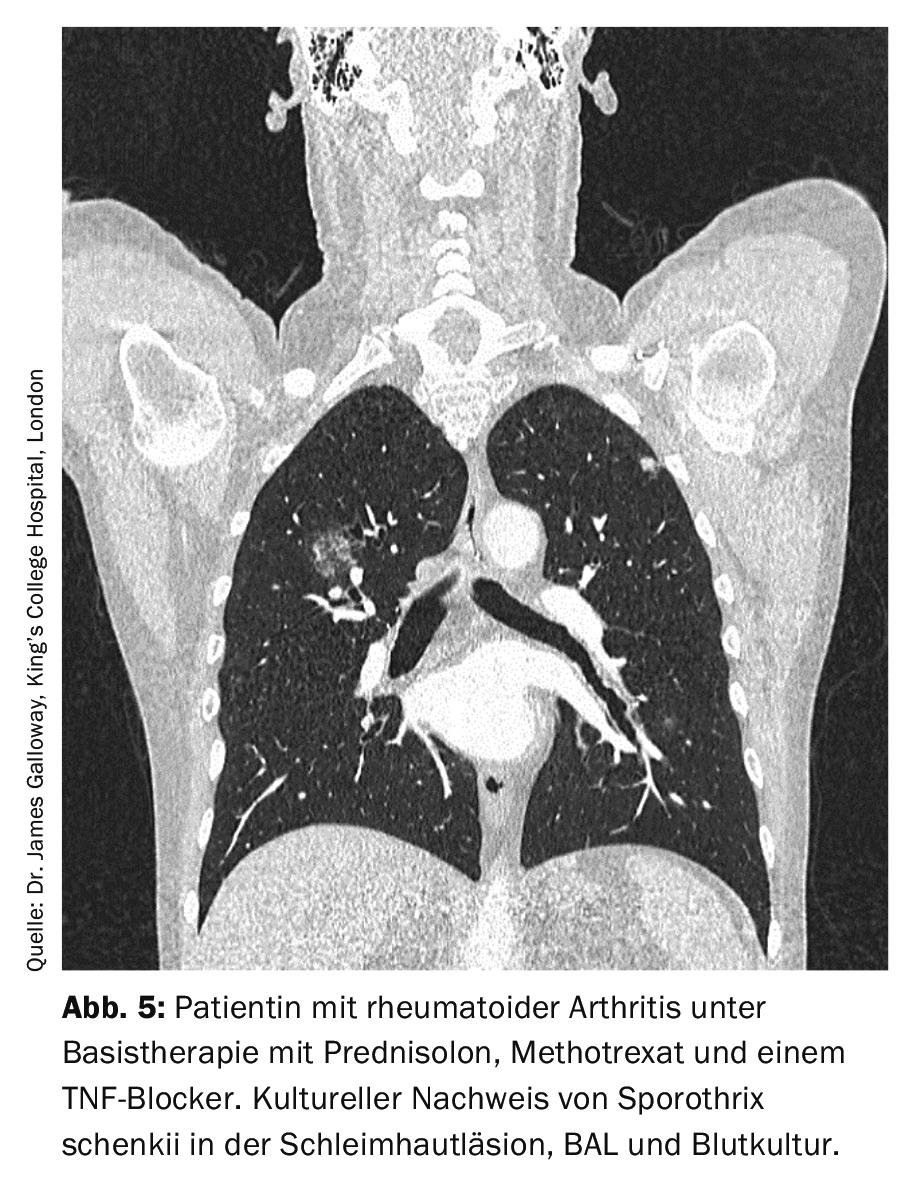
Si no se trata, la esporotricosis pulmonar es mortal, por lo que siempre es necesaria una terapia antifúngica. En cursos leves, puede utilizarse p.o. Puede utilizarse itraconazol 2×200 mg/día. En caso de una manifestación grave, se recomienda primero la anfotericina i.v. B y sólo en el curso se pasa al itraconazol. La duración de la terapia debe ser de al menos 1 año [8].
Inmunodeficiencias primarias
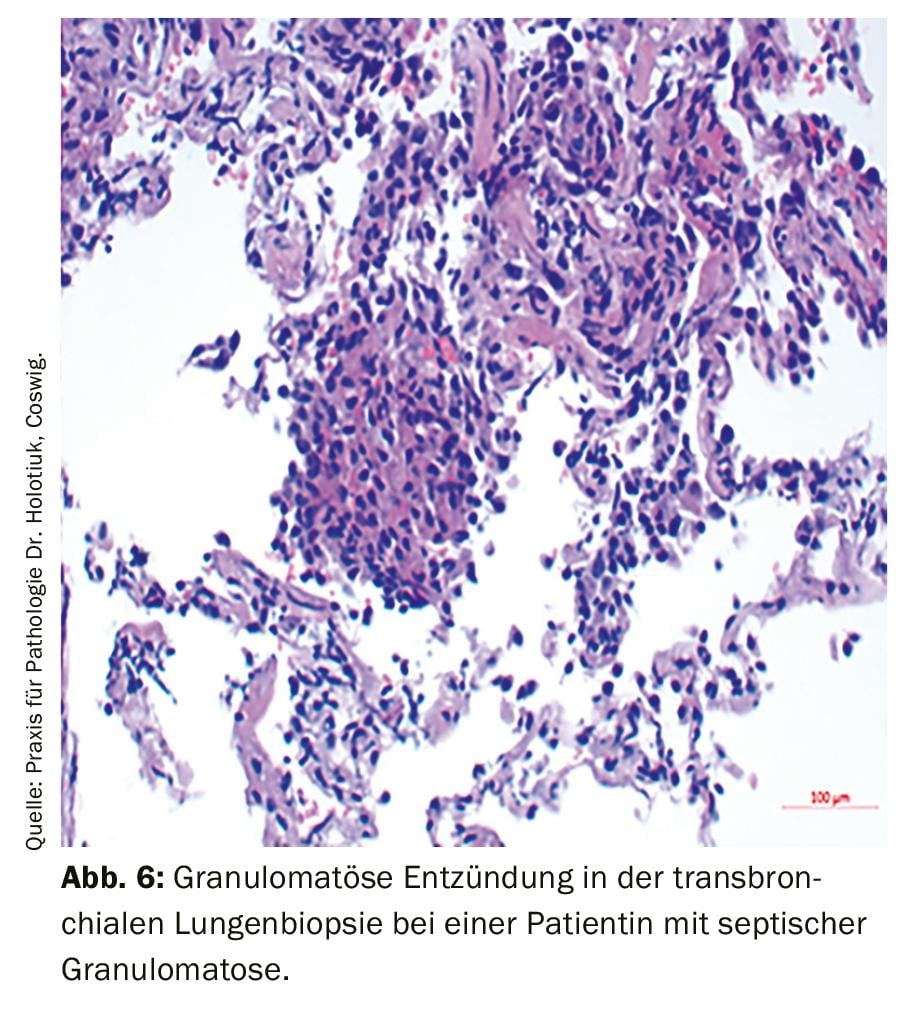
Por último, cabe mencionar el complejo grupo de las inmunodeficiencias primarias. En particular, los pacientes con infecciones recurrentes y fenómenos autoinmunes también deben tenerse en cuenta para este diagnóstico diferencial. El acrónimo ELVIS describe la susceptibilidad patológica a la infección (patógenos y localizaciones atípicas, curso prolongado, intensidad inusual y número de infecciones [Summe]). El acrónimo GARFIELD resume las posibles manifestaciones como expresión de una perturbación de la regulación inmunitaria: Granulomas (Fig. 6), fenómenos autoinmunes, fiebre recurrente, cambios eccematosos en la piel, linfoproliferación (linfadenopatía, esplenomegalia) e inflamación intestinal crónica [9]. Si existe una sospecha justificada, deben iniciarse otros diagnósticos con un estado inmunológico celular (recuento sanguíneo diferencial, tipificación de linfocitos) y humoral (determinación de inmunoglobulinas, si es necesario también con subclases de IgG, factores del complemento) y una aclaración adecuada por parte de un médico con experiencia en el diagnóstico y tratamiento de inmunodeficiencias.
Mensajes para llevarse a casa
- En caso de cambios pulmonares granulomatosos, también deben tenerse en cuenta las enfermedades reumatológicas como la vasculitis de pequeños vasos, los nódulos reumatoides, pero también las infecciones atípicas bajo terapéutica básica y las inmunodeficiencias primarias con fenómenos autoinmunes.
- Si se sospecha una vasculitis pulmonar, debe iniciarse el diagnóstico ANCA con determinación de anticuerpos contra la proteinasa 3 y la mieloperoxidasa y, si se confirma el diagnóstico, debe iniciarse rápidamente una inmunosupresión adecuada.
- Los nódulos reumatoides pulmonares no son infrecuentes en la artritis reumatoide seropositiva, pero a menudo son difíciles de distinguir de los tumores malignos cuando se manifiestan por primera vez.
- Las infecciones pulmonares atípicas deben tenerse en cuenta especialmente en pacientes tratados con biológicos y/o con dosis altas de esteroides.
- Las inmunodeficiencias primarias cursan frecuentemente con fenómenos autoinmunes, por lo que también deben descartarse si existe una sospecha fundada.
Literatura:
- de Groot K, Harper L, Jayne DR, et al: Pulse versus daily oral cyclophosphamide for induction of remission in antineutrophil cyto-plasmic antibody-associated vasculitis: a randomized trial. Ann Intern Med 2009; 150(10): 670-680.
- Walsh M, et al: Intercambio plasmático y glucocorticoides en la vasculitis grave asociada a ANCA. N Engl J Med 2020; 382: 622-631.
- Hiemstra TF, Walsh M, Mahr A, et al: Mycophenolate mofetil vs azathioprine for remission maintenance in antineutrophil cytoplasmic antibody-associated vasculitis: a randomized controlled trial. JAMA 2010; 304(21): 2381-2388.
- Merkel PA, Jayne DR, Wang C, et al: Evaluation of the Safety and Efficacy of Avacopan, a C5a Receptor Inhibitor, in Patients With Antineutrophil Cytoplasmic Antibody-Associated Vasculitis Treated Concomitantly With Rituximab or Cyclophosphamide/Azathioprine: Protocol for a Randomized, Double-Blind, Active-Controlled, Phase 3 Trial. JMIR Res Protoc 2020; 9(4): e16664.
- Wechsler ME, Akuthota P, Jayne D, et al: Mepolizumab o placebo para la granulomatosis eosinofílica con poliangitis. N Engl J Med 2017; 376(20): 1921-1932.
- Horvath IF, Szanto A, Csiki Z, et al: Nódulos reumatoides intrapulmonares en un paciente con artritis reumatoide de larga evolución tratado con leflunomida. Pathol Oncol Res 2008; 14(1): 101-104.
- Rozin A, Yigla M, Guralnik L, et al: Nodulosis pulmonar reumatoide y osteopatía asociadas al tratamiento con leflunomida. Clin Rheumatol 2006; 25(3): 384-388.
- Kauffman CA, Bustamante B, Chapman SW, et al: Directrices de práctica clínica para el tratamiento de la esporotricosis: actualización de 2007 de la Sociedad Americana de Enfermedades Infecciosas. Clin Infect Dis 2007; 45(10): 1255-1265.
- Directriz de la AWMF “Diagnóstico de la presencia de una inmunodeficiencia primaria” Situación: 31.10.2017, válida hasta el 31.10.2020.
InFo NEUMOLOGÍA Y ALERGOLOGÍA 2020; 2(3): 12-16