Una inflamación periódica, muy dolorosa y extensa de los ganglios linfáticos también puede indicar una rara enfermedad de Castleman. La forma multicéntrica es una enfermedad sistémica grave que no es fácil de diagnosticar.
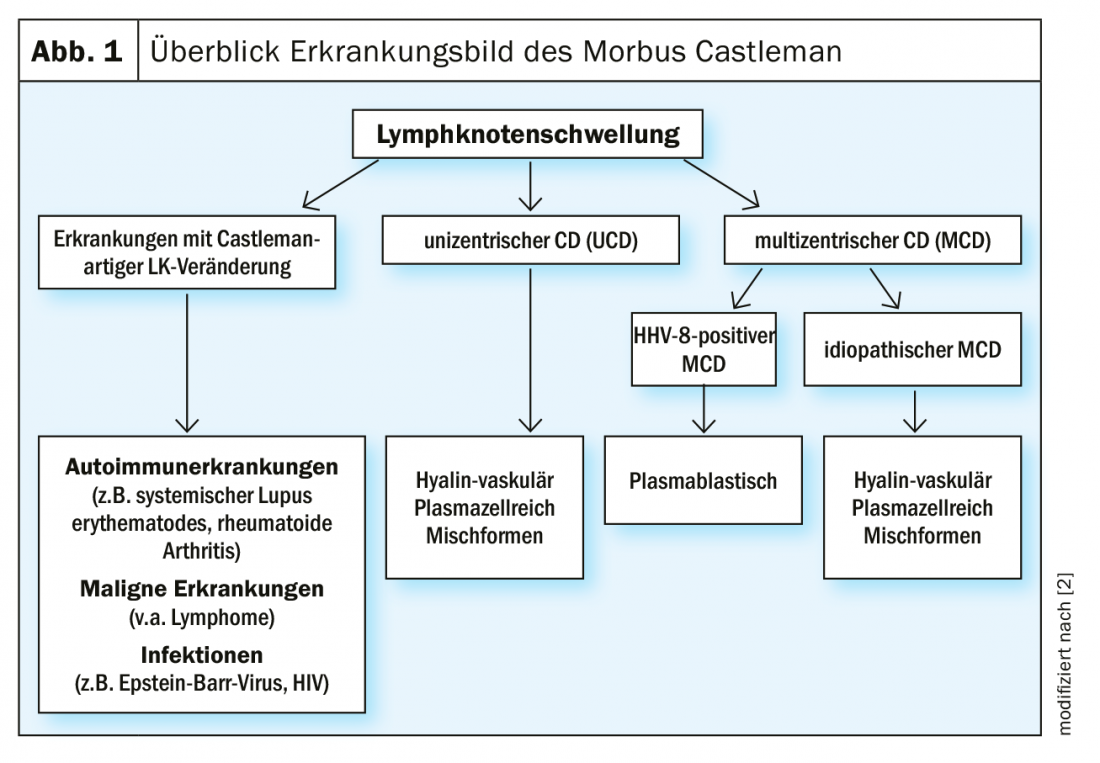
En el caso de una inflamación extensa de los ganglios linfáticos de aparición periódica, muy dolorosa y marcada, también hay que pensar en la enfermedad de Castleman. Esta enfermedad rara se divide en enfermedad de Castleman unicéntrica (ECU) y formas multicéntricas y a menudo se pasa por alto. La UCD es una forma benigna de la enfermedad con hiperplasia localizada del tejido linfático [1]. En este caso, la escisión del ganglio linfático afectado es el método de elección [2]. Sin embargo, se vuelve más problemática con la enfermedad de Castleman multicéntrica (ECM). Se trata de una enfermedad sistémica grave con un pronóstico frecuentemente desfavorable. La sobreproducción de diferentes citoquinas, especialmente la interleucina-6 (IL-6), da lugar a una sintomatología heterogénea. Existe una estrecha asociación con el virus del herpes humano 8 (VHH-8). Esto, a su vez, es en gran medida congruente con las infecciones por VIH. En consecuencia, más del 90% de los pacientes infectados por el VIH son también positivos al VHH-8. Por el contrario, en los pacientes seronegativos, la tasa de es sólo del 10-15% – aquí predomina la MCD idiopática [3] (Fig. 1).
Epidemiología
Básicamente, todas las formas de la enfermedad de Castleman son muy poco frecuentes y, sin duda, una gran proporción nunca se diagnostica adecuadamente. Por millón de habitantes, se esperan 2,4 casos, lo que corresponde a unos 20 casos en Suiza [4]. Con un 35,4%, la MCD parece ocurrir con menos frecuencia que la UCD (64,6%) [5]. Sin embargo, la incidencia es mayor en los pacientes infectados por el VIH. Según un estudio británico, es de 4,3 casos por cada 10.000 pacientes-año, con una ligera tendencia al alza en los últimos años [2,6]. En estudios observacionales, la mortalidad en los primeros 5 años tras el diagnóstico fue del 30-35% [7]. Según una revisión sistémica, la supervivencia libre de enfermedad en la iMCD después de 3 años fue del 45,7% [8].
Patogénesis
La forma multicéntrica con agrandamiento de numerosos ganglios linfáticos se describió por primera vez en 1978. Se da con mayor frecuencia en pacientes seropositivos. El VHH8 es responsable de la enfermedad de Castleman multicéntrica en casi todos los pacientes seropositivos y de aproximadamente la mitad de las enfermedades en pacientes seronegativos [9]. Producen una interleucina viral que es muy similar a la IL-6 humana y tiene efectos similares. Sólo necesita unirse a una de las dos subunidades del receptor de IL-6 para ser activa. Esto explica el efecto significativamente más amplio sobre las células diana y probablemente también las típicas “tormentas de citoquinas” [10,11,2]. La interleucina-6 y otras citocinas proinflamatorias inducen la proliferación de células B y plasmáticas, la secreción de factores de crecimiento endotelial vascular y la angiogénesis.
Por otro lado, las causas de la iMCD siguen siendo objeto de un controvertido debate. Los científicos suponen que una enfermedad inflamatoria autoinmune, una infección vírica y una predisposición genética podrían ser las responsables [12]. Además de la IL-6, intervienen otras moléculas de señalización, como el VEGF (“factor de crecimiento endotelial vascular”), el TNF-alfa y la interleucina-1 [13]. La proliferación linfocítica en la iMCD suele ser policlonal y consecuencia de la hipercitoquinemia [14,2]. Sin embargo, se ha observado una proliferación monoclonal en algunas lesiones del subtipo vascular hialino [15,2].
Síntomas y quejas
Los síntomas se presentan de forma muy heterogénea, lo que a menudo dificulta un diagnóstico eficaz. Sin embargo, la enfermedad suele ir acompañada de dolor en los ganglios linfáticos afectados. Estas hinchazones suelen producirse en episodios, especialmente en la MCD HHV-8 positiva. Además, existen claros síntomas B como fiebre, sudores nocturnos y pérdida de peso. Casi todos los pacientes se quejan de debilidad y sensación de enfermedad, náuseas, vómitos y pérdida de apetito. El bazo y el hígado también están agrandados. También hay hepatomegalia, síntomas respiratorios y tendencia al edema con hipalbuminemia. Suele haber una anemia hematológica grave, que a menudo puede ir acompañada de una trombocitopenia masiva.
Normalmente, la enfermedad progresa en episodios que duran de unos días a semanas, durante los cuales los pacientes suelen tener fiebre alta y estar gravemente enfermos. Entre medias, hay periodos más largos que pueden durar semanas, durante los cuales los pacientes vuelven a sentirse mucho mejor. El tamaño de los ganglios linfáticos puede volver casi a la normalidad. La frecuencia y la intensidad de las recaídas suelen aumentar con el tiempo, aunque también se conocen cursos autolimitados. Sin embargo, existe un riesgo significativamente mayor de linfomas malignos, especialmente subtipos de linfoma bastante raros como los linfomas plasmablásticos o los linfomas de efusión primaria [2,12].
Una iMCD se manifiesta con un pronunciado síntoma de fatiga, especialmente en las fases iniciales. A diferencia de la MCD, los síntomas como la fiebre, la inflamación de los ganglios linfáticos y la anemia son mucho menos pronunciados y el curso recidivante es menos brusco. Los síntomas pueden variar desde síntomas constitucionales leves hasta cursos potencialmente mortales con anasarca y fallo orgánico múltiple. Se definió recientemente un subtipo grave de iMCD, el síndrome TAFRO. Se trata de un complejo sintomático de trombocitopenia, ascitis, fiebre, fibrosis reticular en la médula ósea y organomegalia con γ-globulina normal . Además, son frecuentes las asociaciones con el síndrome POEMS, un cuadro clínico consistente en neuropatía periférica, organomegalia, endocrinopatía, gammapatía monoclonal y cambios cutáneos [2].
Diagnóstico
La enfermedad de Castleman debe diferenciarse de los linfomas y otras enfermedades graves. La forma grave en particular se confunde a menudo con un linfoma. El examen histopatológico de un ganglio linfático extirpado es obligatorio. Un pinchazo no suele ser suficiente. El preparado muestra una linfadenitis reactiva con proliferación de células plasmáticas en la pulpa y cambios regresivos en los centros germinales, que suelen estar estratificados como pieles de cebolla e intercalados con vasos. En la MCD positiva para el VHH-8, suele observarse una imagen plasmablástica, a menudo con el denominado patrón apolillado en el área de la zona del manto. El patrón característico de la piel de cebolla suele estar parcialmente destruido. El VHH-8 se detecta mediante tinción para LANA-1 (“latency-associated-nuclear-antigen”). La sangre extraída durante un episodio de la enfermedad muestra niveles elevados de IL-6 y PCR. La tríada de síntomas B, viremia por VHH-8 y hallazgos histológicos es útil para el diagnóstico [17].
El diagnóstico de la iMCD es mucho más difícil, ya que hay que excluir muchas otras enfermedades. Los cambios histopatológicos también se encuentran, por ejemplo, en una variedad de infecciones (incluido el virus de Epstein-Barr) o en el lupus eritematoso, la artritis reumatoide, el síndrome de Sjögren y algunas neoplasias, incluidos especialmente los linfomas malignos. Por lo tanto, además de los cambios histopatológicos, siempre deben tenerse en cuenta los parámetros clínicos y de laboratorio. La iMCD se diferencia en tres subtipos histopatológicos: el tipo hialino-vascular, el tipo de células plasmáticas y el tipo mixto. Todos ellos se dan en alrededor del 20-40% de los casos [18]. El tipo hialino-vascular se caracteriza por células dendríticas foliculares (CDF) displásicas y centros germinales atróficos intercalados con vasos hialinos, alrededor de los cuales se disponen concéntricamente los linfocitos. En el tipo de células plasmáticas, los centros germinales son hiperplásicos en lugar de atróficos y los CDF y la arquitectura de los ganglios linfáticos son normales [2].
Terapia
La enfermedad de Castleman unicéntrica tiene muy buen pronóstico, ya que el ganglio linfático afectado puede extirparse mediante cirugía. La recurrencia de la enfermedad es extremadamente rara. Sin embargo, dado que en la MCD se ven afectados muchos ganglios linfáticos, la intervención quirúrgica no resulta eficaz. El tratamiento sigue siendo difícil. No existe una terapia estándar para los pacientes con enfermedad de Castleman multicéntrica. Conceptualmente, se utilizan sustancias inmunosupresoras y citotóxicas. Los glucocorticoides son eficaces pero a menudo no conducen a un alivio de los síntomas a largo plazo (Fig. 2).
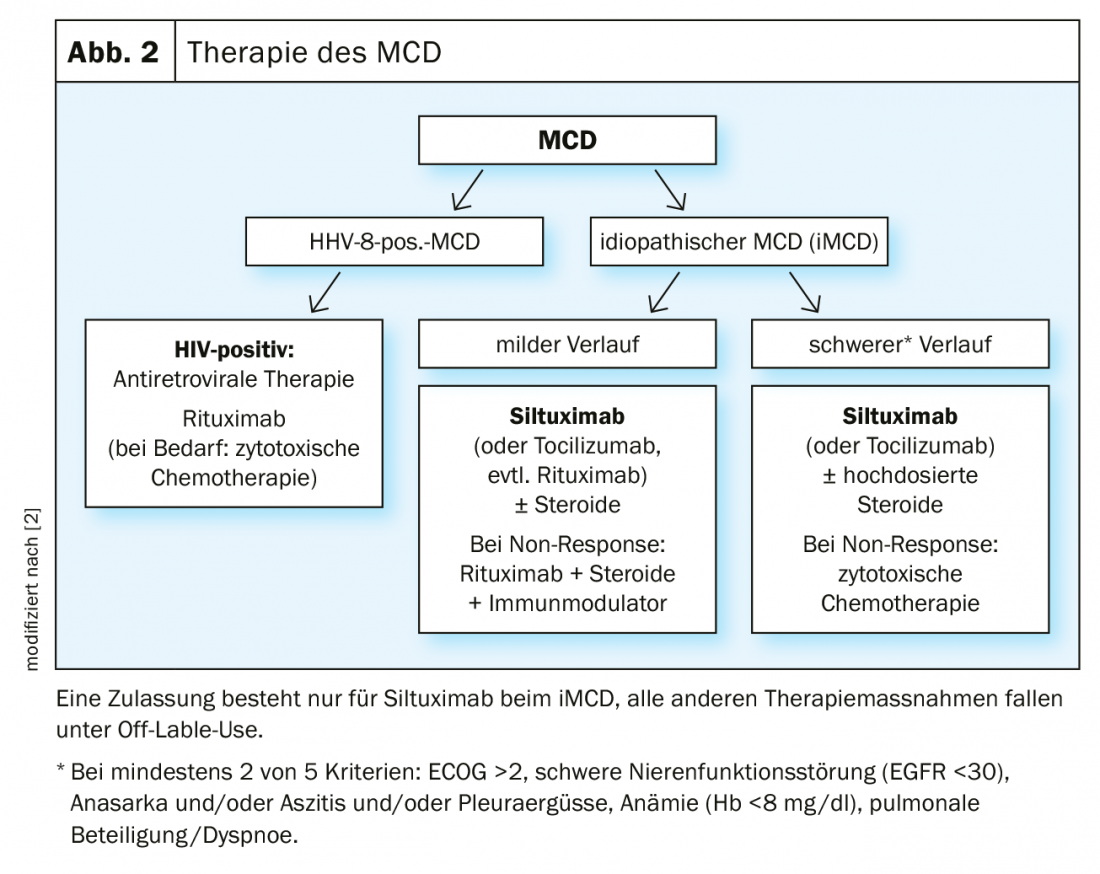
En la iMCD se utiliza principalmente el bloqueo de la vía de señalización de la IL-6 mediante anticuerpos monoclonales como el siltuximab. En la MCD positiva al VHH-8, la atención se centra en la eliminación citotóxica de las células responsables de la sobreproducción de citocinas. Las terapias inmunomoduladoras son principalmente los esteroides, así como sustancias antivirales como el valganciclovir. Desde 2018, existen por primera vez recomendaciones consensuadas para la iMCD [19]. Se basan en la experiencia con 344 pacientes que se han sometido a un total de 479 terapias, tienen en cuenta la gravedad de la enfermedad, las terapias anteriores y la respuesta.
El único fármaco aprobado hasta ahora para el tratamiento de la iMCD es el siltuximab, un anticuerpo monoclonal contra la IL-6 humana. Se utiliza para todas las formas de iMCD con o sin esteroides. En el estudio pivotal, 79 pacientes con iMCD fueron tratados con siltuximab o placebo durante tres semanas [20,7]. El criterio de valoración primario fue una respuesta duradera en términos de tamaño tumoral y mejora de una puntuación de síntomas clínicos durante al menos 18 semanas. Mientras que no se observó ninguna respuesta en el grupo placebo, las tasas en el grupo verum fueron del 34%. El siltuximab fue bien tolerado en general. Los efectos secundarios más frecuentes y característicos son picor cutáneo, infecciones de las vías respiratorias superiores, exantema y edema local, predominantemente de gravedad 1 y 2. Los efectos secundarios graves son fatiga (12%) y sudores nocturnos (8%). Sin embargo, la tasa en este caso no fue mayor que con placebo, por lo que es más probable que estos síntomas se atribuyan a la enfermedad subyacente [7].
El tocilizumab, un anticuerpo contra el receptor de IL-6, se considera una alternativa al siltuximab en las recomendaciones internacionales, pero sólo está aprobado en Europa para la artritis reumatoide.
El rituximab, un anticuerpo monoclonal contra el CD20, tampoco está aprobado para el tratamiento de la MCD. Especialmente los pacientes con ECM positiva al VHH-8 parecen responder bien a ella. En varias series de casos se observó una mejora significativa de la supervivencia globala y de la supervivencia libre de enfermedad. Las citocinas, pero también la PCR, las inmunoglobulinas y la carga viral del VHH-8 disminuyeron [2,21]. Sin embargo, en aproximadamente un tercio de los casos se ha producido una progresión del sarcoma de Kaposi, que suele acompañar a la enfermedad. En este caso, una combinación con sustancias citostáticas con actividad KS podría ser útil [22]. En situaciones de riesgo vital, debe considerarse la esplenectomía. Reduce el conjunto de células infectadas por el VHH-8 [2].
Mensajes para llevarse a casa
- La enfermedad de Castleman se divide en la forma benigna unicéntrica (UCD) y la enfermedad de Castleman multicéntrica (MCD).
- La MCD es una enfermedad sistémica que a menudo no se reconoce debido a su heterogeneidad y a su rara aparición.
- La inflamación dolorosa de los ganglios linfáticos se produce en episodios, a menudo acompañados de síntomas B como fiebre o sudores nocturnos.
- El siltuximab es actualmente el único fármaco aprobado para el tratamiento de la ECM idiopática.
Literatura:
- Castleman B, Towne VW: Registros de casos del Hospital General de Massachusetts; ejercicios clinicopatológicos semanales. N Engl J Med 1954; 251: 396-400
- Hoffmann C, Tiemann M: Enfermedad de Castleman multicéntrica: rara vez se diagnostica correctamente. Dtsch Arztebl 2019; 116(46): [32]; DOI: 10.3238/PersOnko.2019.11.15.06
- Hoffmann C: Enfermedad de Castleman multicéntrica (ECM): un cuadro clínico poco frecuente y a menudo no reconocido. Trillium 2015. www.trillium.de/zeitschriften/trillium-krebsmedizin/archiv/ausgaben-2015/heft-12015/multizentrischer-morbus-castleman-mcd-ein-seltenes-oft-verkanntes-krankheitsbild.html (última consulta: 06.04.2020)
- Robinson D Jr, Reynolds M, Casper C, et al: Epidemiología clínica y pautas de tratamiento de los pacientes con enfermedad de Castleman multicéntrica: resultados de dos centros de tratamiento estadounidenses. Br J Haematol 2014; 165: 39-48.
- Haap M, Wiefels J, Horger M, et al: Hallazgos clínicos, de laboratorio y de imagen en la enfermedad de Castleman – El subtipo decide. Blood Rev 2018; 32: 225-234.
- Powles T, Stebbing J, Bazeos A, et al: El papel de la inmunosupresión y el VHH-8 en la creciente incidencia de la enfermedad de Castleman multicéntrica asociada al VIH. Ann Oncol 2009; 20: 775-779.
- www.dgho.de/publikationen/stellungnahmen/fruehe-nutzenbewertung/siltuximab/siltuximab-dgho-stellungnahme-20141006.pdf (última consulta: 06.04.2020)
- Talat N, Schulte KM: Enfermedad de Castleman: análisis sistemático de 416 pacientes de la literatura. Oncologist 2011; 16:1316-24
- Fajgenbaum DC, van Rhee F, Nabel CS: Enfermedad de Castleman multicéntrica idiopática HHV-8 negativa: nuevos conocimientos sobre biología, patogenia y terapia. Sangre 2014; 123: 2924-2933. DOI: 10.1182/blood-2013-12-545087.
- Li H, Wang H, Nicholas J. Detección de la unión directa de la interleucina-6 codificada por el herpesvirus humano 8 (vIL-6) tanto a la gp130 como al receptor de la IL-6 (IL-6R) e identificación de los residuos de aminoácidos de la vIL-6 importantes para la señalización dependiente e independiente de la IL-6R. J Virol 2001; 75: 3325-3334.
- Moore PS, Boshoff C, Weiss RA, Chang Y: Molecular mimicry of human cytokine and cytokine response pathway genes by KSHV. Science 1996; 274: 1739-1744.
- https://medlexi.de/Morbus_Castleman (última consulta: 06.04.2020)
- Pierson S, Stonestrom A, Ruth J, et al: La cuantificación de proteínas plasmáticas de reagudizaciones y remisiones de la enfermedad de Castleman multicéntrica idiopática revela una “tormenta de quimiocinas” y separa los subtipos clínicos (resumen). Sangre 2017; 130(Supl. 1).Resumen 3592
- Ohyashiki JH, Ohyashiki K, Kawakubo K, et al. Análisis genético molecular, citogenético e inmunofenotípico Enfermedad de Castleman de tipo células plasmáticas. Am J Clin Pathol 1994; 101: 290-295.
- Chang KC, Wang XC, Hung YL: Monoclonalidad y anomalías citogenéticas en la enfermedad de Castleman vascular hialina. Mod Path 2014; 7: 823-831.
- Iwaki N, Fagenbaum D, Nabel CS, et al: El análisis clinicopatológico del síndrome TAFRO demuestra un subtipo distinto de enfermedad de Castleman multicéntrica HHV-8 negativa. Am J Hematol 2016; 91: 220-226.
- Bower M, Pria AD, Coyle C, et al: Esquemas de criterios diagnósticos para la enfermedad de Castleman multicéntrica en 75 casos. J Acquir Immune Defic Syndr 2014; 65(2): e80-82.
- Liu AY, Nabel CS, Finkelman BS, et al: Enfermedad de Castleman idiopática multicéntrica: una revisión sistemática de la literatura. Lancet Hematol 2016; 3: e163-175.
- van Rhee F, Voorhees P, Dispenzieri A, et al: Directrices de tratamiento consensuadas, internacionales y basadas en la evidencia para la enfermedad de Castleman idiopática multicéntrica. Sangre 2018; 132: 2115-2124.
- van Rhee F, Wong RS, Munshi N, et al: Siltuximab for multicentric Castleman’s disease: a randomised, double-blind, placebo-controlled trial. Lancet Oncol 2014; 15: 966-974, DOI: 10.1016/S1470-2045(14)70319-5.
- Bower M, Veraitch O, Szydlo R, et al: Cambios de las citocinas durante el tratamiento con rituximab en la enfermedad de Castleman multicéntrica asociada al VIH. Sangre 2009; 113: 4521-4524.
- Uldrick TS, Polizzotto MN, Aleman K, et al: Rituximab más doxorrubicina liposomal en pacientes infectados por el VIH con enfermedad de Castleman multicéntrica asociada al KSHV. Sangre 2014; 124: 3544-3552.
InFo ONCOLOGÍA Y HEMATOLOGÍA 2020; 8(2): 4-7