El número de personas con EM en Suiza está aumentando. Las encuestas actuales pintan un panorama alarmante. Esto hace que sea aún más importante un tratamiento eficaz que se adapte individualmente a la situación vital del paciente y a la evolución de su enfermedad. El objetivo debe ser mantener la participación en la vida social el mayor tiempo posible.
Hasta ahora se suponía que en Suiza vivían unas 10.000 personas con esclerosis múltiple (EM). Un estudio reciente del Registro de EM ha tenido que revisar ahora esta suposición: al menos 15.000 personas padecen la enfermedad, y la tendencia sigue en aumento [1]. La proporción entre sexos también se está desplazando aún más hacia las mujeres. Las nuevas proyecciones sugieren que el 73% de las mujeres están afectadas. Es dudoso que esta evolución se deba únicamente al crecimiento de la población y al aumento de la esperanza de vida. Todavía se están descifrando los mecanismos de la enfermedad. Los primeros resultados apuntan a una disposición genética y a una influencia considerable de los factores ambientales. La investigación actual se centra, entre otras cosas, en la neurodegeneración [2,3]. Es responsable en gran medida del desarrollo de discapacidades debidas a la transección axonal y la pérdida de neuronas. El aumento de la neurodegeneración, que muy probablemente comienza antes de lo que se pensaba, parece ser una de las principales causas de la progresión de la enfermedad. La investigación de biomarcadores, como la proteína ligera de neurofilamentos, que detecta el daño axonal o neuronal general y puede utilizarse para evaluar mejor el pronóstico de cada paciente, son los primeros pasos prometedores hacia una terapia personalizada [4].
Clínicamente, la remitente-recurrente puede distinguirse de los cursos progresivos primario y secundario. Además de los síntomas neurológicos, muchos pacientes sufren déficits cognitivos, fatiga y depresión manifiesta. Dado que la EM se manifiesta en diferentes formas y facetas, la gestión del tratamiento debe ser correspondientemente exhaustiva, competente y adaptada individualmente al paciente.
El modelo de pilares como base de la terapia
Cuanto antes pueda iniciarse la terapia, mejor. En la actualidad se dispone de varias opciones de tratamiento eficaces que a menudo pueden ralentizar en gran medida la progresión de la enfermedad. Básicamente, la terapia debe basarse en cuatro pilares (tab. 1). El objetivo del tratamiento es reducir la extensión de las reacciones inflamatorias, estabilizar las limitaciones funcionales y mejorar los síntomas acompañantes. El objetivo debe ser un estado NEDA (Sin Evidencia de Actividad de la Enfermedad)-3, es decir, la ausencia de nuevas lesiones en la resonancia magnética, recaídas de la enfermedad y progresión de la discapacidad.

En los últimos años, se han desarrollado varios regímenes de tratamiento para diferentes cursos de la enfermedad (tab. 2). Los preparados pueden dividirse en cuatro grupos según su mecanismo de acción:
- Inhibición de la proliferación: azatioprina, cladribina, mitoxantrona, teriflunomida
- Inmunomodulación: fumarato de dimetilo, acetato de glatiramero, iterferón-β, iterferón-β pegilado, teriflunomida
- Inhibición de la migración: Fingolimod, Natalizumab
- Depleción: Alemtuzumab, Rituximab/Ocrelizumab
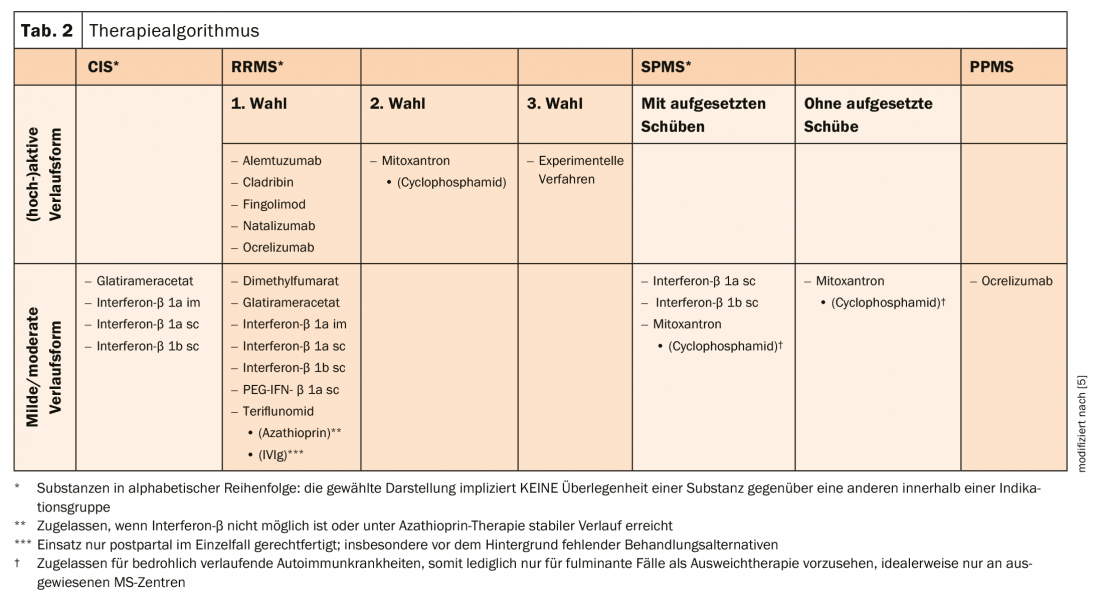
En los cursos moderados, el interferón-β (IFN-β), el acetato de glatiramero, las inmunoglobulinas y la azatioprina se utilizan como terapia básica para el curso remitente-recurrente. Estos preparados inmunomoduladores inhiben los procesos perjudiciales y favorecen los procesos protectores del sistema inmunitario. En los pacientes con un curso (altamente) activo (es decir, muchas y graves recaídas en un corto periodo de tiempo y/o una IRM (altamente) activa) o en los pacientes que no responden suficientemente a los inmunoterápicos básicos, se utilizan fármacos de terapia de intensificación. Entre ellas se incluyen, por ejemplo, las terapias orales de corta duración como los comprimidos de cladribina, que se dirigen de forma selectiva y periódica a los linfocitos en la EM remitente-recurrente. Al reducir el recuento de linfocitos, debería reducirse la frecuencia de las recaídas. Otra opción es bloquear el receptor de esfingosina-1-fosfato con fingolimod, que retiene las células inmunitarias en los ganglios linfáticos. Las terapias de infusión mensual con el anticuerpo monoclonal natalizumab también impiden que las células inmunitarias migren a los focos inflamatorios del SNC [6–8].
Literatura:
- www.multiplesklerose.ch/das-schweizer-ms-register/
- Ziemssen T, Derfuss T, de Stefano N, et al: Optimización del éxito del tratamiento en la esclerosis múltiple. J Neurol 2016; 263: 1053-1065
- De Stefano N, Airas L, Grigoriadis N, et al: Relevancia clínica de las medidas del volumen cerebral en la esclerosis múltiple. CNS Drugs 2014; 28: 147-156
- Barro C, Benkert P, Disanto G, et al: El neurofilamento sérico como predictor del empeoramiento de la enfermedad y de la atrofia cerebral y de la médula espinal en la esclerosis múltiple. Cerebro 2018; 141(8): 2382-2391
- www.multiple-sklerose.com/medikamente-zur-behandlung/
- www.neurologen-und-psychiater-im-netz.org/neurologie/erkrankungen/multiple-sklerose-ms/therapie
- www.mpg.de/411133/forschungsSchwerpunkt
- DGN/KKNMS: Directriz sobre el diagnóstico y la terapia de la esclerosis múltiple
InFo NEUROLOGÍA Y PSIQUIATRÍA 2020; 18(1): 22-23