La carencia de hierro es una comorbilidad frecuente en la insuficiencia cardiaca crónica y se asocia a una mayor morbilidad y mortalidad independientemente de la presencia de anemia. En caso de insuficiencia cardiaca crónica, debe realizarse un cribado anual de la anemia. Debe realizarse el estado del hierro (ferritina sérica, saturación de transferrina) y la PCR. Los criterios de diagnóstico de la ferropenia según el estudio FAIR-HF son: ferritina sérica <100 μg/l (ferropenia absoluta), ferritina sérica 100-299 μg/l y saturación de transferrina <20% (ferropenia funcional). Para la insuficiencia cardiaca sistólica sintomática, debe considerarse la sustitución parenteral con hierro, preferiblemente con carboximaltosa de hierro, para mejorar los síntomas.
La insuficiencia cardiaca crónica es una enfermedad frecuente, afecta a muchos sistemas orgánicos y sigue teniendo un mal pronóstico a pesar de las pautas de tratamiento bien establecidas. Ésta es una de las razones por las que la investigación sobre los factores de riesgo modificables ha cobrado importancia en los últimos años. La anemia y la carencia de hierro, como cofactores frecuentes, desempeñan un papel importante desde el punto de vista pronóstico. La prevalencia de la carencia de hierro en pacientes con insuficiencia cardiaca crónica es de aproximadamente el 50% [1]. Los pacientes hospitalizados con insuficiencia cardiaca NYHA IV y anemia mostraron carencia de hierro hasta en un 73% según las biopsias de médula ósea [2]. La presencia de anemia o deficiencia de hierro es también un factor independiente y fuerte de mal pronóstico [3]. En el estudio FAIR-HF (Ferric Carboxymaltose in Patients with Heart Failure and Iron Deficiency) más amplio realizado hasta la fecha, la corrección de la carencia de hierro mediante suplementos de hierro intravenoso no tuvo ningún efecto sobre la mortalidad y la morbilidad, pero fue capaz de mejorar significativamente la capacidad de ejercicio y los síntomas de insuficiencia cardiaca en pacientes con insuficiencia cardiaca sistólica, incluso en caso de carencia de hierro sin anemia [4]. También se han investigado varias veces otros enfoques para el tratamiento de la anemia, como los derivados de la eritropoyetina. Debido a su controvertida eficacia y a sus efectos secundarios cardiovasculares a largo plazo, no se mencionan en las directrices de la ESC (Sociedad Europea de Cardiología) para el tratamiento de la insuficiencia cardiaca crónica [5].
Fisiopatología
Los mecanismos subyacentes de la anemia o la carencia de hierro son multifactoriales y en gran medida análogos a los de otras enfermedades sistémicas crónicas como la artritis reumatoide o la enfermedad de Crohn. Con diferencia, las formas más comunes de anemia en la insuficiencia cardiaca son la anemia inflamatoria crónica (60%), seguida de la anemia ferropénica (21%) [3]. A menudo se trata de una carencia de hierro “funcional”, por la que las reservas de hierro están suficientemente llenas, pero la liberación y la reabsorción intestinal de hierro y, por tanto, la biodisponibilidad están inhibidas. Además de la eritropoyesis, el hierro también tiene funciones importantes en los procesos metabólicos del corazón y el músculo esquelético (enzima de la cadena respiratoria), que pueden influir en el rendimiento.
Inflamación crónica
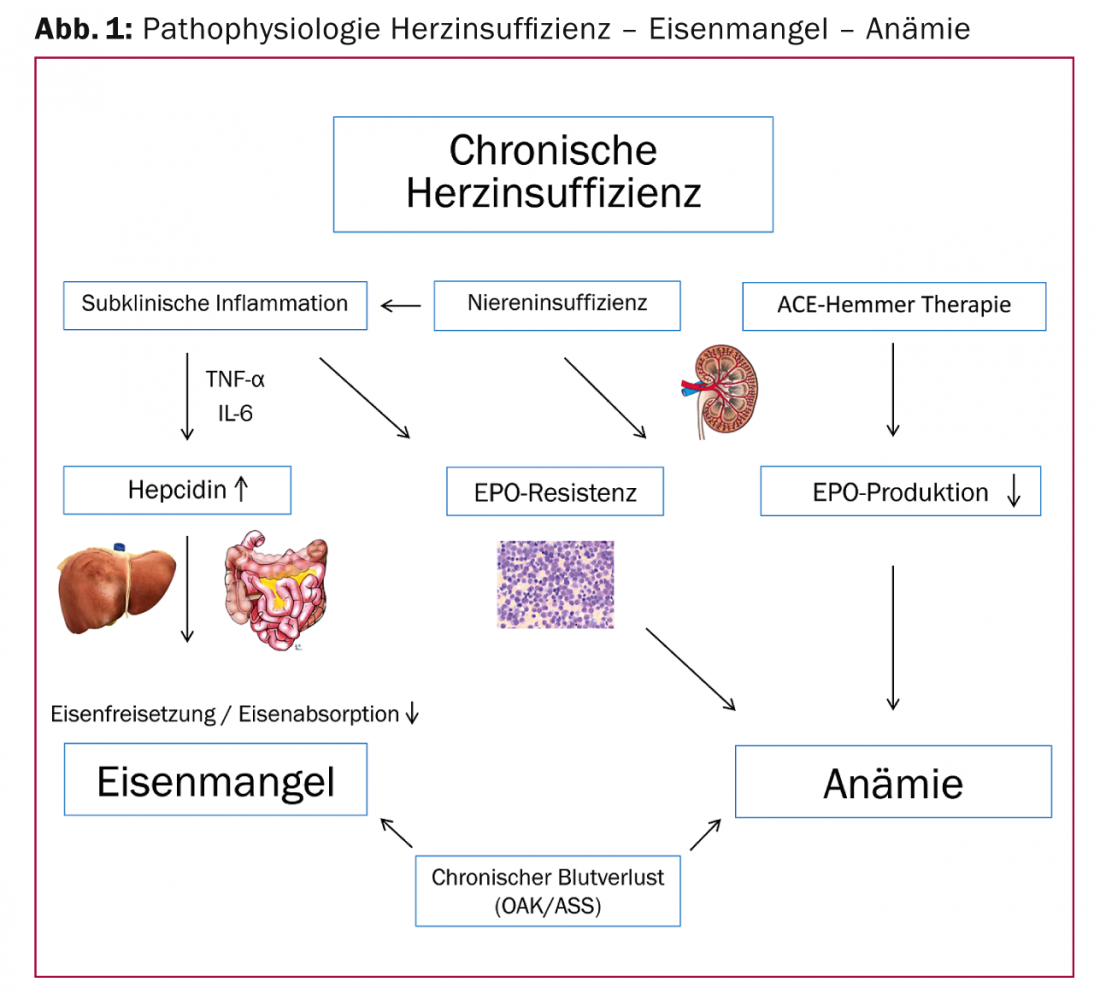
La insuficiencia cardiaca está asociada a un proceso inflamatorio crónico, en su mayor parte subclínico. Esto provoca la liberación de citoquinas proinflamatorias (IL-6) y del factor de necrosis tumoral (TNF), que reducen la producción de EPO y la sensibilidad de la médula ósea a la EPO. Además, la IL-6 promueve la síntesis hepática y la liberación de la proteína de fase aguda hepcidina. Esto, a su vez, inhibe la ferroportina, de modo que se inhiben la absorción intestinal de hierro y la movilización desde las reservas.
Otros cofactores importantes que pueden causar anemia o deficiencia de hierro son la reducción de la producción de eritropoyetina en la insuficiencia renal crónica, la deficiencia de vitamina B12 o ácido fólico debida a la malnutrición y la pérdida de sangre gastrointestinal oculta bajo anticoagulantes orales. El uso de inhibidores de la ECA y de bloqueantes de los receptores de angiotensina también puede favorecer el desarrollo de anemia al inhibir la síntesis de EPO [6] (Fig. 1).
Diagnóstico de la carencia de hierro
Todo paciente con insuficiencia cardiaca sintomática NYHA II debe someterse a un cribado de anemia que incluya un análisis de sangre. Estado del hierro (hemograma, ferritina plasmática, saturación de transferrina, receptor soluble de transferrina). Esto también se corresponde con las directrices de la ESC de 2012 [7]. En presencia de anemia (Hb <12 g/dl en mujeres, Hb <13 g/dl en hombres), debe realizarse un examen rutinario de las causas más comunes de anemia. La ferritina sérica, como proteína de fase aguda, puede elevarse con la actividad inflamatoria, por lo que una ferritina sérica normal no descarta la deficiencia de hierro. Por lo tanto, siempre debe determinarse también una PCR para estimar la actividad inflamatoria y el valor diagnóstico de la ferritina sérica.
En cuanto a la ferritina sérica, se aplican valores de referencia de aproximadamente >20 μg/l en mujeres y >30 μg/l en hombres en individuos sanos. En las enfermedades crónicas, sin embargo, ya puede existir una carencia de hierro con una ferritina de <100 μg/l.
La diferenciación entre la ferropenia absoluta y la funcional en la anemia inflamatoria crónica puede hacerse sobre la base de la ferritina sérica y la saturación de transferrina (Tab. 1).

En caso de anemia ferropénica absoluta, también debe excluirse la pérdida de sangre gastrointestinal.
Cálculo del déficit y las necesidades de hierro
La fórmula de Ganzoni (Fig. 2), conocida desde 1970, sigue siendo hoy en día el método más utilizado para calcular el déficit de hierro [8]. El peso corporal y la hemoglobina objetivo pueden utilizarse para calcular las necesidades de hierro.

Según la recomendación del fabricante de la carboximaltosa de hierro (Ferinject®), debe utilizarse una Hb objetivo de 13 g/dl y una reserva de hierro de 15 mg/kg para un peso corporal inferior a 35 kg. Para un peso corporal superior a 35 kg, se recomienda un objetivo de Hb de 15 g/dl y una reserva constante de hierro de 500 mg. Como regla general, puede suponerse un déficit de hierro de aproximadamente 1000 mg de hierro para la mayoría de los pacientes.
Terapia de la carencia de hierro – ¿Cómo sustituirla?
Sustitución oral: La experiencia previa ha demostrado que la sustitución oral con hierro, especialmente en pacientes con insuficiencia cardiaca crónica, ha tenido poco éxito debido a los cambios fisiopatológicos de la pared intestinal, el perfil desfavorable de efectos secundarios y la duración de la terapia. En los pacientes con anemia inflamatoria crónica, el hierro administrado por vía oral se absorbía mal y sólo podía llenar de forma insuficiente las reservas de hierro medidas por la ferritina sérica [9].
Sustitución de hierro por vía intravenosa: La aplicación de hierro por vía parenteral evita el deterioro de la absorción enteral y también la inhibición de la liberación de hierro mediada por la hepcidina. En las directrices de la ESC de 2012, también se menciona por primera vez la sustitución parenteral de hierro con carboximaltosa de hierro, que se utilizó en el estudio FAIR-HF, como opción terapéutica para la ferropenia o la anemia ferropénica en la insuficiencia cardíaca [7].
El estudio FAIR-HF se publicó en 2009 y fue el primer gran estudio prospectivo doble ciego controlado con placebo que investigó el tratamiento de la deficiencia de hierro en la insuficiencia cardiaca mediante carboximaltosa de hierro i.v. [4]. Un total de 459 pacientes con insuficiencia cardiaca sistólica (NYHA II [LVEF <40%] y NYHA III [LVEF <45%]) y ferropenia (ferritina sérica <100 μg/l o ferritina sérica de 100-299 μg/l y saturación de transferrina <20%) fueron aleatorizados 2:1 (terapia frente a placebo). Se incluyeron pacientes con y sin anemia para un rango de hemoglobina de 9,5-13,3 g/dl.
Utilizando la fórmula de Ganzoni descrita anteriormente, se calculó el déficit de hierro y se administraron 200 mg de hierro carboximaltosa i.v. semanalmente hasta reponer el déficit de hierro calculado. Posteriormente, se administró una dosis de mantenimiento de 200 mg i.v. cada cuatro semanas hasta la semana 24 del estudio. Después de 24 semanas, se produjo una mejora significativa en los criterios de valoración primarios del estado de salud subjetivo (“evaluación global autoinformada por el paciente”) y la clasificación de la NYHA.
Los criterios de valoración secundarios predefinidos de rendimiento físico (distancia en la prueba de marcha de 6 minutos) y calidad de vida subjetiva también mejoraron significativamente en el grupo de la carboximaltosa férrica tras sólo cuatro semanas. Los análisis de subgrupos mostraron beneficios similares en pacientes con o sin anemia subyacente. No hubo diferencias entre los grupos de estudio en cuanto a mortalidad por todas las causas, morbilidad y hospitalizaciones.
Estos resultados también confirmaron los de estudios más pequeños publicados anteriormente, todos los cuales mostraron efectos terapéuticos favorables de la administración de suplementos de hierro i.v. medidos por la capacidad de ejercicio, la clasificación de la NYHA y la calidad de vida en pacientes con insuficiencia cardiaca crónica y anemia o ferropenia [10–12].
Agentes estimulantes de la eritropoyesis (AEE): El uso de darbepoietina en pacientes con insuficiencia cardiaca sistólica y anemia se investigó en el estudio RED-HF (Reducción de eventos por darbepoetina alfa en insuficiencia cardiaca) publicado en 2013 [5]. No se pudo demostrar un beneficio significativo en la supervivencia con la darbepoietina, pero hubo un número significativamente mayor de complicaciones tromboembólicas en el grupo de darbepoietina. Así pues, el tratamiento de la anemia con AEE no suele recomendarse en pacientes con insuficiencia cardiaca crónica, a menos que exista una indicación desde el punto de vista nefrológico.
Conclusiones y recomendaciones terapéuticas para la práctica
La carencia de hierro y la anemia son cofactores de importancia pronóstica y muestran una elevada prevalencia en pacientes con insuficiencia cardiaca crónica. Tienen un impacto significativo en la calidad de vida y el rendimiento. Un análisis de laboratorio rutinario anual con recuento sanguíneo y estado del hierro incl. La ferritina sérica y la saturación de transferrina deben realizarse en todo paciente con insuficiencia cardiaca sintomática. Si existe una carencia inexplicada de hierro, están indicadas las aclaraciones diagnósticas diferenciales de la anemia, en particular una búsqueda endoscópica de hemorragias.
Para mejorar la sintomatología y el rendimiento de los pacientes, recomendamos considerar la sustitución parenteral con hierro, de forma análoga a los criterios de inclusión del estudio FAIR-HF, en pacientes con una ferritina sérica <100 μg/l o una ferritina sérica entre 100 y 299 μg/l y una saturación de transferrina <20%. Basándose en los datos actuales y en la escasa disponibilidad fisiopatológica de hierro en la insuficiencia cardiaca, se recomienda una terapia de sustitución a dosis bajas con 200 mg i.v. una vez a la semana hasta que se alcance el déficit de hierro calculado (véase la fórmula de Ganzoni).
Actualmente se está investigando en ensayos clínicos si la administración de dosis únicas más altas (por ejemplo, 500 mg, 1000 mg) es igual de segura y eficaz en la insuficiencia cardiaca. En cuanto a las pruebas existentes hasta la fecha sobre la mejoría de los síntomas y el perfil de efectos secundarios más favorable, creemos que la carboximaltosa de hierro sin dextrano es preferible a la sacarosa de hierro.
Para evaluar el efecto de los suplementos de hierro en pacientes con insuficiencia cardiaca con respecto a los criterios de valoración duros de mortalidad, hospitalizaciones y efectos a largo plazo, se necesitan más ensayos controlados con placebo y con una potencia adecuada. Por el momento, también sigue sin respuesta la pregunta de si la sustitución con hierro intravenoso proporciona el mismo beneficio en pacientes con insuficiencia cardiaca con fracción de eyección preservada. En este sentido, se está planificando el estudio FAIR-HFpEF.
Dr. Lukas Meier
Literatura:
- Klip IT, et al: Deficiencia de hierro en la insuficiencia cardiaca crónica: un análisis agrupado internacional. Am Heart J 2013; 165(4): 575-582.e3.
- Nanas JN, et al: Etiología de la anemia en pacientes con insuficiencia cardiaca avanzada. J Am Coll Cardiol 2006; 48(12): 2485-2489.
- Ezekowitz JA, McAlister FA, Armstrong PW: La anemia es frecuente en la insuficiencia cardiaca y se asocia a malos resultados: conclusiones de una cohorte de 12.065 pacientes con insuficiencia cardiaca de nueva aparición. Circulation 2003; 107(2): 223-225.
- Anker SD, et al: Carboximaltosa férrica en pacientes con insuficiencia cardiaca y deficiencia de hierro. N Engl J Med 2009; 361(25): 2436-2448.
- Swedberg K, et al: Tratamiento de la anemia con darbepoetina alfa en la insuficiencia cardiaca sistólica. N Engl J Med 2013; 368(13): 1210-1219.
- Sica DS: Farmacoterapia en la insuficiencia cardiaca congestiva: inhibidores de la ECA y anemia en la insuficiencia cardiaca congestiva. Insuficiencia cardíaca congestiva 2000; 6(6): 330-332.
- McMurray JJ, et al: ESC guidelines for the diagnosis and treatment of acute and chronic heart failure 2012: The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Desarrollado en colaboración con la Asociación de Insuficiencia Cardiaca (HFA) de la ESC. Eur J Heart Fail 2012; 14(8): 803-869.
- Ganzoni AM: Hierro-dextrano intravenoso: posibilidades terapéuticas y experimentales. Schweiz Med Wochenschr 1970; 100(7): 301-303.
- Moore RA, et al: Metaanálisis de la eficacia y seguridad de la carboximaltosa férrica intravenosa (Ferinject) a partir de informes de ensayos clínicos y datos de ensayos publicados. BMC Blood Disord 2011; 11: 4.
- Bolger AP, et al: Hierro intravenoso solo para el tratamiento de la anemia en pacientes con insuficiencia cardiaca crónica. J Am Coll Cardiol 2006; 48(6): 1225-1227.
- Toblli JE, et al: El hierro intravenoso reduce el NT-pro-péptido natriurético cerebral en pacientes anémicos con insuficiencia cardiaca crónica e insuficiencia renal. J Am Coll Cardiol 2007; 50(17): 1657-1665.
- Okonko DO, et al: Efecto de la sacarosa de hierro intravenosa sobre la tolerancia al ejercicio en pacientes anémicos y no anémicos con insuficiencia cardiaca crónica sintomática y ferropenia FERRIC-HF: un ensayo aleatorizado, controlado y ciego al observador. J Am Coll Cardiol 2008; 51(2): 103-112.
CARDIOVASC 2014; 13(3): 4-7