Mueren más mujeres de cáncer de ovario que de cualquier otro tumor, principalmente porque suele detectarse muy tarde. Los inhibidores de PARP se han desarrollado para el tratamiento del cáncer de ovario recurrente y se ha demostrado que aumentan la supervivencia libre de progresión (SLP) como terapia de mantenimiento.
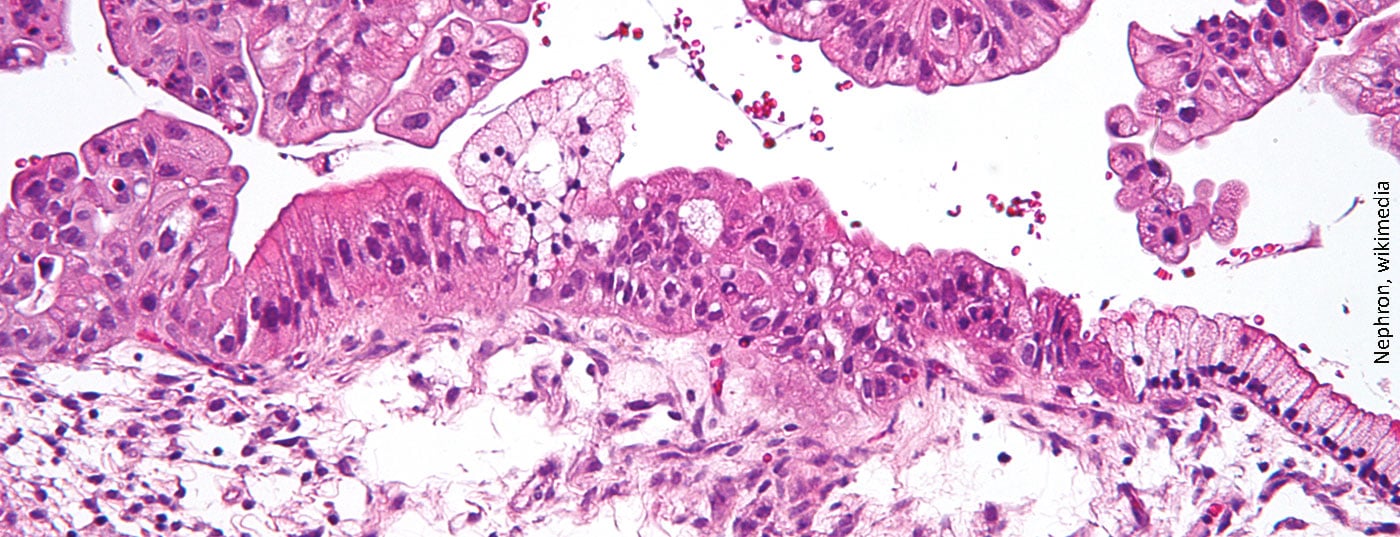
Cada año se diagnostica cáncer de ovario a unas 580 mujeres en Suiza. Casi el 75% de los pacientes no sobreviven a esta enfermedad. Una de las razones es que en aproximadamente tres cuartas partes de los afectados, el tumor se detecta en una fase muy tardía debido a los síntomas inespecíficos. Debido al curso agresivo del cáncer, se asocia a un pronóstico muy malo. Alrededor del 80% de los pacientes sufren una recidiva en los tres años siguientes a la cirugía y la quimioterapia.
Faltan opciones de detección precoz
En el riesgo de desarrollar cáncer de ovario influyen la edad, la obesidad, la falta de hijos, la menarquia precoz, la menopausia tardía y los antecedentes familiares. También aumenta significativamente si existe una mutación en los genes BRCA. Entonces la prevalencia a lo largo de la vida se multiplica por veinte. En la actualidad, no existen métodos de cribado fiables para identificar la enfermedad a tiempo. En el momento del diagnóstico, a menudo el cáncer ya se ha extendido a los órganos cercanos. Sin embargo, cuanto más tarde se haga el diagnóstico, más limitadas serán las opciones de tratamiento. Si la cirugía, los citostáticos y los inhibidores de la angiogénesis no funcionan y se produce una recaída, ahora pueden utilizarse los inhibidores de PARP.
Estos interfieren en el mecanismo de reparación del ADN y conducen a la apoptosis del tumor mediante la inestabilidad genómica. Las células tumorales utilizan las enzimas PARP para reparar los daños en su ADN. Esto incluye también los daños causados por los fármacos citostáticos. Los inhibidores de PARP ya no pueden reparar las roturas de una sola hebra. Las roturas de la doble cadena que se producen durante la siguiente división celular provocan entonces la muerte celular en las células con una reparación de la doble cadena del ADN alterada.
La terapia de mantenimiento convence
En un ensayo de fase III aleatorizado, doble ciego y controlado con placebo, se comparó el inhibidor de PARP niraparib con placebo en el tratamiento de 733 pacientes con cáncer de ovario en estadio III o IV tras quimioterapia basada en platino. Actualmente, el fármaco está aprobado en Suiza, independientemente del estado de la mutación BRCA, como terapia de mantenimiento para el cáncer de ovario recurrente sensible al platino tras la respuesta a la quimioterapia basada en platino, teniendo en cuenta la limitatio. Se evaluó la eficacia del inhibidor de PARP como terapia de mantenimiento, medida por la SLP, en pacientes con tumores deficientes en recombinación homóloga y en pacientes de la población general, determinada por pruebas jerárquicas.
Los resultados de un estudio de fase III prueban la eficacia
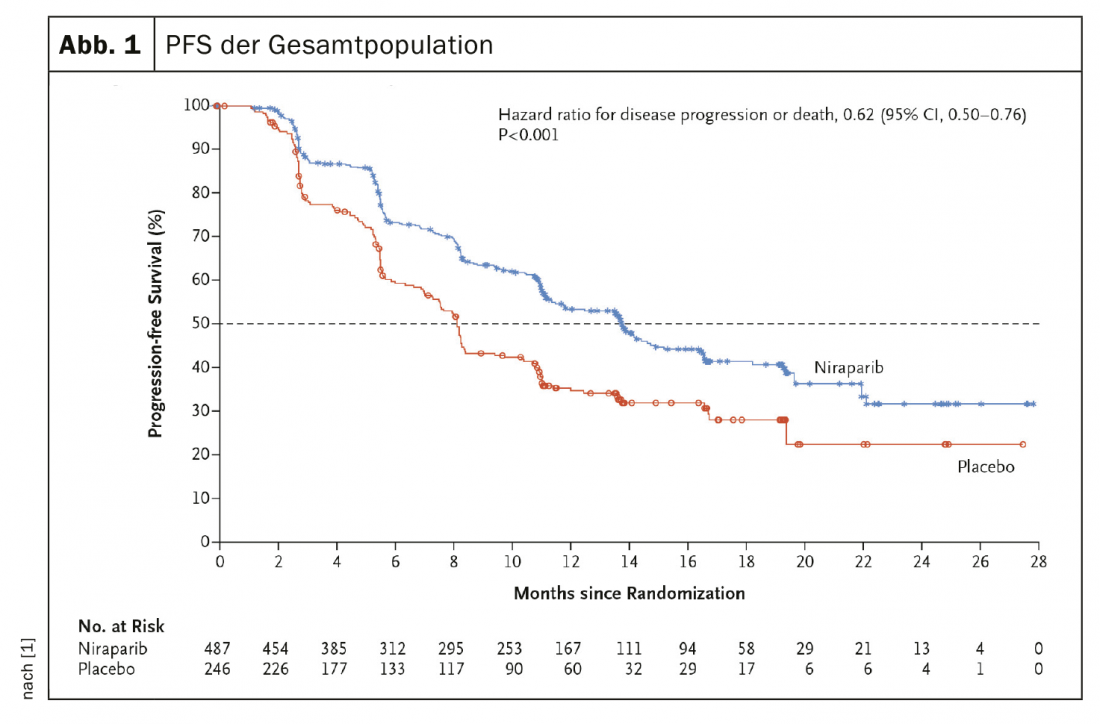
Se incluyeron 373 pacientes (50,9%) con tumores con deficiencia de recombinación homóloga. Entre las pacientes de esta categoría, la mediana de supervivencia sin progresión fue significativamente mayor en el grupo de niraparib que en el de placebo (21,9 meses frente a 10,4 meses; p<0,001). En la población general, la SLP correspondiente fue de 13,8 meses y de 8,2 meses (HR, 0,62; IC 95%, 0,50 a 0,76; p<0,001) (Fig. 1). En un análisis provisional a 24 meses, la tasa de supervivencia global fue del 84% en el grupo verum y del 77% en el grupo placebo (HR, 0,70; IC 95%, 0,44 a 1,11). Las reacciones adversas de grado 3 o superior más frecuentes fueron la anemia (en el 31,0% de los pacientes), la trombocitopenia (en el 28,7%) y la neutropenia (en el 12,8%).
Un inhibidor de PARP mejora significativamente la SLP
Los expertos resumieron que entre las pacientes con cáncer de ovario avanzado recién diagnosticado que respondieron a la quimioterapia basada en platino, las que recibieron el inhibidor de PARP tuvieron una supervivencia libre de progresión significativamente mayor que las que recibieron placebo. Este resultado fue independiente de la deficiencia de recombinación homóloga.
Para saber más:
- González-Martín A, et al: Niraparib in atients with Newly Diagnosed Advanced Ovarian Cancer, NEJM 2019; Online first. DOI: 10.1056/NEJMoa1910962.
Fuente: Sociedad Europea de Oncología Médica (ESMO) 2019
InFo ONCOLOGY & HEMATOLOGY 2019; 7(5): 28 (publicado el 17.10.19, antes de impresión).