Los enfermos de intestino irritable sufren reacciones de intolerancia a los alimentos. Una dieta baja en FODMAP o una dieta sin gluten pueden aliviar significativamente estos síntomas.
En los pacientes con síndrome del intestino irritable (SII), la barrera intestinal, la motilidad, la secreción y/o la sensibilidad visceral están alteradas. A menudo, el SII se asocia a una alteración del equilibrio inmunitario entérico, con procesos microinflamatorios o neuroinmunológicos en la mucosa intestinal que conducen a una proliferación local de células inmunitarias y/o células EC [1].
“Ahora está bien establecido que los pacientes con síndrome del intestino irritable no están simplemente imaginando cosas”, afirma el Prof. Dr. med. Yurdagül Zopf, Jefe de Medicina Nutricional del Hospital Universitario de Erlangen (D), “sino que en el SII tienen lugar procesos inflamatorios que no se dan en los controles sanos”. Se sabe por estudios histológicos que los pacientes con SII tienen mayores proporciones de linfocitos intraepiteliales, mastocitos y células EC. Las biopsias de la mucosa también mostraron una mayor densidad de fibras nerviosas [2–4]. Además, los pacientes con SII mostraron niveles significativamente mayores de serotonina, histamina y triptasa en las mediciones de las concentraciones de mediadores [5]. Este perfil alterado de mediadores de la mucosa activa el sistema nervioso entérico y los nervios aferentes primarios (nociceptivos) [1].
El diagnóstico se realiza mediante el procedimiento de exclusión. Las herramientas de diagnóstico incluyen la medición de patógenos en las heces (diagnóstico microbiano y virológico centrado en los cambios relacionados con la inflamación; huevos de lombriz), ileocolonoscopia con biopsias escalonadas, esofagogastroduodenoscopia con biopsias duodenales y pruebas de aliento H2 de lactosa, fructosa y sorbitol. Los diagnósticos de laboratorio avanzados incluyen electrolitos séricos, valores de retención renal, enzimas hepáticas y pancreáticas, TSH, glucosa en sangre/HbA1c, anticuerpos celíacos (transglutaminasa-AK) y calprotectina A en heces.
Regulación a través de la nutrición
La etiopatogenia del SII es compleja y varía de un individuo a otro. En consecuencia, existen muchos enfoques terapéuticos orientados predominantemente al tratamiento del síntoma principal. Entre ellas se encuentran las medidas farmacológicas (por ejemplo, laxantes, espasmolíticos, antidepresivos, loperamida), la fitoterapia, la psicohigiene y el ejercicio, así como la dieta [6].
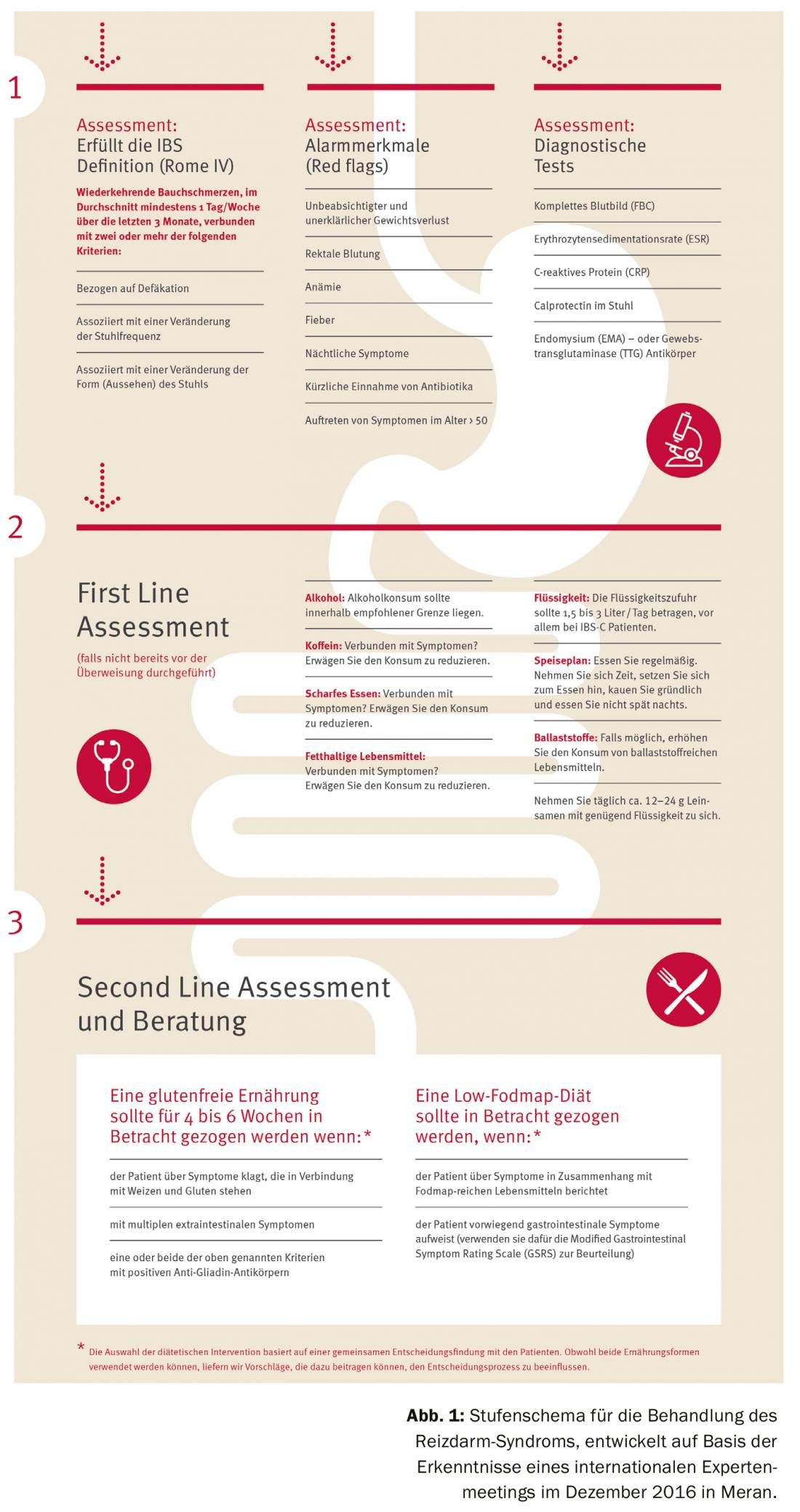
La nutrición, en particular, desempeña un papel importante en la regulación del SII (Fig. 1). Diversos estudios han demostrado que los pacientes con SII reaccionan a diferentes alimentos. Las mujeres tienden a sufrir reacciones de intolerancia con más frecuencia que los hombres, lo que puede explicarse por la mayor densidad de mastocitos en las mujeres. Sin embargo, las reacciones de intolerancia se producen independientemente del sexo, el tipo de SII, la ansiedad o el lugar de tratamiento (hospitalario frente a ambulatorio) [7].
La tolerabilidad de la fibra alimentaria ha sido bien estudiada. Es esencial consumir fibras alimentarias solubles en lugar de insolubles, ya que estas últimas pueden incluso agravar los síntomas: La hemicelulosa, por ejemplo (contenida en el trigo y el centeno), da lugar a una mayor producción de gas. “El paciente tiene molestias más graves que antes e incluso se muestra incomplaciente ante nuevas modulaciones dietéticas con el paso del tiempo”, advierte el Prof. Zopf.
También se ha confirmado que las alergias y las intolerancias son más frecuentes en los pacientes con SII [8]. Aunque sólo pueden detectarse diagnósticamente las alergias inducidas por IgE, los pacientes con una mayor actividad de la triptasa, la histamina y los mastocitos en el intestino tienen un mayor riesgo de reacciones inmunológicas.
La dieta sin gluten también ayuda a los pacientes con SII
Una proteína en particular suele ser el centro de interés: el gluten. Aquí es importante diferenciar quién no tolera realmente el gluten, porque una dieta baja en gluten no es automáticamente más sana para todo el mundo.
Una dieta sin gluten de por vida es la base del tratamiento de la enfermedad celíaca. Los pacientes con intolerancia al gluten/al trigo también se benefician de una dieta adaptada de este tipo, mientras que no se recomienda para las personas sanas, ya que según los estudios actuales no existe ningún beneficio clínico para los individuos sanos.
En muchos pacientes con SII, los síntomas se desencadenan o intensifican con el trigo o el gluten. En estos casos, una dieta sin gluten conlleva una mejora significativa de los síntomas, como demuestra el estudio sobre el síndrome del intestino irritable (SII) publicado en 2017. Allí, los síntomas del 34% de los pacientes con SII mejoraron de forma estadísticamente significativa y clínicamente relevante en el transcurso de una dieta sin gluten de cuatro meses. La adherencia al cambio dietético se mantuvo en muchos sujetos incluso después del estudio: Una proporción muy elevada (todos los que respondieron, el 55% de los que no respondieron) continuaron con una dieta sin gluten [9].
FODMAP – ¡observe el nivel de tolerancia individual!
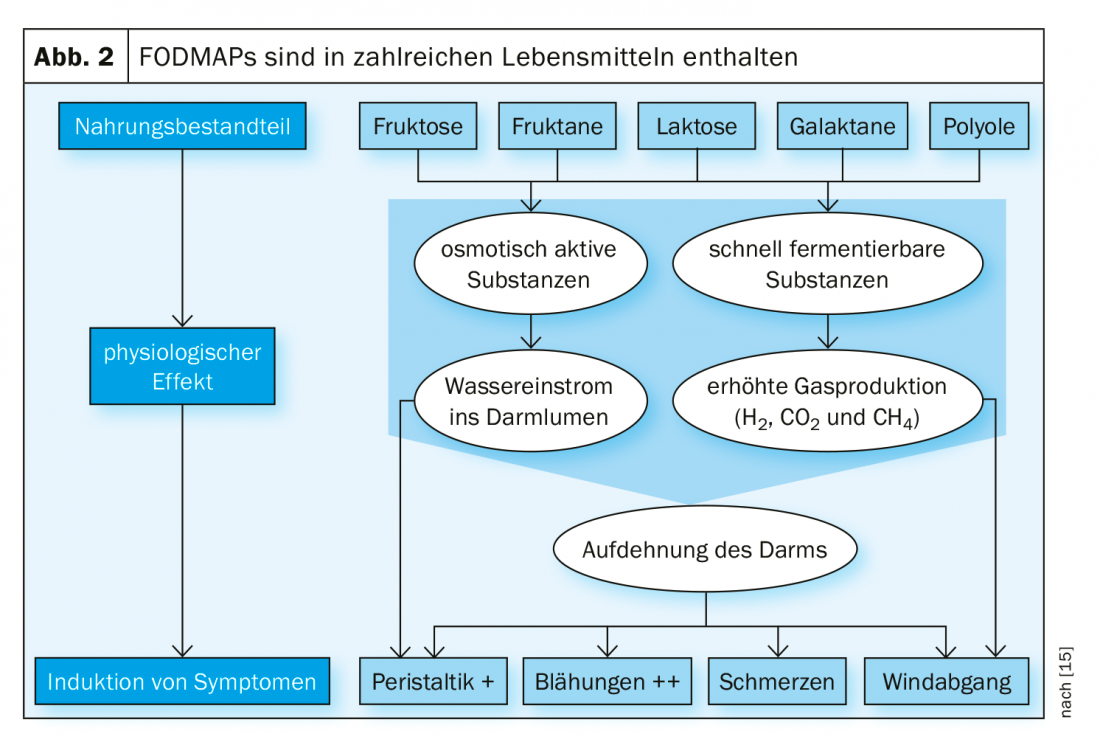
Los FODMAP -oligo-, di- y monosacáridos fermentables, así como los polioles- se absorben poco o nada en el intestino delgado. Los procesos osmóticos y la fermentación provocan una mayor afluencia de agua y la formación de gas. La malabsorción de estos carbohidratos es normal, muchas personas no sienten ningún efecto negativo al consumir FODMAPs. Los pacientes con SII, por su parte, experimentan a veces síntomas graves en respuesta a los FODMAP, como flatulencia, dolor y malestar, flatulencia, cambios en las heces y/o letargo (Fig. 2). Reaccionan con una producción de gas significativamente mayor que los controles sanos [10]. Una dieta baja en FODMAP conlleva una mejora de los síntomas en el 68-76% de los pacientes [11].
El Prof. Zopf subraya la importancia de un enfoque adaptado individualmente: “Cada uno de nosotros tiene un nivel de tolerancia diferente a los FODMAP. Dieta FODMAP no significa: reducción a cero. Debe detectarse el umbral tolerable para el individuo. Así pues, no siempre hay que seguir una dieta baja en FODMAP en su forma máxima. Puede ser suficiente para reducir las acciones.
Para evitar la malnutrición, es importante en cualquier caso que la dieta se lleve a cabo en compañía de un nutricionista profesional. Esto guía al paciente a través de tres etapas:
- Dieta de eliminación
- Reintroducir (para comprobar qué sustancias están causando problemas)
- Adaptación
Una preocupación asociada a la dieta baja en FODMAP es la reducción asociada de bifidobacterias [12]. Este cambio en la flora intestinal es comprensible, sobre todo porque los FODMAP producen diversas sustancias que mantienen la integridad de la mucosa. Sin embargo, un estudio posterior demostró que la terapia probiótica concurrente puede estabilizar la población de bifidobacterias [13].
Un cambio en la dieta también tiene efectos positivos sobre los niveles alterados de serotonina y PYY en los pacientes con SII [14].
Fuente: Zopf Y: “Influencia de la dieta en el SII”. Conferencia en el simposio satélite Dr. Schär “Nutrición en el síndrome del intestino irritable”, DGIM 2019, Wiesbaden (D).
Literatura:
- Layer P, et al.: Síndrome del intestino irritable S3-Leitlinie: Definición, fisiopatología, diagnóstico y terapia. Directriz conjunta de la Sociedad Alemana de Enfermedades Digestivas y Metabólicas (DGVS) y la Sociedad Alemana de Neurogastroenterología y Motilidad (DGNM). Z Gastroenterol 2011; 49(2): 237-293.
- Akbar A, et al: Aumento de las fibras sensoriales que expresan el receptor de capsaicina TRPV1 en el síndrome del intestino irritable y su correlación con el dolor abdominal. Gut 2008; 57(7): 923-929.
- Guilarte M, et al.: Los pacientes con SII con diarrea predominante muestran activación e hiperplasia de mastocitos en el yeyuno. Gut 2007; 56(2): 203-209.
- Spiller RC: Síndrome del intestino irritable postinfeccioso. Gastroenterología 2003; 124(6): 1662-1671.
- Buhner S, et al.: Activación de neuronas entéricas humanas por sobrenadantes de especímenes de biopsias colónicas de pacientes con síndrome del intestino irritable. Gastroenterología. 2009; 137(4): 1425-1434.
- Schaub N, Schaub N: Síndrome del intestino irritable. Perspectivas 2012. SMF 2012; 12(25): 505-513.
- Simrén M: Alteración de la flora gastrointestinal en pacientes con trastornos funcionales intestinales: ¿un camino a seguir? Therap Adv Gastroenterol 2009; 2(4 Suppl): 5-8.
- Boettcher E, Crowe SE: Proteínas alimentarias y trastornos gastrointestinales funcionales. Am J Gastro-enterol 2013; 108(5): 728-736.
- Barmeyer C, et al.: Respuesta a largo plazo a la dieta sin gluten como prueba de sensibilidad al trigo no celíaca en un tercio de los pacientes con síndrome del intestino irritable de tipo mixto y diarrea dominante. Int J Colorectal Dis 2017; 32(1): 29-39.
- Ong DK, et al.: La manipulación de los carbohidratos de cadena corta de la dieta altera el patrón de producción de gases y la génesis de los síntomas en el síndrome del intestino irritable. J Gastroenterol Hepatol 2010; 25(8): 1366-1373.
- Tuck CJ, et al.: Oligosacáridos, disacáridos, monosacáridos y polioles fermentables: papel en el síndrome del intestino irritable. Expert Rev Gastroenterol Hepatol 2014; 8(7): 819-834.
- Staudacher HM, et al.: La restricción de carbohidratos fermentables reduce las bifidobacterias luminales y los síntomas gastrointestinales en pacientes con síndrome del intestino irritable. J Nutrition Disease 2012; 142(8): 1510-1518.
- Staudacher HM, et al: Una dieta baja en FODMAP reduce los síntomas en pacientes con síndrome del intestino irritable y un probiótico restaura las especies de Bifidobacterium: un ensayo controlado aleatorizado. Gastroenterología 2017; 153(4): 936-947.
- Mazzawi T, El-Salhy M: Efecto de la dieta y la orientación dietética individual sobre las células endocrinas gastrointestinales en pacientes con síndrome del intestino irritable (Revisión). Int J Mol Med 2017; 40(4): 943-952.
- Beatrice Schilling: El concepto FODMAP. https://fodmap.ch/de/fodmap-konzept, último acceso 13 de agosto de 2019.
- Leiß O: Fibra, intolerancias alimentarias, FODMAPs, gluten y enfermedades funcionales intestinales – Actualización 2014. Z Gastroenterol 2014; 52(11): 1277-1298.
PRÁCTICA GP 2019; 14(8): 40-41