El objetivo del tratamiento farmacológico del carcinoma de próstata (CaP) es prolongar la supervivencia con unos efectos secundarios aceptables. En la actualidad, se dispone de varios fármacos para lograr una privación androgénica (TDA) eficaz. El objetivo es reducir el nivel de testosterona por debajo de 20 ng/dl. Existe una indicación para el inicio primario de la TAD en el CaP metastásico sintomático. A un paciente asintomático también se le puede ofrecer la TAD, pero en este caso debe realizarse una ponderación detallada de las posibles ventajas e inconvenientes. Si se produce una progresión del PSA a pesar de la manipulación hormonal, se habla de un CaP resistente a la castración. Las opciones de tratamiento para estos pacientes son la quimioterapia (principalmente docetaxel), la abiraterona y la enzalutamida.
El carcinoma de próstata (CaP) es el tipo de cáncer más frecuente en Suiza, con unos 6.000 nuevos casos al año. Con una edad media de aparición de 70 años, el CaP es una enfermedad de hombres mayores. Dependiendo del estadio y la diferenciación del tumor, el curso suele ser progresivo, pero a menudo puede verse influido favorablemente por el uso de medicación [1]. A continuación se resumen brevemente.
Terapia hormonal del carcinoma de próstata
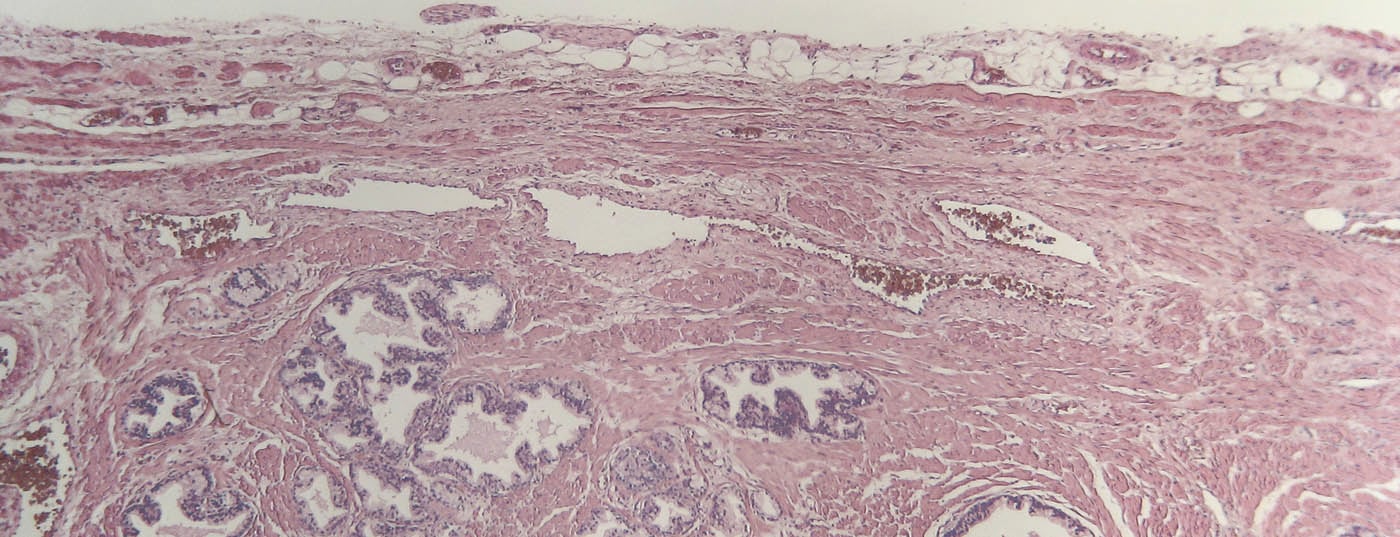
La terapia hormonal es la primera línea de tratamiento farmacológico para el CaP. En 1941, Huggins y Hodges fueron los primeros en describir la influencia positiva de la privación androgénica (TDA) mediante orquiectomía bilateral en el cáncer de próstata, por lo que recibieron el Premio Nobel en 1966 [2]. Hoy en día se dispone de varios fármacos para lograr una TAD eficaz (Fig. 1). Una reducción del valor de testosterona sérica por debajo de 50 ng/dl se indica como eficaz [3]. Sin embargo, datos más recientes muestran que la castración quirúrgica puede llegar a reducir la testosterona por debajo de 20 ng/dl, por lo que también debería aspirarse a este valor en la castración con medicación [4].
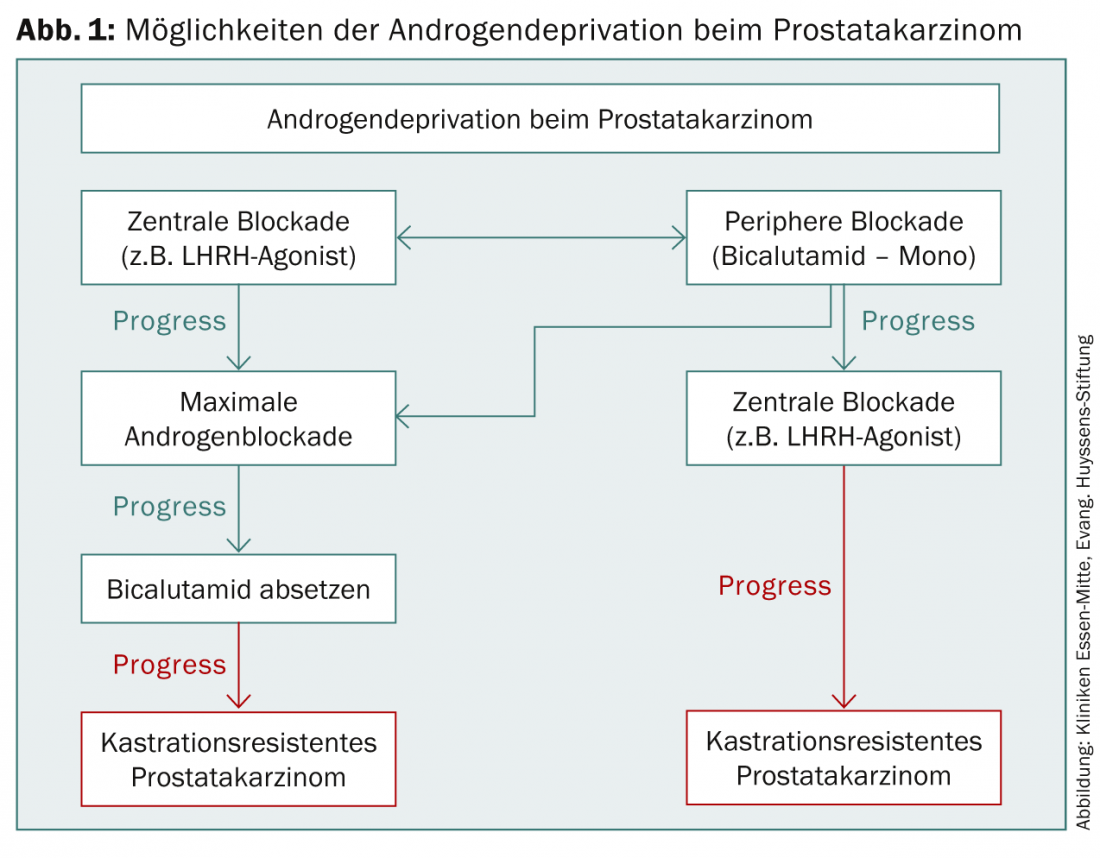
Una de las indicaciones para el inicio primario de la TAD es en el CaP metastásico sintomático. A un paciente asintomático también se le puede ofrecer una TAD primaria, pero en este caso se debe realizar una consideración detallada entre los posibles efectos secundarios adversos, un posible impacto en la calidad de vida, la naturaleza paliativa del tratamiento y la prolongación del intervalo libre de progresión. En caso de progresión tumoral tras una terapia previa, debe iniciarse la TAD con un tiempo de duplicación del PSA inferior a tres meses, progresión local sintomática o metástasis a distancia demostrada. La ADT también se utiliza de forma periintervencionista en pacientes de alto riesgo como parte de la radioterapia percutánea.Antes de la braquiterapia, la crioterapia o los ultrasonidos focalizados de alta intensidad (HIFU), la ADT puede reducir el volumen de la próstata [4].
Agonistas de la LHRH
La ADT más utilizada es un agonista de la LHRH [3]. Ésta se une a los receptores de LHRH y detiene la producción de testosterona al regular a la baja los receptores de la glándula pituitaria. Inicialmente, se produce un aumento de la testosterona porque la unión del agonista al receptor conduce a un aumento de la producción de LH y, por tanto, también de testosterona. Esto debe contrarrestarse administrando un bloqueante de los receptores androgénicos como la bicalutamida 150 mg durante quince días antes y dos semanas después de la administración inicial del agonista de la LHRH. El nivel de castración suele alcanzarse en este plazo [5,6]. Los agonistas de la LHRH se inyectan por vía subcutánea o intramuscular y están disponibles en forma de depósitos mensuales durante 1-12 meses, dependiendo del preparado. Los preparados más comunes son la leuprorelina, la goserelina y la buserelina. Los efectos secundarios habituales son sofocos, pérdida de libido e impotencia, y con una administración prolongada, osteoporosis y atrofia muscular.
El bloqueo androgénico intermitente como alternativa para minimizar los efectos secundarios de la TAD no se recomienda actualmente como tratamiento rutinario en las directrices de la Sociedad Urológica Alemana debido a la falta de datos a largo plazo sobre la supervivencia específica del tumor y global. Sin embargo, tras una educación previa sobre los datos a largo plazo que aún faltan, la TAD intermitente puede utilizarse para reducir el impacto de la medicación en la calidad de vida. La duración más habitual de la terapia es de 6-9 meses con una pausa terapéutica posterior, que puede variar en duración en función de la dinámica del PSA [3,7].
Durante la ADT, además de las determinaciones regulares del PSA, también deben comprobarse regularmente los niveles de testosterona. Si el nivel de castración no se alcanza con el agente elegido, debe iniciarse un cambio de agente, la administración adicional de un bloqueante de los receptores androgénicos (más comúnmente bicalutamida 50 mg) para un bloqueo androgénico completo o una orquiectomía subcapsular [3].
Antagonistas de la LHRH
Una alternativa a los agonistas de la LHRH son los antagonistas de la LHRH Abarelix (no aprobado en Suiza) y Degarelix (Firmagon®). Estos bloqueantes de los receptores de la LHRH no provocan un aumento de la testosterona y ya la reducen por debajo de los niveles de castración en pocos días, lo que constituye una alternativa a la castración en el CaP metastásico muy sintomático. Con la administración de Abarelix existe la posibilidad de una reacción alérgica hasta el shock anafiláctico, este efecto secundario no se observa con Degarelix [8,9].
Bloqueador del receptor de andrógenos
Existe una variedad de bloqueadores de los receptores androgénicos esteroideos (por ejemplo, el acetato de ciproterona) y no esteroideos que inhiben la acción de la dihidrotestosterona directamente a nivel celular. El nivel de testosterona no disminuye por ello. Por razones de practicidad, aquí sólo hablaremos del preparado más común y con menos efectos secundarios, la bicalutamida no esteroidea (Casodex® y genéricos).
La bicalutamida, por vía oral, está aprobada como monoterapia en el cáncer de próstata no metastásico pero localmente avanzado. Se ha demostrado que se pueden conseguir tiempos de supervivencia similares con una dosis de 150 mg diarios que con la castración quirúrgica [10]. Los pacientes con un CaP metastásico y un PSA >400 ng/ml mostraron una menor supervivencia libre de progresión y una menor supervivencia global, pero también en estos pacientes -en vista de la mejor calidad de vida en comparación con la ADT- puede administrarse monoterapia con bicalutamida tras una información adecuada [11]. Uno de los efectos secundarios más comunes suele ser la ginecomastia dolorosa, por lo que se recomienda la irradiación profiláctica de las glándulas mamarias antes de iniciar la terapia.
Bloqueo máximo de andrógenos
Si se produce un aumento del PSA con la monoterapia con LHRH, se añade un bloqueante de los receptores androgénicos. Esto se denomina bloqueo androgénico completo o máximo. También se utiliza cuando los niveles de testosterona no descienden por debajo de los niveles de castración con la monoterapia con LHRH o cuando se produce un aumento del PSA con la monoterapia con bicalutamida. Sin embargo, la posibilidad de que aumenten los efectos secundarios debe discutirse detalladamente con el paciente. En un paciente asintomático con un aumento del PSA, también es posible esperar inicialmente manteniendo la monoterapia e iniciar el bloqueo androgénico máximo sólo cuando aparezcan los síntomas [3].
Manipulación hormonal secundaria
Si el PSA vuelve a aumentar bajo el bloqueo androgénico máximo, la interrupción del bloqueante del receptor androgénico puede provocar un descenso del PSA debido a una mutación puntual en desarrollo en el receptor de testosterona [12]. Además, existen otras numerosas sustancias para la manipulación hormonal secundaria, por ejemplo, corticosteroides, ketoconazol, aminoglutetimida, estrógenos, progestágenos, tamoxifeno, inhibidores de la somatostatina, retinoides y calcitriol. El ketoconazol, en particular, puede prolongar el tiempo de inicio de la quimioterapia [13]. Antes de iniciar la terapia, el paciente debe ser informado detalladamente sobre la naturaleza paliativa de la terapia, los posibles efectos secundarios y la falta de pruebas de una supervivencia prolongada [3].
Quimioterapia
Si se produce una progresión del PSA a pesar de la manipulación hormonal secundaria, se habla de carcinoma de próstata resistente a la castración. En un paciente asintomático, se puede seguir esperando. Las indicaciones para iniciar la quimioterapia son la metástasis progresiva o un tiempo de duplicación del PSA rápido y un PSA >15 ng/ml (Fig. 2).
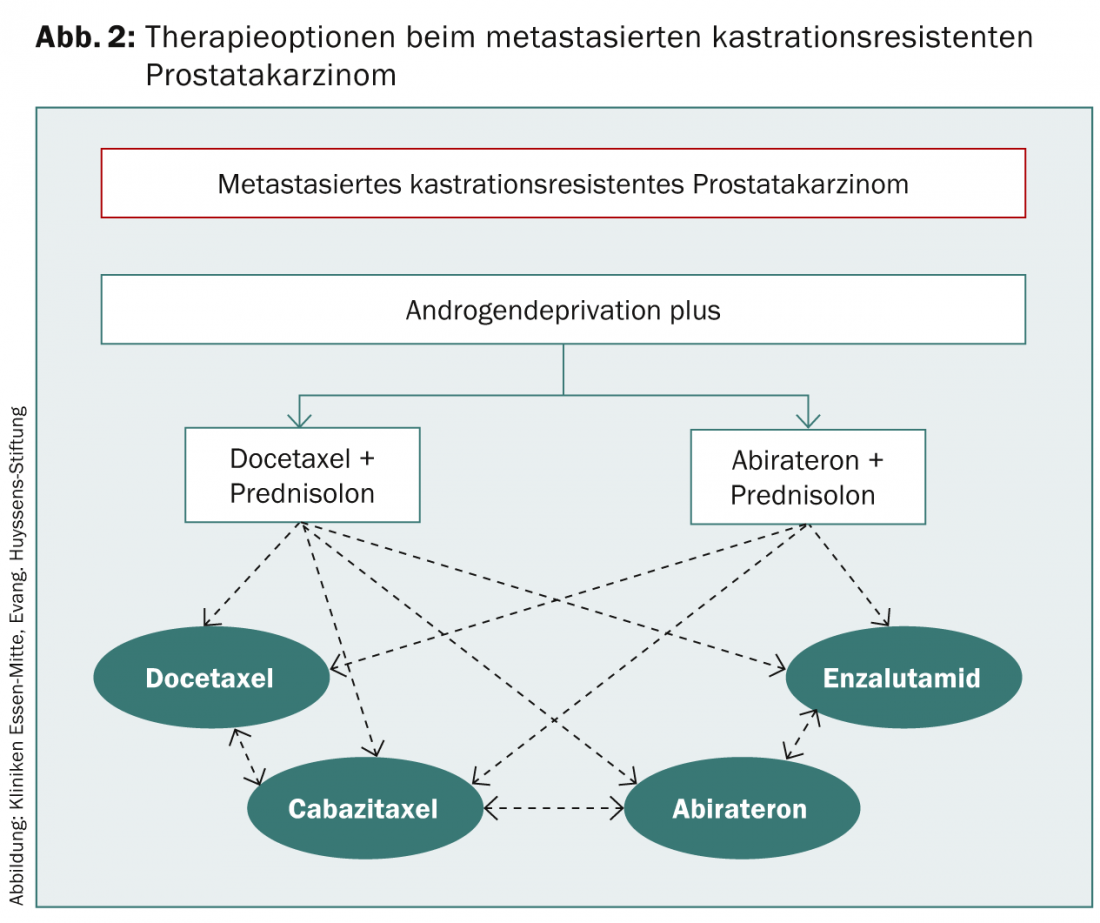
Debido a los efectos secundarios que cabe esperar, debe considerarse cuidadosamente en un paciente asintomático cuándo tiene sentido iniciar la terapia.
El docetaxel se utiliza para la quimioterapia de primera línea. El docetaxel se administra 75 mg/m² a intervalos de tres semanas junto con 2× 5 mg de prednisolona al día durante 6-10 ciclos. La ADT preexistente debe mantenerse, pero los bloqueantes de los receptores androgénicos deben suspenderse al menos cuatro semanas antes de iniciar la quimioterapia [3]. Si la enfermedad progresa con docetaxel, puede considerarse el cambio a cabazitaxel 25 mg/m² cada tres semanas en combinación con prednisolona. En los ensayos, sólo se produjo un beneficio en la supervivencia tras recibir al menos tres ciclos de cabazitaxel. Los nuevos datos también muestran una ventaja de supervivencia para el docetaxel en la terapia de primera línea antes de la ADT, lo que probablemente conducirá a un cambio en la secuencia terapéutica.
Abiraterona (Zytiga®)
La abiraterona (Zytiga®), un inhibidor del CYP17, reduce los niveles de testosterona al inhibir la síntesis de testosterona en los testículos, la próstata y las glándulas suprarrenales. Desde octubre de 2011, la abiraterona está aprobada para el tratamiento del CaP metastásico resistente a la castración tras la progresión del tumor después de la quimioterapia con docetaxel, por lo que también se recomienda en las directrices de las sociedades urológicas. En la actualidad, la abiraterona también está aprobada como tratamiento de primera línea para el CaP metastásico resistente a la castración, pero sólo para pacientes asintomáticos o ligeramente sintomáticos. Debe tenerse en cuenta que los pacientes tratados con abiraterona antes del docetaxel muestran una progresión de la enfermedad más rápida tras la administración de docetaxel que los pacientes sin abiraterona [14].
La abiraterona se toma en comprimidos a una dosis de 1000 mg diarios en combinación con prednisolona; se continúa con la ADT existente. Los efectos secundarios relevantes son principalmente la hipertensión, la hipopotasemia y la retención de líquidos por exceso de mineralocorticoides.
Enzalutamida (Xtandi®)
La enzalutamida (Xtandi®) se aprobó en Europa en junio de 2013 para el tratamiento del CaP metastásico resistente a la castración tras la terapia con docetaxel. El inhibidor del receptor de andrógenos se toma diariamente en forma de comprimidos con o sin prednisolona. Los efectos secundarios relevantes son dolores de cabeza y sofocos. Existe una contraindicación en caso de disfunción hepática grave. En los ensayos, la administración oral de 160 mg diarios de enzalutamida dio lugar a una supervivencia global significativamente prolongada frente al placebo; por lo tanto, la enzalutamida es otra terapia alternativa al cabazitaxel y la abiraterona [15]. Además, la aprobación de la enzalutamida antes de la quimioterapia con docetaxel se espera para otoño de 2014.
Terapia de las metástasis óseas
Para el tratamiento de las metástasis óseas, la directriz recomienda actualmente el bifosfonato ácido zoledrónico (Zometa® y genéricos) o el anticuerpo monoclonal denosumab (Prolia®) [3]. Además, el radio-223 también está disponible para indicaciones estrictas. Sin embargo, una discusión detallada de estos medicamentos excedería el alcance de este artículo, por lo que se hace referencia a la literatura específica del tema.
Conclusión
En la actualidad existen muchos fármacos diferentes para el tratamiento del CaP avanzado. Especialmente en el campo del CaP metastásico resistente a la castración, la aprobación de numerosos fármacos nuevos ha dado lugar a prometedoras alternativas de tratamiento. Sin embargo, se necesitan urgentemente más estudios para desarrollar una terapia secuencial basada en pruebas.
Mensajes para llevar a casa
- El objetivo del tratamiento farmacológico del CaP es prolongar la supervivencia con unos efectos secundarios aceptables.
- La TAD también debe continuarse en la fase de metástasis resistente a la castración.
- Una alternativa a la quimioterapia primaria es actualmente la abiraterona.
- La enzalutamida es otra alternativa después (y desde otoño de 2014 también antes) de la terapia con docetaxel.
- Aún no existen pruebas suficientes para desarrollar un plan escalonado de selección de fármacos en el estadio metastásico resistente a la castración.
- Se dispone de fármacos eficaces para el tratamiento de las metástasis óseas: ácido zoledrónico, denosumab y radio-223.
Literatura:
- Cáncer en Alemania 2007/2008. 8ª edición. Instituto Robert Koch (ed.) y Sociedad de Registros Epidemiológicos del Cáncer de Alemania (ed.). Berlín, 2012.
- Huggins C, et al: Estudios sobre el cáncer de próstata. II. Efectos de la castración en el carcinoma avanzado de la glándula prostática. Arch Surg 1941; 43: 209-223.
- Guía interdisciplinar de calidad S3 para la detección precoz, el diagnóstico y la terapia de los diferentes estadios del carcinoma de próstata.
- Gomella LG: Supresión eficaz de la testosterona para el cáncer de próstata: ¿existe la mejor terapia de castración? Rev Urol 2009; 11(2): 52-60.
- www.awmf.org/uploads/tx_szleitlinien/043-022OLl_S3_Prostatakarzinom_2011.pdf. (Recuperado el 11.08.2014)
- Auclair C, et al.: Inhibición del nivel del receptor testicular de la hormona luteinizante por el tratamiento con un potente agonista de la hormona liberadora de hormona luteinizante de la gonadotropina coriónica humana. Biochem Biophys Res Commun 1977; 76(3): 855-862.
- Huhtaniemi I, et al: Respuesta de los niveles de gonadotropina circulante al tratamiento con agonistas de la GnRH en el cáncer de próstata. J Androl 1991; 12(1): 46-53.
- Tunn U: El estado actual de la terapia de privación intermitente de andrógenos (DAI) para el cáncer de próstata: poniendo la DAI bajo los focos. BJU Int 2007; 99 Suppl 1: 19-22; discusión 23-24.
- Trachtenberg J, et al: A phase 3, multicenter open label, randomized study of abarelix versus leuprolide plus daily antiandrogen in men with prostate cancer. J Urol 2002; 167: 1670-1674.
- Van Poppel H, et al: Degarelix: un nuevo bloqueante de los receptores de la hormona liberadora de gonadotropina (GnRH) – resultados de un estudio de fase 2, aleatorizado, multicéntrico, de búsqueda de dosis, de 1 año de duración, en el tratamiento del cáncer de próstata. Eur Urol 2008; 54(4): 805-813.
- Iversen P, et al: Casodex (bicalutamida) monoterapia de 150 mg en comparación con la castración en pacientes con cáncer de próstata no metastásico no tratado previamente: resultados de dos ensayos aleatorizados multicéntricos con una mediana de seguimiento de 4 años. Urología 1998; 51(3): 389-396.
- Kaisary AV, et al: ¿Tiene algún papel la monoterapia antiandrógena en pacientes con cáncer de próstata metastásico? Cáncer de próstata Prostatic Dis 2001; 4(4): 196-203.
- Small EJ, et al: Terapia hormonal de segunda línea para el cáncer de próstata avanzado: un paradigma cambiante. J Clin Oncol 1997; 15(1): 382-388.
- Lam JS, et al: Terapia hormonal secundaria para el cáncer de próstata avanzado. J Urol 2006; 175(1): 27-34.
- Schweizer MT, et al: Influencia del tratamiento previo con abiraterona en la actividad clínica del docetaxel en hombres con cáncer de próstata metastásico resistente a la castración. Eur Urol 2014; pii: S0302-2838(14)00069-4. doi:10.1016/ j.eururo. 2014.01.018.
- Scher H, et al: Aumento de la supervivencia con enzalutamida en el cáncer de próstata tras la quimioterapia. N Engl J Med 2012; 367: 1187-1197.
InFo ONCOLOGÍA Y HEMATOLOGÍA 2014; 2(8): 10-13