En los hombres con carcinoma de próstata avanzado sometidos a privación androgénica, debe realizarse inicialmente una osteodensitometría y, si se demuestra osteopenia/osteoporosis o aumenta el riesgo de fractura, debe considerarse la terapia antirresortiva de la osteoporosis. Los bifosfonatos o el denosumab no están indicados para el tratamiento de las metástasis óseas en hombres con cáncer de próstata metastásico sin castración y pueden provocar una mayor incidencia de complicaciones como la osteonecrosis de mandíbula. El uso de denosumab o zoledronato es útil en el carcinoma de próstata metastásico óseo resistente a la castración con una suplementación concomitante adecuada de calcio y vitamina D.
Introducción
El cáncer de próstata avanzado suele darse en hombres mayores. Los tratamientos farmacológicos para el cáncer de próstata metastásico, como la terapia de privación de andrógenos (TPA) con la consiguiente deficiencia de testosterona, así como la administración concomitante de esteroides durante la terapia con abiraterona, docetaxel o cabazitaxel, tienen un efecto desfavorable sobre la densidad ósea. Tanto más cuanto que la ADT se realiza a menudo a lo largo de varios años. Por lo tanto, hay que tener en cuenta el desarrollo de la osteoporosis con sus correspondientes complicaciones. Además, se producen metástasis óseas en hasta el 90% de los pacientes con cáncer de próstata metastásico. Los acontecimientos esqueléticos (EES), como las fracturas patológicas, la compresión de la columna vertebral, la radioterapia o la estabilización ortopédica de las metástasis óseas, representan complicaciones potenciales de las metástasis esqueléticas con una elevada morbilidad y costes significativos; por lo tanto, debe prestarse atención a la salud ósea en los hombres con cáncer de próstata avanzado y considerar oportunamente la terapia dirigida a los huesos. Como característica especial del carcinoma de próstata, la mediana de supervivencia con metástasis esqueléticas es de varios años desde el diagnóstico, por lo que el uso de terapias antirresortivas debe adaptarse a la situación individual de la enfermedad. A continuación se discutirán las diferentes opciones terapéuticas, así como las situaciones clínicas típicas.
Bifosfonatos e inhibición del receptor activador del ligando NF-κ (RANKL)
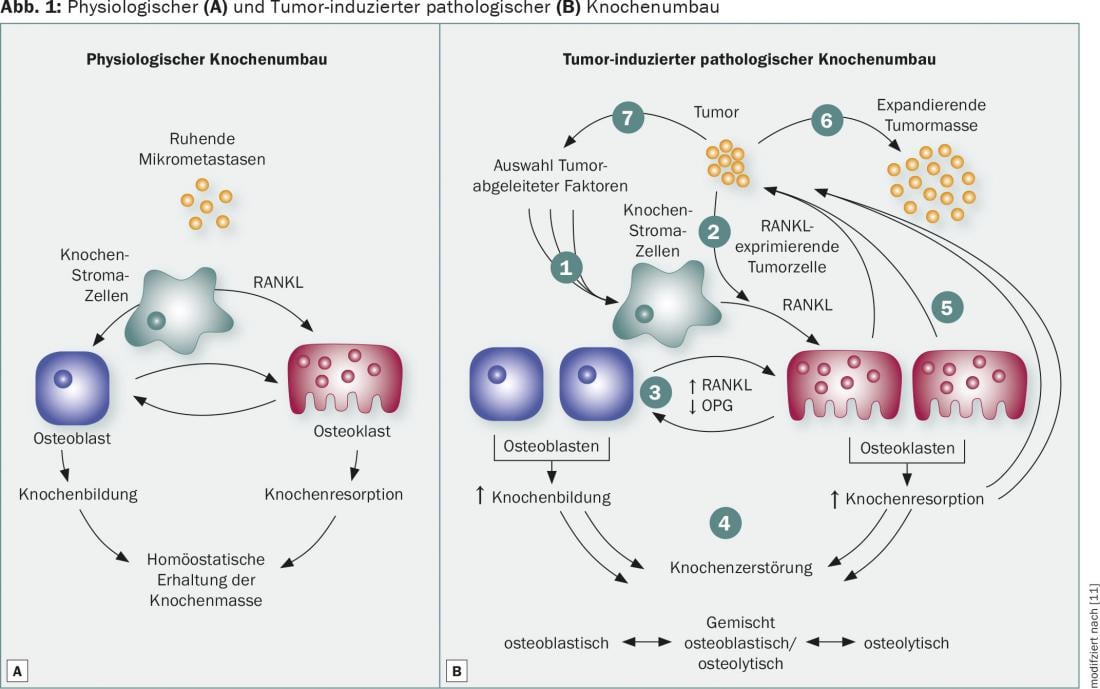
La remodelación ósea está controlada por los osteoblastos que acumulan nueva sustancia ósea y los osteoclastos que reabsorben la matriz ósea inorgánica y orgánica. En la remodelación ósea fisiológica, la función de los osteoblastos y los osteoclastos está en equilibrio, lo que garantiza el mantenimiento de la masa ósea (Fig. 1A). La aparición de metástasis óseas provoca un aumento de la actividad de los osteoclastos con el consiguiente aumento de la resorción ósea, que puede ser responsable de complicaciones esqueléticas. La vía de señalización del RANKL es un mecanismo crítico en la diferenciación, activación y supervivencia de los osteoclastos que está sobrerregulado en pacientes con metástasis óseas (Fig. 1B) . Estos hallazgos han conducido al desarrollo de compuestos antirresortivos diseñados para inhibir la actividad de los osteoclastos y evitar así la resorción ósea. Los bifosfonatos fijan el calcio a la superficie ósea y son fagocitados por los osteoclastos, provocando su apoptosis. El anticuerpo monoclonal humano denosumab se une al RANKL con gran afinidad y especificidad. La inhibición de la interacción con RANK previene la resorción ósea y la destrucción ósea relacionada con el cáncer al reducir el número y la actividad de los osteoclastos.
Profilaxis de la osteoporosis bajo privación androgénica en el carcinoma de próstata
Debido al bloqueo de la síntesis de testosterona, la TAD provoca una reducción de la densidad ósea con el riesgo de desarrollar osteoporosis. Por lo tanto, debería realizarse una osteodensitometría para determinar la densidad ósea al inicio de una TAD de larga duración (>6 meses). Si existe osteopenia, aumenta el riesgo de desarrollar osteoporosis sintomática, por lo que debe prevenirse esta progresión.
Un estudio de fase 3 en hombres con cáncer de próstata tratados con ADT y con osteopenia (puntuación T <-1) o antecedentes de fractura osteoporótica mostraron una reducción significativa de la incidencia de fracturas vertebrales en los dos primeros años de TAD cuando las pacientes recibieron profilaxis de la osteoporosis con denosumab (60 mg cada seis meses) [1].
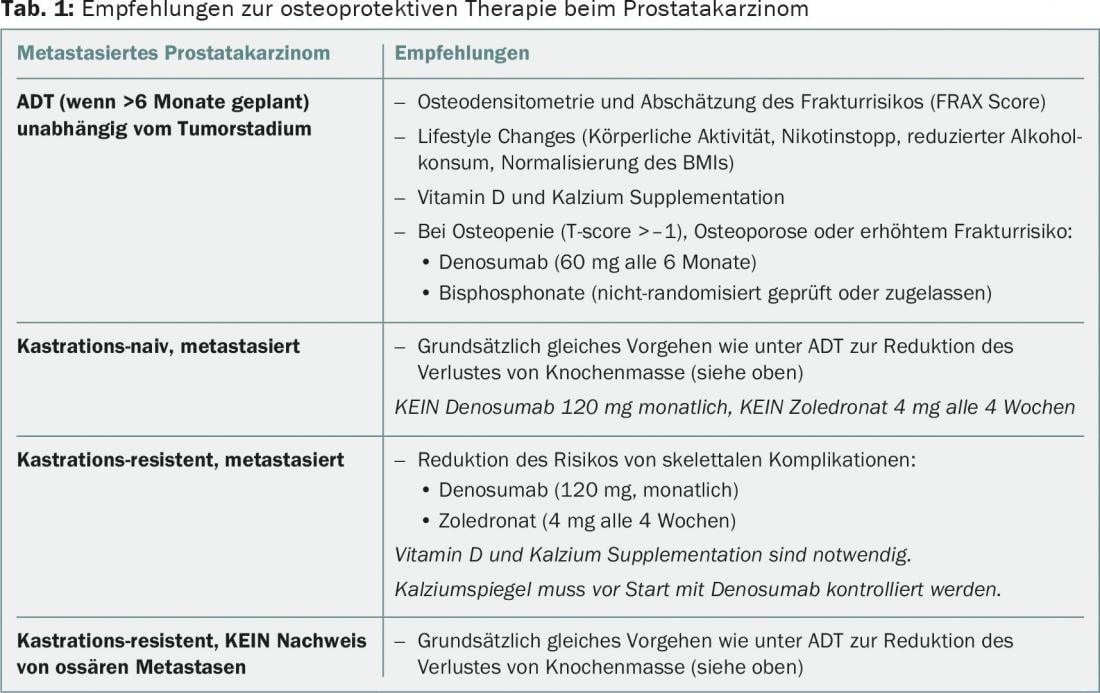
También se ha descubierto que los bifosfonatos mejoran la densidad ósea en los hombres que reciben TDA, pero no se han encontrado ensayos aleatorizados. En consecuencia, debe considerarse el uso de denosumab o bifosfonatos en pacientes en TAD, con osteoporosis demostrada o mayor riesgo de fractura (osteoporosis/fracturas osteoporóticas en el historial médico, medición de la densidad ósea con puntuación T <-1, uso permanente de glucocorticoides), en la dosis y frecuencia correctas para esta indicación (por ejemplo, denosumab 60 mg cada seis meses). También se recomiendan cambios simultáneos en el estilo de vida y una suplementación suficiente de calcio y vitamina D (tab. 1).
Carcinoma de próstata metastásico óseo sin castración
En un estudio aleatorizado de fase 3, se investigó el bifosfonato zoledronato a una dosis mensual de 4 mg en pacientes con carcinoma de próstata metastásico óseo no sometidos a castración (estos pacientes responden a la terapia con ADT en el 90% de los casos) [2]. No se pudo demostrar una reducción del riesgo de eventos esqueléticos, el criterio de valoración principal del estudio, ni una mejora de la supervivencia global. El denosumab no se probó en esta indicación. Por ello, los bifosfonatos y los inhibidores del RANKL no están indicados en hombres con cáncer de próstata metastásico óseo sin castración. El estado de aprobación de los bifosfonatos y el denosumab en Suiza (“tratamiento de pacientes con metástasis óseas de tumores sólidos en combinación con terapia antineoplásica estándar”) lamentablemente no coincide con las pruebas de este estudio, lo que conlleva el riesgo de sobretratamiento de este grupo de pacientes, con un mayor riesgo de toxicidad, especialmente la aparición de osteonecrosis de la mandíbula (ONM) e hipocalcemia (potencialmente mortal). Por otro lado, como ya se ha mencionado, la profilaxis de la osteoporosis también debe considerarse, por supuesto, en este grupo de pacientes.
Carcinoma de próstata óseo metastásico resistente a la castración
En los estudios clave de Saad et al. [3,4], se demostró una reducción significativa del riesgo de acontecimientos esqueléticos con el zoledronato en comparación con el placebo, a una dosis de 4 mg cada tres semanas durante 15 a un máximo de 24 meses en hombres con cáncer de próstata metastásico óseo resistente a la castración. Un estudio de seguimiento demostró la superioridad del denosumab (120 mg por vía subcutánea cada cuatro semanas) sobre el zoledronato en esta indicación [5]. La mediana del tiempo transcurrido hasta el primer acontecimiento esquelético se prolongó 3,5 meses con denosumab frente a zoledronato (20,7 frente a 17,1 meses, HR 0,82, IC 95% 0,71-0,95, p=0,008). Se produjeron más hipocalcemias de grado ≥3 en el grupo de denosumab (5 frente a 1%), las ONM fueron raras en ambos grupos en los dos primeros años (2 frente a 1%). No obstante, debe tenerse en cuenta que la incidencia de ONM aumenta significativamente con varios años de uso de denosumab, alcanzando hasta un 8% a largo plazo. El uso de denosumab o zoledronato es ciertamente útil en el carcinoma de próstata metastásico óseo resistente a la castración con una suplementación simultánea adecuada de calcio y vitamina D. Sin embargo, debe tenerse en cuenta que el reclutamiento de pacientes en estos ensayos se produjo antes de la era de los nuevos agentes antineoplásicos abiraterona, enzalutamida y radio. Para todos estos fármacos, se observó una reducción significativa de los eventos esqueléticos en los ensayos que finalmente condujeron a su aprobación [6–8].
La cuestión de la dosis y frecuencia óptimas de las sustancias antirresortivas sigue sin resolverse. En un ensayo aleatorizado de fase 3, la dosificación trimestral de zoledronato no fue inferior a la dosificación mensual estándar, en pacientes con carcinoma metastásico (incluidos más de 600 pacientes con carcinoma de próstata), con respecto al criterio de valoración primario de SRE [9]. Un estudio de la Asociación Suiza para la Investigación Clínica del Cáncer (estudio SAKK 96/12, véase www.sakk.ch) está probando actualmente la dosis estándar de denosumab frente a una frecuencia reducida en hombres con cáncer de próstata metastásico óseo resistente a la castración, sobre todo teniendo en cuenta la frecuencia creciente de ONM durante el periodo de tratamiento.
Carcinoma de próstata resistente a la castración sin evidencia de metástasis óseas
El denosumab (120 mg cada cuatro semanas) también se estudió en hombres con cáncer de próstata con niveles de PSA crecientes en deprivación androgénica pero sin presencia de metástasis (los denominados pacientes con CPRC M0) en un estudio de fase 3 [10]. Esto demostró una prolongación de la supervivencia libre de metástasis ósea, pero sin una ventaja para la supervivencia global. El beneficio fue evaluado como clínicamente irrelevante tanto por las autoridades reguladoras como por los expertos de la Conferencia de Consenso sobre Cáncer de Próstata Avanzado de St. Gallen (APCCC) en 2015 y, por lo tanto, no se recomienda en general. El denosumab tampoco está aprobado en ningún país para esta indicación.
Resumen y perspectivas
La terapia osteoprotectora es un pilar importante del tratamiento del carcinoma de próstata metastásico óseo en determinadas indicaciones. Nuestras recomendaciones se resumen en el cuadro 1 . Deben evitarse los tratamientos excesivos, sobre todo por el riesgo de efectos secundarios raros pero graves. Los estudios actuales proporcionarán información sobre la dosis y la frecuencia terapéutica de los bifosfonatos y los inhibidores del RANKL a lo largo del tiempo. Hasta la fecha, no existen pruebas de que los inhibidores del RANKL tengan un efecto antineoplásico en el cáncer de próstata que sea clínicamente relevante y se traduzca en una mejora de la supervivencia. Así pues, los bifosponatos o el denosumab sólo deben utilizarse como parte de la terapia de la osteoporosis, o para prevenir los SRE, en el cáncer de próstata refractario a la castración.
Literatura:
- Smith MR, et al: Denosumab en hombres que reciben terapia de privación de andrógenos para el cáncer de próstata. NEJM 2009; 361(8): 745-755.
- Smith MR, et al: Ensayo controlado aleatorizado de ácido zoledrónico precoz en hombres con cáncer de próstata sensible a la castración y metástasis óseas: resultados del CALGB 90202 (alianza). J Clin Oncol 2014; 32: 1143-1150.
- Saad F, et al: Ensayo aleatorizado controlado con placebo de ácido zoledrónico en pacientes con carcinoma de próstata metastásico refractario a las hormonas. J Natl Cancer Inst 2002; 94: 1458-1468.
- Saad F, et al: Eficacia a largo plazo del ácido zoledrónico para la prevención de complicaciones esqueléticas en pacientes con cáncer de próstata metastásico refractario a las hormonas. J Natl Cancer Inst 2004; 96: 879-882.
- Fizazi K, et al: Denosumab frente a ácido zoledrónico para el tratamiento de las metástasis óseas en hombres con cáncer de próstata resistente a la castración: un estudio aleatorizado a doble ciego. Lancet 2011; 377: 813-822.
- Logothetis CJ, et al: Efecto del acetato de abiraterona y la prednisona en comparación con placebo y prednisona sobre el control del dolor y los acontecimientos relacionados con el esqueleto en pacientes con cáncer de próstata metastásico resistente a la castración: análisis exploratorio de los datos del ensayo aleatorizado COU-AA-301. Lancet Oncol 2012; 13: 1210-1217.
- Fizazi K, et al: Efecto de la enzalutamida sobre el tiempo transcurrido hasta el primer acontecimiento relacionado con el esqueleto, el dolor y la calidad de vida en hombres con cáncer de próstata resistente a la castración: resultados del ensayo aleatorizado de fase 3 AFFIRM. Lancet Oncol 2014; 15: 1147-1156.
- Sartor O, et al: Efecto del dicloruro de radio-223 sobre los acontecimientos esqueléticos sintomáticos en pacientes con cáncer de próstata resistente a la castración y metástasis óseas: resultados de un ensayo aleatorizado doble ciego de fase 3. Lancet Oncol 2014; 15: 738-746.
- Himelstein AL, et al. CALGB 70604 (Alianza): Un estudio aleatorizado de fase III sobre la dosis estándar frente a la dosis a intervalos más largos de ácido zoledrónico en el cáncer metastásico. Reunión anual de la ASCO 2015. Resumen 9501.
- Smith MR, et al: Denosumab y supervivencia libre de metástasis ósea en hombres con cáncer de próstata resistente a la castración: resultados de un ensayo de fase 3, aleatorizado y controlado con placebo. Lancet 2012; 379: 39-46.
- Dougall WC: Vías moleculares: papeles dependientes e independientes de los osteoclastos de la vía RANKL/RANK/OPG en la tumorigénesis y la metástasis. Clin Cancer Res 2012; 18(2): 326-335.
InFo ONCOLOGÍA Y HEMATOLOGÍA 2016; 4(5): 8-12