La modificación del estilo de vida (ejercicio, dieta) y la metformina siguen siendo las piedras angulares en el tratamiento de la diabetes mellitus tipo 2. Antes de iniciar la terapia antidiabética, se recomienda fijar un objetivo individual de HbA1c. Las ventajas de los nuevos fármacos antidiabéticos orales (ADO) son el bajo riesgo de hipoglucemia, la pérdida de peso o la neutralidad ponderal y, por lo general, una buena tolerabilidad. Los inhibidores del SGLT2 inducen una pérdida renal de glucosa y sólo son eficaces con una función renal preservada. Debido a su novedoso mecanismo de acción, pueden combinarse bien con otros ACOD. Basándose en la eficacia y el perfil de efectos secundarios de los nuevos fármacos antidiabéticos, debe buscarse una combinación terapéutica óptima e individualizada para cada paciente.
Debido a los nuevos descubrimientos y avances, se han establecido nuevos principios importantes en el tratamiento de la diabetes tipo 2 que se han incorporado a las directrices actuales: Debe fijarse un objetivo individual de HbA1c en el intervalo de 6,5-8,0% para cada paciente, teniendo en cuenta la duración de la enfermedad, las enfermedades concomitantes, la esperanza de vida y los recursos personales y sociales. También puede lograrse una reducción de las complicaciones macrovasculares si se consigue un control óptimo sostenible de la diabetes desde el inicio de la enfermedad (HbA1c 6,5-7,0%). Por otra parte, una reducción de la HbA1c <7,0% “a cualquier precio” conduce a hipoglucemias frecuentes y a un aumento de la mortalidad en caso de complicaciones cardiovasculares ya existentes y de larga duración de la enfermedad [1]. Aunque el papel de la metformina como terapia de primera línea junto con la modificación del estilo de vida es indiscutible, existen numerosas opciones de combinación entre las que elegir en el segundo escalón tras la introducción de las incretinas y las gliflozinas, que se analizarán en detalle a continuación.
Novedades sobre los “antiguos” antidiabéticos orales
Metformina: En el momento del diagnóstico de la diabetes de tipo 2 o poco después, todos los pacientes deben recibir tratamiento con metformina si no se puede lograr un control óptimo de la diabetes mediante la modificación del estilo de vida y el tratamiento se tolera gastrointestinalmente. La metformina disminuye fuertemente la HbA1c, reduce las complicaciones micro y macrovasculares, retrasa la progresión de la diabetes, no provoca hipoglucemia, favorece la pérdida de peso y es rentable. La insuficiencia renal con una TFGe <30 ml/min es una contraindicación importante debido al riesgo de acidosis láctica potencialmente mortal. Si la TFGe desciende a 30-45 ml/min, la terapia preexistente puede continuarse con un máximo de 1000 mg diarios; no se recomienda iniciar la terapia. El tratamiento puede reiniciarse a partir de una TFGe de 45-60 ml/min, con recomendaciones de dosis máximas diarias variables de 1000-2000 mg [2].
Es crucial instruir a los pacientes para que interrumpan la terapia en caso de enfermedades intercurrentes (operaciones, infecciones, insuficiencia cardiaca, etc.). Si está previsto utilizar medios de contraste radiográfico que contengan yodo, debe suspenderse la metformina 48 horas antes con una TFGe <45 ml/min (administración intravenosa) o <60 ml/min (administración intrarterial). Con una función renal estable documentada, es posible reiniciar el tratamiento 48 horas después de la administración del contraste [3]. Como resultado de la interferencia con la absorción de vitamina B12, la deficiencia de esta vitamina se produce en un 10-15% de los pacientes que toman metformina y debe buscarse y sustituirse si se presentan signos, especialmente en la polineuropatía periférica.
Gliclazida: De las sulfonilureas disponibles, sólo se recomienda el uso de gliclazida, ya que los preparados de acción más prolongada, especialmente la glibenclamida, presentan un mayor riesgo de hipoglucemia y su uso puede asociarse a un aumento de la mortalidad [4]. Con sólo un ligero aumento del riesgo de hipoglucemia, la seguridad cardiovascular y la reducción de la incidencia de complicaciones microvasculares se han demostrado adecuadamente con la gliclazida [5]. La gliclazida es un potente reductor de la HbA1c, su uso se asocia a un ligero aumento de peso.
Glitazonas: De las glitazonas, sólo la pioglitazona sigue disponible después de que la rosiglitazona fuera retirada del mercado en 2010 porque se observó un aumento de los eventos cardiovasculares con la terapia. El mecanismo de acción se basa en una mejora de la sensibilidad a la insulina, lo que se traduce en un potente efecto reductor de la HbA1c sin un mayor riesgo de hipoglucemia. Las glitazonas provocan un aumento de peso debido a un incremento del tejido adiposo subcutáneo y a la retención de líquidos, por lo que no pueden utilizarse en la insuficiencia cardiaca. Además, estudios recientes han demostrado una mayor incidencia de fracturas osteoporóticas en mujeres posmenopáusicas [6]. La asociación de la toma de pioglitazona con un mayor riesgo de cáncer de vejiga ha sido cuestionada o relativizada por un estudio publicado recientemente [7]. Sin embargo, la pioglitazona ha perdido importancia con la disponibilidad de nuevas sustancias y ahora se utiliza relativamente poco, al menos en Suiza.
Nuevos fármacos antidiabéticos (orales)
Gliflozina: Desde el siglo XIX se sabe que la clorizina, un glucósido aislado por primera vez de la corteza del manzano en 1835, tiene un efecto glucosúrico. En 1987, la clorizina se utilizó por primera vez como antidiabético en modelos animales y poco después se reconoció como inhibidor de los cotransportadores de sodio y glucosa (SGLT) 1 y 2 (cotransportadores de sodio y glucosa del riñón). El SGLT2 se encuentra principalmente en el túbulo proximal de los riñones, el SGLT1 en el túbulo proximal y en el intestino delgado. Debido a su escasa biodisponibilidad oral, la clorizina no llegó a la clínica, pero estimuló el desarrollo de nuevos inhibidores de SGLT. Hasta el momento, se dispone de tres inhibidores de SGLT2 relativamente selectivos, canagliflozina (Invokana®), dapagliflozina (Forxiga®) y empagliflozina (Jardiance®), cuyo uso conlleva una pérdida renal de glucosa de 60-90 g/d [8]. Estas sustancias reducen la HbA1c en torno a un 0,5-1% en comparación con el placebo, independientemente de si se administró un inhibidor de SGLT2 como monoterapia o en combinación. Se observó una reducción de los niveles de glucosa en sangre tanto en ayunas como posprandiales. Los efectos secundarios bienvenidos fueron una reducción de la presión arterial sistólica (2-8 mmHg en seis meses) y una disminución del peso corporal (1-3 kg en seis meses). En caso de deterioro de la función renal (TFG <45-60 ml/min), el efecto de los inhibidores de SGLT2 disminuye rápidamente [9].
Con los inhibidores de SGLT2, las micosis genitales son más frecuentes (aprox. 10%), por lo que debe observarse una buena higiene íntima. En caso de micosis, preferimos una única terapia oral con fluconazol. Las infecciones urinarias también son algo más frecuentes. Debido a la diuresis osmótica, pueden producirse molestias ortostáticas, por lo que debe considerarse el ajuste de cualquier tratamiento diurético existente al iniciar la terapia [8].
Aún no se dispone de datos a largo plazo sobre la seguridad y la reducción de los criterios de valoración micro y macrovasculares. Así, en diversos estudios se observó un ligero aumento del colesterol LDL y una disminución del colesterol HDL de aproximadamente 4%. Recientemente, también se ha observado una acumulación de cetoacidosis asociada al uso de inhibidores de SGLT2 en pacientes con diabetes de tipo 2. En la mayoría de los casos, pudo identificarse un factor predisponente: una enfermedad grave, una ingesta reducida de alimentos y líquidos o una reducción de la dosis de insulina utilizada. También cabe mencionar que las cetoacidosis se produjeron con niveles de glucosa en sangre sólo ligeramente elevados (cetoacidosis euglucémica), lo que dificultó el diagnóstico [10]. Los inhibidores de SGLT2, al igual que la metformina, deben pausarse en caso de enfermedades intercurrentes, intervenciones quirúrgicas, etc.
Las gliflozinas pueden combinarse con metformina, gliclazida, gliptinas, análogos del GLP-1 e insulina. La combinación con una gliptina es potente reductora de la HbA1c y no provoca hipoglucemia (Fig. 1) [11]. En Suiza, actualmente sólo la dapagliflozina puede combinarse con las gliptinas sin aprobación previa. La combinación con análogos del GLP-1 también es potencialmente muy eficaz, pero aún no ha sido aprobada en Suiza. Los inhibidores de SGLT2 también pueden combinarse con insulina y entonces permiten a menudo reducir la dosis de insulina. También son eficaces en la diabetes de tipo 1, pero no están aprobados para esta indicación.
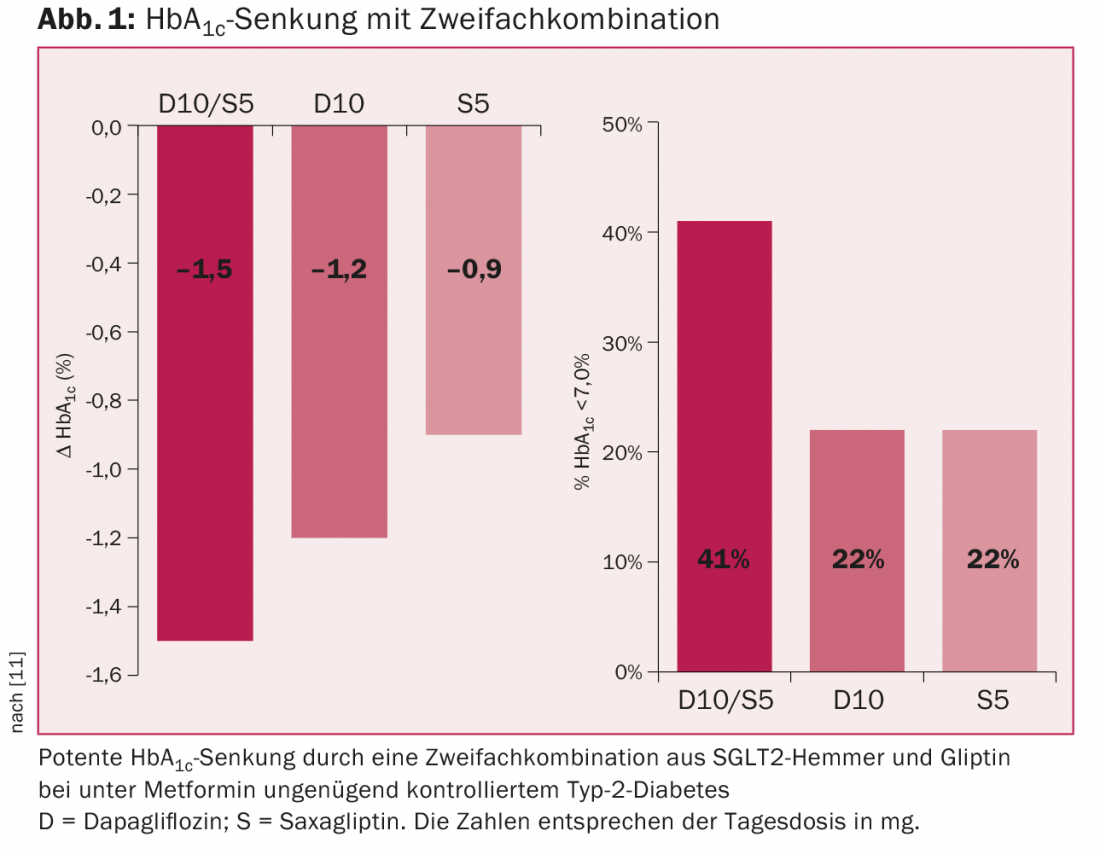
En resumen, el uso de un inhibidor de SGLT2 está especialmente indicado para los pacientes obesos más jóvenes con una función renal normal, en los que la hipoglucemia debe evitarse a toda costa (por ejemplo, los chóferes).
Incretinas (gliptinas y análogos del GLP-1): Las gliptinas son inhibidores de la dipeptidil peptidasa 4 y, por tanto, impiden la rápida descomposición de las incretinas, especialmente la GLP-1 (“péptido similar al glucagón 1”). La potenciación del efecto incretina o GLP-1 conduce, entre otras cosas, a un retraso del vaciado gástrico, a la activación de las células β con un aumento de la secreción de insulina y a la inhibición de las células α (secreción de glucagón) y de la gluconeogénesis en el hígado. Así, las gliptinas mejoran los niveles de glucosa en sangre en ayunas y postprandiales. Puede esperarse una reducción de la HbA1c con monoterapia del orden del 0,5-1,0% [12]. Las gliptinas tienen un peso neutro y no provocan hipoglucemia debido a su efecto dependiente de la glucosa. En general, las gliptinas se toleran muy bien. Después de que surgieran preocupaciones sobre la seguridad cardiovascular basadas en resultados anteriores (aumento de las hospitalizaciones por insuficiencia cardiaca con saxagliptina en el estudio Savor-TIMI 53), los estudios de seguimiento no mostraron un aumento de la insuficiencia cardiaca ni del riesgo cardiovascular [13–15]. Sin embargo, aún no se dispone de datos a largo plazo que demuestren una reducción de los criterios de valoración micro y/o macrovasculares.
En función renal moderada y gravemente alterada (TFGe <30 ml/min), sólo puede utilizarse linagliptina sin ajuste de dosis. Las gliptinas pueden combinarse con metformina, gliclazida, inhibidores SGLT2 e insulina básica. No se recomienda la combinación con una terapia intensificada de insulina debido al escaso beneficio adicional.
La modificación de la molécula de GLP-1 también puede impedir su rápida degradación por la dipeptidil transferasa 4. La aplicación subcutánea de estos análogos del GLP-1 consigue niveles suprafisiológicos de GLP-1, por lo que el efecto de los análogos del GLP-1 es mayor que el de las gliptinas. La reducción de la HbA1c conseguida en los ensayos clínicos es del 1,0-1,8%. Los análogos del GLP-1 actualmente disponibles difieren principalmente en su duración de acción: exenatida (Byetta®) y la lixisenatida (no disponible en Suiza) son de acción corta (semivida <5 horas) y reducen principalmente los niveles de glucosa en sangre posprandiales, mientras que los preparados de acción prolongada (semivida >12 Horario: Liraglutida [Victoza®], Exenatida LAR [Bydureon®], Dulaglutida [Trulicity®] y Albiglutida [Eperzan®]) reducen más los niveles de glucosa en sangre en ayunas. Todos los análogos del GLP-1 provocan una pérdida de peso, por término medio de entre 1 y 4 kg, y no causan hipoglucemia. Los efectos secundarios gastrointestinales como las náuseas, la hinchazón y la diarrea son relativamente frecuentes y más pronunciados con los preparados de acción corta, pero suelen remitir al cabo de unas semanas. Si los síntomas persisten, puede intentarse el tratamiento con un análogo del GLP-1 de acción prolongada alternativo. La aplicación subcutánea es diaria (liraglutida) o semanal (exenatida LAR, dulaglutida, albiglutida). Los análogos del GLP-1 pueden combinarse con metformina, gliclazida y pioglitazona; la prescripción simultánea de gliptinas carece de sentido debido al mismo objetivo. Sólo la liraglutida puede combinarse con la insulina básica (aprobación y reembolso) [16]. Los análogos del GLP-1 no se han estudiado ni aprobado en función renal significativamente alterada (eGFR <30 ml/min) .
La combinación fija recientemente disponible (IDegLira, Xultophy®) de una insulina básica (Degludec, Tresiba®) con un análogo del GLP-1 (liraglutida) es una opción de tratamiento muy potente, con pocos efectos secundarios y asociada a un riesgo muy bajo de hipoglucemia. En pacientes ya tratados con una insulina básica y metformina, se podría conseguir una reducción de la HbA1c del 1,9% cambiando a esta terapia. El ajuste regular de la dosis (una o dos veces por semana) en función de los niveles matinales de glucosa en sangre es crucial para el éxito del tratamiento [17].
Conclusión
Los nuevos fármacos antidiabéticos abren nuevas opciones de tratamiento para los pacientes cuya diabetes no se controla suficientemente con metformina o con una combinación de dos fármacos. Los inhibidores del SGLT2, en particular, pueden combinarse con todos los medicamentos hipoglucemiantes debido a su mecanismo de acción especial. Con terapias combinadas, se puede conseguir una reducción muy potente de la HbA1c(>1,5%). Todavía no se ha demostrado que ninguno de los nuevos grupos de sustancias conlleve una reducción de las complicaciones microvasculares y/o macrovasculares. Los estudios a largo plazo demuestran la seguridad cardiovascular de las gliptinas.
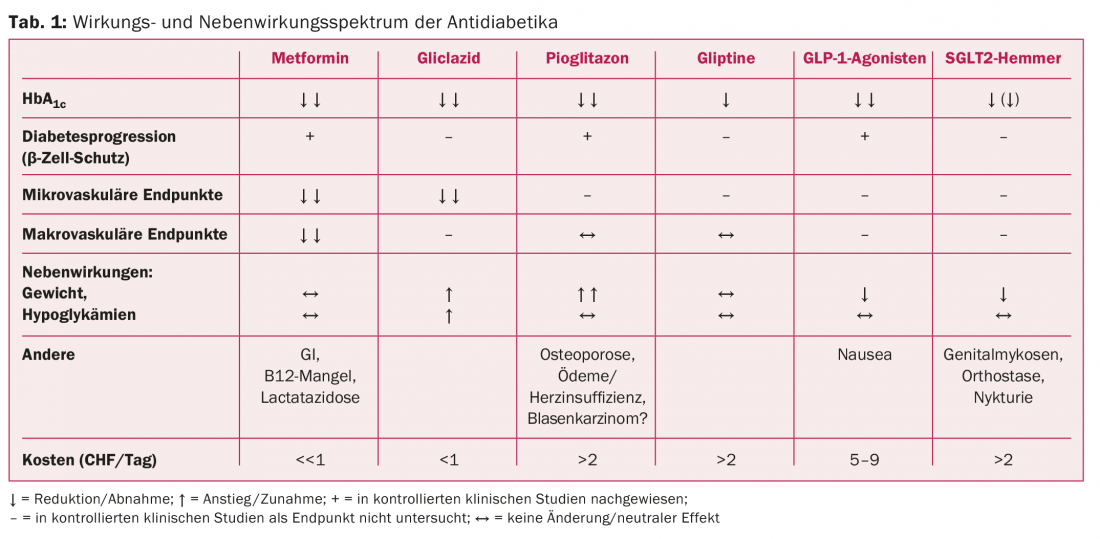
La tabla 1 muestra el espectro de efectos y efectos secundarios de los fármacos antidiabéticos.
Literatura:
- Asociación Americana de Diabetes, Declaración de posición de la ADA 2015: 7. Enfoques del tratamiento glucémico. Diabetes Care 2015 Ene 1; 38(Suplemento 1): S41-48.
- Inzucchi SE, et al: Metformina en pacientes con diabetes tipo 2 y enfermedad renal: una revisión sistemática. JAMA 2014 dic 24; 312(24): 2668.
- Sociedad Suiza de Endocrinología y Diabetología: Metformina y medios de contraste roentgen que contienen yodo [Internet]. Directrices. 2014 [cited 2015 Jul 29]. Disponible en: www.sgedssed.ch/fileadmin/files/news/Metformin_und_jodhaltige_Roentgenkontrastmittel.pdf
- Simpson SH, et al: Riesgo de mortalidad entre las sulfonilureas: una revisión sistemática y un metaanálisis en red. Lancet Diabetes Endocrinol 2015 Ene; 3(1): 43-51.
- Grupo de colaboración ADVANCE, Patel A, et al: Control intensivo de la glucemia y resultados vasculares en pacientes con diabetes tipo 2. N Engl J Med 2008 Jun 12; 358(24): 2560-2572.
- Soccio RE, Chen ER, Lazar MA: Las tiazolidinedionas y la promesa de la sensibilización a la insulina en la diabetes de tipo 2. Cell Metab 2014 Oct 7; 20(4): 573-591.
- Lewis JD, et al: Uso de pioglitazona y riesgo de cáncer de vejiga y otros cánceres comunes en personas con diabetes. JAMA 2015 Jul 21; 314(3): 265-277.
- Tahrani AA, Barnett AH, Bailey CJ: Inhibidores de SGLT en el tratamiento de la diabetes. Lancet Diabetes Endocrinol 2013; 1(2): 140-151.
- Vasilakou D, et al: Inhibidores del cotransportador 2 de sodio-glucosa para la diabetes tipo 2: revisión sistemática y metaanálisis. Ann Intern Med 2013 Ago 20; 159(4): 262-274.
- Peters AL, et al: Cetoacidosis diabética euglucémica: una complicación potencial del tratamiento con inhibición del cotransportador 2 de sodio y glucosa. Diabetes Care 2015 Jun 15; dc150843 (Epub ahead of print).
- Rosenstock J, et al: Terapia dual de adición en la diabetes tipo 2 mal controlada con monoterapia de metformina: un ensayo aleatorizado doble ciego de adición de saxagliptina más dapagliflozina frente a la adición única de saxagliptina o dapagliflozina a la metformina. Diabetes Care 2015 Mar; 38(3): 376-383.
- Karagiannis T, et al: Inhibidores de la dipeptidil peptidasa-4 para el tratamiento de la diabetes mellitus tipo 2 en el ámbito clínico: revisión sistemática y metaanálisis. BMJ 2012; 344: e1369.
- Scirica BM, et al: Saxagliptina y resultados cardiovasculares en pacientes con diabetes mellitus tipo 2. N Engl J Med 2013 Oct 3; 369(14): 1317-1326.
- Zannad F, et al: Resultados de insuficiencia cardiaca y mortalidad en pacientes con diabetes tipo 2 que toman alogliptina frente a placebo en EXAMINE: un ensayo multicéntrico, aleatorizado y doble ciego. Lancet 2015 23 de mayo; 385(9982): 2067-2076.
- Green JB, et al: Efecto de la sitagliptina sobre los resultados cardiovasculares en la diabetes tipo 2. N Engl J Med 2015 Jul 16; 373(3): 232-242.
- Meier JJ: Agonistas del receptor de GLP-1 para el tratamiento individualizado de la diabetes mellitus tipo 2. Nat Rev Endocrinol 2012 dic; 8(12): 728-742.
- Buse JB, et al: Contribución de la liraglutida en la combinación de relación fija de insulina degludec y liraglutida (IDegLira). Diabetes Care 2014 Nov; 37(11): 2926-2933.
CARDIOVASC 2015; 14(4): 4-8











