El principal problema de la angioplastia es la estenosis recurrente, un gran porcentaje de la cual se debe al desarrollo de hiperplasia neointimal (HIN). Esto puede suprimirse eficazmente aplicando fármacos antiproliferativos a los stents y balones. Los estudios iniciales sobre el tema muestran resultados alentadores, y se espera que nuevos ensayos aleatorios proporcionen más información sobre los posibles efectos secundarios, la selección de pacientes y también sobre la relación coste-beneficio.
Numerosos estudios epidemiológicos que utilizan técnicas de exploración objetivas muestran una prevalencia de la enfermedad arterial periférica (EAP) del 3-10% y del 15-20% a partir de los 70 años. Clínicamente, la PAOD se presenta por etapas, desde pacientes asintomáticos hasta la isquemia crítica de las extremidades (ICM). Tras el diagnóstico de CLI, el 30% de los pacientes sufre una amputación en el primer año, el 20% tiene dolor persistente y ulceración [1]. La tasa de mortalidad a un año en este caso es del 20%, siendo los eventos cardiacos y cerebrales los que dominan el destino de los pacientes. La revascularización es, por tanto, un objetivo terapéutico primordial. El éxito técnico de la angioplastia transluminal percutánea (ATP) suele ser muy elevado. Para acontecimientos agudos como las disecciones que limitan el flujo y el “retroceso elástico” de la arteria, la endoprótesis ofrece una solución mecánica en el sentido de un soporte del vaso. El principal problema del método es la aparición de estenosis recurrentes, que se dan en un 30-50%/año dependiendo de la longitud y la localización de la lesión. La principal causa de estenosis recurrente es el desarrollo de hiperplasia neointimal (HIN). Esto puede suprimirse eficazmente mediante la aplicación tópica de fármacos antiproliferativos. En la angioplastia coronaria percutánea, este concepto se aplica con éxito desde hace casi una década y está ampliamente respaldado por varios ensayos aleatorizados. En cambio, las pruebas de este método en la zona de flujo periférico son significativamente inferiores. Ya se publicó un artículo de revisión sobre el tema en VASA 02/2012 [2]. A continuación se añaden los resultados del estudio actual.
Estenosis recurrente tras angioplastia
La NIH es el resultado de una cascada vasoproliferativa que comienza en un traumatismo vascular por ATP con daño endotelial y activación plaquetaria. Los complejos mecanismos bioquímicos implicados en el desarrollo de los NIH aún no se comprenden del todo. Acontecimientos secundarios como el estrés oxidativo y la inflamación provocan la expresión de diversas metaloproteinasas de la matriz (MMP) a través de un aumento de los radicales libres, que contribuyen a la degradación del colágeno y la elastina de la pared arterial y permiten así la migración de las células hacia la íntima vascular. El paradigma de que estas células son únicamente células musculares lisas vasculares que han perdido la expresión de desmina y la contractilidad y ahora expresan vimentina ha sido cuestionado por investigaciones de varios grupos. Se ha demostrado que tras una angioplastia coronaria o una cirugía de bypass, los fibroblastos también migran desde la adventicia a través de la media hacia la íntima y adquieren la expresión de SMA (“actina de músculo liso”) y se transforman así en miofibroblastos [3–5]. Tras la ATP de las derivaciones de diálisis, también se detectaron células musculares lisas y células endoteliales derivadas de células madre circulantes procedentes de la médula ósea [6]. Desde el punto de vista terapéutico, se está creando aquí una base prometedora para nuevos enfoques terapéuticos.
Una vez en la íntima vascular, los miofibroblastos proliferan y sintetizan proteínas de la matriz extracelular. Este proceso suele terminar unos tres o cuatro meses después del traumatismo vascular en una capa celular neointimal que, dependiendo de su grosor, puede constreñir la luz del vaso hasta tal punto que se produzca una estenosis recurrente. La aplicación de fármacos inhibidores del ciclo celular antiproliferativo en balones y stents (paclitaxel, sirolimus, everolimus) suprime eficazmente la formación de la capa neointimal. La administración tópica permite altas concentraciones locales del fármaco sin causar potencialmente efectos secundarios sistémicos.
El sirolimus (rapamicina) es un macrólido natural con efectos inmunosupresores. Es capaz de aumentar la concentración de la proteína inhibidora del ciclo celular p27, que inhibe la transición de la fase G1 a la fase S de la célula. El everolimus, que es un derivado del sirolimus, tiene el mismo mecanismo de acción. La sustancia activa Paclitaxel (PTX) se aisló originalmente de la corteza del tejo del Pacífico (Taxus brevifolia). Recientemente, se puede sintetizar parcialmente a partir del tejo europeo. El paclitaxel se une irreversiblemente a la beta-tubulina e impide así la degradación de los microtúbulos, por lo que la célula ya no puede dividirse mitóticamente. El paclitaxel es altamente lipofílico, por lo que se absorbe rápidamente en la pared vascular.
Situación del estudio
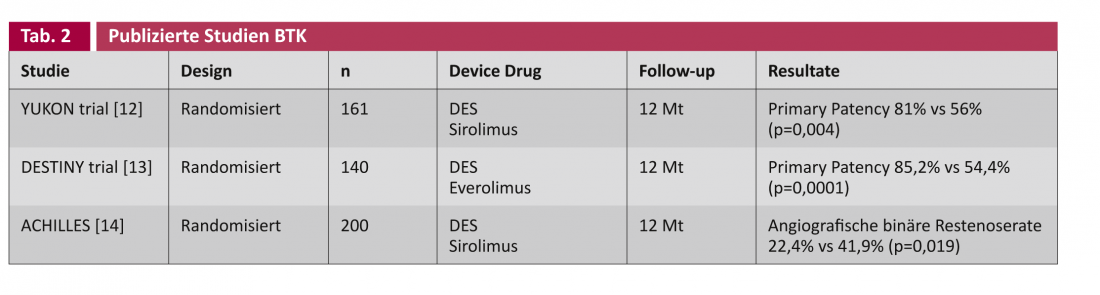
En los estudios sobre los stents liberadores de fármacos (DES) y los balones recubiertos de fármacos (DCB), se hace una distinción general entre las aplicaciones en las arterias femoropoplíteas (tabla 1) y en las correspondientes arterias más estrechas por debajo de la rodilla (BTK) (tabla 2).
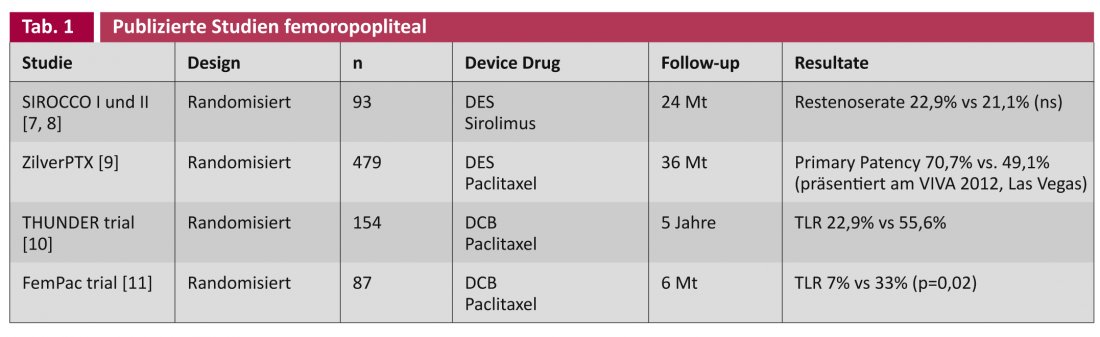
Los estudios SIROCCO se realizaron en 2002 y 2002 respectivamente. En 2006, se comparó aleatoriamente un stent liberador de sirolimus frente al mismo stent sin recubrimiento en el tratamiento de la arteria femoral superficial [7, 8]. Después de dos años, no se encontraron diferencias en la aparición de estenosis recurrentes, posiblemente debido a que la concentración de sirolimus era demasiado baja (90 μg/cm2). El reciente estudio prospectivo, aleatorizado y multicéntrico sobre el stent ZilverPTX® comparó un stent de nitinol liberador de paclitaxel (3 μg/mm2) con la angioplastia simple con balón (POBA) y el mismo stent metálico sin recubrimiento (BMS) en 479 pacientes. El estudio se diseñó para cinco años, y los resultados provisionales se comunicaban continuamente en los congresos: Actualmente, después de tres años, el stent recubierto muestra una clara superioridad estadísticamente significativa en permeabilidad primaria (= “ausencia angiográfica o dúplex ecográfica de estenosis recurrente”) del 70,7% frente al 49,1% (presentado en VIVA 2012, Las Vegas).
En principio, en el tratamiento de lesiones vasculares es deseable que no haya que dejar ningún material extraño, como un stent. El concepto DCB tiene esto en cuenta. En el ensayo THUNDER, existe una ventaja significativa para la DCB con respecto a la tasa de reintervención (“revascularización de la lesión diana”, TLR) incluso después de cinco años, aunque sólo con lesiones vasculares cortas (Curso de Intervencionismo de Leipzig 2012). La cuestión clave sigue siendo si también hay un lugar para el DCB en las lesiones largas y muy calcificadas. Están en marcha estudios que investigan la BCD junto con otras tecnologías como la aterectomía, así como toda una serie de estudios sobre la BCD en uso primario (Tab. 3).
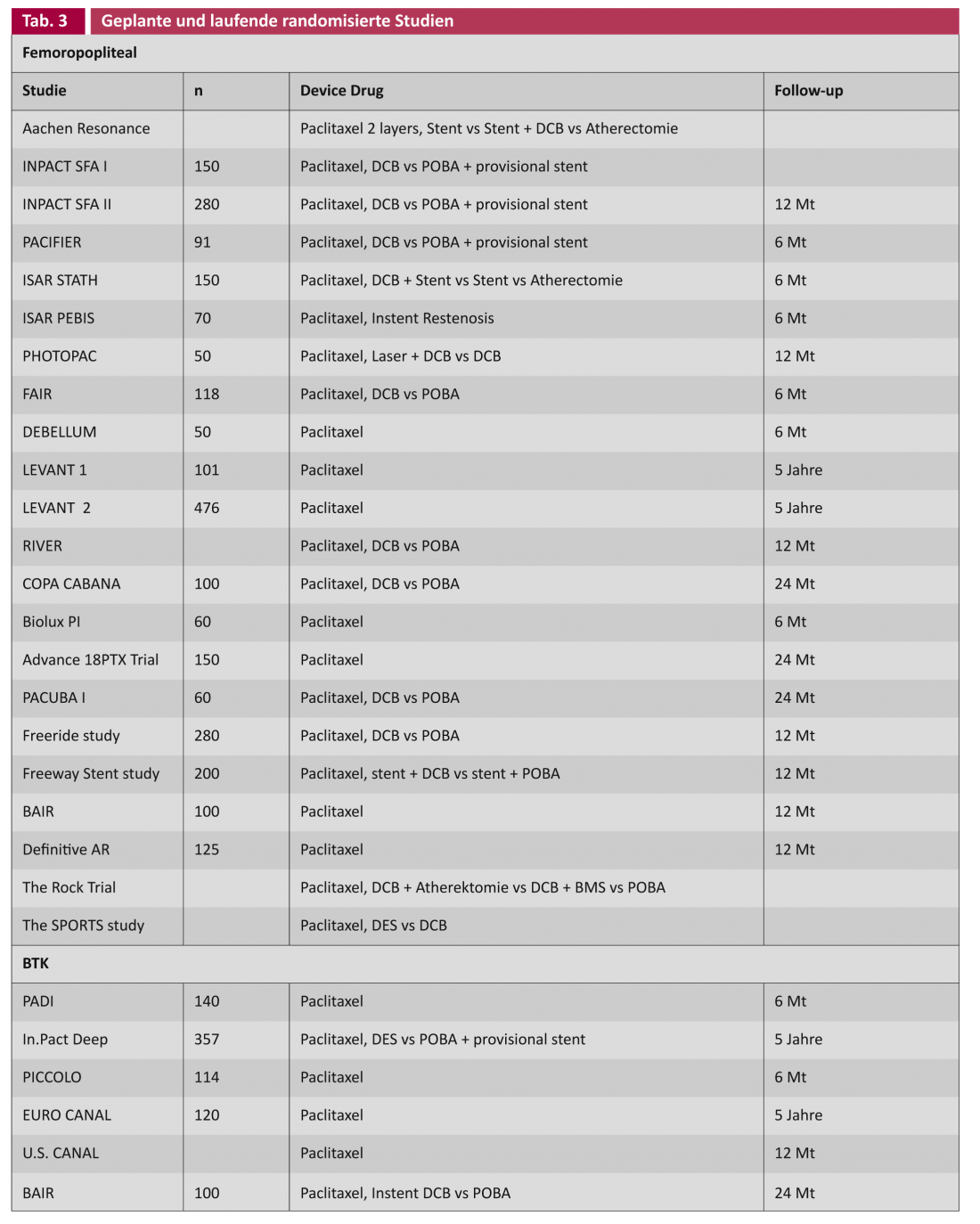
El uso de la tecnología de liberación de fármacos en el segmento arterial infrapoplíteo requiere una consideración aparte. Los pacientes con isquemia crítica de las extremidades suelen presentar obstrucciones múltiples de las arterias de la parte inferior de la pierna, como ocurre en los diabéticos y en los pacientes con insuficiencia renal grave. Asegurando al menos un vaso abierto al pie (“flujo en línea recta”), debería mejorarse la cicatrización de la herida y reducirse la tasa de amputaciones. Sin embargo, la angioplastia sólo en las arterias de la parte inferior de la pierna produce a menudo un resultado de dilatación insuficientemente bueno, entre otras cosas por la longitud de las oclusiones de los vasos. La disección y el retroceso suelen producirse aquí, lo que puede provocar una oclusión precoz en las arterias de calibre fino.
Scheinert et al. fueron los primeros en insertar un stent coronario liberador de fármacos por vía infrapoplítea en 30 pacientes en 2006. Después de seis meses, no se encontró ni una sola estenosis recurrente [15]. El ensayo YUKON-BTK lo aleatorizó a un stent liberador de sirolimus y también halló una superioridad estadísticamente significativa del DES en permeabilidad primaria (81% frente a 56%, p=0,004) [12]. Otros ensayos aleatorizados publicados sobre el tema incluyen DESTINY [8] y ACHILLES [14], que también encuentran esta paternidad primaria estadísticamente significativa mejor para el DES.
Sin embargo, en lo que respecta a los importantes criterios clínicos de valoración de la amputación y la muerte, la tecnología aún no aporta ninguna ventaja demostrable, como Rastan et al. en una revisión de los datos agrupados de 1039 pacientes de los estudios mencionados [16].
Debate
Además de los estudios aleatorizados enumerados anteriormente, existe toda una serie de datos de registro [2]. La interpretación de los resultados sugiere que el recubrimiento con fármacos, análogo a la angioplastia coronaria, es un método prometedor en el tratamiento de la PAVK. Cada vez hay más pruebas de que la tasa de estenosis recurrente, y por tanto potencialmente de reintervenciones, puede reducirse tanto femoropoplíteamente como infrapoplíteamente. Sin embargo, es prematuro formular un patrón oro a partir de esto, sobre todo porque los estudios aleatorizados con los criterios de inclusión no siempre reflejan las condiciones cotidianas habituales. Los resultados de los grandes estudios en curso proporcionarán más información sobre los posibles efectos secundarios, sobre la selección adecuada de los pacientes y también sobre la relación coste-beneficio (Tab. 3). Este último requiere una atención especial, ya que se espera que la reducción potencial de la tasa de reintervención conlleve una reducción de los costes, como se ha demostrado comparativamente en los estudios de cardiología mediante el uso de SLF. [17].
No existen datos prospectivos aleatorizados sobre el postratamiento con antiagregación dual. Según el consenso suizo, la antiagregación dual se lleva a cabo generalmente durante un mes tras la implantación periférica del BMS [18]. Debido al retraso en la reendotelización tras la implantación de DES/DCB, ésta se lleva a cabo durante más tiempo, de forma análoga a la cardiología. En los estudios citados, fue de entre uno y seis meses, dependiendo de la región vascular tratada.
Literatura:
- Norgren L, et al; grupo de trabajo TASC II: J Vasc Surg 2007; 45 Suppl: S5-67.
- Buechel R, Stirnimann A, Zimmer R, Keo H, Groechenig E: VASA 2012; 41(4): 248-261.
- Scott NA, et al: Circulation 1996; 93(12): 2178-2187.
- Shi Y, et al: Circulation 1996; 94(7): 1655-1664.
- Shi Y, et al: Circulation 1997; 95(12): 2684-2693.
- Sata M, et al: Nat Med 2002; 8(4): 403-409.
- Duda SH, et al: Circulation 2002; 106(12): 1505-1509.
- Duda SH, et al: J Endovasc Ther 2006; 13(6): 701-710.
- Dake MD, et al; en nombre de los investigadores de Zilver PTX: Circ Cardiovasc Intervent 2011; 4(5): 495-504.
- Tepe G, et al: NEJM 2008; 358(7): 689-699.
- Werk M, et al: Circulation 2008; 118(13): 1358-1365.
- Rastan A, et al: Eur Heart J 2011; 32: 2274-2281.
- Bosiers M, et al: J Vasc Surg 2012; 55(2): 390-398.
- Scheinert D, et al; ACHILLES Investigators: J Am Coll Cardiol 2012; 60(22): 2290-2295.
- Scheinert D, et al: EuroIntervention 2006; 2(2): 169-174.
- Rastan A, Noory E, Zeller T: Vasa 2012; 2: 90-95.
- Filion KB, et al: Am J Cardiol 2009; 103(3): 338-344.
- Jäger K, et al: Schweiz Med Forum 2009; 9(39): 690.
CARDIOVASC 2013; 12(1), 15-19