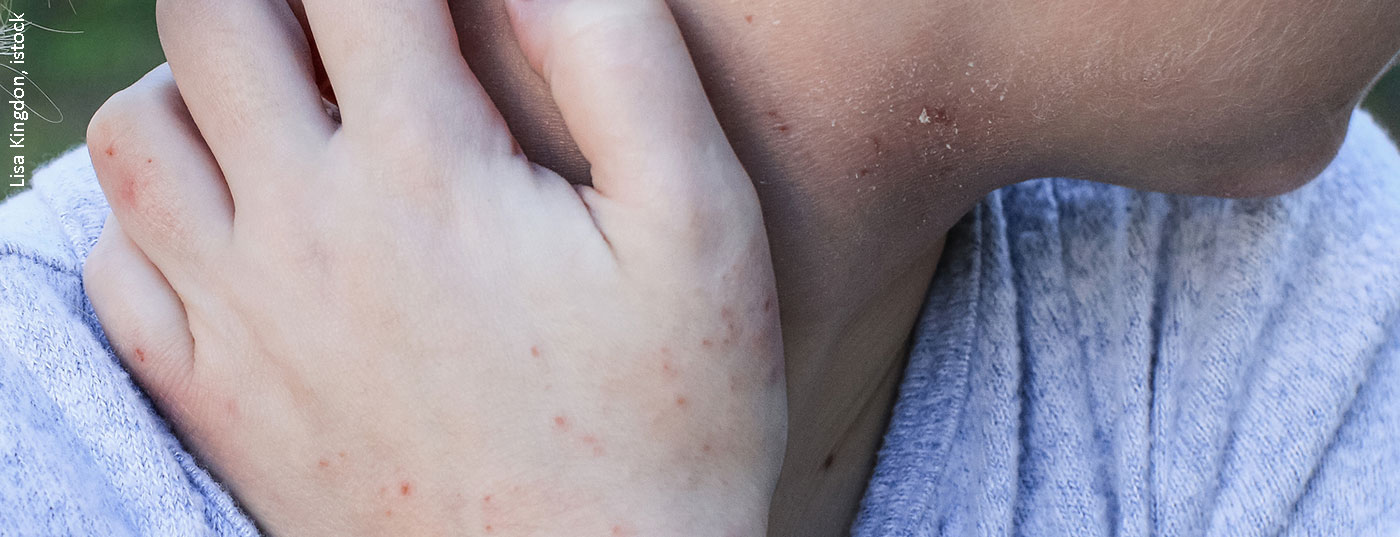
El eccema es la enfermedad cutánea más común que se observa en la práctica general y es uno de los síntomas típicos de la dermatitis atópica. Una barrera cutánea alterada es común a todos los eccemas y se ve influida favorablemente por una terapia básica coherente.
Lo característico de esta enfermedad cutánea crónica recurrente es una piel sensible muy seca y picores de gravedad variable. El curso de la dermatitis atópica (también: neurodermatitis) se caracteriza por episodios de duración y gravedad variables. El cuadro clínico es individualmente diferente y varía en función de la fase (aguda o de intervalo), la edad y otros factores [1]. Los lugares de predilección del eccema atópico en adultos son las grandes curvas, aunque las alteraciones cutáneas también pueden producirse en otras partes del cuerpo (por ejemplo, manos, cara). En los lactantes, se ven afectados principalmente la cara, el cuero cabelludo (“costra láctea”) y los lados extensores de las extremidades; en los niños, el eccema tiende a aparecer en los lados flexores de los brazos y las piernas y en las muñecas y los tobillos. Aproximadamente un tercio de los afectados por dermatitis atópica en la infancia también padecen eccema atópico en la edad adulta. Las causas son multifactoriales. Además de la predisposición genética, numerosos factores desencadenantes también intervienen en la manifestación inicial de la enfermedad y son muchos los posibles desencadenantes de la aparición de los episodios de la enfermedad.
Un pilar importante de la terapia en todas las fases
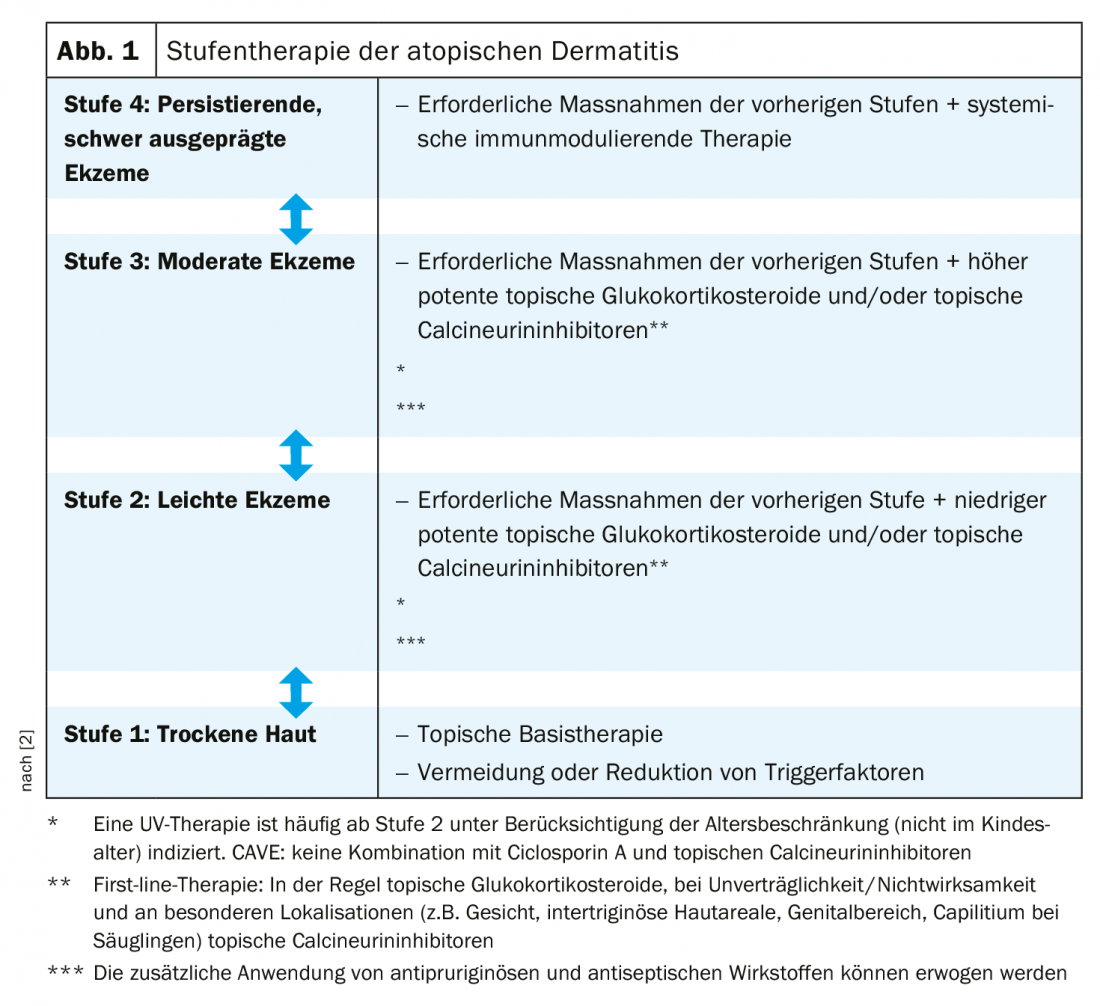
El tratamiento de la dermatitis atópica sigue siendo un reto. La terapia debe adaptarse individualmente a las distintas fases, gravedad y cronicidad. Siguiendo a los comités internacionales, la directriz actual de la AWMF recomienda una terapia escalonada (Fig. 1) [2]. Este esquema de tratamiento aproximado debe adaptarse en función de la edad, el curso, la localización y el sufrimiento del paciente. La terapia básica es un pilar en el tratamiento de la dermatitis atópica y está indicada en todos los estadios, independientemente de la gravedad de la enfermedad [3]. Así pues, unos cuidados básicos constantes contribuyen decisivamente a restaurar la función de barrera alterada, a reducir la xerosis y el picor. En el tratamiento a largo plazo de la enfermedad, una terapia básica constante puede conducir a un intervalo prolongado libre de recidivas [3]. La elección de los preparados tópicos debe adaptarse a la fase de la enfermedad o al estado actual de la piel y lo ideal es aplicarlos dos veces al día en todo el tegumento [3]. Los cambios en los lípidos de barrera y en el complejo de diferenciación epidérmica están determinados en gran medida genéticamente, por lo que es aconsejable un tratamiento de por vida.
Beneficio relevante para el curso
Para una terapia básica óptima, pueden aplicarse diferentes sustancias activas en combinación. La urea es el principio activo más utilizado y un componente del factor hidratante natural (FHN) de la epidermis [4]. Se ha demostrado que la aplicación tópica de un externum que contenga entre un 5 y un 10% de urea provoca la hidratación del estrato córneo y una reducción del SCORAD [5,6]. Los estudios in vitro también han demostrado que la urea reduce la proliferación de la epidermis e induce una mayor síntesis de lípidos de barrera y péptidos antimicrobianos. La regulación de la expresión de genes implicados en la diferenciación de los queratinocitos (TG-1, involucrina, loricrina, filagrina) y en la síntesis de péptidos antimicrobianos (LL-37, β-defensina-2), así como de lípidos relevantes para la barrera, desempeña un papel importante [7]. En este contexto, se supone que la urea como componente de la terapia básica influye positivamente en la función de los queratinocitos y en la síntesis de los lípidos de barrera [7]. Se ha demostrado empíricamente que el uso de preparados tópicos que contienen urea puede prolongar significativamente el intervalo libre de recaídas de la dermatitis atópica [8]. Además de la urea, la glicerina y las ceramidas son sustancias de eficacia probada en las formulaciones externas de productos para la terapia básica [9,10]. El glicerol favorece la hidratación del estrato córneo y las ceramidas son lípidos esenciales del estrato córneo, que se reducen en pacientes con dermatitis atópica [9,10].
Literatura:
- Werfel T, et al: El diagnóstico y la terapia graduada de la dermatitis atópica. Dtsch Arztebl Int 2014; 111: 509-520.
- AWMF: Directriz Neurodermatitis, Número de registro 013 – 027, ClasificaciónS2k Estado: 31.03.2015 (en revisión), válido hasta el 30.03.2020 www.awmf.org/uploads/tx_szleitlinien/013-027l_S2k_Neurodermitis_2016-06-verlaengert.pdf
- Chylla R, Schnopp C, Volz T: Terapia básica para la dermatitis atópica – nueva y probada. JDDG 2018; 16(8): 976-979. DOI: 10.1111/ddg.13594
- Rawlings AV, Harding CR: Hidratación y función de barrera de la piel. Dermatol Ther 2004; 17 (Suppl 1): 43-48.
- Bissonnette R, et al: Estudio doble ciego de tolerancia y eficacia de una nueva crema hidratante con urea en pacientes con dermatitis atópica. J Cosmet Dermatol 2010; 9: 16-21.
- Loden M, Andersson AC, Lindberg M: Mejora de la función de barrera de la piel en pacientes con dermatitis atópica tras el tratamiento con una crema hidratante (Canoderm). Br J Dermatol 1999; 140: 264-267.
- Grether-Beck S, et al.: La captación de urea mejora la función de barrera y la defensa antimicrobiana en humanos mediante la regulación de la expresión génica epidérmica. J Invest Dermatol 2012; 132: 1561-1572.
- Akerström U, et al. Comparación de cremas hidratantes para la prevención de la recaída de la dermatitis atópica: un ensayo clínico multicéntrico aleatorizado, doble ciego y controlado. Acta Derm Venereol 2015; 95: 587-592.
- Lindh JD, Bradley M: Eficacia clínica de las cremas hidratantes en la dermatitis atópica y trastornos relacionados: una revisión sistemática. Am J Clin Dermatol 2015; 16: 341-359.
- Di Nardo A, et al: Composición de ceramidas y colesterol de la piel de pacientes con dermatitis atópica. Acta Derm Venereol 1998; 78: 27-30.
PRÁCTICA GP 2020; 15(2): 16