Hay 400 millones de enfermos de EPOC en todo el mundo. Es la cuarta causa de mortalidad mundial. En el Internal Medicine Update Refresher 2017 de Zúrich se presentaron los últimos hallazgos para el diagnóstico y la terapia basados en la evidencia.
Hay 400 millones de enfermos de EPOC en todo el mundo. Es la cuarta causa de mortalidad mundial [1]. En Suiza hay 300.000 personas afectadas, con una prevalencia del 2,5% en personas de 30 a 39 años y del 8% en >personas de 70 años. Además de fumar tabaco, los factores de riesgo incluyen la exposición a partículas de polvo (por ejemplo, en la agricultura) y la exposición a partículas de humo de estufas de leña. Para un tratamiento lo más específico posible, adaptado a las necesidades individuales, las directrices diagnósticas y terapéuticas se han adaptado al estado actual de la investigación. La importancia de los broncodilatadores (LAMA = anticolinérgicos de acción prolongada/LABA = agonistas β-2 de acción prolongada) ha aumentado considerablemente en los últimos años, mientras que los esteroides inhalados (CSI) se utilizan con menos frecuencia que antes, informó el Dr. Robert Thurnheer, Jefe de Diagnóstico Médico del Hospital Cantonal de Münsterlingen.
Fenotipado según la Iniciativa Global para la Enfermedad Pulmonar Obstructiva Crónica (GOLD)
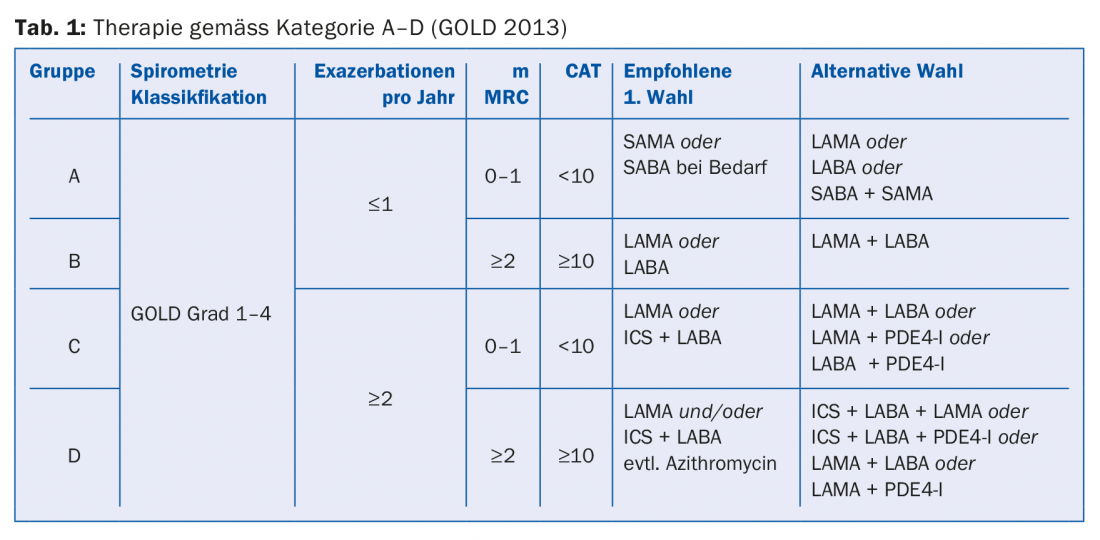
La clasificación A-D actualmente vigente (tab. 1) ya no se basa en la función pulmonar, sino en los síntomas y el riesgo de exacerbación, y sirve de base para una terapia basada en pruebas. Los cuestionarios “CAT” (Prueba de evaluación de la EPOC) y “mMRC” (Detección de la disnea) se utilizan como herramientas de diagnóstico. Para los pacientes del grupo A (pocos síntomas, sin exacerbaciones), puede utilizarse un broncodilatador (LABA o LAMA). En los pacientes del grupo B (síntomas pero sin exacerbaciones), también debe utilizarse un broncodilatador. Si los síntomas persisten, cambie a un preparado combinado (Anoro® o Spiolto® o Ultibro®). Si las exacerbaciones son más frecuentes, se recomienda la combinación con un esteroide inhalado (ICS) según las directrices GOLD. En los pacientes del grupo C (exacerbaciones), la primera elección es la monoterapia con LAMA. Si las exacerbaciones continúan, cambie a una terapia combinada: LABA y LAMA o LABA e ICS. La terapia del grupo D también puede llevarse a cabo según un esquema graduado (Tab. 1), en el que el profesor Thurnheer aconseja precaución respecto al uso profiláctico de macrólidos debido a los riesgos de efectos secundarios (por ejemplo, pérdida auditiva neurosensorial, síndromes de QT largo, resistencias, falta de datos a largo plazo).
Broncodilatación: ¿Cuál es el beneficio terapéutico y cómo conseguir los mejores efectos?
En resumen, los siguientes argumentos respaldan la eficacia de la broncodilatación (LAMA, LABA): mejora de la función pulmonar [2], disminución de la hiperinsuflación [3], mejora de los síntomas [4], disminución de la tasa de exacerbaciones [4]. Para los grupos A y B, no importa si se utiliza primero LABA o LAMA. Para los grupos C y D se recomienda utilizar primero LAMA. En el estudio POET, el LAMA (Spiriva®) fue superior al salmeterol (Serevent®) en la prevención de las exacerbaciones [5].
Según los nuevos hallazgos, iniciar la terapia lo antes posible (es decir, en el estadio funcional pulmonar 2 = objetivo de FEV1 50-80%) tiene un efecto positivo; por ejemplo, los estudios han demostrado que el uso de tiotropio (Spiriva®) la disminución del FEV1 (Volumen Espiratorio Forzado en el primer segundo de espiración) después de dos años es menos pronunciada que en la condición placebo [6] y los pacientes también se ven menos afectados por la “hiperinflación” (sobreinflación dinámica) en una fase temprana durante el ejercicio.
Varios estudios clínicos [7,8] han demostrado que los preparados combinados de LAMA y LABA (Anoro®, Spiolto®, Ultibro®) son superiores a la monoterapia (LAMA o LABA) con respecto a los siguientes objetivos: mejor función pulmonar, menos síntomas, reducción de la tasa de exacerbaciones. En el estudio SPARK, por ejemplo, se demostró que Ultibro® lograba mejores efectos que los respectivos agentes únicos [7]. El uso de un fármaco combinado se recomienda principalmente a los pacientes con EPOC con una respuesta insuficiente a la monoterapia a dosis bajas con LAMA o LABA [9] y a los pacientes con EPOC grave y síntomas de disnea [10,11].
Según el compendio, siempre debe realizarse primero una monoterapia y sólo debe utilizarse un preparado combinado si hay falta de efecto, pero según las directrices, también se permite un tratamiento primario con un preparado combinado. Además de la eficacia, la manipulación también puede influir en la decisión sobre cuál de los tres preparados combinados (Anoro®, Ultibro®, Spiolto®) se utiliza.
Corticosteroides inhalados (CSI): controversia sobre el beneficio terapéutico
A diferencia del asma, donde los esteroides inhalados (CSI) son el tratamiento básico, el uso de CSI en la EPOC es controvertido.
En el estudio FLAME [12], los broncodilatadores combinados (LABA+LAMA) lograron una reducción significativamente mayor de las exacerbaciones en comparación con LABA+ICS. En el estudio WISDOM [8], la omisión de los CSI no aumentó la frecuencia de las exacerbaciones, aunque los pacientes sin CSI mostraron un empeoramiento de los valores de FEV1 a largo plazo [8]. En un subgrupo de pacientes con EPOC con eosinofilia (>2% de eosinofilia en sangre) y mayor riesgo de exacerbación, los CSI redujeron la tasa de exacerbación [13,14]. Según el estudio SUMMIT (n=16 485, 43 países), el uso de CSI en pacientes con EPOC con mayor riesgo cardiovascular no redujo la mortalidad, pero redujo ligeramente la tasa de deterioro de la función pulmonar [15].
Los efectos del uso combinado de broncodilatadores y CSI (“terapia triple”) pueden resumirse como sigue según la investigación actual [16]: ningún efecto sobre la mortalidad y los criterios de valoración cardiovasculares, apenas ningún efecto sobre la función pulmonar, cierta reducción de las exacerbaciones [17,18], pero un número significativamente mayor de neumonías (efecto secundario de los CSI).
Terapia de la EPOC avanzada: “rasgos tratables” y medidas conductuales
El preparado Prolastin® puede utilizarse como sustituto en caso de deficiencia de α-1-antitripsina (inhibidor de la proteasa), por lo que hasta ahora sólo se han demostrado efectos positivos para los criterios estructurales pulmonares. Daxas® (principio activo: roflumilast) produce una ligera mejoría de la función pulmonar y una disminución ligeramente significativa de la tasa de exacerbaciones, aunque también pueden aparecer efectos secundarios: Pérdida de peso, mayor riesgo de trastornos del sueño, cambios de humor [19]. El mepolizumab (por ejemplo, Nucala®) ya se utiliza con éxito para los asmáticos con eosinofilia y también pueden conseguirse efectos positivos en la EPOC y la eosinofilia en lo que respecta a la reducción de la tasa de exacerbaciones, aunque actualmente el preparado aún no está aprobado para pacientes con EPOC para esta indicación [20].
En cuanto a la oxigenoterapia en la hipoxemia grave, el profesor Thurnheer mencionó que una ventaja en la supervivencia sólo llega a ser significativa tras unos cuatro años de terapia y que no se demostraron efectos con sólo una hipoxemia leve en lo que respecta a la calidad de vida subjetiva, el riesgo de hospitalización y la exacerbación [21].
En cuanto a las medidas médicas conductuales, la fisioterapia y el asesoramiento nutricional (a menudo desnutrición calórica debida al enfisema y al desgaste muscular) han demostrado su eficacia, además del apoyo para dejar de fumar. En caso de exacerbaciones, se recomienda crear un plan de acción. Por ejemplo, los esteroides sistémicos (cinco dosis diarias de 40 mg cada una) [22] deben tomarse cuando se viaja y los antibióticos (por ejemplo, co-amoxicilina, tetraciclina, etc.) deben mantenerse en reserva en caso de síntomas bronquiales. Otras medidas mencionadas son el control de la técnica de inhalación, la vacunación anual contra la gripe y la vacunación antineumocócica única (Prevenar-13® en niños).
Fuente: Actualización en Medicina Interna, 5-9 de diciembre de 2017, Zúrich
Literatura:
- Bridevaux P-O, et al: Prevalencia de la obstrucción al flujo aéreo en fumadores y nunca fumadores en Suiza. Revista Respiratoria Europea 2010; 36: 1259-1269.
- Tashkin DP, et al: Capacidad de respuesta a los broncodilatadores en pacientes con EPOC. Revista Respiratoria Europea 2008; 31: 742-750.
- Dellaca RL, et al: Efecto de la broncodilatación sobre la limitación del flujo espiratorio y la mecánica pulmonar en reposo en la EPOC. Revista Respiratoria Europea 2009; 33: 1329-1337.
- Jones PW, et al: Correlación de los cambios en la función pulmonar con los resultados de los pacientes en la enfermedad pulmonar obstructiva crónica: un análisis agrupado. Respir Res 2011; 12: 161.
- Vogelmeier C, et al: Tiotropio frente a salmeterol para la prevención de las exacerbaciones de la EPOC (POET). N Engl J Med 2011; 364: 1093-1103.
- Zhou Y, et al: Tiotropio en la enfermedad pulmonar obstructiva crónica en fase inicial. N Engl J Med 2017; 377: 923-935.
- Wedzicha JA, et al: Análisis de las exacerbaciones de la enfermedad pulmonar obstructiva crónica con el broncodilatador dual QVA149 en comparación con el glicopirronio y el tiotropio (SPARK): un estudio aleatorizado, doble ciego y de grupos paralelos. Lancet Respir Med 2013; 1: 199-209.
- Magnussen H, et al: Retirada de los glucocorticoides inhalados y exacerbaciones de la EPOC. N Eng J Med 2014; 371: 1285-1294.
- Donohue JF, et al: Eficacia y seguridad del umeclidinio/vilanterol 62,5/25 mcg una vez al día en la EPOC. Respir Med 2013; 107(10): 1538-1546.
- Kessler R, et al: Variabilidad de los síntomas en pacientes con EPOC grave; un estudio transversal paneuropeo. Eur Respir J 2011; 37: 264-272.
- Price D, et al: Impacto de los síntomas nocturnos en la EPOC, un estudio del mundo real en cinco países europeos. Int J Chron Obstruct Pulmon Dis 2013; 8: 595-603.
- Wedzicha JA, et al: Indacaterol-glicopirronio frente a salmeterol-fluticasona para la EPOC. N Engl J Med 2016; 374(23): 2222-2234.
- Vedel-Krogh S, et al: Eosinófilos en sangre y exacerbaciones en la enfermedad pulmonar obstructiva crónica. Estudio de la población general de Copenhague. AJRCCM 2016; 93(9): 965-974.
- Pascoe S, et al: Recuento de eosinófilos en sangre, exacerbaciones y respuesta a la adición de furoato de fluticasona inhalado al vilanterol en pacientes con enfermedad pulmonar obstructiva crónica: un análisis secundario de los datos de dos ensayos controlados aleatorios paralelos. Lancet Respir Med 2015; 3: 435-442.
- Vestbo J, et al: Fluticasone furoate and vilanterol and survival in chronic obstructive pulmonary disease with increased cardiovascular risk (SUMMIT): a double-blind randomised controlled trial. Lancet 2016; 387: 1817-1826.
- Vogelmeier CF, et al: Estrategia mundial para el diagnóstico, tratamiento y prevención de las enfermedades pulmonares crónicas y obstructivas Informe 2017 : Resumen ejecutivo de GOLD. Eur Respir J 2017; 49: 1700214.
- Vestbo J, et al: Terapia triple extrafina con inhalador único frente a terapia con antagonistas muscarínicos de acción prolongada para la enfermedad pulmonar obstructiva crónica (TRINITY). Lancet 2017; 389: 1919-1929.
- Singh D, et al: Terapia triple con un solo inhalador frente a terapia con corticosteroides inhalados más agonistas β2 de acción prolongada para la enfermedad pulmonar obstructiva crónica (TRILOGY): un ensayo doble ciego, de grupos paralelos, aleatorizado y controlado. Lancet 2016; 388: 936-973.
- Chong J, Leung B, Poole P, Black PN: Inhibidores de la fosfodiesterasa 4 para la enfermedad pulmonar obstructiva crónica. Cochrane Database Syst Rev 2011; (5): CD002309.
- Pavord ID, et al: Mepolizumab para la enfermedad pulmonar obstructiva crónica eosinofílica. N Engl J Med 2017; 377: 1613-1629.
- Grupo de investigación del ensayo LTOT: A Randomized Trial of Long-Term Oxygen for COPD with Moderate Desaturation. N Engl J Med 2016; 375(17): 1617-1627.
- Leuppi JD, et al: Tratamiento con glucocorticoides a corto plazo frente a tratamiento convencional en las exacerbaciones agudas de la enfermedad pulmonar obstructiva crónica: el ensayo clínico aleatorizado REDUCE. JAMA 2013; 309(21):2223-2231.
PRÁCTICA GP 2018; 13(1): 41-43