A principios de 2022 se publicó la nueva directriz sobre urticaria de la Sociedad Alemana de Alergología e Inmunología Clínica y la Sociedad Dermatológica Alemana. Los antihistamínicos de segunda generación y el omalizumab como complemento siguen actuando como pilar del tratamiento. Pero en lo que respecta a los regímenes de dosificación, se han incluido nuevas recomendaciones, basadas en las conclusiones del grupo internacional de expertos EAACI/GA²LEN.
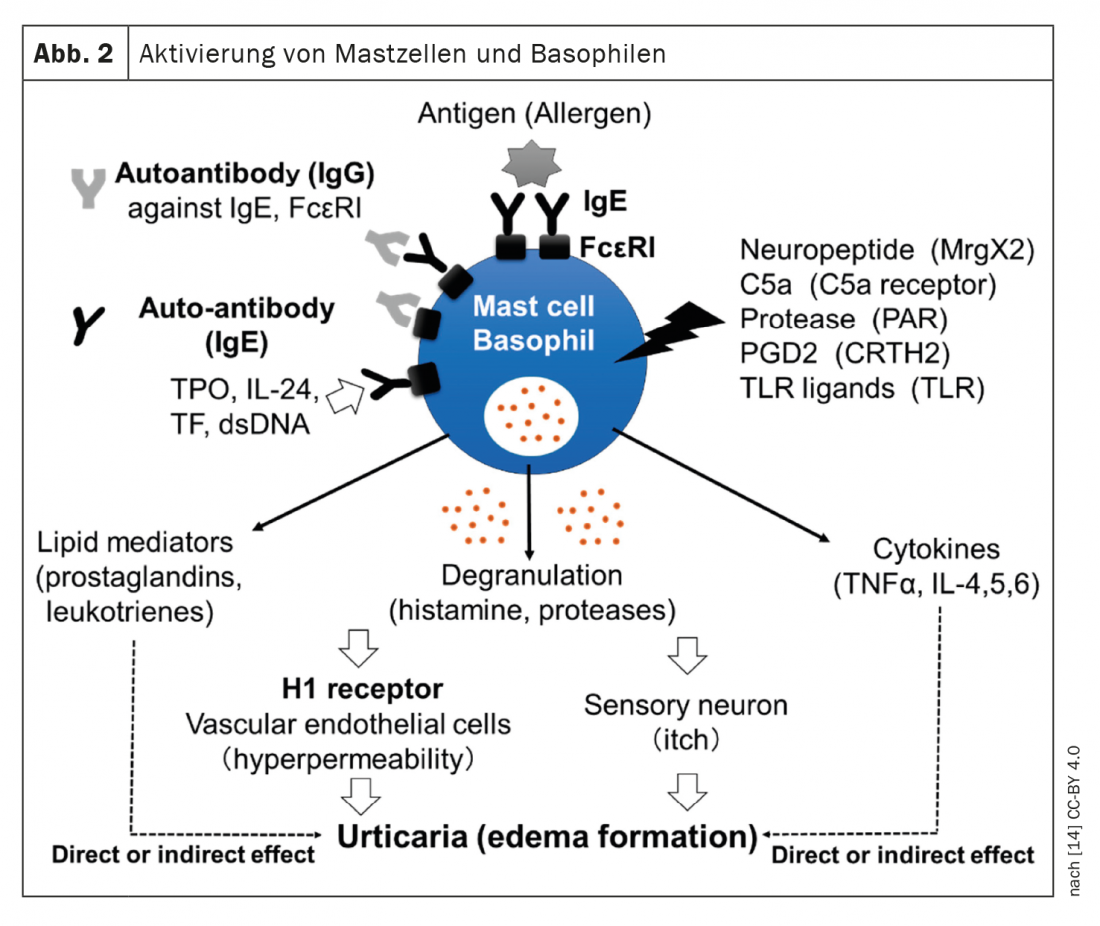
La directriz S3 actualizada es una adaptación al alemán de la directriz EAACI/GA²LEN/EuroGuiDerm/APAAACI en inglés [1,2]. El Prof. Dr. med. Torsten Zuberbier, Jefe de Investigación de Consecuencias Alérgicas de la Clínica de Dermatología, Venereología y Alergología de la Charité Universitätsmedizin de Berlín, las presentó en la Reunión Anual de la EEACI de este año [3]. La urticaria es una enfermedad común mediada por mastocitos que se caracteriza por la aparición de habones y/o angioedema. Las opciones de tratamiento recomendadas actualmente se refieren a mediadores de mastocitos como la histamina o activadores como los autoanticuerpos (Fig.1). Mientras que la urticaria aguda es autolimitada y no suele requerir pruebas diagnósticas aparte de los antecedentes para detectar posibles factores desencadenantes, las pruebas diagnósticas en pacientes con urticaria crónica espontánea (UCE) incluyen un hemograma diferencial, incluida la PCR y/o la velocidad de sedimentación globular. En pacientes bajo atención especializada, también deben recogerse IgE total e IgG-anti-TPO. La razón es que los pacientes con IgE muy baja no suelen responder bien al omalizumab, mientras que aquellos con IgG anti-TPO positiva suelen mostrar una respuesta muy buena a este anticuerpo monoclonal, explicó el Prof. Zuberbier [3]. En pacientes individuales, pueden ser útiles otras pruebas diagnósticas, dice el experto y añade: “En el caso de la urticaria inducible, recomendamos fijarse sólo en los ‘umbrales'”, es decir, probar estímulos fríos, etc. [3].
El objetivo terapéutico general para todos los pacientes con urticaria es lograr un control completo de los síntomas.
Dosifique los antihistamínicos H1 de 2ª generación, pero no los mezcle
La actividad de la enfermedad debe evaluarse en el primer examen y en cada uno de los siguientes. Para ello pueden utilizarse cuestionarios validados como la puntuación de actividad de la urticaria (UAS) y la puntuación de actividad del angioedema (AAS). El UAS7 se basa en el UAS (caja). “Para mí, personalmente, es la herramienta de diagnóstico más importante”, afirma el profesor Zuberbier [3]. Se trata de valores medidos muy robustos, que también proporcionan información sobre las fluctuaciones en el transcurso de una o varias semanas. De este modo, pueden detectarse correlaciones relevantes para la terapia.

Para que los pacientes comprendan que es necesario un tratamiento enérgico y de eficacia constante, es importante explicarles que, incluso cuando la piel está libre de síntomas, puede haber actividad inflamatoria bajo la superficie cutánea, subraya el experto. El concepto de “inflamación crónica mínima persistente” es conocido por otras enfermedades asociadas a la alergia y también se ha confirmado en la urticaria.
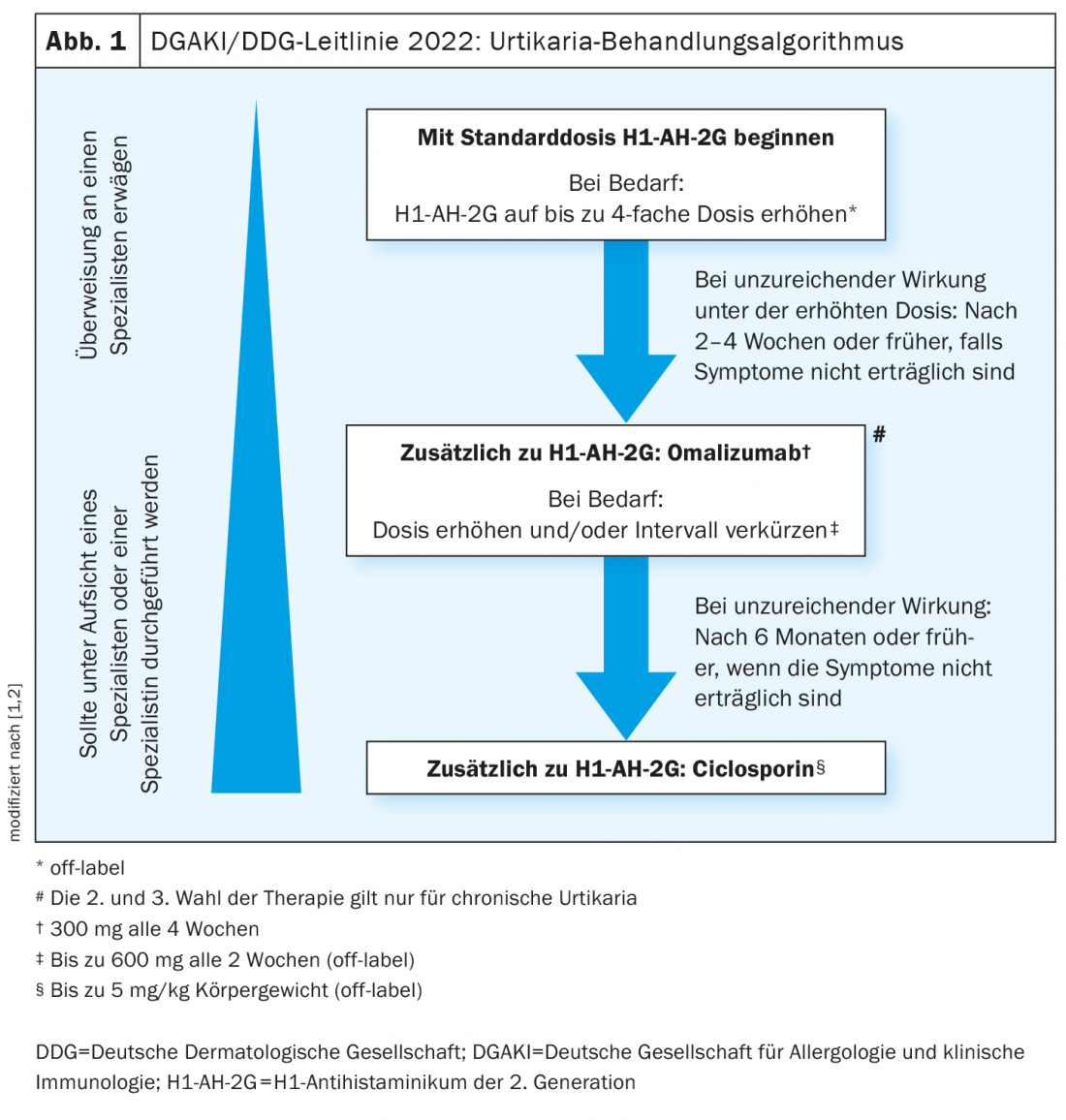
Se recomienda utilizar un antihistamínico H1 de 2ª generación como terapia de primera línea para todos los tipos de urticaria [1,2] . Estos agentes anulan el efecto de la histamina en el receptor H1. Según la directriz, las sustancias basadas en pruebas, eficaces y aprobadas en Suiza son, por ejemplo, la bilastina, la cetirizina, la desloratadina, la fexofenadina y la levocetirizina [1,2], En pacientes con urticaria crónica, se recomienda aumentar la dosis hasta cuatro veces la dosis estándar* como opción de tratamiento de segunda elección si hay falta de respuesta. “Dosificar más ayuda a reducir la liberación de citoquinas”, explica el profesor Zuberbier [3]. Sin embargo, no se recomienda el uso simultáneo de diferentes antihistamínicos H1. Una de las razones es que no sólo intervienen las histaminas, sino también otras citocinas, explica el ponente [3].
* off-label
Omalizumab como complemento: Evaluar la respuesta al tratamiento
En los pacientes que no muestren una respuesta suficiente al tratamiento antihistamínico (con dosis aumentada) después de 2-4 semanas, se recomienda una terapia adicional con omalizumab [1,2]. Si la dosis estándar de 300 mg cada 4 semanas no resulta eficaz, recientemente se ha aconsejado prescribir omalizumab en dosis más altas y/o a intervalos más cortos. Los estudios apoyan el uso de omalizumab en dosis de hasta 600 mg e intervalos de 2 semanas. Existen numerosos estudios sobre la predicción de la respuesta a la terapia. Según esto, los valores bajos de IgE al inicio se correlacionan negativamente con una respuesta terapéutica al omalizumab, pero se correlacionan positivamente con una respuesta a la ciclosporina [3,4]. Los resultados de un estudio observacional multicéntrico [5] muestran que un aumento de la dosis puede ser útil en caso de falta de respuesta al omalizumab. A un subgrupo de pacientes con UAS7 >6 que tomaban omalizumab 300 mg cada cuatro semanas se les subió la dosis a 450 mg y a algunos se les subió posteriormente a 600 mg, a intervalos de dosis de cuatro semanas cada uno. El 75% de los pacientes con el tratamiento de dosis ascendente alcanzaron un UAS7 ≤6, es decir, un buen control de los síntomas.
Tal y como demuestra un estudio realizado durante la pandemia de corona, los pacientes entrenados pueden autoadministrarse omalizumab en casa [6]. El 83% de los encuestados deseaba una continuación a largo plazo de la terapia en el entorno doméstico. Las preocupaciones sobre la administración a domicilio, como los errores de inyección o el olvido de una dosis, se mencionaron muy raramente.
¿Es eficaz el omalizumab incluso tras la interrupción del tratamiento?
Un control completo implica un manejo flexible de la urticaria, afirma el Prof. Zuberbier [3]. Por ejemplo, en función del resultado del tratamiento, puede suspenderse el omalizumab o plantearse un aumento de la dosis. En el estudio OPTIMA [7,8] se pudo demostrar que el anticuerpo anti-IgE también es eficaz tras una interrupción de la terapia. Los pacientes adultos con UCE recibieron tratamiento con omalizumab 150 mg o 300 mg como complemento, además de antihistamínicos H1, a intervalos de dosis de 4 semanas. 115 del total de 314 pacientes con CSU tratados de este modo lograron un buen control de los síntomas (UAS7 ≤6) en la semana 24. Sin embargo, una media del 44,5% del grupo de 150 mg y del 50% del grupo de 300 mg sufrieron una recaída (UAS7 ≥16) 4,7 semanas después de la interrupción del omalizumab. Tras la reanudación del tratamiento con omalizumab, el 87,8% de los afectados lograron un control renovado de los síntomas (UAS7 ≤6).
Ciclosporina A como “ultima ratio
En pacientes con urticaria crónica que no responden a dosis altas de antihistamínicos H1 y omalizumab, puede recomendarse el uso de ciclosporina A (CSA) además de la terapia antihistamínica. La CSA tiene un efecto inmunosupresor y un efecto moderado y directo sobre la liberación de mediadores de los mastocitos. La eficacia de la CSA en combinación con un antihistamínico H1 de 2ª generación modificado se ha demostrado en ensayos controlados con placebo [9–11] en UCE, pero este fármaco no puede recomendarse como tratamiento estándar debido a una mayor incidencia de efectos adversos [10].
En la directriz [1,2] no se recomienda el uso prolongado o regular de glucocorticosteroides sistémicos.
Congreso: Reunión anual de la EEACI
Literatura:
- Zuberbier Z, et al: Directriz alemana S3 sobre la clasificación, el diagnóstico y la terapia de la urticaria, adaptada de la directriz internacional S3, 2022. Registro de directrices de la AWMF (013-028).
- Zuberbier T, et al: Directriz internacional EAACI/GA²LEN/EuroGuiDerm/APAAACI para la definición, clasificación, diagnóstico y tratamiento de la urticaria. Alergia 2022; 77(3): 734-766.
- “Urticaria – la actualización de 2021 sobre diagnóstico y tratamiento”, Prof. Dr. Torsten Zuberbier, Congreso Híbrido de la EEACI, 1-3 de julio de 2022.
- Ertas R, et al.: La respuesta clínica al omalizumab en pacientes con urticaria crónica espontánea está relacionada con los niveles de IgE y su cambio, y puede predecirse por los mismos. Alergia 2018; 73(3): 705-712.
- Curto-Barredo L, et al: La dosis ascendente de omalizumab permite controlar la actividad de la enfermedad en pacientes con urticaria crónica espontánea refractaria. Br J Dermatol 2018; 179(1): 210-212.
- King C, et al: Transición rápida al tratamiento domiciliario con omalizumab para la urticaria crónica espontánea durante la pandemia COVID-19: La perspectiva de un paciente. World Allergy Organ J 2021; 14(10): 100587.
- Lynde C, et al: Retratamiento con omalizumab de pacientes con urticaria crónica idiopática/urticaria crónica espontánea tras la reaparición de los síntomas: Resultados primarios del estudio OPTIMA EADV. Resumen de póster presentado en la Conferencia de Dermatología Clínica 2017.
- Sussman G, et al: Retratamiento con omalizumab y escalonamiento en pacientes con urticaria crónica espontánea: ensayo OPTIMA. J Allergy Clin Immunol Pract 2020; 8(7): 2372-2378.e5.
- Grattan CE, et al: Estudio doble ciego aleatorizado de ciclosporina en la urticaria crónica “idiopática”. Br J Dermatol 2000; 143(2): 365-372.
- Vena GA, et al: Ciclosporina en la urticaria idiopática crónica: un ensayo doble ciego, aleatorizado y controlado con placebo. Revista de la Academia Americana de Dermatología. Oct 2006; 55(4): 705-709.
- Kulthanan K, et al: Ciclosporina para la urticaria crónica espontánea: un metaanálisis y una revisión sistemática. J Allergy Clin Immunol Pract 2018; 6(2): 586-599.
- Mlynek A, et al.: ¿Cómo evaluar la actividad de la enfermedad en pacientes con urticaria crónica? Alergia 2008;63(6): 777-780.
- Mathias SD, et al: Desarrollo de un diario para pacientes con urticaria idiopática crónica. Ann Allergy Asthma Immunol 2010;105(2): 142-148.
- Yanase Y, et al.: El papel de los factores de coagulación y del complemento para la activación de los mastocitos en la patogénesis de la urticaria crónica espontánea. Células 2021; 10(7): 1759.
DERMATOLOGIE PRAXIS 2022; 32(4): 16-18 (publicado el 22.8.22, antes de impresión).