El pronóstico de la amiloidosis de cadenas ligeras (AL), una discrasia de células plasmáticas, viene determinado en gran medida por la presencia de afectación cardiaca. La estadificación convencional se basa en biomarcadores cardíacos y en la diferencia de cadenas ligeras libres. Un nuevo estudio pretendía ahora evaluar el papel de los parámetros ecocardiográficos como marcadores pronósticos en la amiloidosis AL e investigar su utilidad en comparación con la estadificación convencional.
La amiloidosis cardiaca es el arquetipo de miocardiopatía infiltrativa y suele presentarse con el fenotipo clínico de insuficiencia cardiaca con fracción de eyección preservada. La amiloidosis sistémica de cadenas ligeras (amiloidosis AL) es una discrasia de células plasmáticas con afectación multisistémica; sin embargo, el pronóstico de la amiloidosis AL suele estar relacionado con la afectación cardiaca. Esto se refleja en el uso de la “puntuación Mayo” en la estadificación de la amiloidosis AL. Esta puntuación incluye los biomarcadores cardíacos troponina de alta sensibilidad (hs-Trop) y pro-péptido natriurético cerebral N-terminal (NT-proBNP), así como la diferencia de cadenas ligeras libres (dFLC) [2].
Aunque las puntuaciones originales y revisadas de Mayo para clasificar la amiloidosis AL han demostrado su utilidad pronóstica, existen limitaciones en el uso de estos biomarcadores. Las diferencias en las pruebas de troponina utilizadas en los distintos centros, por ejemplo hs-TropI y hs-TropT, cada una de las cuales tiene sus propios rangos definidos, dificultan las comparaciones a lo largo del tiempo. Las pruebas de NT-proBNP también han cambiado con el tiempo, con implicaciones similares a las de la troponina. Además, tanto la troponina como el NT-proBNP se ven influidos por factores como el índice de masa corporal y la insuficiencia renal coexistente, siendo esta última relativamente frecuente en la amiloidosis sistémica AL.
Por el contrario, los marcadores ecocardiográficos tradicionales de la estructura y la función cardiacas están estandarizados y tienen rangos normales definidos universalmente. Además, se realiza de forma rutinaria un ecocardiograma transtorácico (ETT) en pacientes con amiloidosis AL para evaluar la afectación cardiaca, ya que es barato y está ampliamente disponible. Se han validado nuevos índices ecocardiográficos como la deformación longitudinal global del ventrículo izquierdo (LVGLS) para una amplia gama de procesos patológicos y se utilizan cada vez más en la evaluación clínica de la amiloidosis AL [3]. Por ello, un estudio reciente investigó la utilidad pronóstica de los parámetros ecocardiográficos en comparación con la estadificación de Mayo en pacientes con amiloidosis AL [1].
Características de los pacientes y parámetros ecocardiográficos
Se identificaron retrospectivamente 75 pacientes consecutivos con amiloidosis AL que fueron evaluados en una clínica de amiloidosis de referencia y se sometieron a un examen ecocardiográfico completo. La edad media era de 61,8 ± 10 años y 51/75 pacientes eran varones. 71 de 75 pacientes recibieron quimioterapia, la mayoría de ellos con bortezomib (Velcade), ciclofosfamida y dexametasona (VCD; 30/75); 11 pacientes se sometieron a un trasplante alogénico de células madre. 25 pacientes fueron clasificados como estadio I de Mayo, 22 como estadio II, mientras que los estadios III y IV comprendían 15 y 13 pacientes, respectivamente.
Los parámetros ecocardiográficos estudiados incluyeron la fracción de eyección del ventrículo izquierdo, la masa, los parámetros de función diastólica, la deformación longitudinal global (GLS) y el volumen de la aurícula izquierda (AI). La mortalidad se determinó mediante una revisión de las historias clínicas. Durante una mediana de seguimiento de 51 meses, 29/75 (39%) pacientes fallecieron. Los pacientes se dividieron en dos subgrupos en función de la mortalidad, que no diferían en edad, sexo o índice de masa corporal, aunque la presión arterial sistólica alcanzó significación estadística (p=0,051). 11 pacientes presentaron FA; la tasa de FA fue similar en ambos grupos: 6/46 (13%) en los supervivientes frente a 5/29 (17%) en los no supervivientes (p=0,617). Los pacientes que fallecieron tenían un volumen de AI significativamente mayor (35 ± 10 frente a 47 ± 12 mL/m2, p<0,001) y un E/e’ más alto (14 ± 6 frente a 18 ± 10, p=0,026); tanto la masa del VI como el GVI se acercaron a la significación estadística. No hubo diferencias entre los grupos en la función sistólica del VI evaluada por la FEVI. Como era de esperar, la mortalidad aumentó con el incremento del estadio Mayo y fue del 8, 45, 60 y 62%, respectivamente, para los pacientes en los estadios Mayo I-IV.
Estadio de Mayo y predictores ecocardiográficos univariantes de supervivencia
El análisis univariante mostró que los parámetros ecocardiográficos que predecían la mortalidad con una significación de p<0,1 incluían LAVI, velocidad e’, E/e’ y LVGLS. El estadio Mayo también fue un factor predictivo independiente de la supervivencia. Los predictores ecocardiográficos univariantes de mortalidad (significación de p<0,1) se introdujeron en un modelo multivariable de riesgos proporcionales de Cox e incluyeron E/e’ y el volumen de la LA y el LVGLS (la velocidad e’ no se incluyó en el modelo debido a la colinealidad con E/e’). En este modelo multivariable de parámetros ecocardiográficos, el LAVI fue el único predictor ecocardiográfico independiente de mortalidad. El volumen auricular izquierdo indexado se correlacionó con el estadio Mayo (coeficiente de correlación de Spearman 0,5, p<0,001), y todos los pacientes en los estadios Mayo III y IV tenían aurículas izquierdas dilatadas (LAVI ≥34 mL/m2).
Clasificación de los pacientes en tres grupos de riesgo diferentes
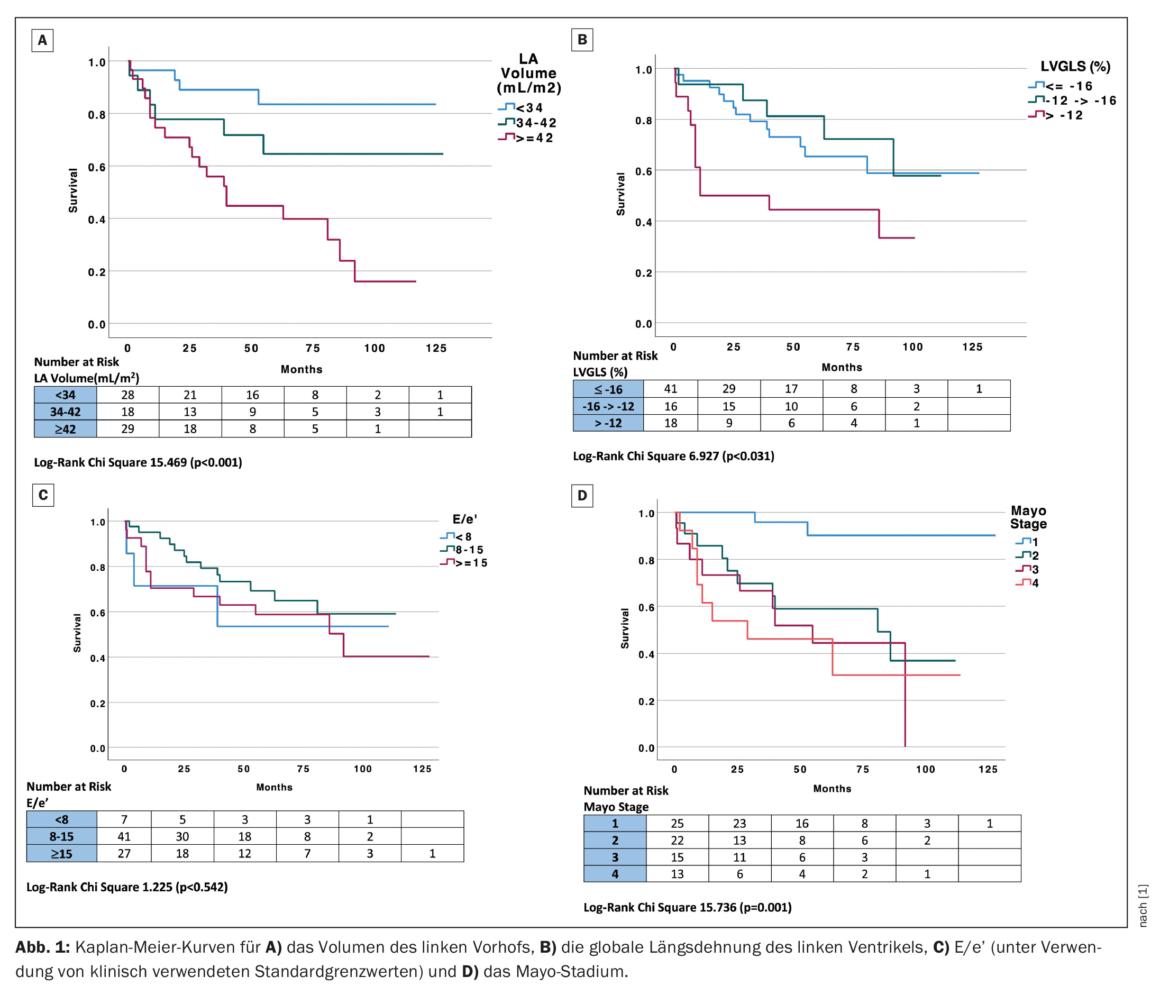
El LVGLS (función sistólica ventricular izquierda), el LAVI y la E/e’ (función diastólica) se analizaron como variables categóricas utilizando valores de corte clínicamente aplicables para evaluar su impacto en la mortalidad en comparación con el estadio de Mayo. La deformación ventricular izquierda longitudinal global se dividió en tres grupos basándose en el punto de corte clínico comunicado previamente de mejor que -16, -12 a -16% y peor que -12% para GLS normal, reducida y gravemente reducida, respectivamente [4]. El volumen auricular izquierdo indexado se dividió en tres grupos utilizando un punto de corte clínico de ≤34, 34-42 y ≥42 mL/m2, correspondientes a normal, dilatación de la aurícula izquierda de leve a moderada o dilatación de la aurícula izquierda superior a moderada [5]. ‘E/e’ se clasificó en tres grupos en función de los valores clínicos de <8, 8-15 y ≥15, correspondientes a una presión de llenado del VI normal, probablemente anormal y elevada [6]. La estratificación por grupos clínicos de LAVI (p<0,001), LVGLS (p=0,031) y estadio de Mayo (p=0,001) fueron predictores significativos de mortalidad, mientras que E/e’ no alcanzó significación en el análisis de Kaplan-Meier (Fig. 1) [1]. Cabe destacar que los pacientes con un LAVI normal <34 mL/m2 tuvieron unos resultados a largo plazo especialmente buenos (mediana de seguimiento de 60,5 ± 46 meses) y, por el contrario, los pacientes con un LVGLS inferior al -12% tuvieron un mal resultado.
Sistema de puntuación para la dilatación de la aurícula izquierda y la reducción de la tensión longitudinal global del ventrículo izquierdo
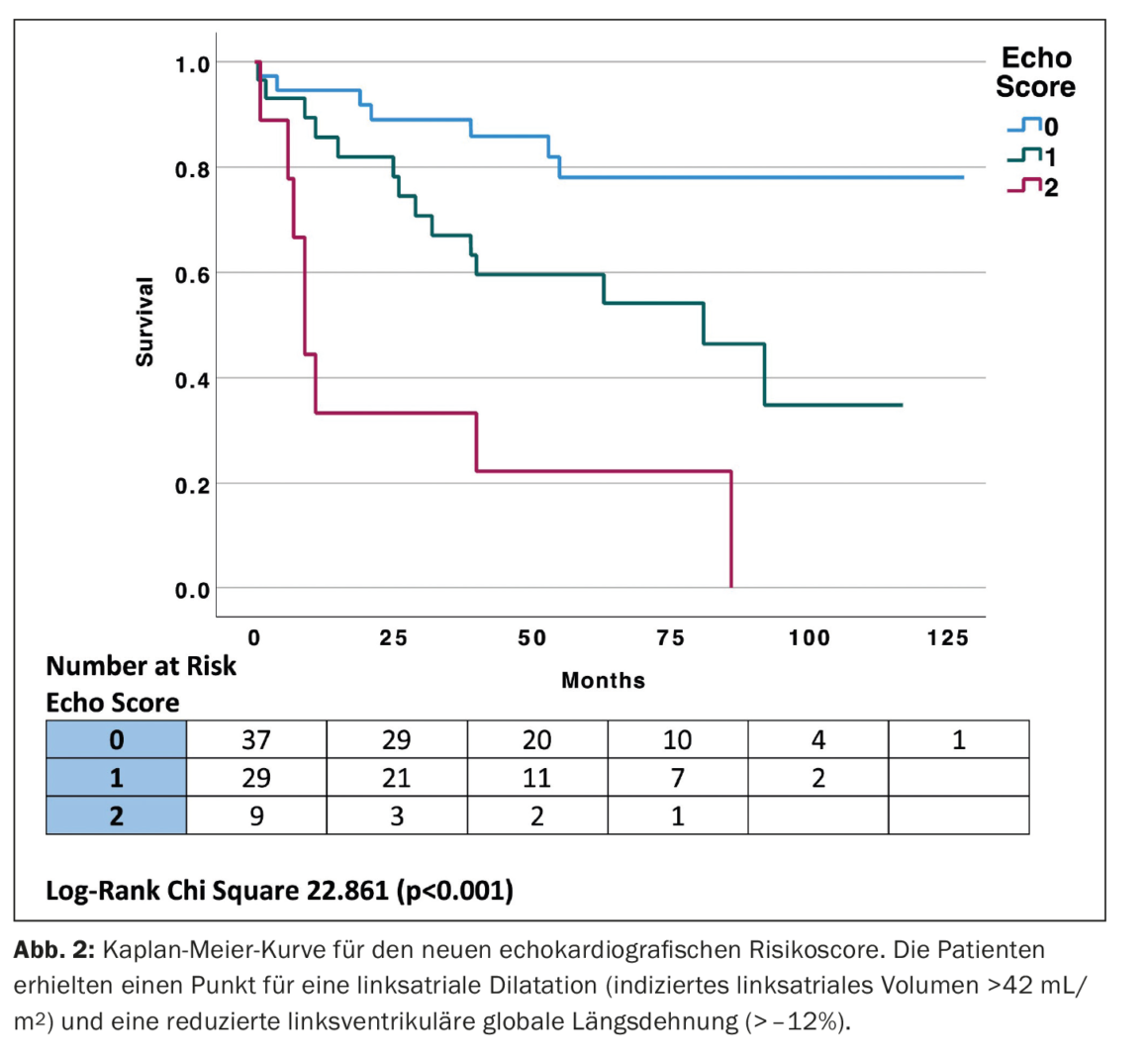
Utilizando los valores de corte clínicos para el LVGLS y el LAVI para generar una puntuación ecocardiográfica simple, el grupo de mayor riesgo mostró tanto LVGLS (peor que -12%) como LAVI (>42 mL/m2), el grupo de riesgo intermedio tenía un LVGLS de -12 a -16% y un LAVI de 34-42 mL/m2, y el grupo de riesgo más bajo tenía un LVGLS mejor que -16% y un LAVI <34 ml/m2. A continuación se generó una puntuación de riesgo asignando un punto a cada LVGLS peor que -12% y LAVI >34 mL/m2, colocando a los pacientes en uno de tres grupos. El grupo de mayor riesgo tenía tanto LVGLS (peor que -12%) como LAVI (>42 mL/m2), el grupo de riesgo intermedio tenía un LVGLS peor que -12% o un LAVI >42 mL/m2 y el grupo de menor riesgo tenía un LVGLS mejor que -12% y un LAVI <42 mL/m2 con dos, uno y cero puntos respectivamente. Se crearon curvas de Kaplan-Meier para la nueva puntuación de riesgo ecocardiográfico (Puntuación Echo) (Fig. 2) [1]. La nueva “puntuación eco” tuvo un rendimiento pronóstico similar al del estadio Mayo [AUC 0,745, intervalo de confianza (IC) del 95% 0,638-0,853 frente a AUC 0,752, IC del 95% 0,645-0,858, p=0,911].
Predicción de mortalidad por todas las causas comparable con el sistema de estadificación Mayo existente
La variabilidad intraobservador e interobservador del LAVI fue excelente, con un coeficiente de correlación intraclase de 0,987 (IC 95%: 0,946-0,997), mientras que el coeficiente de correlación interobservador fue de 0,935 (IC 95%: 0,731-0,984). El LVGLS también fue muy reproducible, con un coeficiente de correlación intraclase de 0,989 (IC del 95%: 0,864-0,998), mientras que el coeficiente de correlación interobservador fue de 0,980 (IC del 95%: 0,924-0,995). La fracción de eyección ventricular izquierda mostró una buena variabilidad dentro del observador y entre observadores, con un coeficiente de correlación intraclase de 0,871 (IC del 95%: 0,517-0,967) y un coeficiente interobservador de 0,772 (IC del 95%: 0,115-0,943). Estos resultados demuestran que las imágenes cardiacas pueden utilizarse para identificar a los pacientes con mayor mortalidad, de modo que dicha estratificación del riesgo puede conducir potencialmente a la selección de terapias óptimas.
Mensajes para llevarse a casa
- Un simple parámetro ecocardiográfico, el LAVI, fue un marcador pronóstico independiente en pacientes con amiloidosis AL.
- El volumen auricular izquierdo indexado y el LAVI estratificados por valores de corte clínicos mostraron peores resultados con un peor LAVI y un LAVI creciente.
- Una puntuación ecocardiográfica compuesta derivada de LAVI y LVGLS tiene un valor predictivo similar a la estadificación de Mayo.
Literatura:
- Genty P, et al.: A novel echocardiographic risk score for light-chain amyloidosis. Eur Heart J 2023; https://doi.org/10.1093/ehjopen/oead040.
- Kumar S, et al.: Revised prognostic staging system for light chain amyloidosis incorporating cardiac biomarkers and serum free light chain measurements. J Clin Oncol 2012; 30: 989–995.
- Cohen OC, Ismael A, Pawarova B, et al.: Longitudinal strain is an independent predictor of survival and response to therapy in patients with systemic AL amyloidosis. Eur Heart J 2021; 43: 333–341.
- Potter E, Marwick TH: Assessment of left ventricular function by echocardiography: the case for routinely adding global longitudinal strain to ejection fraction. JACC Cardiovasc Imaging 2018; 11: 260-274.
- Lang RM, et al.: Recommendations for cardiac chamber quantification by echocardiography in adults: an update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. J Am Soc Echocardiogr 2015; 28: 1–39.e14.
- Ommen SR, et al.: Clinical utility of Doppler echocardio-graphy and tissue Doppler imaging in the estimation of left ventricular filling pressures: a comparative simultaneous Doppler-catheterization study. Circulation 2000; 102: 1788–1794.
CARDIOVASC 2023; 22(2): 50–52
| Imagen de portada: Micrografía a gran aumento de la amiloidosis cardiaca senil. Congo red stain. Muestra de autopsia. ©Wikimedia (Nephron) |