El carcinoma de próstata es el cáncer más frecuente en los hombres. No todos los cánceres de próstata son iguales (estratificación del riesgo mediante palabras clave). No todos los carcinomas de próstata necesitan tratamiento (palabra clave sobreterapia). En función del perfil de riesgo, existen varias opciones terapéuticas curativas para el tratamiento del carcinoma de próstata localizado.
En Suiza, cada año se diagnostica cáncer de próstata a unos 6.100 hombres. Esto convierte al carcinoma de próstata en el tipo de cáncer más común de todos. En la mayoría de los casos, el estadio inicial del tumor es localizado o circunscrito a un órgano. En este caso, el urólogo tratante tiene a su disposición diversas opciones de tratamiento. Éstas van desde la vigilancia activa hasta la prostatectomía radical.
Antes de decidirse a favor o en contra de una forma de terapia, debe evaluarse el estado general, la esperanza de vida y las características del tumor (estratificación del riesgo) de cada paciente. La esperanza de vida desempeña un papel más importante que la edad biológica a la hora de considerar las modalidades de tratamiento. Con una edad avanzada del paciente o una esperanza de vida reducida, las comorbilidades del paciente reducen el riesgo de morir de cáncer de próstata: Así pues, los pacientes mueren con el carcinoma de próstata, pero no a causa del carcinoma de próstata.
Estratificación del riesgo
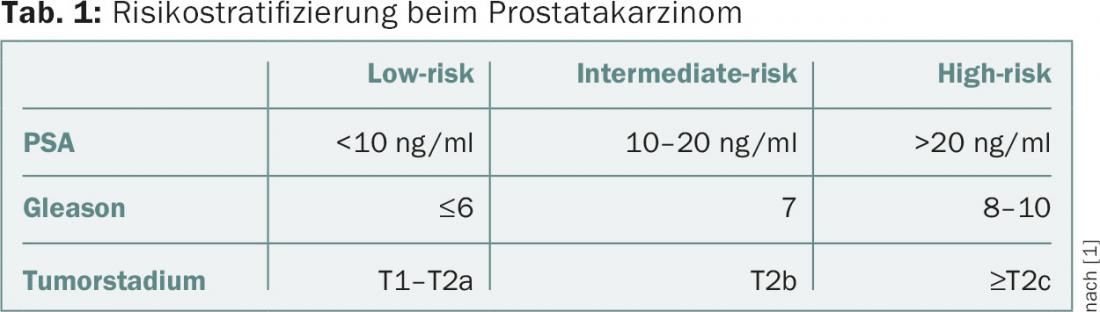
La estratificación del riesgo en el cáncer de próstata se basa en el valor del PSA, la puntuación bióptica de Gleason y el estadio clínico. Una clasificación común es, según D’Amico et al. [1]. Aquí, los pacientes con carcinoma de próstata localizado se dividen en tres grupos de riesgo (tab. 1).
Vigilancia activa
El desequilibrio entre incidencia y mortalidad en el cáncer de próstata localizado sugiere que algunos pacientes no se benefician del tratamiento (sobretratamiento). Los hombres que no buscan tratamiento inmediato pueden optar por la Vigilancia Activa (VA) en presencia de un tumor de bajo riesgo [2]. Se controlan el estado local y el valor del PSA y se realizan rebiopsias según un calendario. AS tiene dos objetivos: En primer lugar, los hombres con un carcinoma de próstata localizado no deben recibir una terapia curativa de inmediato, sino a tiempo en caso de progresión. En segundo lugar, para reducir los riesgos de complicaciones inducidas por el tratamiento (por ejemplo, disfunción eréctil, incontinencia) en hombres con carcinomas de bajo riesgo.
Con una buena selección de pacientes, los resultados son prometedores. La supervivencia global de los pacientes en el curso a largo plazo es la misma que la de los pacientes que recibieron directamente una terapia curativa. Aproximadamente el 25% de los pacientes sometidos a AS reciben terapia curativa durante el periodo de observación. La carga psicológica a veces elevada de los pacientes y un posible empeoramiento del pronóstico con el retraso de la terapia hablan en contra del concepto de AS. Por ejemplo, existen datos que indican que los pacientes que esperaron más de 180 días para recibir terapia tras el diagnóstico de carcinoma de próstata tenían un riesgo de recidiva postoperatoria 2,7 veces mayor que los pacientes sometidos a prostatectomía radical en los tres primeros meses [3].
La AS ocupa sin duda un lugar en el tratamiento del carcinoma de próstata localizado, pero en la actualidad aún se carece de predictores fiables para la estimación segura del pronóstico. Por lo tanto, los pacientes deben ser informados y educados sobre las ventajas y desventajas respectivas de la AS.
Braquiterapia de baja tasa de dosis
En la braquiterapia de baja tasa de dosis (LDR), se introducen clavos metálicos radiactivos (semillas) en la próstata a través del perineo mediante agujas huecas bajo control ecográfico. Las semillas permanecen en la glándula prostática y administran allí la dosis radiactiva necesaria. La intervención se realiza bajo anestesia y dura entre dos horas y media y tres horas, incluidos todos los preparativos, con una estancia hospitalaria de normalmente sólo una noche tras la operación.
De gran importancia para la braquiterapia es la selección de los pacientes. Debido a la heterogeneidad de los datos, la braquiterapia LDR sólo es una opción de tratamiento para pacientes con carcinoma de bajo riesgo (es decir, pacientes que también cumplen los requisitos para la AS), un tamaño de próstata <50 cm3 y sin síntomas miccionales relevantes (IPSS ≤12). La supervivencia libre de enfermedad a los cinco años es del 71-93%, y a los diez años del 65-85% [4]. Hasta la fecha, ningún estudio aleatorizado ha comparado la braquiterapia con ninguna otra terapia curativa para el cáncer de próstata localizado.
Radioterapia externa
La radioterapia percutánea externa (“radioterapia de haz externo”, EBRT) es una alternativa terapéutica para el carcinoma de próstata órgano-confinado. En comparaciones retrospectivas, la EBRT muestra resultados oncológicos comparables a la prostatectomía radical en los tumores bien diferenciados; la prostatectomía radical presenta ventajas en los tumores poco diferenciados. La EBRT se realiza como radiación individual guiada por imagen (TC, IRM, PET-TAC) utilizando fotones con una utilización óptima del órgano diana al tiempo que se preservan en la medida de lo posible los órganos de riesgo circundantes. La duración de la EBRT es de varias semanas (por ejemplo, una dosis total de 78 Gy con dosis únicas de 2 Gy = 39 fracciones = ocho semanas de terapia).
Dependiendo del grupo de riesgo según D’Amico et al. Los pacientes con EBRT reciben terapia de privación androgénica (ADT) neoadyuvante, concomitante o adyuvante. Por lo tanto, debido a la dependencia hormonal del cáncer de próstata, los resultados de la EBRT son difíciles de comparar con los resultados de otras modalidades de terapia curativa. Si se produce una recidiva tras la EBRT primaria, en principio también puede tratarse y curarse mediante una prostatectomía radical de rescate, pero el procedimiento se asocia a un riesgo significativamente mayor de complicaciones graves (incontinencia en el 56%, disfunción eréctil en el 81%) [5]. Sigue sin estar claro si se producen segundos cánceres tras la EBRT y con qué frecuencia.
Prostatectomía radical
En la prostatectomía radical (PR) se extirpa toda la glándula prostática con las vesículas seminales y las ampollas de los conductos deferentes. En los centros de tratamiento, la intervención se realiza hoy en día preferentemente mediante un procedimiento mínimamente invasivo asistido por robot (RARP) con el sistema da Vinci. Estudios recientes informan de una menor morbilidad perioperatoria y una mejor función eréctil postoperatoria con el sistema da Vinci en comparación con la técnica abierta [6,7]. En cambio, las observaciones iniciales a largo plazo con un seguimiento de diez años indican una eficacia oncológica equivalente de la cirugía asistida por robot y la cirugía abierta [8].
Dependiendo de las características del tumor y de la función sexual del paciente, la RP se realiza preservando los nervios (para preservar la función eréctil) o sin preservar los nervios. Dependiendo del perfil de riesgo, se realiza una linfadenectomía pélvica al mismo tiempo que la RP. De los diversos métodos curativos para el tratamiento del carcinoma de próstata localizado, la RP es el único para el que existe un nivel de evidencia I con respecto al control tumoral. Otra ventaja potencial de la RP en comparación con la EBRT es que, en caso de recidiva tras la RP, una proporción sustancial de pacientes puede curarse con una morbilidad aceptable (incontinencia en el 13%, disfunción eréctil en el 61%) mediante radiación aditiva (la denominada radioterapia de rescate) [5].
Otros tratamientos
Además de las modalidades de tratamiento establecidas ya descritas, existe una variedad de otras formas de terapia. Entre ellas se incluyen la crioterapia, los ultrasonidos focalizados de alta intensidad (HIFU), la braquiterapia intersticial de próstata de alta dosis y las terapias combinadas (por ejemplo, la EBRT y la braquiterapia intersticial de próstata). Todavía está pendiente una evaluación científica de estos procedimientos, por lo que no permite hacer recomendaciones claras.
Conclusión
A los hombres con un carcinoma de próstata recién diagnosticado, localmente limitado y una elevada esperanza de vida se les pueden ofrecer ahora todos los métodos establecidos (EBRT, RP, braquiterapia de próstata LDR o AS) en función del perfil de riesgo. Elegir el procedimiento óptimo para cada paciente es todo un reto y requiere una estrecha colaboración entre todas las disciplinas implicadas. La mejor forma de conseguirlo es en el marco de una junta interdisciplinar de tumores.
Literatura:
- D’Amico AV, et al: Resultado bioquímico tras prostatectomía radical, radioterapia de haz externo o radioterapia intersticial para el cáncer de próstata clínicamente localizado. JAMA 1998; 280(11): 969-974.
- Klotz L: Vigilancia activa: selección de pacientes. Curr Opin Urol 2013; 23(3): 239-244.
- Lellig K, et al: [Active surveillance of low risk prostate cancer]. Urólogo A 2014; 53(7): 1031-1039.
- Mottet N, et al: Directrices sobre el cáncer de próstata. Asociación Europea de Urología. Directrices sobre el cáncer de próstata. Asociación Europea de Urología 2015.
- van der Poel HG, et al: Tratamiento secuencial para el cáncer de próstata localizado recidivante. Revista de Oncología Quirúrgica 2008; 97(5): 377-382.
- Ficarra V, et al: Revisión sistemática y metaanálisis de los estudios que informan de la recuperación de la continencia urinaria tras la prostatectomía radical asistida por robot. Eur Urol 2012; 62(3): 405-417.
- Haglind E, et al: Incontinencia urinaria y disfunción eréctil tras prostatectomía radical robótica frente a abierta: un ensayo prospectivo, controlado y no aleatorizado. Eur Urol 2015; 68(2): 216-225.
- Díaz M, et al: Resultados oncológicos a los 10 años de la prostatectomía radical robótica. Eur Urol 2015; 67(6): 1168-1176.
InFo ONCOLOGÍA Y HEMATOLOGÍA 2015; 3(11-12): 8-10