Hubo grandes novedades en el Congreso ASCO 2017. En primer lugar, la abiraterona se está imponiendo en el ámbito de la primera línea en el cáncer de próstata metastásico. Por otro lado, existe una nueva norma en la terapia adyuvante de los tumores del sistema biliar. Ahora se espera que los datos cambien la práctica clínica “de la noche a la mañana”, por así decirlo.
Los pacientes con un nuevo diagnóstico de cáncer de próstata metastásico tienen un mal pronóstico. Esto es aún más cierto si también presentan características de alto riesgo. Por término medio, mueren de su enfermedad al cabo de menos de cinco años. Los enfoques para mejorar la supervivencia en este grupo sin perder de vista las toxicidades de la terapia intensiva han recibido ahora un impulso significativo con los dos ensayos presentados en ASCO 2017 denominados LATITUDE y STAMPEDE.
Esto por adelantado: En lugar de utilizarse tras la resistencia a la castración , la abiraterona se utiliza desde el principio al mismo tiempo que la terapia hormonal (ADT), es decir, en primera línea, lo que en los estudios condujo a un beneficio (al menos) comparable al de la quimioterapia con docetaxel. Sin embargo, en comparación con esta última, la abiraterona se tolera mucho mejor, y muchos pacientes no muestran ningún efecto secundario. Por lo tanto, es probable que un número significativamente mayor de personas pueda optar a esta terapia. Los expertos del congreso ya hablaron de “resultados que cambiarán la práctica de la noche a la mañana”. ¿Es realmente así?
Antecedentes
La testosterona impulsa el crecimiento de un carcinoma de próstata: La testosterona se acumula en unos puntos de unión especiales de las células de la próstata, los receptores de andrógenos, lo que provoca posteriormente la división celular y el crecimiento de las células – en las células del carcinoma de próstata, este mecanismo se altera y se produce un crecimiento incontrolado. La terapia hormonal, a su vez, suprime la formación de andrógenos o inhibe su efecto sobre las células tumorales.
La terapia de privación de andrógenos (TPA) consiste en suprimir la producción de hormonas en los testículos. Sin embargo, se siguen produciendo pequeñas cantidades de andrógenos, por ejemplo, por la corteza suprarrenal. La abiraterona interviene en el circuito regulador hormonal bloqueando una enzima que convierte otras hormonas en testosterona en varios pasos (biosíntesis endógena de andrógenos). Esta inhibición impide la producción de testosterona no sólo en los testículos, sino también en las glándulas suprarrenales y la próstata o en el propio tejido tumoral. Actualmente está aprobado:
- para el tratamiento en combinación con agonistas de la LHRH y prednisona o prednisolona en pacientes con cáncer de próstata metastásico avanzado en progresión tras el tratamiento con docetaxel.
- para el tratamiento en combinación con agonistas de la LHRH y prednisona o prednisolona en pacientes asintomáticos o ligeramente sintomáticos con cáncer de próstata metastásico resistente a la castración sin metástasis viscerales y sin metástasis hepáticas, tras el fracaso del bloqueo de los receptores androgénicos, cuando la quimioterapia no esté clínicamente indicada.
LATITUD – cegamiento eliminado en una fase temprana
Se aleatorizó a unos 1.200 pacientes con cáncer de próstata metastásico, sin hormonas y de alto riesgo diagnosticado tres meses o menos antes de la aleatorización. El estado de rendimiento ECOG era de 0-2.
El ensayo de fase III se desenmascaró antes de tiempo debido a los resultados convincentes de un primer análisis provisional. Los pacientes de placebo pasaron al grupo de estudio. En ese momento, había transcurrido una media de 30 meses. Tanto en el criterio de valoración co-primario como en todos los secundarios, la combinación de abiraterona (1 g/d) más prednisona (5 mg/d) y ADT significativamente superior a la ADT sola (más placebo) (Tab.1). La mediana de la supervivencia global en el grupo de abiraterona aún no pudo calcularse (“aún no se ha alcanzado”), ya que más de la mitad de los pacientes de este grupo seguían vivos cuando se realizó el análisis.
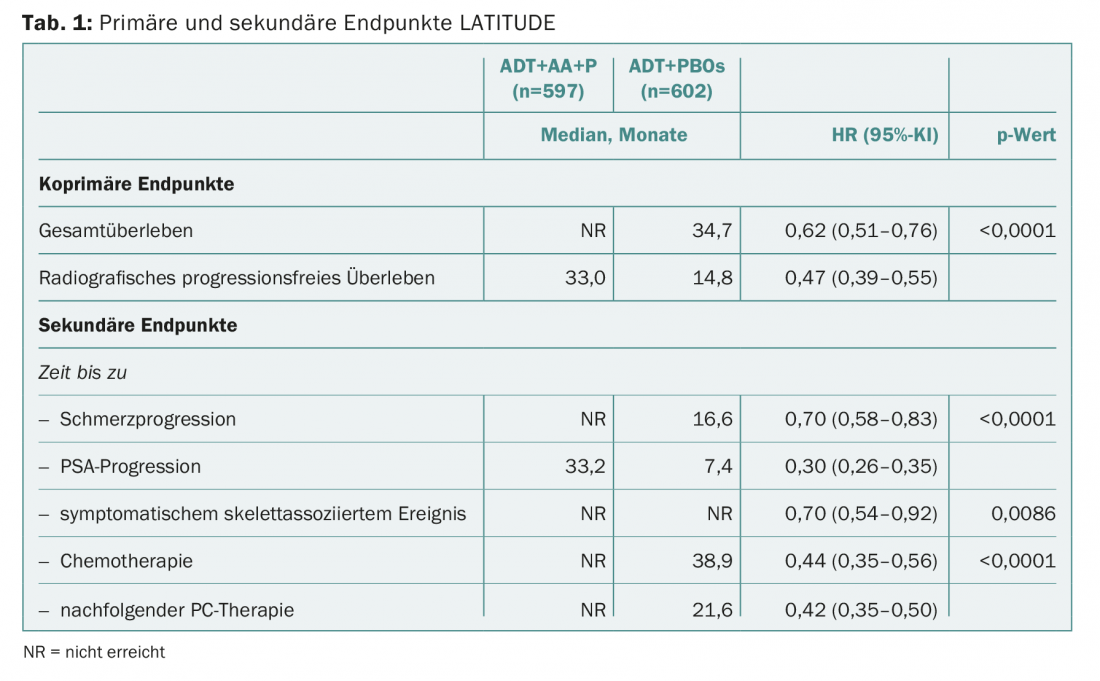
Con una reducción del riesgo de muerte del 38% y del riesgo de progresión de más del 50%, ahora se plantea naturalmente la cuestión de si la abiraterona en primera línea puede convencer no sólo en términos de eficacia sino también de seguridad. En conjunto, el perfil de riesgo-beneficio era claramente favorable al fármaco y, por tanto, al uso precoz de la abiraterona en esta población de pacientes. Como acontecimientos adversos de grado 3/4, que se produjeron con mayor frecuencia en comparación con el placebo, los autores mencionaron la hipertensión (20,3% frente a 10%) y la hipopotasemia (10,4% frente a 1,3%), que son típicas y conocidas con abiraterona, así como el aumento de las transaminasas. Por lo tanto, según los autores del estudio, se recomienda precaución en pacientes con un mayor riesgo de problemas cardiacos, por ejemplo diabetes o cardiopatía coronaria.
STAMPEDE – Confirmación de los resultados
Tras décadas de tratamiento del cáncer de próstata metastásico con enfoques hormonales, en 2015 se publicaron pruebas de un beneficio para la supervivencia con la adición de quimioterapia con docetaxel con el ensayo CHAARTED [1]. Ahora, en 2017, ocurre lo mismo con la abiraterona (pero con muchos menos efectos secundarios). En lo sucesivo aún habría que aclarar si la abiraterona puede aumentar aún más el beneficio además de la quimioterapia.
El llamado ensayo STAMPEDE con participación suiza no ofrece una respuesta directa a esta pregunta. El objetivo es más bien mostrar una vez más, resumido en un diseño de estudio innovador, cómo se comportan los dos enfoques en comparación con la ADT sola y si una variante es superior en términos de eficacia. Ahora bien, el Congreso de la ASCO no sería la mayor y más importante reunión internacional de oncología si no tuviera que ofrecer también los resultados iniciales de este estudio. STAMPEDE examina un total de seis estrategias terapéuticas, solas o en combinación y siempre además de la terapia hormonal. Se incluyen el docetaxel y la abiraterona, pero sólo se comparan indirectamente, no combinados.
Los datos presentados confirmaron las señales positivas de LATITUDE: de nuevo se compararon la ADT sola y con adición inmediata de abiraterona. La TAD durante al menos dos años más la radioterapia obligatoria para la enfermedad N0M0 y la radioterapia recomendada para la enfermedad N+M0 se consideró el “tratamiento estándar”. La muestra estaba formada por pacientes con cáncer de próstata de alto riesgo localmente avanzado o metastásico. Esto último se aplicó al 52% de los carcinomas, el 95% se consideraron de nuevo diagnóstico. Se aleatorizó a un total de 1917 personas. Se trata, por tanto, del mayor estudio sobre la abiraterona en primera línea y en esta indicación.
Cuando se añadieron abiraterona y prednisolona a las mismas dosis que en LATITUDE, también se prolongó la supervivencia. Tras una mediana de 40 meses, el riesgo de muerte se redujo significativamente en un 37% similar (HR 0,63; IC 95% 0,52-0,76). Después de tres años, el 83% frente al 76% de los pacientes estaban vivos. El riesgo de fracaso del tratamiento se redujo hasta en un 71% con la adición de abiraterona (HR 0,29; IC 95% 0,25-0,34) – la diferencia fue significativa. En esta ocasión, un empeoramiento de los síntomas o del valor del PSA también se consideró un fracaso. Los efectos fueron coherentes en los distintos subgrupos (incl. metástasis/sin metástasis, estado ganglionar, etc.).
El perfil de efectos secundarios se consideró de nuevo tolerable y controlable. En cuanto al número total de efectos secundarios, los dos grupos eran comparables. Los acontecimientos adversos de grado 3, por otra parte, se encontraron en el 41% frente al 29% y los de grado 4 en el 5% frente al 3%. Los acontecimientos de grado 5 se produjeron en 9 frente a 3 personas, y estuvieron relacionados con el tratamiento en dos casos frente a uno. Con la abiraterona, los problemas cardiovasculares como la hipertensión y las elevaciones de las aminotransferasas fueron más frecuentes.
Los autores del STAMPEDE concluyeron a partir de sus resultados que la ADT (+/- radioterapia) y la abiraterona constituyen un nuevo estándar de tratamiento para esta población.
¿Ha encontrado una nueva norma?
Si varias voces en el congreso sirven de algo -incluidos el autor principal del estudio, Nicholas James, y el responsable médico del congreso de la ASCO, Richard Schilsky-, la abiraterona está siendo ahora claramente impulsada hacia el escenario de primera línea. Tanto la tasa de supervivencia del 83% frente al 76% como la tasa de pacientes sin fracaso terapéutico del 75% frente al 45% al cabo de tres años son resultados extremadamente gratificantes e impresionantes del STAMPEDE, afirmó James. El hecho de que el riesgo de acontecimientos esqueléticos sintomáticos pudiera reducirse a más de la mitad al cabo de tres años con abiraterona complementa el balance positivo del principio activo. Todas las ventajas anteriores son compartidas por los datos de LATITUDE.
El principal grupo destinatario de la nueva norma serían los hombres con cáncer de próstata de alto riesgo recién diagnosticado y en estadio localmente avanzado o metastásico.
Algunas voces advirtieron del peligro de sacar conclusiones precipitadas. En cualquier caso, es un arma de doble filo. Los riesgos cardiovasculares deben tenerse muy en cuenta en la selección de pacientes: parte de la mejora de la mortalidad por cáncer puede deberse a que las muertes se desplazan hacia las enfermedades cardiacas (es decir, menos pacientes mueren de cáncer en general, ya que algunos sucumben antes a problemas cardiacos).
Ambos estudios se publicaron simultáneamente con el congreso en la revista New England Journal of Medicine [2,3].
Tumores del sistema biliar – innovador también en este caso
Los tumores del sistema biliar son poco frecuentes, pero por desgracia también se asocian a un mal pronóstico. Sólo una quinta parte de los pacientes son aptos para un enfoque curativo, es decir, la resección quirúrgica, en el momento del diagnóstico. Incluso entonces, la supervivencia a 5 años sigue estando por debajo del 10%. Por primera vez, un estudio suficientemente amplio ha demostrado ahora una clara ventaja de supervivencia de la terapia adyuvante concomitante, concretamente con capecitabina.
El ensayo de fase III denominado BILCAP comparó la conducta de esperar y observar tras la cirugía radical con capecitabina 1250 mg/m2 en los días 1-14 cada 21 días durante ocho ciclos. En el momento en que se planificó e inició el estudio, la observación era el procedimiento estándar tras la resección. Los investigadores eligieron la capecitabina porque puede administrarse en forma de comprimido y había demostrado su eficacia en el cáncer de páncreas (una enfermedad con un pronóstico igualmente malo). Los participantes fueron 447 pacientes del Reino Unido con un colangiocarcinoma o un cáncer de vesícula biliar completamente resecados, con un drenaje biliar/una función renal, hematológica y hepática adecuados, sin infección existente y un estado de rendimiento ECOG superior a 2 (mayoría 0 y 1). Los márgenes de resección eran dos tercios R0 y algo más de un tercio R1. Aproximadamente la mitad tenían ganglios linfáticos negativos.
La mediana de supervivencia global fue de 51 meses con terapia adyuvante y de 36 meses sin ella. El resultado no alcanzó la significación estadística (p=0,097). Sin embargo, algunos pacientes habían suspendido el fármaco del estudio antes de tiempo. Si nos fijamos en el grupo aún amplio de 430 pacientes que tomaron capecitabina durante seis meses como estaba previsto en el protocolo, la diferencia alcanza la significación: con la terapia adyuvante, las pacientes vivieron 53 meses, sin ella sólo 36 meses (reducción significativa del riesgo del 25%, p=0,028).
El efecto del fármaco fue tan claro que la falta de significación en la población general no puso en duda la eficacia, según los autores del estudio. Además, la balanza riesgo-beneficio se inclina claramente hacia el lado del beneficio, ya que la toxicidad de la terapia resultó ser menor de lo esperado. No hubo muertes asociadas al tratamiento, siendo la más común la erupción en manos y pies que se sabe que se produce con la capecitabina. La conclusión inequívoca de los investigadores: se ha encontrado un nuevo estándar de terapia adyuvante para los tumores biliares. Sobre todo porque la capecitabina está ampliamente disponible y se utiliza, por lo que los médicos ya tienen mucha experiencia con el fármaco.
No hay muchos ensayos de fase III de quimioterapia adyuvante en este contexto. El BILCAP es uno de los mayores y, por tanto, tiene una relevancia para la práctica clínica que no debe subestimarse. Otro estudio sobre gemcitabina y cisplatino está en curso, pero los resultados no se esperan hasta dentro de unos años. Hasta entonces, la capecitabina es claramente preferible, afirman los autores. Lo que queda por determinar es qué subtumores del sistema biliar se benefician especialmente. Para ello se están realizando los correspondientes análisis de subgrupos del BILCAP, ya que las localizaciones tumorales estaban distribuidas de forma relativamente uniforme en el estudio principal. Estudios anteriores sugieren una diferencia en función del tipo de tumor.
Fuente: Sociedad Americana de Oncología Clínica (ASCO) 2017; Reunión anual, 2-6 de junio de 2017, Chicago.
Literatura:
- Sweeney CJ, et al: Terapia quimiohormonal en el cáncer de próstata metastásico sensible a las hormonas. NEJM 2015; 373: 737-746.
- James ND, et al: Abiraterona para el cáncer de próstata no tratado previamente con terapia hormonal. NEJM 2017. DOI: 10.1056/NEJMoa1702900 [Epub ahead of print].
- Fizazi K, et al: Abiraterona más prednisona en el cáncer de próstata metastásico sensible a la castración. NEJM 2017. DOI: 10.1056/NEJMoa1704174 [Epub ahead of print].
InFo ONCOLOGÍA Y HEMATOLOGÍA 2017; 5(4): 37-40











