El esclarecimiento de la causa de las crisis epilépticas es esencial para tomar una decisión terapéutica. El gran número de preparados disponibles permite una terapia individual para la persona afectada. El riesgo de recidiva es un factor decisivo en la decisión de un tratamiento precoz.
La farmacoterapia ha sido la base del tratamiento de la epilepsia desde el descubrimiento de los primeros medicamentos anticonvulsivos eficaces. Todas las sustancias disponibles actualmente tienen un efecto puramente sintomático de supresión de las convulsiones y no influyen en la fisiopatología subyacente, por lo que deberíamos hablar de medicación anticonvulsiva y no antiepiléptica. Sin embargo, dado que no todos los ataques epilépticos son “convulsivos”, es decir, con sacudidas musculares, el término anticonvulsivos no es del todo exacto. El Instituto de Medicina (IOM) propone que las sustancias utilizadas para tratar las crisis epilépticas se denominen “medicación anticonvulsiva” [1].
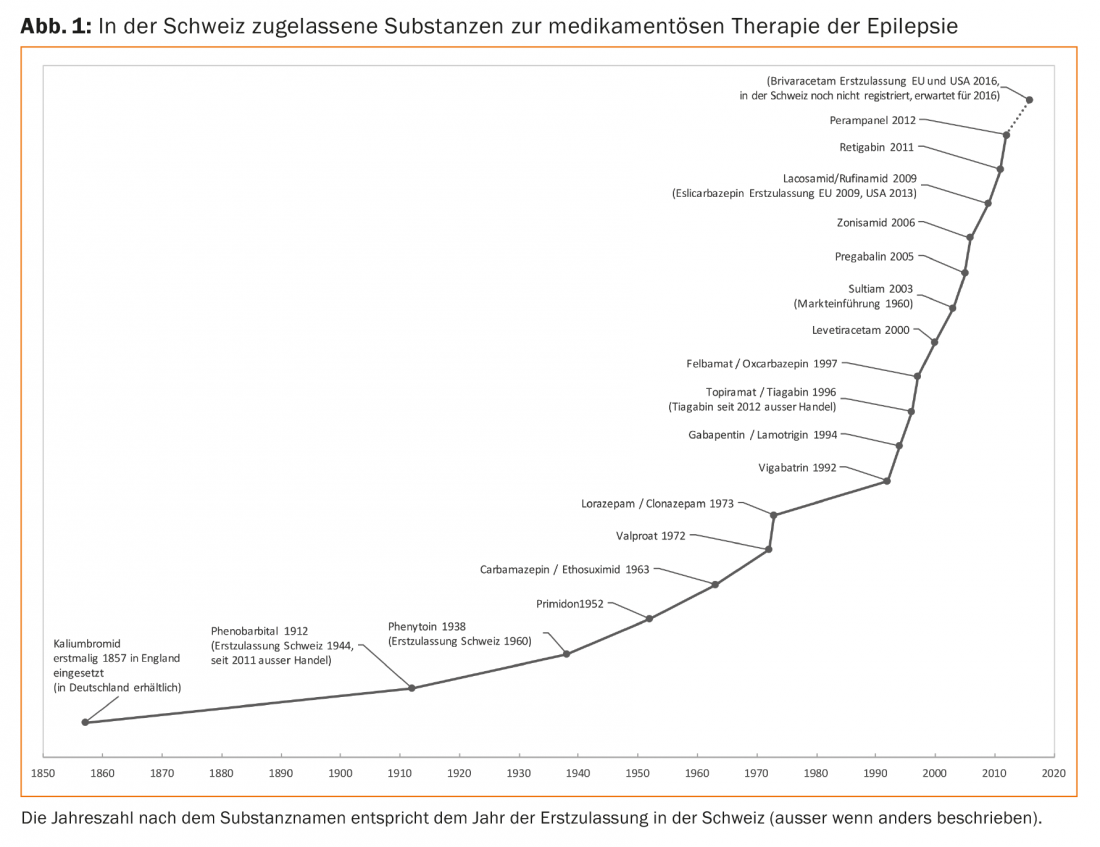
Además de las antiguas sustancias estándar aún en uso, como la fenitoína, la primidona, la carbamazepina, la etosuximida y el ácido valproico, existen otras sustancias (Fig. 1). A estas alturas, algunos de estos nuevos medicamentos anticonvulsivos llevan utilizándose mucho tiempo, por lo que sus ventajas e inconvenientes son bien conocidos.
¿Tratamiento ya después de la primera convulsión no provocada?
El esclarecimiento de la causa de las crisis epilépticas es esencial para tomar una decisión terapéutica. Según la última clasificación de la epilepsia de la Liga Internacional contra la Epilepsia (ILAE), el diagnóstico de epilepsia ya puede realizarse tras una primera crisis no provocada si, según los resultados de la aclaración correspondiente, existe un riesgo de recurrencia de una nueva crisis de al menos el 60% en diez años y el riesgo de recurrencia es, por tanto, igual de alto que tras dos crisis no provocadas.
Si existe un alto riesgo de recurrencia, según las directrices internacionales, como las de la Sociedad Alemana de Neurología, también puede iniciarse una terapia anticonvulsiva tras una primera crisis no provocada. En general, sin embargo, suele ser una decisión terapéutica individual que también tiene en cuenta la actitud del paciente ante la medicación, el miedo a los efectos secundarios y también la necesidad de seguridad del paciente (y de sus familiares) o su disposición a asumir riesgos [2].
Dos grandes estudios multicéntricos (FIRST – First Seizure Trail Group; MESS – Multicentre Epilepsy and Single Seizure Study) investigaron el riesgo de recurrencia y el pronóstico a largo plazo con el tratamiento inmediato de las crisis frente al tardío [3–6]. En ambos estudios, se demostró que el tratamiento inmediato tras una primera crisis no provocada reducía el riesgo de recurrencia en un 50% y un 30% respectivamente; sin embargo, la mitad de los participantes en el estudio no sufrieron una segunda crisis. El inicio precoz del tratamiento no tuvo ningún efecto sobre la frecuencia de las crisis al cabo de tres o cinco años en ninguno de los dos estudios.
Según los datos del estudio MESS, el número necesario a tratar (NNT) para prevenir una nueva crisis epiléptica es de 14 tras una primera crisis y de 5 tras una segunda crisis epiléptica. El pronóstico a largo plazo de la terapia no se deteriora si se espera a una posible segunda crisis epiléptica [4,5].
En general, muchos estudios han demostrado que el riesgo de recurrencia es mayor poco después del primer ataque. El 80-90% de los pacientes que vuelven a tener convulsiones sufren una recaída en los dos primeros años. Sin embargo, los resultados de los estudios disponibles en la actualidad suelen ser difíciles de trasladar a la rutina clínica actual porque, por ejemplo, en el ensayo MESS no se realizaron imágenes estructurales en todos los participantes del estudio. Así lo exigen ahora las directrices y es también práctica habitual, ya que las lesiones cerebrales estructurales conllevan un mayor riesgo de recurrencia y pueden ser, por tanto, motivo de terapia anticonvulsiva precoz [7–9].
Sin embargo, el estado actual de los estudios no permite hacer una recomendación general sobre si la terapia anticonvulsiva está ya indicada tras la primera crisis epiléptica. Sin embargo, hay hallazgos de exámenes resp. Diagnósticos para los que debe suponerse un mayor riesgo de recurrencia y que, por tanto, son motivo de una farmacoterapia más temprana (tab. 1).

Terapia anticonvulsiva inicial
Generalmente se recomienda empezar con una monoterapia y dosificarla primero. Elegir un fármaco para la terapia inicial no es fácil, dado el gran número de fármacos disponibles. Sin embargo, hay ciertos criterios que deben tenerse en cuenta en el proceso de selección: Tipo de crisis, clasificación del síndrome epiléptico, sexo, enfermedades concomitantes, medicación concomitante y urgencia del tratamiento. En general, alrededor del 60-70% de los pacientes adultos quedan libres de crisis con la primera medicación anticonvulsiva administrada. A la hora de elegir una sustancia, también deben tenerse en cuenta la tolerabilidad y la influencia de las comorbilidades, ya que alrededor del 60% de los pacientes tienen que tomar la medicación para controlar las convulsiones durante el resto de su vida.
Según las directrices, todos los fármacos anticonvulsivantes son adecuados para la monoterapia inicial en epilepsias focales, excepto la etosuximida, que sólo se utiliza en casos de ausencias (crisis de petit mal).
La lamotrigina y el levetiracetam han demostrado ser igual de eficaces; se prefieren a la carbamazepina debido a su mejor tolerabilidad [10]. El levetiracetam, en particular, se utiliza a menudo en la práctica clínica habitual porque no es necesario dosificarlo durante mucho tiempo, no induce enzimas y provoca menos interacciones con otros fármacos. El levetiracetam y la lamotrigina apenas suelen provocar crisis en las epilepsias generalizadas idiopáticas (EGI), a diferencia, por ejemplo, de la carbamazepina. En el reciente gran ensayo controlado aleatorizado SANAD (Standard And New Antiepileptic Drugs), la lamotrigina fue superior a la carbamazepina, la gabapentina y el topiramato en cuanto al tiempo hasta la interrupción del tratamiento y los efectos secundarios no tolerables en epilepsias focales (brazo A) [11]. En otro estudio, la pregabalina fue menos eficaz en una comparación directa con la lamotrigina [12].
Las monoterapias iniciales adecuadas para la epilepsia generalizada o no clasificada incluyen el valproato, la lamotrigina y el topiramato, que se compararon en el brazo B del estudio SANAD [13]. El valproato mostró mejor eficacia que la lamotrigina y mejor tolerabilidad que el topiramato. Para lograr la ausencia de convulsiones durante un año, el topiramato era comparable al valproato.
Tratamiento de mujeres en edad fértil
La anticoncepción fiable está indicada para las mujeres en edad fértil tratadas con anticonvulsivos. Debe prestarse atención a las interacciones clínicamente relevantes de los anticonceptivos con los medicamentos anticonvulsivos (por ejemplo, con la lamotrigina), ya que ambos pueden debilitar el efecto de los medicamentos anticonvulsivos y viceversa. Para la mayoría de las sustancias más nuevas, no existen actualmente datos suficientes que permitan una evaluación definitiva de un posible efecto sobre el feto. En un amplio estudio de registro, se descubrió que las mujeres tratadas con medicamentos anticonvulsivos durante el embarazo presentaban un riesgo muy bajo de malformaciones congénitas importantes del 4,2% (tasa de malformaciones del 2-4% en la población normal) [14]. En un estudio danés [15] no se demostró un mayor riesgo de defectos congénitos graves al tomar un medicamento anticonvulsivo más reciente durante el embarazo. En un estudio publicado en 2014, el topiramato se asoció con un posible mayor retraso del crecimiento en el feto [16].
El valproato debe utilizarse con gran precaución en mujeres en edad fértil. Las razones son el riesgo teratogénico y el efecto negativo sobre el desarrollo cognitivo a largo plazo de los niños expuestos al valproato en el útero [17]. Basándose en los datos actuales, la recomendación es utilizar valproato sólo si es absolutamente necesario y entonces en forma de liberación lenta y a una dosis lo más baja posible, preferiblemente por debajo de 1000 mg/d.
Tratamiento posterior tras un tratamiento inicial infructuoso
Se habla de farmacorresistencia cuando no se consigue una ausencia sostenida de crisis tras intentos adecuados de tratamiento con dos fármacos antiepilépticos tolerados, adecuados y a dosis suficientemente altas (ya sea en monoterapia o en combinación). A continuación, el diagnóstico de epilepsia debe revisarse críticamente de nuevo, por ejemplo con un vídeo-EEG de 24 horas, y también deben buscarse diagnósticos diferenciales. También debe considerarse a tiempo una posible cirugía de la epilepsia. Las posibles causas de resistencia al tratamiento se enumeran en la tabla 2.

En principio, todas las sustancias aprobadas son concebibles para un tratamiento combinado. Se recomienda precaución con la administración simultánea de bloqueantes de los canales de sodio, ya que puede provocar efectos secundarios más graves en el sistema nervioso central. Las nuevas sustancias aprobadas para la terapia combinada, algunas de las cuales tienen un mecanismo de acción diferente, como la lacosamida, la rufinamida, la retigabina y el perampanel, permiten albergar la esperanza de que, en casos individuales, aún pueda conseguirse la ausencia de convulsiones mediante efectos sinérgicos y aditivos en casos de farmacorresistencia.
Uso de genéricos
La terapia inicial puede llevarse a cabo sin problemas con un preparado genérico. Los medicamentos genéricos también pueden utilizarse o sustituirse para la epilepsia que aún no ha sido tratada con éxito. Debido a la biodisponibilidad variable y al consiguiente aumento del riesgo de convulsiones, debe rechazarse el cambio del fármaco originario al genérico, del genérico al originario o incluso de un genérico a otro en pacientes sin convulsiones [18].
Finalización de la terapia
Hay pocos datos fiables sobre la cuestión de dejar la medicación tras muchos años sin convulsiones. La práctica clínica es continuar con la medicación mientras no se produzcan efectos secundarios graves. Sólo se recomienda suspenderlo cuando la situación desencadenante de la crisis ya no esté presente. Además, algunas formas de epilepsia infantil y adolescente pueden “salir”. Antes de interrumpir la terapia, la persona afectada debe ser informada sobre las posibles consecuencias de dejarla.
Literatura:
- Epilepsia en todo su espectro: promover la salud y la comprensión – Instituto de Medicina [Internet], 2012. www.iom.edu/epilepsy
- Elger CE: Primera crisis epiléptica y epilepsias en la edad adulta – ¿Qué hay de nuevo? Las recomendaciones más importantes de un vistazo. Definición y clasificación 2016; 1-23.
- Grupo de prueba de la primera incautación (Grupo FIR.S.T.): Ensayo clínico aleatorizado sobre la eficacia de los fármacos antiepilépticos para reducir el riesgo de recaída tras una primera crisis tónico-clónica no provocada. Neurología 1993; 43(3 Pt 1): 478-483.
- Musicco M, et al: El tratamiento de la primera crisis tónico-clónica no mejora el pronóstico de la epilepsia. Grupo de prueba de la primera incautación. Neurología 1997; 49(4): 991-998.
- Marson A, et al: Tratamiento farmacológico antiepiléptico inmediato frente al diferido para la epilepsia precoz y las crisis únicas: un ensayo controlado aleatorizado. Lancet 2005; 365(9476): 2007-2013.
- Kim LG, et al: Predicción del riesgo de recurrencia de crisis tras una única crisis y epilepsia precoz: Resultados adicionales del ensayo MESS. Lancet Neurol 2006; 5(4): 317-322.
- Eickhoff SB, et al.: Conectividad anatómica y funcional de las áreas citoarquitectónicas dentro del opérculo parietal humano. J Neurosci 2010; 30(18): 6409-6421.
- Hauser W, et al: Recurrencia de convulsiones tras una 1ª convulsión no provocada: un seguimiento ampliado. Neurología 1990; 40(8): 1163-1170.
- Krumholz A, et al: Directriz basada en la evidencia: Manejo de una primera crisis no provocada en adultos: Informe del Subcomité de Desarrollo de Directrices de la Academia Americana de Neurología y la Sociedad Americana de Epilepsia. Neurología 2015 oct; 85(17): 1526-1527.
- Rosenow F, et al: The LaLiMo Trial: lamotrigine compared with levetiracetam in the initial 26 weeks of monotherapy for focal and generalised epilepsy – an open-label, prospective, randomised controlled multicenter study. J Neurol Neurosurg Psychiatry 2012; 83(11): 1093-1098.
- Marson AG, et al: The SANAD study of effectiveness of carbamazepine, gabapentin, lamotrigine, oxcarbazepine, or topiramate for treatment of partial epilepsy: an unblinded randomised controlled trial. Lancet 2007; 369(9566): 1000-1015.
- Kwan P, et al: Eficacia y seguridad de la pregabalina frente a la lamotrigina en pacientes con crisis parciales recién diagnosticadas: un ensayo de fase 3, doble ciego, aleatorizado y de grupos paralelos. Lancet Neurol 2011; 10(10): 881-890.
- Marson AG, et al: The SANAD study of effectiveness of valproate, lamotrigine, or topiramate for generalised and unclassifiable epilepsy: an unblinded randomised controlled trial. Lancet 2007; 369(9566): 1016-1026.
- Morrow J, et al: Riesgos de malformaciones de los fármacos antiepilépticos en el embarazo: un estudio prospectivo del Registro de Epilepsia y Embarazo del Reino Unido. J Neurol Neurosurg Psychiatry 2006; 77(2): 193-198.
- Mølgaard-Nielsen D, Hviid A: Los fármacos antiepilépticos de nueva generación y el riesgo de defectos congénitos graves. JAMA 2011; 305(19): 1996-2002.
- Veiby G, et al: Restricción del crecimiento fetal y defectos congénitos con fármacos antiepilépticos nuevos y antiguos durante el embarazo. J Neurol 2014; 261(3): 579-588.
- Meador KJ, et al: Exposición fetal a fármacos antiepilépticos y resultados cognitivos a la edad de 6 años (estudio NEAD): un estudio observacional prospectivo. Lancet Neurol 2013; 12(3): 244-252.
- Rueegg S, et al.: Uso de fármacos antiepilépticos genéricos en la terapia de la epilepsia – Declaración de la Liga Suiza contra la Epilepsia (SLgE). Swiss Arch for Neurol and Psychiatr 2012; 163(3): 104-106.
InFo NEUROLOGÍA Y PSIQUIATRÍA 2016; 14(3): 8-11