La quimioterapia neoadyuvante siempre es posible si también está indicada la quimioterapia adyuvante. Durante la quimioterapia neoadyuvante, debe documentarse la respuesta a la terapia para poder modificar el tratamiento en caso necesario. La quimioterapia neoadyuvante permite la cirugía dentro de nuevos límites. Con la quimioterapia neoadyuvante se puede ganar tiempo sin retrasar la terapia.
La quimioterapia para el carcinoma de mama se administra cada vez más antes de la cirugía como terapia neoadyuvante en toda Europa. En Suiza también se observa una tendencia en este sentido. Este artículo se centrará en las indicaciones de la quimioterapia neoadyuvante y sus beneficios.
Conservación de la mama en lugar de mastectomía
Incluso hoy en día, la mastectomía sigue siendo necesaria en alrededor del 25% de las pacientes con carcinoma de mama porque el tamaño del tumor en relación con el tamaño de la mama no permite ningún otro procedimiento que sea oncológicamente seguro. En estos casos, la quimioterapia neoadyuvante puede reducir la extensión de la cirugía si se consigue una buena respuesta, ya que la cirugía puede realizarse dentro de unos nuevos límites sin afectar a la supervivencia global ni al control locorregional [1].
Antes de iniciar la terapia, el tumor debe marcarse con una pinza para poder localizar el lecho tumoral durante la cirugía en caso de remisión completa tras la quimioterapia neoadyuvante.
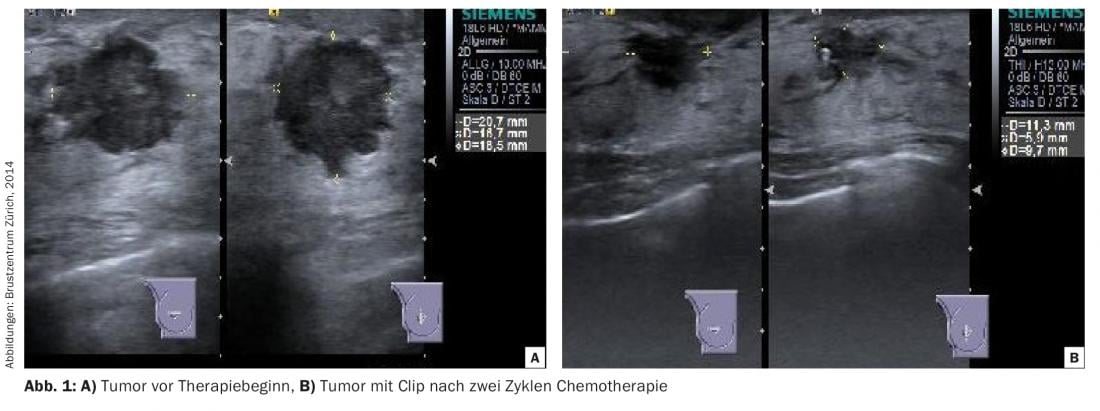
Durante la terapia, debe documentarse la respuesta (“monitorización de la respuesta”). La ecografía suele ser la más adecuada para este fin, aunque la delimitación del tumor residual puede resultar difícil debido a la fibrosis tisular (Fig. 1) . En el caso de los carcinomas lobulillares o multicéntricos, que a menudo quedan ocultos en su extensión global en las imágenes por mamografía y ecografía, puede ser necesario realizar controles de avance mediante resonancia magnética.
Descenso axilar
En axilas clínicamente negativas, suele realizarse una linfonodectomía centinela antes (posiblemente con implantación de un port-à-cath), pero a veces también después de la quimioterapia neoadyuvante. Si la axila es clínicamente positiva, la metástasis se confirma primero histológicamente mediante una biopsia en sacabocados. El procedimiento posterior se ha definido en el estudio SENTINA y ACOSOG Z1071 en la Conferencia de Consenso de St. Gallen 2015.
Tras la estadificación descendente de una axila inicialmente afectada, la linfonodectomía centinela después de la quimioterapia neoadyuvante es un procedimiento adecuado. El marcaje centinela debe realizarse con azul patente además del radiocoloide. La fiabilidad de la linfonodectomía centinela en esta situación depende del número de ganglios linfáticos extirpados. Sólo con la extirpación de tres ganglios linfáticos libres de tumor la tasa de falsos negativos (FNR) es comparable a la FNR con cirugía primaria, y puede omitirse la linfonodectomía axilar. Por otro lado, si uno o dos ganglios linfáticos centinela están afectados tras la quimioterapia neoadyuvante, debe realizarse una linfonodectomía axilar [2–4].
Carcinoma inflamatorio de mama
Un rasgo característico del carcinoma inflamatorio de mama es su propagación a lo largo de las vías linfáticas, lo que significa que el potencial de metástasis es elevado. La quimioterapia neoadyuvante es obligatoria en esta situación. La respuesta a la terapia es un factor importante para el pronóstico del paciente. En cuanto a la cirugía, no ha habido ningún cambio hasta la fecha; la mastectomía es la regla de oro incluso en caso de remisión clínica completa.
Pruebas in vivo
Durante la terapia, se realizan controles de imagen, normalmente ecográficos, para documentar la respuesta del tumor. Si resulta que el tumor no responde o apenas responde a la terapia, se puede cambiar el régimen terapéutico (“tratamiento guiado por la respuesta”), lo que mejora el pronóstico de los pacientes con carcinomas menos agresivos [5].
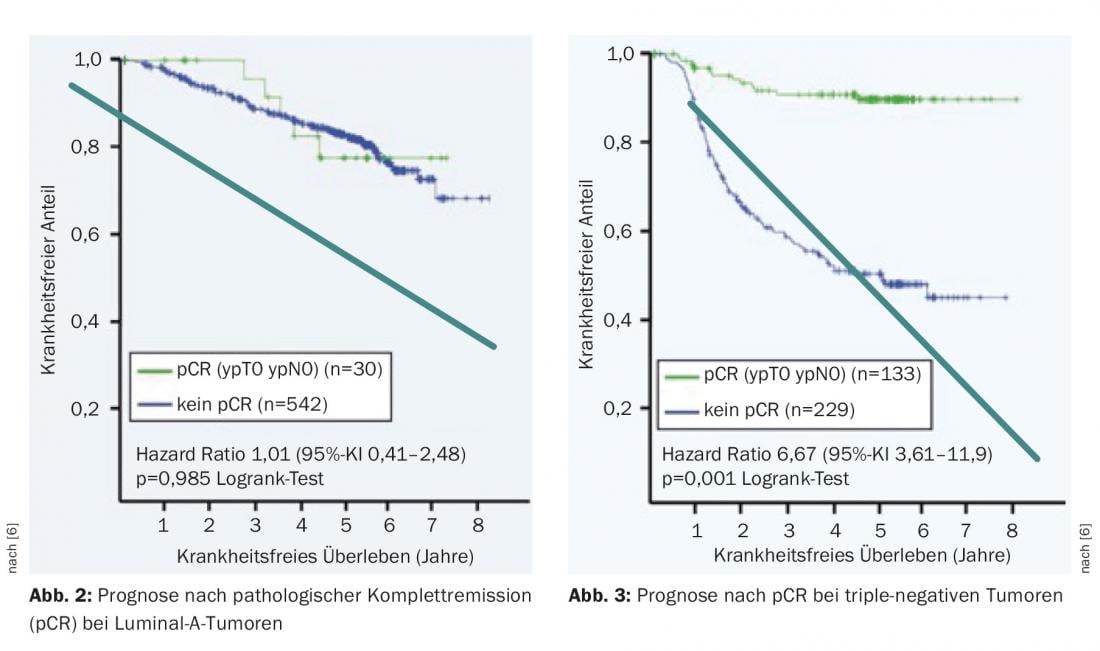
En el caso de la respuesta tumoral, se distingue entre remisión parcial y completa. La remisión patológica completa (pCR) es un factor pronóstico importante en los tipos tumorales más agresivos. En las pacientes con carcinomas con receptores hormonales positivos y Her2 negativo (Luminal-A), una pCR es insignificante desde el punto de vista pronóstico (Fig. 2) . Por el contrario, las pacientes con tumores triples negativos tienen la posibilidad de un resultado significativamente mejor en términos de supervivencia libre de enfermedad (Fig. 3) . Además, es motivador para la paciente si puede observar cómo el tumor se va reduciendo. Este efecto psicológico conduce a un mejor cumplimiento para soportar la estresante terapia.
Ahorro de tiempo
Algunas situaciones requieren un margen de tiempo antes de la operación en el que se puedan hacer más aclaraciones. Cada vez se realizan más exámenes genéticos que requieren mucho tiempo, con posibles consecuencias para el procedimiento quirúrgico (por ejemplo, mastectomía en lugar de terapia conservadora de la mama, mastectomía bilateral). El resultado de una prueba genética suele tardar tres semanas en estar disponible. En el caso de una intervención quirúrgica planificada principalmente, se produce un retraso significativo en la terapia.
Las posibles consecuencias de una prueba genética positiva deben tenerse muy en cuenta y representan un factor de estrés nada desdeñable para la paciente, por lo que resulta valioso disponer de un margen de tiempo de tres a cuatro meses antes de la operación. Además, si se planea una mastectomía (por ejemplo, en caso de carcinoma multicéntrico o inflamatorio), el tiempo ganado puede utilizarse para evaluar la reconstrucción mamaria.
Conclusión
En resumen, la quimioterapia debe considerarse siempre antes de la cirugía si también está indicada en el postoperatorio. Las ventajas residen en la determinación y el seguimiento de la respuesta con posible ajuste de la terapia en ausencia de remisión, la reducción del tamaño del tumor con posible conservación de la mama en caso de mastectomía planificada previamente y el tiempo ahorrado para aclaraciones preoperatorias (por ejemplo, prueba genética). En el carcinoma inflamatorio, la quimioterapia neoadyuvante es obligatoria.
A pesar de las ventajas mencionadas, la quimioterapia en el contexto neoadyuvante no proporciona una ventaja de supervivencia sobre la terapia adyuvante. En futuros estudios deberá examinarse más a fondo el valor de la terapia neoadyuvante.
Literatura:
- Mieog JS: Quimioterapia neoadyuvante para el cáncer de mama precoz. Expert Opin Pharmacother 2009; 10(9): 1423-1434.
- Boughey JC, et al: Cirugía del ganglio linfático centinela tras quimioterapia neoadyuvante en pacientes con cáncer de mama con ganglios positivos: el ensayo clínico ACOSOG Z1071 (Alliance). JAMA 2013; 310: 1455-1461.
- Kuehn T, et al: Biopsia del ganglio linfático centinela en cáncer de mama antes y después de la quimioterapia neoadyuvante (SENTINA): un estudio prospectivo de cohortes multicéntrico. Lancet Oncol 2013; 14: 609-618.
- Boughey JC, et al: Métodos que influyen en la tasa de falsos negativos de la cirugía del ganglio linfático centinela en pacientes con cáncer de mama con ganglios positivos (T0-T4, N1-2) que reciben quimioterapia neoadyuvante – Resultados de un ensayo prospectivo – ACOSOG Z1071 (Alianza). Simposio sobre el cáncer de mama de San Antonio 2014, P2-01-02.
- von Minckwitz, G: Actualización sobre la terapia neoadyuvante/preoperatoria del cáncer de mama: experiencias del Grupo Alemán de Mama. Curr Opin Obstet Gynecol 2013; 25(1): 66-73.
- von Minckwitz G, et al: La quimioterapia neoadyuvante adaptada por respuesta provisional mejora la supervivencia global de las pacientes con cáncer de mama primario: resultados del ensayo GeparTrio. Cancer Res 2011; 71(Suppl 24): 103s.
InFo ONCOLOGÍA Y HEMATOLOGÍA 2016; 4(1): 16-18