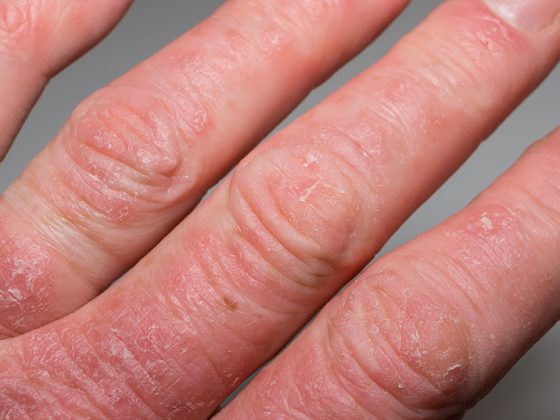
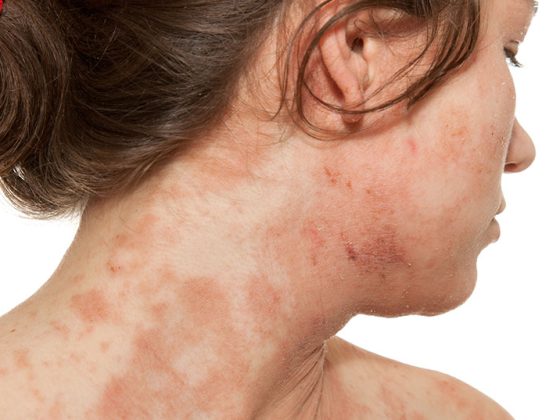
En el peor de los casos, la enfermedad arterial periférica (EAP) puede provocar una oclusión vascular y hacer necesarias las amputaciones; el riesgo de infarto de miocardio o de ictus también aumenta considerablemente en los afectados. Sin embargo, este grave trastorno circulatorio de los vasos sanguíneos que irrigan las extremidades a menudo pasa desapercibido y no se trata adecuadamente. Las posibilidades terapéuticas son múltiples.
Los estudios demuestran que los pacientes con PAOD simple están infratratados en lo que respecta a sus factores de riesgo y enfermedades concomitantes, afirma el doctor Jan-Tobias Hensel, médico jefe de la Clínica Médica Universitaria del Hospital Cantonal de Baselland [1,2]. Esto es así a pesar de que la prevalencia de la DAEP sintomática o manifiesta en pacientes de 45 a 75 años en la población general es del 8,2% (hombres) y del 5,5% (mujeres) [3]. Entre los grupos de riesgo se encuentran las personas mayores de 65 años y los pacientes mayores de 50 años con factores de riesgo de arteriosclerosis, es decir, diabetes mellitus, consumo de nicotina, dislipidemia, hipertensión arterial o antecedentes familiares positivos. También incluye a pacientes de cualquier edad con diabetes mellitus y otro factor de riesgo de aterosclerosis, así como a pacientes con aterosclerosis conocida en otro órgano, como enfermedad arterial coronaria, estenosis carotídea, estenosis subclavia, estenosis de la arteria renal o estenosis de la arteria mesentérica. En los pacientes mayores de 65 años, el 21% tiene un índice tobillo-brazo (ITB) <0,9 o una DAVDp manifiesta. Además, la PAOD se asocia a un aumento significativo de la mortalidad tanto en pacientes sintomáticos como asintomáticos [4].
Historia clínica y examen clínico
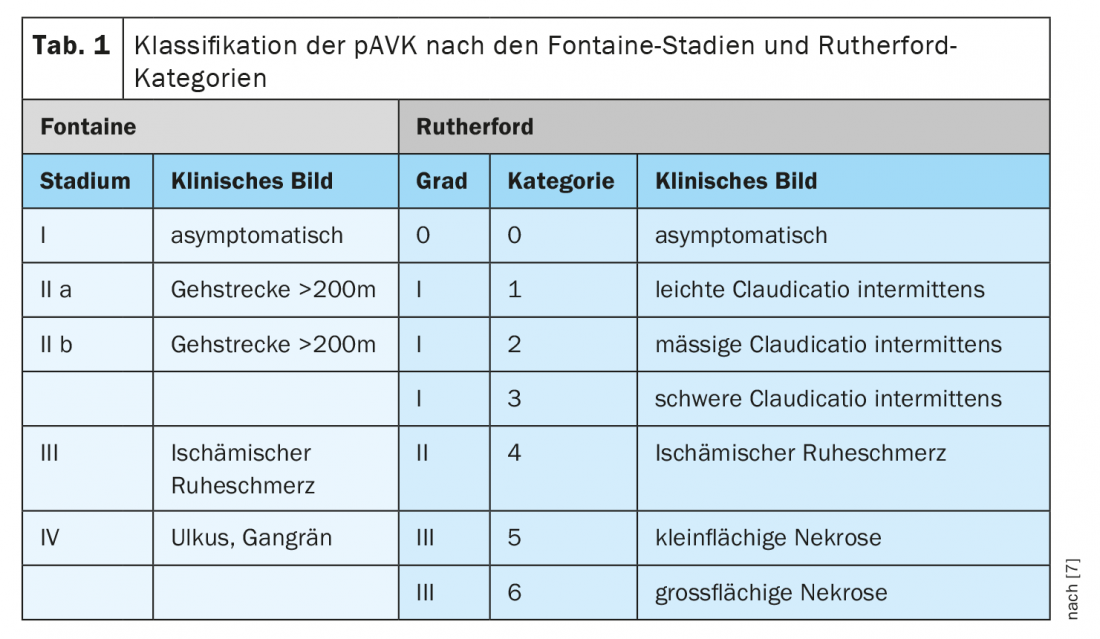
La arteriopatía periférica está causada por el estrechamiento de las arterias de las extremidades o de la aorta, normalmente debido a depósitos arterioscleróticos. Una serie de influencias pueden favorecer estos procesos, como el tabaquismo, la obesidad y la falta de ejercicio. Clásicamente, la DAVDp se caracteriza por la claudicación intermitente, la llamada enfermedad de escaparate, como signo de restricción de la circulación periférica. Se produce una sensación de cansancio, así como tensión, calambres musculares o dolor en las extremidades inferiores, que pueden reproducirse con el esfuerzo físico y mejorar de nuevo con el reposo constante [5]. Aunque la EVPp también se conoce coloquialmente como “enfermedad de escaparate”, hay que tener en cuenta que aproximadamente dos tercios de los pacientes con EVPp confirmada no presentan los síntomas clásicos de claudicación, sino que tienen síntomas “atípicos” o no presentan síntomas [6]. La clasificación de la DAVDp según Fontaine o Rutherford va desde la DAVDp asintomática, pasando por la limitación de la marcha, hasta el dolor isquémico en reposo y las manifestaciones necróticas (Tab. 1) [7] Por definición, el dolor isquémico en reposo se produce sobre >2 semanas, especialmente por la noche, lo que puede explicarse por una disminución del gasto cardíaco y la consiguiente reducción de la perfusión de la extremidad.
Durante el examen clínico, no deben despreciarse el estado del pulso y el sonido de flujo. Aunque la palpación del pulso por sí sola, con una sensibilidad del 20%, no es suficiente para detectar una EAP, debe comprobarse el estado del pulso en los territorios vasculares inguinal, poplíteo, tibial y pedal. La sensibilidad de los ruidos de flujo es del 75%, la especificidad del 40% en combinación con la palpación del pulso.
Otro examen clínico para el esclarecimiento diagnóstico de la FAVDp es la prueba de posicionamiento según Ratschow, que proporciona información inicial sobre la extensión funcional de la enfermedad oclusiva. La prueba de Ratschow puede ser muy informativa en términos de diagnóstico diferencial, explica el Dr. Hensel. Se coloca al paciente boca arriba y se le pide que levante las piernas verticalmente y realice movimientos circulares en la articulación del tobillo durante dos minutos. A continuación, se pide al paciente que se siente, con las piernas colgando libremente de la camilla. En los pacientes sanos, no hay dolor durante los movimientos, después de sentarse, el pie se enrojece en cinco segundos y las venas se llenan en los cinco segundos siguientes. Si hay pAVD, la pierna afectada ya se desprende durante la fase de movimiento. Después de sentarse, se produce un retraso en el enrojecimiento de la pierna afectada y, en consecuencia, las venas se llenan con retraso.
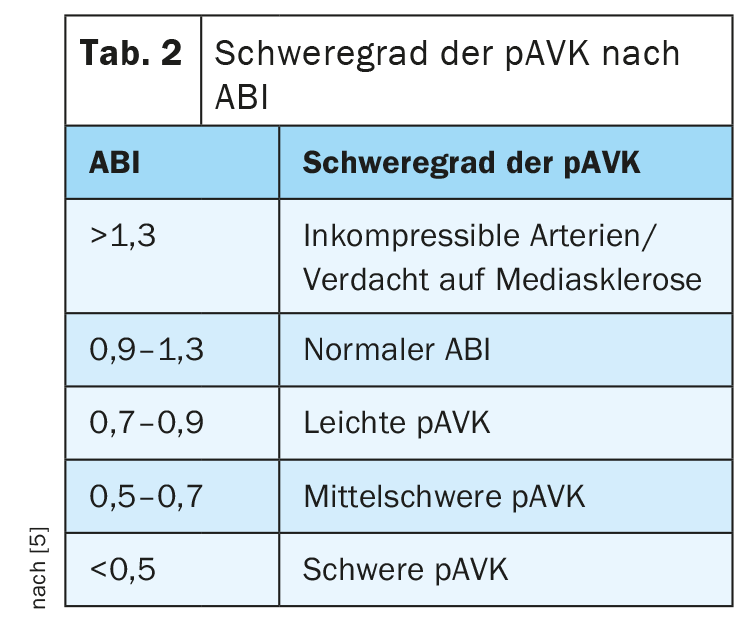
El índice tobillo-brazo (ITB) también puede utilizarse para evaluar el riesgo cardiovascular y la progresión de la PAOD, aunque los valores patológicos tienen una alta especificidad pero una baja sensibilidad. En pacientes vascularmente sanos, el ITB se sitúa entre 0,9 y 1,3; un valor de ITB inferior a 0,9 es patognomónico de una DAVDp (Tab. 2) [8].
En caso de sospecha clínica, debe realizarse una clarificación de urgencia
Los signos clínicos de la isquemia externa aguda incluyen las 6 P de Pratt: dolor, palidez, falta de pulso, parálisis, parestesia y postración; y etiología cardiaca o arterial, u oclusión de reconstrucciones arteriales. En estos casos, debe realizarse una revascularización intervencionista o quirúrgica lo antes posible. Idealmente, se inhibe la progresión de la arteriosclerosis, y la terapia también pretende reducir el riesgo de eventos vasculares periféricos, reducir los eventos cardiovasculares y cerebrovasculares, reducir el dolor y mejorar la capacidad de recuperación, el rendimiento al caminar y la calidad de vida. De acuerdo con la directriz S3, tanto la cirugía vascular como la reconstrucción arterial endovascular deben ser el resultado de una consideración interdisciplinar razonable, adecuada al estadio, del esfuerzo, el riesgo y el acontecimiento [7].
El entrenamiento regular a pie aporta beneficios
El entrenamiento estructurado para caminar es la terapia no farmacológica más importante para el tratamiento coherente de los factores de riesgo cardiovascular, así lo han demostrado varias revisiones Cochrane [7]. Además, el resultado funcional a largo plazo del entrenamiento de la marcha por sí solo no es inferior a las intervenciones vasculares en pacientes con claudicación [9]. Se observa un aumento significativo del rendimiento de la marcha en la cinta rodante y una disminución de la claudicación tras el entrenamiento de la marcha [10]. No obstante, hay que señalar que la eficacia del entrenamiento diario de la marcha sin supervisión es significativamente peor que la eficacia de un programa de entrenamiento estructurado y supervisado.
Medidas básicas de un vistazo
Cambios en el estilo de vida: Los fundamentos del tratamiento básico incluyen, sobre todo, el ejercicio, la pérdida de peso, la optimización de la dieta y el entrenamiento para caminar de forma independiente o estructurada. Además, en cada visita al médico debe hacerse una recomendación para dejar la nicotina, si es necesario con el apoyo de medicación.
Hipertensión arterial: En la hipertensión, el objetivo de presión arterial debe ser <140/90 mmHg, si se tolera la terapia intensificada también muestra beneficios, como se demostró por ejemplo en el estudio SPRINT (“Systolic Pressure Intervention Trial”) [13]. En caso contrario, deben utilizarse preferentemente inhibidores de la ECA y antagonistas de los ITIA [7].
Dislipidemia: En caso de dislipidemia, el objetivo de LDL debe ser <1,4 mmol/l². Para los pacientes que no alcanzan los niveles objetivo de LDL a pesar del tratamiento con estatinas tolerado al máximo, los inhibidores de la PCSK9 pueden considerarse otra opción de tratamiento. [12]. No obstante, debe presentarse una solicitud al médico responsable (angiología, cardiología, endocrinología, nefrología, neurología). Además, es necesario que el paciente reciba instrucciones especiales para su aplicación.
Diabetes mellitus: La diabetes mellitus también debe tener un corredor objetivo de HbA1c en función de la edad/comorbilidades (6,5-7%/<7,5%). Y debe prestarse atención al cuidado meticuloso de los pies y, si es necesario, utilizar plantillas que alivien la presión, especialmente en casos de polineuropatía.
Arteriosclerosis: En la arteriosclerosis, debe administrarse monoterapia con aspirina o clopidogrel debido a la agregación plaquetaria. También está disponible Xarelto vascular® (2,5 mg 1-0-1 además de asperina). Xarelto vascular® es una opción válida cuando ya no es necesaria la terapia antiplaquetaria dual. Especialmente los pacientes jóvenes de alto riesgo <65 años se benefician de esta medicación. Los pacientes mayores >75 años tienen un mayor riesgo de hemorragia [11].
Literatura:
- Hensel JT: Enfermedad oclusiva arterial periférica. Jornadas de formación para médicos de familia, 08.09.2021.
- Hirsch AT, et al: Lagunas en el conocimiento público de la enfermedad arterial periférica: la primera encuesta nacional de concienciación pública sobre la arteriopatía periférica. Circulation 2007, doi: 10.1161/CIRCULATIONAHA.107.725101.
- Kröger K, et al: Prevalencia de la enfermedad arterial periférica – resultados del estudio de recuerdo Heinz Nixdorf. Eur J Epidemiol 2006, doi: 10.1007/s10654-006-0015-9.
- Diehm C, et al: Alta mortalidad por todas las causas en pacientes con enfermedad arterial periférica en atención primaria: resultados a cinco años del estudio getabi. Circulation 2007.
- Gerhard-Herman MD, et al: 2016 AHA/ACC Guideline on the Management of Patients with Lower Extremity Peripheral Artery Disease: Executive Summary. Vasc Med 2017, doi: 10.1177/1358863X17701592.
- Hirsch, AT et al: Detección, concienciación y tratamiento de la enfermedad arterial periférica en atención primaria. JAMA 2001, doi: 10.1001/jama.286.11.1317.
- Deutsche Gesellschaft für Angiologie – Gesellschaft für Gefässmedizin: S3-Leitline zur Diagnostik, Therapie und Nachsorge der peripheren arteriellen Verschlusskrankheit. www.awmf.org/uploads/tx_szleitlinien/065-003l_S3_PAVK_periphere_arterielle_Verschlusskrankheit_2020-05.pdf.
- Jeanneret-Gris C: Enfermedad arterial oclusiva periférica (EAP). El diagnóstico diferencial más importante en el dolor de piernas. Flebología 2014, doi: 10.12687/phleb2241-6-2014.
- Nordanstig J. et al: Rendimiento de la marcha y calidad de vida relacionada con la salud tras el tratamiento quirúrgico o endovascular invasivo frente al no invasivo para la claudicación intermitente. Eur J Vasc Endovasc Surg 2011, doi: 10.1016/j.ejvs.2011.02.019. Epub 2011 mar 11.
- Nicolai SP, et al: Ensayo clínico aleatorizado multicéntrico de terapia de ejercicio supervisada con o sin retroalimentación frente a consejos de marcha para la claudicación intermitente. J Vasc Surg 2010, doi: 10.1016/j.jvs.2010.02.022. Epub 2010 May 15.
- Steffel J, et al: Swiss expert report on the practical use of rivaroxaban 2.5 mg 2× daily plus ASA for the treatment of patients with coronary artery disease (CAD) and/or peripheral arterial disease. https://dreicast.com/wp-content/uploads/2021/01/3_Schweizer-Experten-Bericht_Xarelto-vascular.pdf.
- Gencer B, et al.: Impacto previsto de la aplicación de los nuevos criterios de las directrices sobre colesterol de la AHA/ACC de 2013 en la consecución del objetivo lipídico recomendado tras los síndromes coronarios agudos. Aterosclerosis 2015, doi: 10.1016/j.atherosclerosis.2014.12.049.
- Wright JT Jr, et al: Ensayo aleatorizado de control intensivo frente a control estándar de la presión arterial. Grupo de investigación SPRINT. N Engl J Med 2015; 373(22): 2103-2116.
PRÁCTICA GP 2021; 16(12): 26-27