El anticuerpo monoclonal dupilumab bloquea el componente receptor común de la interleucina (IL)-4 y la IL-13, los motores centrales de la inflamación de tipo 2. Está autorizado en Suiza desde 2019, y nuevos estudios han analizado su eficacia y seguridad en pacientes con EPOC de moderada a grave con inflamación T2 y en niños con asma de moderada a grave no controlada. Los resultados se presentaron en el Congreso DGP 2024.
Las exacerbaciones de la EPOC se asocian a un mayor riesgo de nuevas exacerbaciones, a un deterioro de la función pulmonar y a una elevada morbilidad y mortalidad. Las enfermedades EPOC con inflamación de tipo 2 se ven especialmente afectadas.
BOREAS fue un estudio de fase 3, doble ciego, aleatorizado y controlado, de 52 semanas de duración, sobre la eficacia y la seguridad de dupilumab 300 mg bisemanal en pacientes con EPOC con eosinófilos en sangre ≥300 células/µl. Lo ideal sería que ya hubieran recibido una terapia triple consistente en un corticosteroide inhalado (CSI), un agonista β2 de acción prolongada (LABA) y un antagonista muscarínico de acción prolongada (LAMA). Esto se aplicaba al 98% de la población, como explicó el PD Dr. Henrik Watz, del Instituto de Investigación Neumológica de la Clínica Pulmonar de Grosshansdorf (Alemania) [1]. En casos excepcionales, como cuando los CSI estaban contraindicados, también se permitía la combinación LAMA/LABA. Las exacerbaciones deberían haberse producido ya durante el tratamiento como indicador de la necesidad de una terapia adicional. Los antecedentes de asma fueron un criterio de exclusión.
939 pacientes con eosinófilos en sangre ≥300 células/µl fueron incluidos en BOREAS y aleatorizados en una proporción 1:1 a dupilumab 300 mg (n=468) o placebo (n=471) por vía subcutánea (SC) una vez cada 2 semanas (q2w) durante 52 semanas. Los pacientes tenían entre 40 y ≤80 años. El criterio de valoración primario fue la tasa anualizada de exacerbaciones de moderadas a graves desde el inicio del estudio hasta la semana 52. Los criterios de valoración secundarios incluyeron el cambio en el FEV1valor antes de la broncodilatación en la semana 12 y en la semana 52 en comparación con el valor inicial (BL), las exacerbaciones acumuladas a lo largo del tiempo y la seguridad o la calidad de vida relacionada con la salud de los pacientes en tratamiento como Resultados comunicados por los pacientes (PRO).
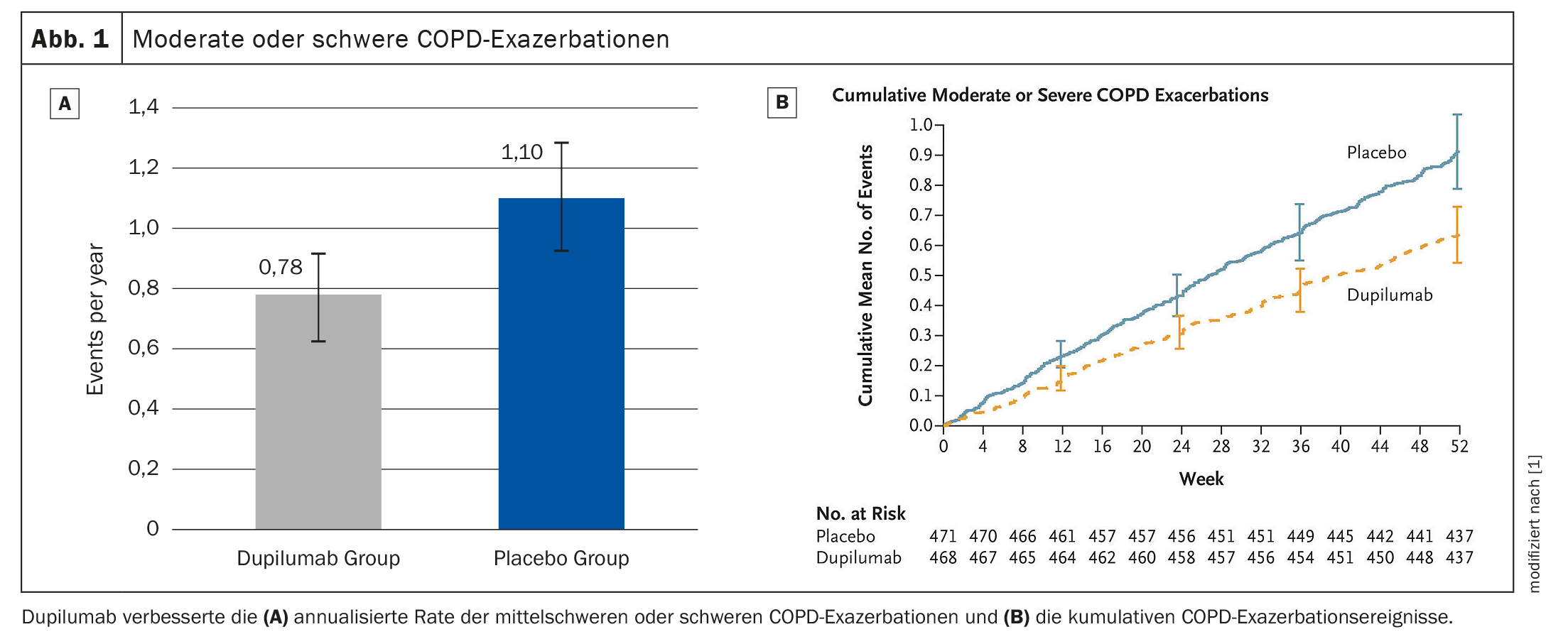
La tasa de exacerbación de la EPOC se redujo en un 30%.
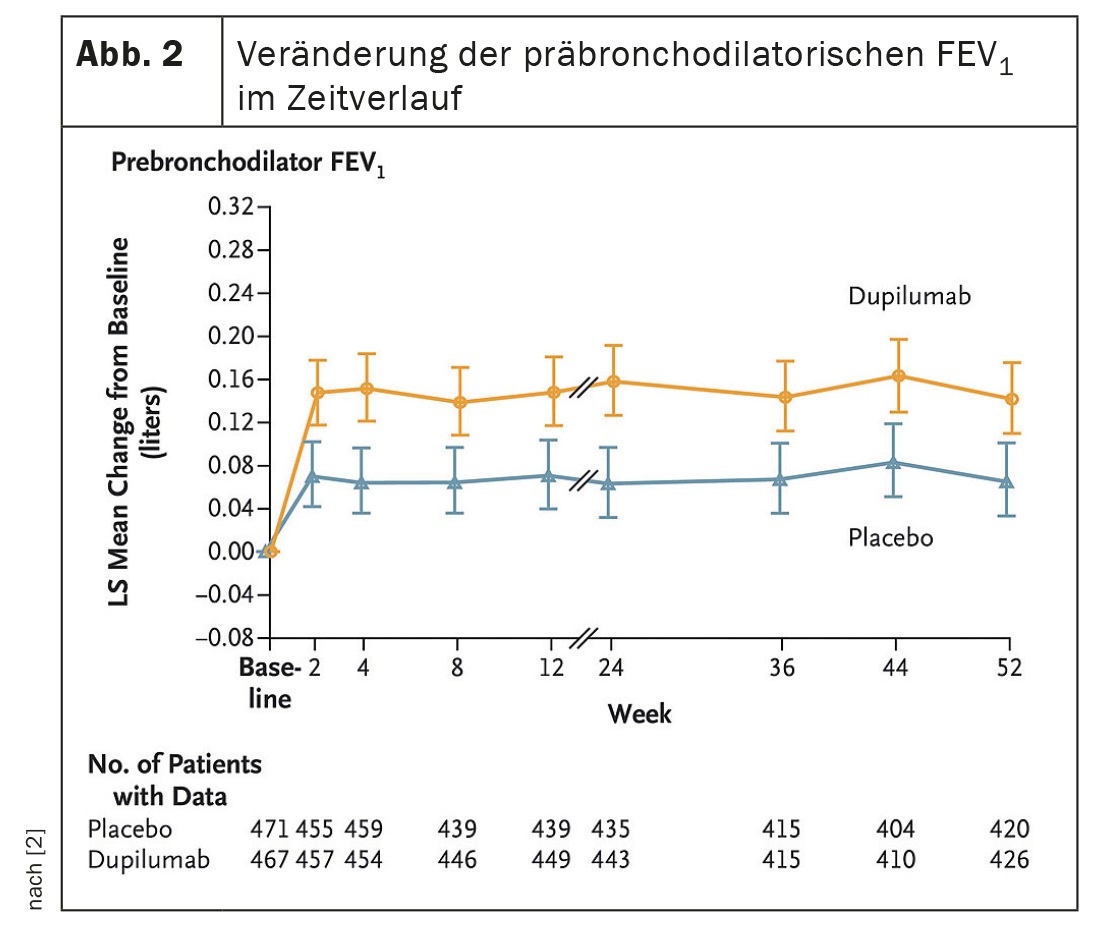
Tras 52 semanas, el dupilumab redujo la tasa de exacerbaciones en un 30% en comparación con el grupo placebo (p=0,0005) (Fig. 1A, 1B). El anticuerpo IgG4 aumentó el FEV pre-BD1 en la semana 12 fue significativo (diferencia de LSM frente a placebo: 83 ml, p<0,0001); que persistió hasta la semana 52 (83 ml, p=0,0003) (Fig. 2) . Esto tendió a dar lugar a un menor tratamiento anual asociado a las exacerbaciones con corticosteroides sistémicos (CS) en el grupo dupilumab- (13,57 días [SD 13,17] en comparación con el brazo placebo (19,09 días [SD 20,65]). La seguridad fue similar en ambos grupos, los acontecimientos adversos fueron iguales.
Así pues, el dupilumab mejoró significativamente las exacerbaciones de moderadas a graves, la función pulmonar, la calidad de vida y los síntomas en pacientes con EPOC con inflamación T2, concluyó el Dr. Watz. El uso de días de SCS necesarios para el tratamiento de la AECOPD tendió a disminuir con dupilumab.
Efecto a largo plazo sobre la función pulmonar en pacientes pediátricos con asma
Minimizar el deterioro de la función pulmonar es un objetivo primordial en el tratamiento del asma pediátrica. El uso a largo plazo de dupilumab en el estudio Excursión produjo una mejora sostenida de la función pulmonar en pacientes de 6 a 11 años con asma de tipo 2 de moderada a grave no controlada que completaron el estudio Voyage; se observó una rápida mejora de la función pulmonar en los pacientes que pasaron de placebo (PBO) a dupilumab (DPL).
En Voyage, el dupilumab redujo significativamente las exacerbaciones graves y mejoró la función pulmonar durante 52 semanas. Excursión fue un estudio de extensión abierto, de un solo brazo, con niños que habían participado previamente en Viaje. La Dra. Theresa Guilbert, neumóloga pediátrica del Hospital Infantil de Cincinnati y de la Universidad de Cincinnati (EE.UU.), presentó un análisis post-hoc de la Excursión que evaluó las mejoras numéricamente superiores de la función pulmonar observadas en los brazos de DPL/DPL frente a los de PBO/DPL en la Excursión [3].
Los niños recibieron dupilumab 100 mg o 200 mg cada 2 semanas según el peso corporal durante un periodo de un año. Los investigadores analizaron el cambio respecto al valor basal en el estudio principal (PSBL) y el porcentaje de FEV1 antes de la broncodilatación a lo largo de 104 semanas, así como el impacto de las características basales como la edad de inicio del asma, el tiempo transcurrido desde el diagnóstico, la dosis de corticosteroides inhalados (ISC) al inicio y el control del asma sobre la eficacia del dupilumab.
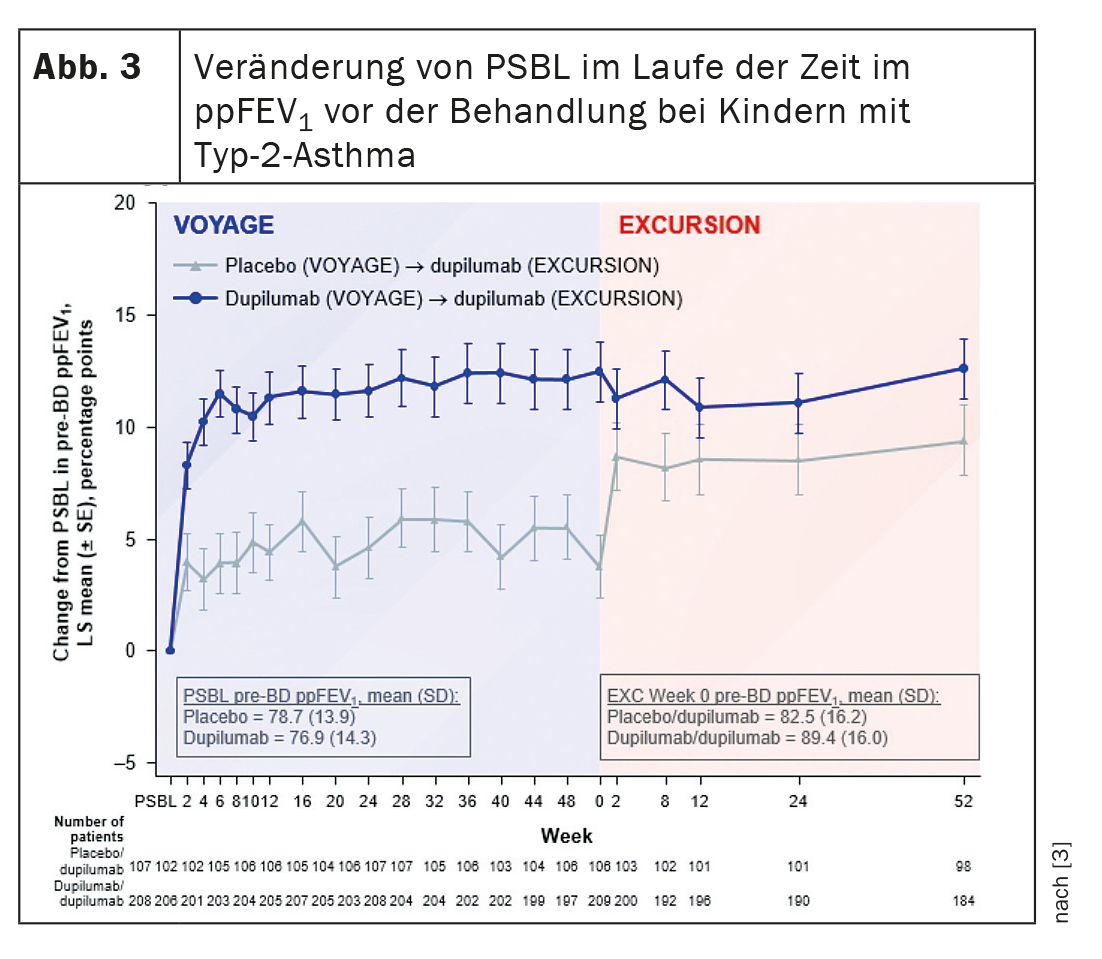
El dupilumab mejoró rápidamente la función pulmonar durante el viaje, lo que continuó durante la excursión. En la excursión, los pacientes que recibieron placebo durante el viaje mostraron una mejora rápida y sostenida de la función pulmonar desde el inicio del tratamiento con dupilumab (Fig. 3) . El dupilumab fue capaz de mejorar y mantener el porcentaje de FEV1 previsto antes de la broncodilatación hasta 104 semanas, resumió los resultados el Dr. Guilbert. La respuesta de la función pulmonar al biológico durante un periodo de 1 a 2 años no difirió según la duración del asma o la edad al inicio de la terapia.
La discusión con estos datos es que los pacientes que pasaron del placebo al dupilumab no recuperaron totalmente su función pulmonar, señaló el Prof. Dr. Marek Lommatzsch, de la University Medicine Rostock (Alemania). Así que la pregunta es: ¿se trata de un efecto real y significa esto que un retraso de un año en la terapia supone una pérdida de la función pulmonar? La Dra. Guilbert explicó que su grupo de investigación tuvo inicialmente la misma idea. “Sin embargo, no se trata de una diferencia estadística. El valor es numéricamente superior, pero no alcanza significación estadística en comparación con el grupo placebo”. Probablemente se necesiten números más grandes para determinar esta diferencia. Además, “por supuesto, existe un gran debate sobre si deberíamos hablar de remisión clínica en el tratamiento con la llegada de las terapias biológicas”. Existe cierto debate sobre si esto es apropiado o no en pediatría.
Congreso: DGP 2024
Fuentes:
- Watz H: Eficacia y seguridad del dupilumab para la EPOC con inflamación de tipo 2 indicada por eosinófilos elevados. Sesión “Novedades sobre ensayos clínicos en asma y EPOC”. 64º Congreso de la Sociedad Alemana de Neumología y Medicina Respiratoria e.V., 20-24 de marzo de 2024, Mannheim (D).
- Bhatt SP, Rabe KF, Hanania NA, et al: Dupilumab para la EPOC con inflamación de tipo 2 indicada por recuentos de eosinófilos. N Engl J Med 2023; 389: 205-214; doi: 10.1056/NEJMoa2303951.
- Guilbert T: Efecto a largo plazo del Dupilumab sobre la función pulmonar en pacientes pediátricos con asma no controlada. Sesión “Novedades sobre ensayos clínicos en asma y EPOC”. 64º Congreso de la Sociedad Alemana de Neumología y Medicina Respiratoria e.V., 20-24 de marzo de 2024, Mannheim (D).
InFo PNEUMOLOGIE & ALLERGOLOGIE 2024; 6(2): 36-37 (publicado el 30.5.24, antes de impresión)