Las opciones de tratamiento para los pacientes de psoriasis en la infancia y la adolescencia son mucho más limitadas en comparación con el espectro terapéutico para los adultos. Pero los pacientes pediátricos también pueden beneficiarse de un tratamiento específico. Así lo demuestran, entre otros, los datos de los ensayos clínicos correspondientes sobre el secukinumab. Los datos a largo plazo de la fase de extensión de los estudios de registro también fueron convincentes.
La aprobación en la UE del secukinumab en pacientes pediátricos se basó en los resultados de un programa de estudios de fase III en el que el secukinumab produjo una curación rápida y duradera de las lesiones cutáneas en los participantes del estudio de edades comprendidas entre los 6 y los <18 años con psoriasis en placas de moderada a grave [1]. El biológico no sólo demostró ser eficaz, sino que también fue bien tolerado en general [2,3]. El perfil de seguridad se correspondió con el de los pacientes adultos con psoriasis.
| Terapia dirigida para la psoriasis en placas juvenil |
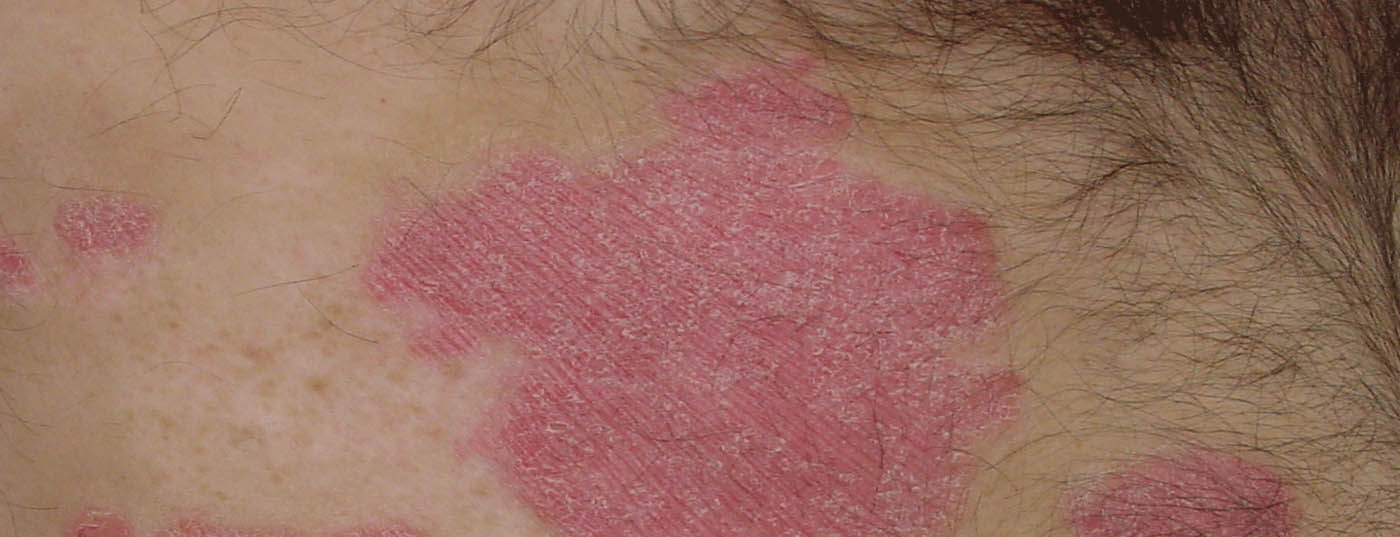
| Alrededor del 1% de los niños y adolescentes están afectados por la psoriasis en placas . [8–12]La psoriasis suele asociarse a comorbilidades metabólicas, cardiovasculares, gastrointestinales y psicológicas y a una calidad de vida significativamente reducida [8–12]. En los pacientes pediátricos, se cree que el impacto de la psoriasis en la calidad de vida es similar al del asma o la artritis [7]. |
| Aunque se dispone de muchas terapias eficaces y bien toleradas para el tratamiento de la psoriasis en adultos, las opciones terapéuticas para los pacientes pediátricos y adolescentes son mucho más limitadas [8–12]. Esto se debe, al menos en parte, a la falta de predictibilidad de la respuesta a las opciones terapéuticas aprobadas para adultos [8]. Recientemente se han aprobado en la UE varios agentes biológicos dirigidos para el tratamiento de la psoriasis en placas pediátrica, entre ellos el secukinumab (Cosentyx®), un antagonista de la IL-17A cuyas propiedades farmacológicas han sido ampliamente estudiadas . [14]La IL-17 es una importante citocina proinflamatoria implicada en la patogénesis de la psoriasis, la IL-17A está regulada al alza en la piel psoriásica lesional y no lesional [13]. |
Respuesta clínica sostenida durante un periodo de tratamiento de 2 años
El primero de los ensayos de fase III incluyó a pacientes pediátricos a los que se había diagnosticado psoriasis en placas crónica grave al menos tres meses antes y que cumplían los requisitos para recibir tratamiento sistémico [2]. Al inicio del estudio, los participantes tenían una puntuación PASI* ≥20, una puntuación IGA# de 4 y una afectación de la superficie corporal (BSA**) ≥10%. La edad media era de 13,5 años, la mayoría (77,2%) tenía ≥12 años. La media del BSA total era del 40% y la duración media de la psoriasis en placas era de 5,22 años. La artritis psoriásica comórbida estaba presente en el 8,6% de los pacientes [2]. < < < Los pacientes fueron distribuidos aleatoriamente en diferentes grupos de dosis según el peso corporal (pc): dosis baja (LD): 75 mg para pc 50 kg y 150 mg para pc ≥50 kg, dosis alta (HD): 75 mg para pc 25 kg, 150 mg para pc 25 a 50 kg y 300 mg para pc ≥50 kg. En el brazo de tratamiento de comparación, se administró etanercept (s.c) 0,8 mg/kg de peso vivo (hasta un máximo de 50 mg).
* PASI = Psoriasis Area Severity Index (Índice de gravedad del área de psoriasis)
# IGA = Investigator’s Global Assessment Modified 2011 (Evaluación global del investigador modificada en 2011)
** BSA = Body Surface Area (Área de superficie corporal)
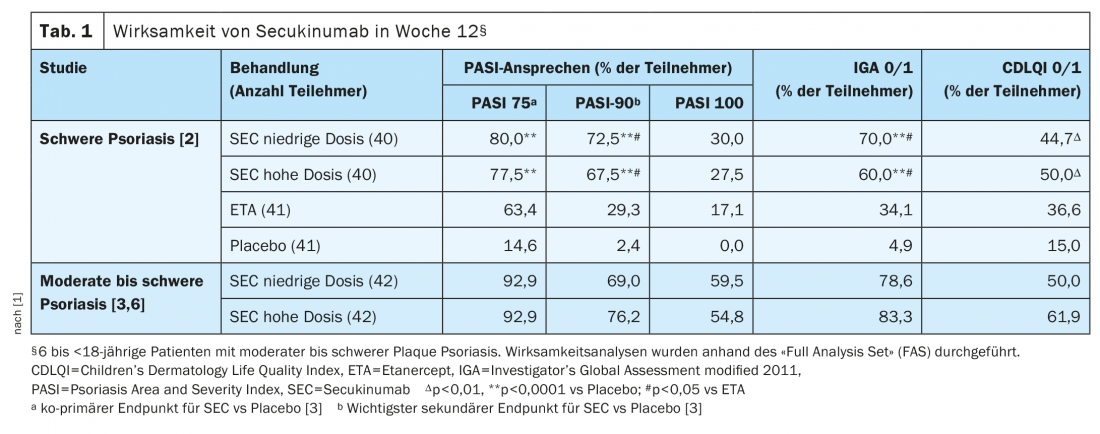
La eficacia clínica de secukinumab ya era evidente en la semana 4. En la semana 12, las tasas de respuesta PASI-75, IGA 0/1 y PASI-90 fueron significativamente superiores con secukinumab tanto a dosis bajas como altas que con placebo ( Tabla 1). Y en comparación con etanercept, secukinumab (LD y HD) mostró tasas de respuesta IGA 0/1 y PASI-90 significativamente superiores y tasas de respuesta PASI-75 y PASI-100 numéricamente superiores en la semana 12 (Tab. 1). <En pacientes con un peso corporal ≥25 a 50 kg, las tasas de respuesta PASI-75/90/100 e IGA 0/1 en la semana 12 fueron numéricamente superiores con secukinumab en dosis altas (n=15) que en los grupos de secukinumab en dosis bajas (n=17) [2]. Durante el mismo periodo, las puntuaciones medias del PASI mejoraron con respecto al valor inicial en un 82,9% en el grupo de dosis bajas de secukinumab y en un 79,9% en el grupo de dosis altas de secukinumab, en comparación con el 29,3% en el grupo de placebo y el 74,2% con etanercept [2]. Tanto las tasas de respuesta PASI como la respuesta IGA 0/1 persistieron con secukinumab hasta la semana 104. En la semana 52, la proporción con respuesta PASI-75 fue numéricamente superior en las dosis alta y baja en comparación con etanercept (87,5% y 87,5% frente a 68,3%).
Tasas de respuesta IGA 0/1 superiores al 80% en la semana 52
<18 Jahren, die seit mindestens drei Monaten von einer mittelschwer bis schwer ausgeprägten Plaque-Psoriasis betroffen waren und für eine systemische Therapie geeignet waren [3]. Einschlusskriterien waren ein PASI-Score>El segundo de los ensayos clínicos pivotales aleatorizados y controlados incluyó a pacientes de 6 a 12 años, puntuación IGA >3 y afectación de la BSA de >10%. Al inicio del estudio, el 72,6% de los pacientes tenían psoriasis moderada y el 27,4% psoriasis grave. La edad media de los pacientes era de 12,6 años y el 60,7% de los pacientes tenían entre 12 y <18 años. La participación media de la BSA fue del 30%. También en este estudio, los pacientes recibieron dosis bajas (LD) o altas de secukinumab (HD), según el peso corporal y la gravedad de la enfermedad. En el subgrupo de LD, los pacientes con un peso corporal (PC) <50 kg fueron tratados con 75 mg y los que tenían un PC ≥50 kg con 150 mg de secukinumab. En el grupo de HD, los pacientes con un PC <25 kg recibieron una dosis de secukinumab de 75 mg, los que tenían un PC entre 25 y <50 kg recibieron una dosis de 150 mg y los pacientes con un PC ≥50 kg recibieron 300 mg.
Se administró secukinumab en las semanas 0, 1, 2, 3 y 4 y posteriormente cada 4 semanas. Para los análisis de los criterios de valoración primarios y secundarios principales se utilizaron datos de placebo de ensayos controlados anteriores en pacientes adultos y pediátricos con psoriasis en placas. El criterio de valoración coprimario fue la proporción de pacientes que lograron una respuesta PASI-75 y una respuesta IGA 0/1 en la semana 12 con secukinumab en comparación con placebo (documentado a partir de estudios anteriores) [3].
En la semana 12, tanto las dosis bajas como las altas de secukinumab fueron superiores a las tasas de respuesta al placebo de PASI-75, IGA 0/1 y PASI-90 documentadas en estudios anteriores. La probabilidad estimada de un efecto positivo del tratamiento fue de 1 (100%) [3]. [3,4]Las tasas de respuesta PASI-75 e IGA 0/1 aumentaron hasta la semana 24 (grupos LD: 95,2% y 88,1%; grupos HD: 95,2% y 92,9%) y persistieron hasta la semana 52 (LD: 88,1% y 85,7%; HD: 90,5% y 83,3%) . Las tasas de respuesta PASI 90/100 en la semana 52 fueron de 76,2/52%/52,4% en el grupo de dosis bajas de secukinumab y de 83,3/69%/69,0% en el grupo de dosis altas de secukinumab [4]. Las tasas de respuesta PASI90 en las semanas 32, 48 y 52 fueron numéricamente superiores en los grupos de dosis altas de secukinumab en comparación con el grupo de dosis más bajas. Las tasas de respuesta PASI-100 de la semana 32 a la 52 mostraron un patrón similar. En general, el secukinumab demostró ser eficaz en todos los subgrupos, independientemente del peso corporal (<25 kg, de 25 a <50 kg y ≥50 kg) y de la edad (de 6 a <12 años y de 12 a <18 años) [5].
| Cosentyx® para pacientes pediátricos: Ampliación del espectro terapéutico |
| El secukinumab (Cosentyx®) ha demostrado ser un tratamiento eficaz para niños y adolescentes con psoriasis en placas de moderada a grave, con una tolerabilidad generalmente buena. Constituye una valiosa adición a las limitadas opciones de tratamiento para esta población de pacientes y recibió la aprobación de la EMA en 2020. |
| Las terapias dirigidas con biológicos ofrecen varias ventajas frente a las terapias sistémicas convencionales, como una dosificación menos frecuente, una mayor eficacia y una menor necesidad de control de laboratorio. |
| Al igual que otros biológicos aprobados para la psoriasis vulgar pediátrica, el secukinumab se administra mediante inyección subcutánea.
Siguiendo las instrucciones adecuadas, el Cosentyx® puede ser administrado por un cuidador adulto utilizando una jeringa o pluma precargada. A diferencia del etanercept, que se administra una vez a la semana, y del adalimumab, que se administra cada 2 semanas, el intervalo de dosis del secukinumab en la terapia de mantenimiento es de 4 semanas. La administración menos frecuente y la posibilidad de tratamiento en casa son factores que pueden tener un efecto favorable en la adherencia al tratamiento. |
| a [1,7] |
Perfil de seguridad comparable al de los adultos
El perfil de tolerabilidad de secukinumab en los pacientes pediátricos fue coherente con los datos de seguridad observados en pacientes adultos con psoriasis. En general, el secukinumab fue bien tolerado, siendo la nasofaringitis el acontecimiento adverso (EA) notificado con más frecuencia. Las tasas de EA de especial interés fueron en general bajas. No se identificaron nuevas señales de seguridad durante los periodos de tratamiento de 52 y 104 semanas del estudio de extensión.
Literatura:
- Blair HA: Secukinumab: A Review in Moderate to Severe Pediatric Plaque Psoriasis. Pediatric Drugs 2021; 23: 601–608.
- Bodemer C, et al.: Secukinumab demonstrates high efficacy and a favourable safety profile in paediatric patients with severe chronic plaque psoriasis: 52-week results from a phase 3 double-blind randomized, controlled trial. J Eur Acad Dermatol Venereol 2020; 35(4): 938–947.
- Magnolo N, et al.: A phase III open-label, randomized multicenter study to evaluate efficacy and safety of secukinumab in pediatric patients with moderate to severe plaque psoriasis: 24-week results. J Am Acad Dermatol 2021; S0190-9622(21)02509-3
- Reich A, et al.: Secukinumab treatment demonstrated high efficacy and safety in paediatric patients with moderate-to-severe plaque psoriasis: 52-week results from a randomised trial [abstract no. P121 plus poster]. Pediatr Dermatol 2021; 38(Suppl. 1): 57–58.
- Szepietowski JC, et al.: Secukinumab demonstrated consistent efficacy across age and weight subgroups in pediatric patients with psoriasis: analyses from two phase 3 pediatric studies [abstract no. 78 plus poster]. In: Society for Pediatric Dermatology. 2021.
- Beissert S, et al. Secukinumab improves quality of life of paediatric patients with moderate-to-severe plaque psoriasis: 52-week results from a phase III, randomised study [abstract no. P080 plus poster]. Pediatr Dermatol. 2021;38(Suppl. 1): 43.
- Cordoro KM: Toward optimal care of the pediatric patient with psoriasis: the new AAD-NPF management guideline. J Psoriasis Psoriatic Arthritis 2020; 5(1): 7–11.
- Nogueira M, Paller AS, Torres T: Targeted therapy for pediatric psoriasis. Paediatr Drugs 2021; 23(3): 203–212.
- Wu JJ, et al.: Treatment of psoriasis with secukinumab in challenging patient scenarios: a review of the available evidence. Dermatol Ther 2020; 10(3): 351–364.
- Menter A, et al.: Joint American Academy of Dermatology-National Psoriasis Foundation guidelines of care for the management and treatment of psoriasis in pediatric patients. J Am Acad Dermatol 2020; 82(1): 161–201.
- Eisert L, et al.: S2k guidelines for the treatment of psoriasis in children and adolescents – short version part 1. J Dtsch Dermatol Ges 2019; 17(8): 856–870.
- Haulrig MB, Zachariae C, Skov L: Off-label treatments for pediatric psoriasis: lessons for the clinic. Psoriasis (Auckl) 2021; 11: 1–20.
- Información sobre medicamentos, www.swissmedicinfo.ch,(última consulta: 26 de noviembre de 2021)
- Blauvelt A, Chiricozzi A: The immunologic role of IL-17 in psoriasis and psoriatic arthritis pathogenesis. Clin Rev Allergy Immunol 2018; 55(3): 379–390.
DERMATOLOGIE PRAXIS 2021; 31(6): 28–29