El tratamiento de la artritis reumatoide (AR) ha avanzado mucho en los últimos 20 años. Esto se refiere tanto a la gama de fármacos disponibles como a los avances en términos de rapidez de acción y tasas de respuesta. Los inhibidores de JAK han demostrado ser una alternativa a los biológicos, con algunas ventajas.
El tratamiento de la artritis reumatoide (AR) ha avanzado mucho en los últimos 20 años. Esto se refiere tanto a la gama de fármacos disponibles como a los avances en términos de rapidez de acción y tasas de respuesta. Los inhibidores de JAK han demostrado ser una alternativa a los biológicos, con algunas ventajas.
Teniendo en cuenta su manejo nada fácil (necesidad de refrigeración, administración parenteral), los biológicos no son la forma óptima de terapia para todos los pacientes, sobre todo porque sólo una minoría consigue una remisión clínica continua con ellos. Por otro lado, el dolor, las limitaciones funcionales, la fatiga y la depresión suponen una elevada carga de enfermedad para los afectados. Los inhibidores de JAK se posicionan en el tratamiento de la artritis reumatoide tras el fracaso terapéutico con csDMARDs o biológicos.
La Liga Europea contra el Reumatismo (EULAR) ha recomendado que los pacientes con una respuesta deficiente a los csDMARD (por ejemplo, metotrexato, MTX) y un pronóstico desfavorable sean tratados con bDMARD o con un inhibidor de JAK [1]. Si esto no conduce a una respuesta terapéutica, debe intentarse un cambio de sustancia o de clase (de bDMARD a JAKi o viceversa). Tanto para los DMARD biológicos como para los sintéticos dirigidos (b/tsDMARD), se recomienda la terapia combinada con un csDMARD. Si esto se descarta (por ejemplo, debido a contraindicaciones), la EULAR aconseja que se prefieran los inhibidores de la IL-6 y la JAK a otros bDMARD.
En la actualidad hay tres inhibidores de JAK disponibles en Suiza para el tratamiento de la AR: Tofacitinib, baricitinib y upadacitinib. Además, el filgotinib está aprobado en Alemania desde 2020 y el peficitinib está disponible en el mercado japonés desde 2019, pero aún no está permitido su uso en EE.UU. ni en Europa. A la hora de elegir el inhibidor de JAK adecuado, la cuestión de las diferencias específicas de cada compuesto en cuanto a eficacia y perfil de seguridad suele ser la de mayor interés para los encargados del tratamiento.
Tofacitinib
La selectividad de los inhibidores de JAK, es decir, la inhibición de isoformas individuales a una determinada concentración intracelular, es el principal objetivo de los estudios. Se busca así la relación óptima entre eficacia y efectos secundarios, como en el caso de la anemia, por ejemplo. En el caso del tofacitinib, aprobado en Suiza desde 2013, un análisis post hoc de pacientes seropositivos y seronegativos mostró una respuesta comparable en ambos grupos [2]. Las tasas de remisión DAS28 fueron ligeramente inferiores a las de los pacientes con CCP. En el análisis, se agruparon los datos de cinco estudios de fase III y se definieron subgrupos en función de la serología: RF+CCP+, RF+CCP-, RF-CCP+ y RF-CCP-. Como resultado, los pacientes con RF+CCP+ tuvieron una mayor probabilidad de lograr una respuesta ACR-20, -50 o -70 que los pacientes con RF-CCP. Este resultado se mostró para la respuesta ACR-20 y -50 tanto para el tofacitinib 5 mg dos veces al día como para el tofacitinib 10 mg dos veces al día. Por el contrario, la respuesta ACR-70 sólo fue mejor con la dosis más alta.
Otro estudio analizó el riesgo de eventos cardiovasculares con el tofacitinib. La evaluación de un estudio de fase IV que comparaba el tofacitinib con los bloqueantes del TNF (adalimumab, etanercept) en pacientes mayores de 50 años y con al menos un factor de riesgo adicional de acontecimientos cardiovasculares demostró que el riesgo de acontecimientos tromboembólicos asociado al tofacitinib debe considerarse aumentado.
El riesgo de embolia pulmonar también aumentó significativamente con el tofacitinib en la dosis de 10 mg y también fue mayor con 5 mg dos veces al día que en estudios anteriores. Además, la mortalidad por todas las causas fue mayor con 10 mg dos veces al día que con 5 mg dos veces al día. Por ello, la EMA ha emitido en 2019 una recomendación según la cual el tofacitinib no debe utilizarse en pacientes con mayor riesgo de tromboembolismo. Los pacientes con AR mayores de 65 años sólo deben ser tratados con tofacitinib si no existe alternativa terapéutica.
Upadacitinib
Se realizó una comparación de upadacitinib frente a adalimumab frente a placebo en pacientes MTX-IR con AR activa en el ensayo SELECT-COMPARE [3]. En este estudio, existía la opción de cambiar de upadacitinib a adalimumab en la semana 12 y viceversa (en las semanas 14, 18, 22 y 26) si se producía una mejoría inferior al 20% en las articulaciones dolorosas e inflamadas (criterios de valoración coprincipales ACR20 y DAS28-CRP <2,6).
El estudio de 1629 pacientes con AR activa a pesar del MTX demostró que el upadacitinib (aprobado en Suiza desde la primavera de 2020) era estadísticamente más eficaz que el adalimumab: el 71% de los pacientes lograron una respuesta ACR20 con upadacitinib, sólo el 63% con adalimumab y el 36% con placebo. El 29% de los pacientes alcanzaron la remisión según el DAS28-CRP, frente a sólo el 18% con adalimumab y el 6% con placebo. En cuanto a los efectos secundarios, el herper zoster y las elevaciones de la CK fueron más frecuentes con el upadacitinib, el tromboembolismo venoso (TEV) se produjo en 3 pacientes con adalimumab frente a 2 pacientes con upadacitinib. En cuanto a los no respondedores, se observó que el cambio de upadacitinib a adalimumab hizo que el 13% lograra la remisión, mientras que, a la inversa, el cambio de adalimumab a upadacitinib hizo que el 26% lograra el resultado deseado.
En el ensayo SELECT-MONOTHERAPY, 648 pacientes con AR activa a pesar del MTX fueron aleatorizados a la continuación del tratamiento con MTX o a upadacitinib 15 mg o 30 mg como monoterapia [4]. De nuevo, se observó una respuesta significativamente mejor con el upadacitinib: tras 14 semanas, el 68% de los pacientes con upadacitinib 15 mg y el 71% con upadacitinib 30 mg lograron una respuesta ACR20, en comparación con sólo el 41% de los pacientes que continuaron con la terapia MTX.
Baricitinib
El baricitinib está aprobado en Suiza desde 2017 en una dosis de 4 mg (2 mg en pacientes de edad avanzada o con insuficiencia renal). En los ensayos clínicos, el principio activo una vez al día en dosis de 2 mg y 4 mg ya ha demostrado una eficacia clínica significativa con una seguridad aceptable en el pasado [5,6]. Los acontecimientos adversos graves (AAG) notificados con mayor frecuencia durante el periodo controlado con placebo fueron las infecciones.
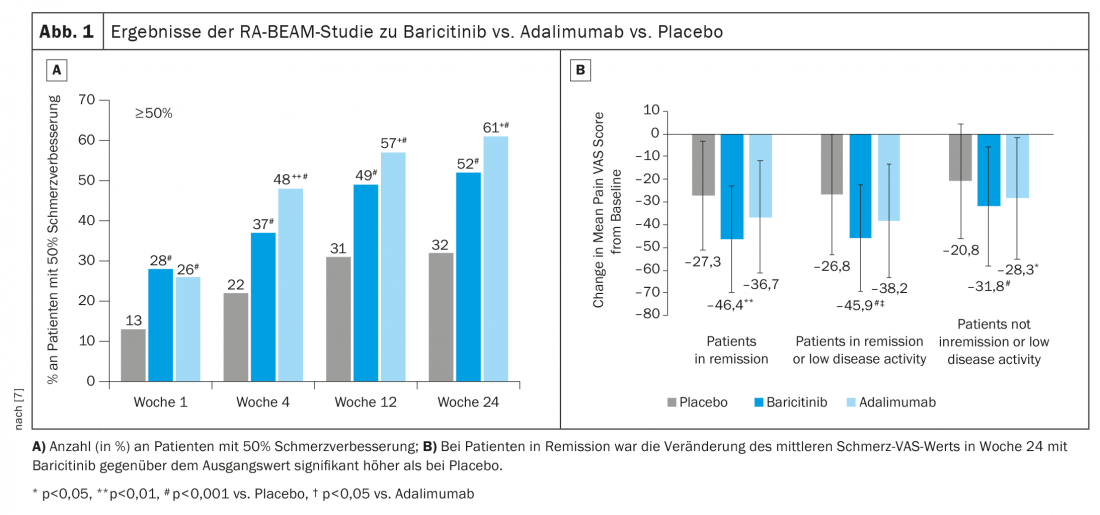
En el ensayo RA-BEAM, se comparó baricitinib 4 mg + MTX con adalimumab + MTX y placebo + MTX [7]. En este caso, se ha demostrado que la mejora del dolor del 50% es mejor con baricitinib. (Fig. 1A). Si observamos más detenidamente sólo a los pacientes que están en remisión o tienen una baja actividad de la enfermedad, seguimos viendo un efecto significativo sobre el dolor con baricitinib. (Fig. 1B). El efecto positivo pudo seguir observándose tras un cambio de adalimumab a baricitinib después de la semana 16.
En cuanto a la respuesta de vacunación con baricitinib, se han probado la PCV13 y el toxoide tetánico (TT). 106 pacientes del estudio RA-BEYOND con 2 mg o 4 mg de baricitinib (con y sin MTX) fueron vacunados con PCV13 y contra el tétanos. En general, el 68% de los pacientes mostraron una respuesta de vacunación suficiente contra el neumococo, el 43% lograron un aumento de los títulos de vacunación de más de 4 veces para el tétanos. El 74% de los pacientes consiguió un aumento de más de 2 veces tras la PCV13 [8].
Nuevo estudio sobre el efecto a largo plazo
La seguridad a largo plazo del baricitinib en 3.770 pacientes (10.127 pacientes-año de exposición, PYE) durante el programa de desarrollo clínico se ha comunicado anteriormente [9]. Dado que el baricitinib, al igual que otros fármacos antirreumáticos modificadores de la enfermedad (FAME), se utiliza de forma crónica en pacientes con AR, es importante vigilar y evaluar continuamente la evolución del perfil de seguridad a largo plazo. Estos datos a largo plazo son más relevantes para evaluar la incidencia y el riesgo de acontecimientos adversos inusuales de especial interés (AESI), incluidos los tumores malignos y los acontecimientos cardiovasculares adversos graves (MACE). Desde el análisis anterior, se ha completado el estudio de extensión a largo plazo (LTE) y el Prof. Peter C. Taylor, del Departamento de Ortopedia, Reumatología y Ciencias Musculoesqueléticas de la Universidad de Oxford, y sus colegas han presentado los resultados en una actualización de los datos de hasta 9,3 años de tratamiento [10].
Su revisión analizó los datos agrupados de pacientes ≥18años de edad con AR activa de moderada a grave procedentes de nueve ensayos clínicos aleatorizados (cinco de fase III, tres de fase II y uno de fase Ib) y un LTE completado. Los criterios de exclusión incluían infecciones actuales o recientes (<30 días antes de la entrada en el estudio), clínicamente graves que requirieran tratamiento antimicrobiano, y anomalías de laboratorio seleccionadas (por ejemplo, pruebas de función hepática/renal, hematología seleccionada y marcadores de infección). Las dosis de baricitinib oscilaron entre 1 mg y 15 mg diarios, utilizándose dosis de 2 mg y 4 mg diarios en los ensayos de fase III y LTE.
Los pacientes que completaron los ensayos de fase III y fase II fueron elegibles para la LTE. Los pacientes aleatorizados a baricitinib 2 mg en el estudio original que no se salvaron continuaron la terapia a la misma dosis en el LTE; todos los demás pacientes recibieron baricitinib 4 mg al entrar en el LTE. Los pacientes que recibieron 4 mg durante al menos 15 meses sin rescate y lograron una actividad baja sostenida de la enfermedad (puntuación del Índice de Actividad Clínica de la Enfermedad [ICE] ≤10) o la remisión (puntuación del ICE ≤2,8) fueron aleatorizados de nuevo a ciegas a 4 mg o reducidos a 2 mg.
Pacientes con AR con mayor riesgo de infección
La incidencia de muerte, acontecimientos adversos graves (incluidas infecciones), MACE y malignidad para baricitinib es similar a la observada en otros ensayos terapéuticos con inhibidores de JAK y DMARD biológicos, señalaron los autores. Pocos pacientes (tasa de incidencia ajustada a la exposición, TEAI, 4,7) interrumpieron el tratamiento debido a acontecimientos adversos. En los subgrupos de baricitinib 2 mg y 4 mg, la incidencia de AESI fue similar entre los dos grupos de dosificación.
El riesgo de mortalidad en los pacientes tratados con baricitinib no aumentó en comparación con la población general tras controlar la edad y el sexo, con una razón de mortalidad estandarizada (RME) para el baricitinib de <1. Las causas de muerte de los pacientes tratados con baricitinib concuerdan con los porcentajes de muertes globales en la población general de EE.UU. y con los notificados en ensayos clínicos de otras terapias para la AR.
Debido a las enfermedades y a las intervenciones terapéuticas, los pacientes con AR tienen un mayor riesgo de infección. La incidencia global de infecciones graves se ha mantenido estable a lo largo del tiempo. El EAIR de infecciones graves en el grupo de baricitinib 2 mg podría ser numéricamente inferior al de 4 mg, lo que está relacionado con una menor actividad de la enfermedad y un menor uso de corticosteroides y MTX al inicio. Las infecciones que provocaron la muerte fueron poco frecuentes en esta población de pacientes. La incidencia de herpes zóster se mantuvo estable y similar a la de otros inhibidores de JAK, incluidos el tofacitinib [11] y el upadacitinib [12].
Desde su evaluación anterior, ha habido 54 casos adicionales de malignidad (excluyendo el CPNM) con un IR similar (0,9 en el análisis actual frente a 0,8), escriben Taylor et al. [10]. Los pacientes con AR están predispuestos a un mayor riesgo de malignidad, especialmente linfoma, cáncer de pulmón y CPNM (cáncer de piel no melanocítico). La incidencia de linfoma se mantuvo en 0,06 con respecto a los informes anteriores sobre baricitinib y fue similar a la de otros tratamientos de la AR, incluido un IR de 0,1 para el adalimumab y de 0,096 para los pacientes que utilizan inhibidores del TNF.
Los riesgos de tumores malignos siguen sin estar claros
Los efectos de los inhibidores JAK sobre el riesgo de malignidad siguen sin estar claros y requieren más investigación. Los datos de una reciente revisión sistemática y metaanálisis concluyeron que no existía un mayor riesgo de malignidad en los pacientes que combinaban un inhibidor de JAK con MTX en comparación con los pa-cientes tratados sólo con MTX [13]. El Prof. Taylor y sus colegas señalan que el 79% de los pacientes incluidos en su análisis utilizaron MTX al mismo tiempo. Además, en estudios observacionales no se ha informado de un mayor riesgo de malignidad entre otros inhibidores de JAK (tofacitinib) en comparación con los DMARD sintéticos convencionales o los DMARD biológicos como el TNFi [14].
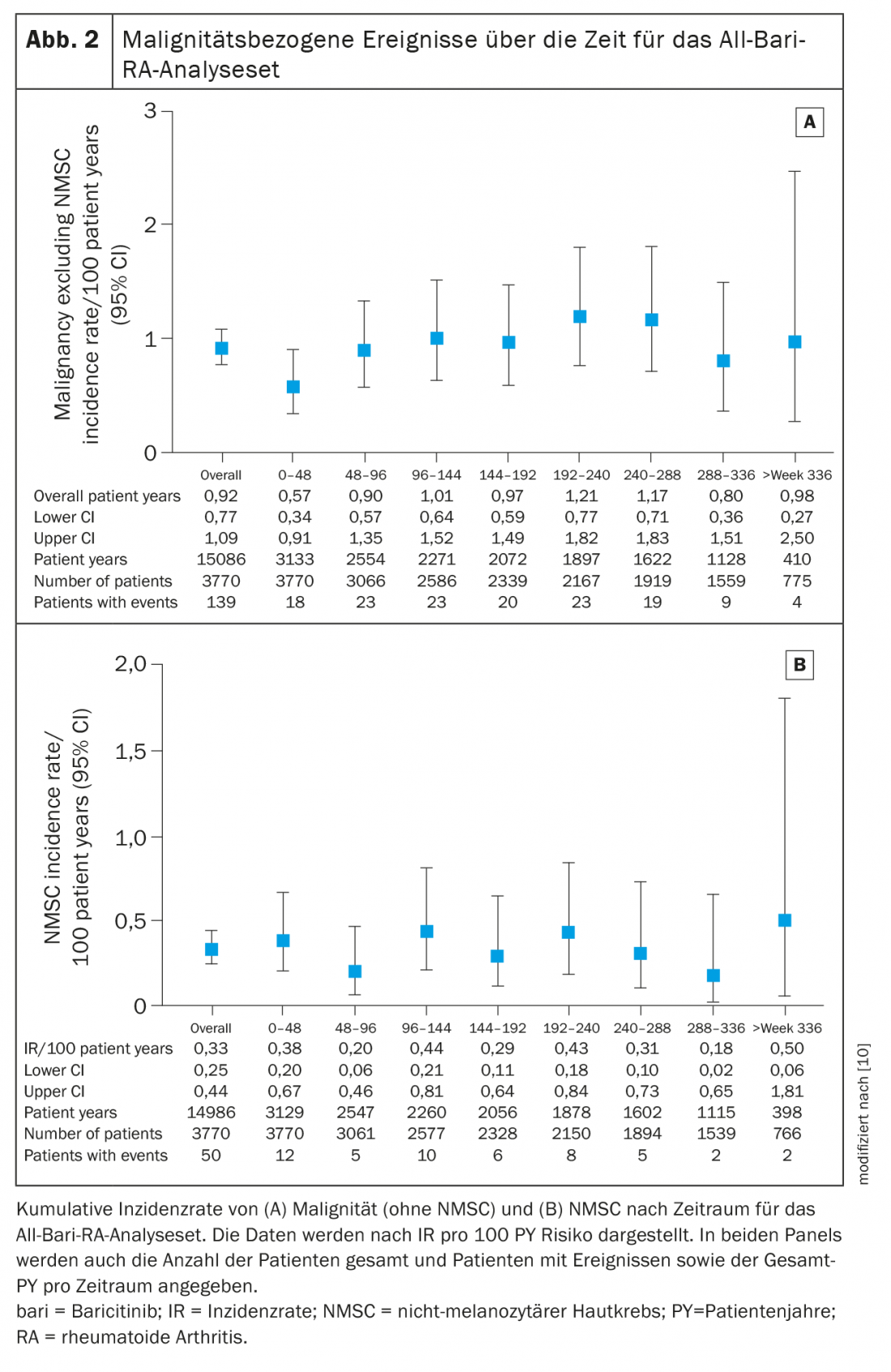
El IR de malignidad (excluyendo NMSC) durante las primeras 48 semanas en su evaluación fue de 0,6 (IC 95% 0,34-0,91) y se mantuvo estable después en aproximadamente 1,0 (IR global 0,9, IC 95% 0,77-1,09). (Fig. 2A). Los tipos de neoplasia maligna notificados con más frecuencia fueron respiratorias y mediastínicas (n=26, EAIR=0,17), de mama (n=23, EAIR=0,15) y gastrointestinales (n=19, EAIR=0,13). El IR para NMSC fue de 0,3 (IC 95%: 0,25-0,44) y no aumentó con el tiempo (Fig. 2B) . El IR para el linfoma fue de 0,06 (IC del 95%: 0,03-0,11), siendo el linfoma difuso de células B grandes el subtipo más común.
Los pacientes con AR tienen un mayor riesgo de trombosis venosa profunda (TVP) y embolia pulmonar (EP) (IR 0,3-0,8/100 pacientes-año) en comparación con la población general [15,16]. En este análisis, el IR de TVP/EP en pacientes tratados con baricitinib fue coherente con los datos comunicados anteriormente y comparable al de otros inhibidores de JAK [9]. En el subgrupo de pacientes que recibieron baricitinib 2 mg o 4 mg, los EAIR fueron similares entre los grupos de dosis y comparables a los comunicados anteriormente. Aunque los metaanálisis recientes de los ensayos controlados aleatorios de los inhibidores de la JAK (incluidos el tofacitinib, el baricitinib y el upadacitinib) en pacientes con AR no han mostrado un aumento del riesgo de episodios tromboembólicos venosos durante los periodos controlados con placebo, se necesitan datos a más largo plazo para caracterizar plenamente el riesgo de estos episodios, según los autores. La incidencia de MACE en el estudio actual (0,5) también se mantuvo baja y estable en comparación con los informes anteriores. El EAIR de MACE fue similar entre baricitinib 2 mg (0,42) y 4 mg (0,54). De los pacientes, el 55% tenía al menos uno de los cinco factores de riesgo cardiovascular al inicio del estudio utilizados en el análisis (fumador actual, hipertensión, diabetes, antecedentes de trastorno aterosclerótico o colesterol HDL <40 mg/dl); como era de esperar, el IR de MACE fue mayor en esta subpoblación de riesgo (0,70).
El EAIR para la diverticulitis en el estudio actual (0,15) es coherente con los datos publicados en pacientes con AR [17]. Los factores de riesgo importantes para la diverticulitis en la población general son la edad, la obesidad, la dieta, el tabaquismo y el consumo de medicamentos, especialmente opiáceos, corticosteroides y AINE. La diverticulitis en el estudio a largo plazo se produjo en pacientes con factores de riesgo. El IR de perforaciones gastrointestinales (0,06) sigue siendo bajo en el contexto de los informes sobre tofacitinib, tocilizumab y otros DMARD biológicos en datos del mundo real y en relación con el upadacitinib (0,08/100 pacientes-año) [18].
Mensajes para llevarse a casa
- Como fármacos antirreumáticos modificadores de la enfermedad, los inhibidores JAK se utilizan de forma crónica en pacientes con AR. Es importante vigilar y evaluar continuamente la evolución del perfil de seguridad a largo plazo.
- El perfil de seguridad de los inhibidores de JAK en los ensayos clínicos incluye un mayor riesgo de herpes zóster y asociaciones con un aumento de eventos cardiovasculares, eventos tromboembólicos venosos (TEV) y neoplasias malignas.
- En un reciente estudio a largo plazo del baricitinib, el fármaco se mantuvo estable en cuanto a acontecimientos relacionados con la seguridad, incluidas muertes, neoplasias, MACE y TVP/EP durante un periodo de hasta 9,3 años y, en general, fue similar entre los grupos de 2 mg y 4 mg.
- Los resultados sugieren que el baricitinib tiene un perfil de seguridad consistente y en línea con otros inhibidores de JAK y fármacos antirreumáticos modificadores de la enfermedad biológica.
- Se necesita un seguimiento continuado y más investigación, incluidos estudios poblacionales a largo plazo, para comprender plenamente el riesgo de los criterios de valoración, incluidos los tumores malignos, los MACE y la TEV, y el riesgo comparativo en el mundo real del baricitinib y las terapias en la AR.
Literatura:
- Smolen JS, et al: Recomendaciones de la EULAR para el tratamiento de la artritis reumatoide con fármacos antirreumáticos modificadores de la enfermedad sintéticos y biológicos: actualización de 2019. Ann Rheum Dis 2020;79: 685-699; doi: 10.1136/annrheumdis-2019-216655.
- Bird P, Hall S, Nask P, et al: RMD open 2019; 5: e000742; doi: 10.1136/rmdopen-2018-000742.
- Fleischmann R, Pangan AL, Song ICH et al: Arthritis Rheumatol 2019; 71(11): 1788-1800.
- Smolen JS, Pangan AL, Emery P, et al: Lancet 2019; 393: 2303-2311.
- Taylor PC, Keystone EC, van der Heijde D, et al: Baricitinib frente a placebo o adalimumab en la artritis reumatoide. N Engl J Med 2017; 376: 652-662; doi: 10.1056/NEJMoa1608345
- Genovese MC, Kremer J, Zamani O, et al: Baricitinib en pacientes con artritis reumatoide refractaria. N Engl J Med 2016; 374: 1243-1252; doi: 10.1056/NEJMoa1507247
- Fautrel B, Kirkham B, Pope JE, et al: J Clin Med 2019; 8: 1394-1408.
- Winthrop K, Bingham CO, Komocsar WJ, et al: Arthritis Res Ther 2019; 21: 102-112.
- Genovese MC, Smolen JS, Takeuchi T, et al: Safety profile of baricitinib for the treatment of rheumatoid arthritis over a median of 3 years of treatment: an updated integrated safety analysis. Lancet Rheumatol 2020; 2: e347-e357; doi: 10.1016/S2665-9913(20)30032-1.
- Taylor PC, Takeuchi T, Burmester GR, et al: Safety of baricitinib for the treatment of rheumatoid arthritis over a median of 4.6 and up to 9.3 years of treatment: final results from long-term extension study and integrated database. Anales de las Enfermedades Reumáticas 2021 (primero en línea); doi: 10.1136/annrheumdis-2021-221276.
- Winthrop KL, Curtis JR, Lindsey S, et al: Herpes zóster y tofacitinib: resultados clínicos y riesgo de la terapia concomitante. Artritis Reumatol 2017;69: 1960-1968; doi: 10.1002/art.40189.
- van Vollenhoven R, Takeuchi T, Pangan AL: A phase 3, randomized, controlled trial comparing upadacitinib monotherapy to MTX monotherapy in MTX-naïve patients with active rheumatoid arthritis [abstract]. Artritis Reumatol 2018; 70.
- Solipuram V, Mohan A, Patel R, et al: Efecto de la combinación de inhibidores de la quinasa Janus y metotrexato sobre la malignidad en pacientes con artritis reumatoide: revisión sistemática y metaanálisis de ensayos controlados aleatorizados. Auto Immune Highlights 2021; 12(8); doi: 10.1186/s13317-021-00153-5.
- Xie W, Yang X, Huang H, et al: Riesgo de malignidad con la terapia biológica sin TNF o tofacitinib en la artritis reumatoide: un metaanálisis de estudios observacionales. Semin Arthritis Rheum 2020; 50: 930-937; doi: 10.1016/j.semarthrit.2020.08.007.
- Kim SC, Schneeweiss S, Liu J, et al: Riesgo de tromboembolia venosa en pacientes con artritis reumatoide. Arthritis Care Res 2013; 65: NA-7; doi: 10.1002/acr.22039.
- Ogdie A, Kay McGill N, Shin DB, et al: Riesgo de tromboembolia venosa en pacientes con artritis psoriásica, psoriasis y artritis reumatoide: un estudio de cohortes basado en la población general. Eur Heart J 2018; 39: 3608-3614; doi: 10.1093/eurheartj/ehx145.
- Bharucha AE, Parthasarathy G, Ditah I, et al: Tendencias temporales en la incidencia e historia natural de la diverticulitis: un estudio basado en la población. Am J Gastroenterol 2015; 110: 1589-1596; doi: 10.1038/ajg.2015.302.
- Cohen SB, van Vollenhoven RF, Winthrop KL: Corrección: Perfil de seguridad del upadacitinib en la artritis reumatoide: análisis integrado del programa clínico de fase III SELECT. Ann Rheum Dis 2021; 80: 304-311; doi: 10.1136/annrheumdis-2020-218510.
InFo DOLOR Y GERIATURA 2021; 3(2): 6-9