Los antipsicóticos son el pilar del tratamiento agudo y a largo plazo de los trastornos esquizofrénicos. Cuanto antes comience el tratamiento antipsicótico, mayores serán las posibilidades de controlar o detener la progresión de la psicosis.
El término esquizofrenia fue acuñado por Eugen Bleuler y publicado por primera vez en 1911 en su monografía “Grupo de esquizofrenias”. Este término técnico de 108 años de antigüedad para el trastorno psicótico más importante sigue utilizándose hoy en día. Hace seis años, el DSM-5, el manual de diagnóstico estadounidense, introdujo el término “trastorno del espectro esquizofrénico”. Sin embargo, el primer tratamiento realmente eficaz para el trastorno esquizofrénico no estuvo disponible en los hospitales psiquiátricos hasta 1952/53. Esta terapia se basaba en fármacos: Clorpromazina. La clorpromazina fue llevada directamente de la clínica universitaria psiquiátrica de París a la clínica universitaria de Basilea ya en 1952 por Felix Labhart. Cabe suponer que esto se hizo sin grandes esfuerzos burocráticos en su momento.
Breve historia de los neurolépticos/antipsicóticos
La clorpromazina/Largactil® provocó en los años siguientes una conmoción en la psiquiatría institucional de la época. Según el profesor Raymond Battegay, los departamentos llamados “inquietos” con los psicóticos agitados se volvieron de repente menos ruidosos y mucho más relajados. Ahora eran posibles formas nuevas y más humanas de tratar a estos enfermos mentales graves.
El término “neuroléptico” procede del griego y fue introducido en la literatura científica por Delay y Deniker en 1955. El objetivo era desarrollar un modelo “etiológico” del modo de acción de los nuevos fármacos antipsicóticos. Los dos franceses habían descubierto que la clorpromazina tiene efectos sedantes y ansiolíticos. En consecuencia, se utilizó para la agitación psicomotriz principalmente en pacientes esquizofrénicos.
La introducción de los neurolépticos abrió una puerta importante en el tratamiento de los trastornos esquizofrénicos. En primer lugar, era un tratamiento reversible (por ejemplo, en contraste con las lobotomías que aún se utilizaban en aquella época) y, en segundo lugar, el efecto era rápido y eficaz. Esto condujo a una reducción masiva de la duración de la estancia de los psicóticos en las instituciones de la época, lo que alivió la saturación de los hospitales. Las recaídas se producían cuando los pacientes dejaban de tomar la medicación. Las razones fueron la falta de conocimiento de la enfermedad o efectos secundarios no insignificantes como sedación masiva, parkinsonismo (EPMS) o fotosensibilidad.
Descubrimiento de la dopamina como neurotransmisor
Más o menos en la misma época en que se introdujo la clorpromazina en los hospitales psiquiátricos, Arvid Carlsson (1923-2018) descubrió en Suecia la dopamina, su estructura y su función como importante neurotransmisor en el cerebro. Con su trabajo, Carlsson y Lindqvist también fundaron la hipótesis dopaminérgica de las psicosis, que más tarde establecieron van Rossum y Snyder y que sigue siendo válida hoy en día. Esto afirma que los antagonistas de la dopamina, es decir, los neurolépticos o los antipsicóticos, ocupan postsinápticamente los receptores de dopamina (especialmente los receptores D2) y bloquean así la neurotransmisión de dopamina. El resultado es una mejora de los síntomas positivos de los trastornos esquizofrénicos. Mientras que los neurolépticos típicos mejoran principalmente los delirios y las alucinaciones, tienen poco efecto o incluso empeoran los rasgos de la enfermedad denominados posteriormente síntomas negativos, como el aplanamiento afectivo, la alogia, el retraimiento social y la apatía. Aquí, la clozapina y los antipsicóticos atípicos, más conocidos como antagonistas de la serotonina-dopamina, supusieron una clara ampliación del espectro de acción.
Introducción de fármacos antipsicóticos
Tras la introducción de la clorpromazina en 1952, en los 20 años siguientes se aprobaron varios de los llamados neurolépticos tricíclicos, algunos de los cuales siguen disponibles en la actualidad:
- Del grupo de las fenotiazinas (clorpromazina, levomepromazina, flufenazina, promazina y triflupromazina),
- Del grupo de sustancias de los tioxantenos (clorprotixeno y flupentixol).
En el mismo periodo de tiempo, se aprobaron otros neurolépticos con estructuras no tricíclicas pero perfiles de efectos secundarios similares:
- Del grupo de sustancias de las butirofenonas (haloperidol, pipamperona, melperona),
- Del grupo de sustancias de las difenilbutilpiperidinas (fluspirileno y pimozida/ hoy ya no se comercializan).
La clasificación anterior según los aspectos químicos estructurales se basa en los libros de texto de Möller et al (2015) y Kaplan Sadock (2015).
En 1972 se aprobó en Suiza la clozapina (descubierta ya en 1959), que presentaba un perfil de acción especial y un espectro de efectos secundarios diferente al de los neurolépticos anteriores. La FDA no aprobó la clozapina hasta 1990, por lo que EE.UU. no descubrió su singularidad hasta más tarde. Fue el primer “antipsicótico atípico”:
- Del grupo de sustancias de las dibenzodiacepinas (clozapina): este grupo también es llamado los “pinos” por St. Stahl en su libro de texto debido a su terminación: Cloza-pina; Entre ellas se incluyen la olanzapina, la quetiapina (ambas estrechamente relacionadas estructuralmente con la clozapina); la asenapina y la zotepina. Lo que estas sustancias tienen en común es su perfil multirreceptor.
Otros antipsicóticos atípicos:
- Del grupo de sustancias de los benzisoxazoles (risperidona y ziprasidona); en aras de la simplicidad, el término paraguas “dones” (risperi-dones) sugerido por St. Stahl también se utiliza para las sustancias que son similares en términos de receptores: Risperidona, Paliperidona, Lurasidona, Ziprasidona. Éstos tienen una farmacología de receptores menos “rica” que los “pinos” y, a dosis más altas con EPMS, tienen UAW similares a los antagonistas sólo dopaminérgicos. La risperidona y la paliperidona también pueden provocar un aumento de la prolactina independiente de la dosis.
- Del grupo de sustancias de los derivados de la piperazina (aripiprazol, brexpiprazol y cariprazina). Estas sustancias muestran un efecto novedoso y farmacológicamente muy interesante. Son agonistas parciales de la dopamina. St. Stahl los denomina “dos pepitas y un rasgón”, lo que se remonta a sus nombres: Ari-pip-razol, Brex-pip-razol y Ca-rip-razina; en nuestro país se les conoce memotécnicamente como el ABC de los agonistas parciales de la dopamina.
Común a todas estas sustancias novedosas (“pines/dones/two pips and a rip”) es el antagonismo combinado de la serotonina (5-HT2A) y la dopamina D2. Se introdujeron en Suiza después de 1990. El aripiprazol está disponible en Suiza desde 2004, la cariprazina y el brexpiprazol desde 2018. Esto fue seguido en Europa (no en EE.UU.) por la introducción de otras sustancias antipsicóticas novedosas del grupo de las benzamidas (sulpirida en 1972 y amisulprida en 1999); la amisulprida también se considera un antipsicótico atípico, aunque es predominantemente un antagonista D2 y D3. En dosis más altas, se conocen los EPMS y especialmente el aumento significativo de prolactina.
Agonismo dopaminérgico parcial
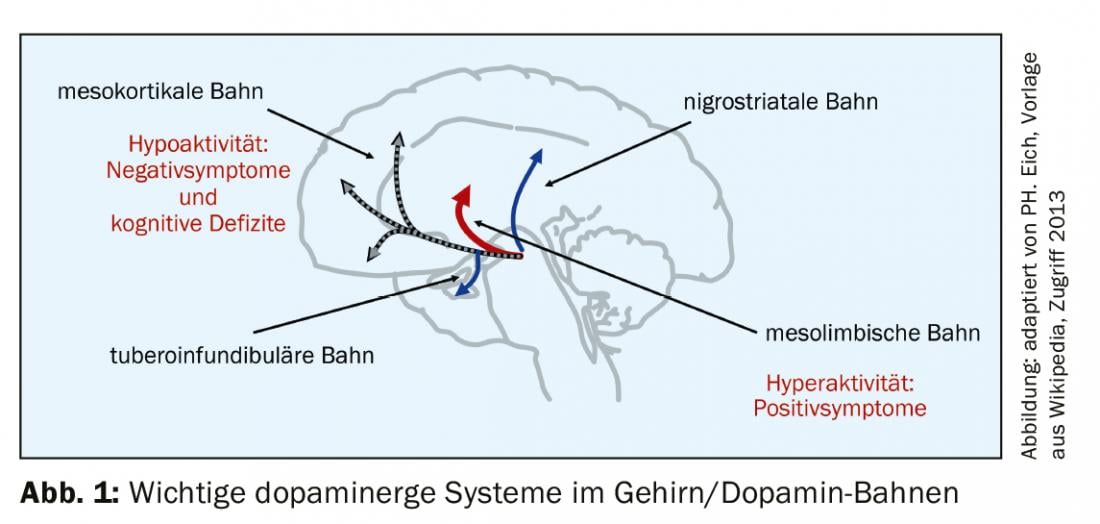
El fundamento del agonismo dopaminérgico parcial es la compensación óptima de la desregulación dopaminérgica asociada a la psicosis (hipótesis dopaminérgica de la psicosis). El trasfondo de esto son las conocidas vías de la dopamina en el cerebro (Fig. 1) . En estas condiciones tiene sentido,
- Disminuir la actividad dopaminérgica en la vía mesolímbica (mejorar los síntomas positivos como los delirios y las alucinaciones mediante una acción antagonista).
- Aumentan la actividad dopaminérgica en la vía mesocortical (los síntomas negativos, también los déficits cognitivos mejoran debido al efecto agonista sobre el receptor de la dopamina).
- no tienen ningún efecto sobre las vías nigroestriatal o tuberoinfundibular (ningún cambio en la función motora, ninguna EPMS y ningún aumento de la prolactina).
El aripiprazol consigue este efecto bloqueando simultáneamente el receptor D2 postsináptico y el autorreceptor presináptico. El resultado es un efecto agonista parcial, también intrínseco de la dopamina, de aproximadamente un 30%. Demasiado antagonismo acerca la sustancia a los antagonistas dopaminérgicos clásicos, demasiado agonismo conduce a un aumento de los síntomas psicóticos.
Los tres agonistas dopaminérgicos parciales presentan la constelación típica de los antipsicóticos atípicos con antagonismo en el eje de la serotonina con 5-HT2A, pero con el agonismo parcial antes mencionado para el receptor D2 y también para el receptor 5-HT1A, lo que podría ser una explicación del efecto antidepresivo de las sustancias.
El aripiprazol muestra escasa evidencia farmacológica de sedación (bajo bloqueo H1 y bajo efecto muscarinérgico/anticolinérgico M1). Además, tiene un escaso aumento de peso y un bajo efecto diabetógeno. El aripiprazol está disponible en Suiza desde 2004 y está a disposición de los médicos tanto por vía oral como intramuscular y también como depósito.
Stahl, el brexpiprazol es un agonista dopaminérgico más débil que el aripiprazol, pero muestra un antagonismo más fuerte sobre el receptor 5-HT2A, un efecto agonista parcial más fuerte sobre el receptor 5-HT1A y más antagonismo alfa-1. Esto significa poco EPMS y especialmente menos acatisia.
La cariprazina se comporta de forma similar al brexpiprazol en términos de antagonismo (5-HT2A) y agonismo parcial (D2 y 5-HT1A), pero tiene un agonismo parcial adicional para el receptor D3, que se cree que promueve la liberación de dopamina en el área mesocortical. Esto sería beneficioso para el tratamiento de los síntomas negativos. Las propiedades reductoras de la acatisia del brexpiprazol están menos presentes con la cariprazina. Además, al igual que con el aripirazol, el receptor de histamina está moderadamente bloqueado, lo que podría explicar cierta fatiga (St. Stahl, 2013).
Las diferencias entre los tres agonistas dopaminérgicos parciales han sido recopiladas por L. Citrome, 2018, aunque debe tenerse en cuenta que las comparaciones no se ponderan cara a cara, sino indirectamente en comparación con el placebo (Tabla 1).

Nomenclatura de los antipsicóticos
La designación química estructural de las sustancias antipsicóticamente activas se utilizaba principalmente en las publicaciones científicas y cuando se introducían nuevas sustancias. No era muy práctico en la práctica diaria de la prescripción. La mayoría de los antipsicóticos introducidos en el mercado antes de la clozapina (CH 1972/USA 1990) diferían en el intervalo de dosis y la sedación (de potencia baja frente a potencia media frente a potencia alta), pero en cuanto a la frecuencia de EPMS sólo hay diferencias menores (Resumen 1).

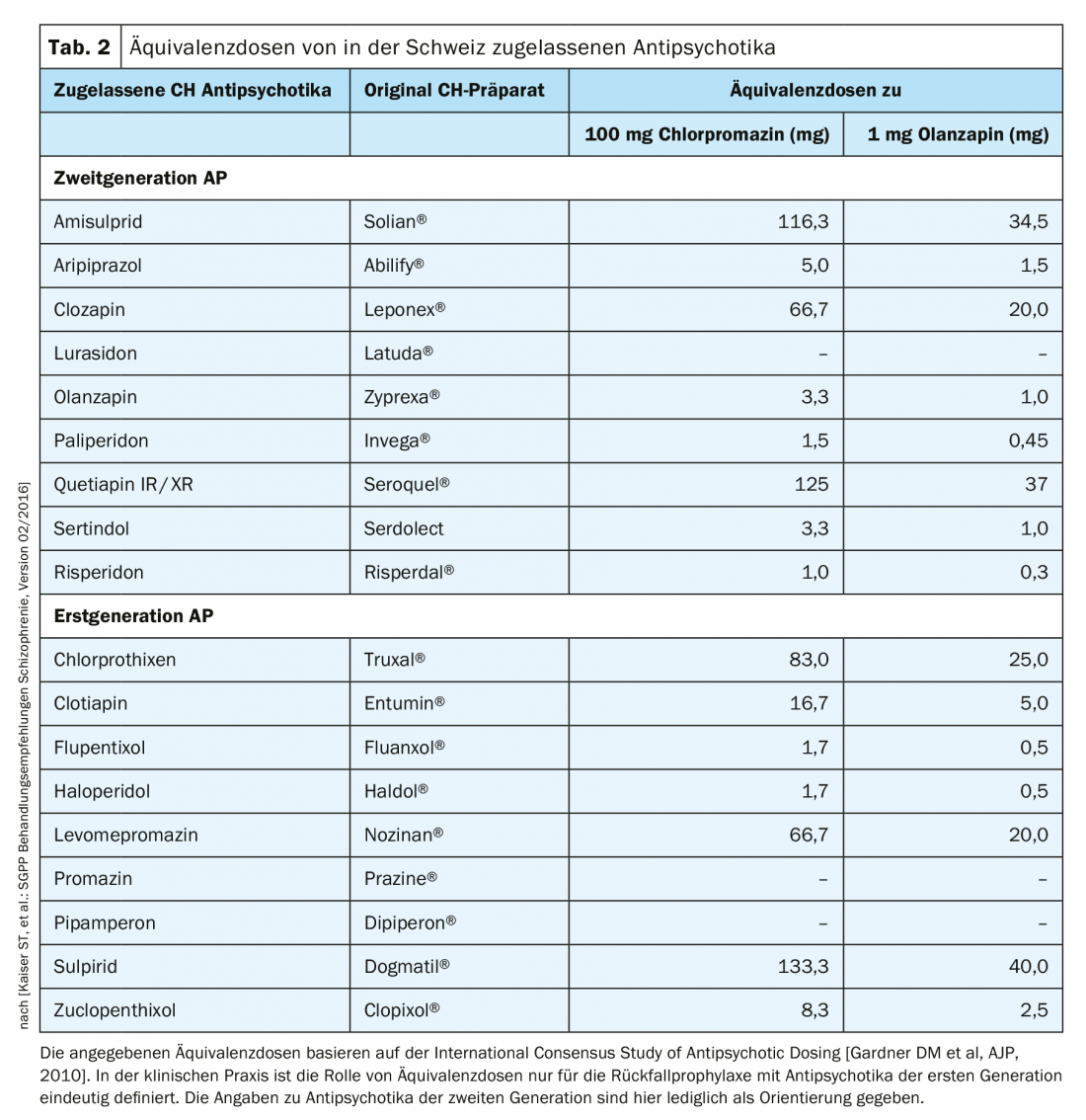
La adopción de esta clasificación según la potencia antipsicótica y las tablas de equivalencia de dosis derivadas de ella, tradicionalmente calibradas para 100 mg de clorpromazina, han quedado obsoletas para los antipsicóticos atípicos y son difíciles de establecer debido a los perfiles de efectos secundarios tan diferentes. El grupo de trabajo suizo en torno a St. Kaiser et al. no obstante, ha incluido dicha evaluación de equivalencia de los antipsicóticos atípicos, medida con 1 mg de olanzapina, en las recomendaciones de tratamiento de 2016 (tab. 2). La clozapina no provoca EPMS, discinesia tardía ni elevación de la prolactina. Su perfil de efectos secundarios se asocia, por ejemplo, a agranulocitosis, aumento de peso o sialo-rrhoea. Así, la clozapina fue la primera en ser asignada al nuevo grupo de antipsicóticos atípicos.
A diferencia de la psiquiatría europea, especialmente la germanófona, en los países anglosajones se impuso pronto el término “antipsicóticos” en lugar de neurolépticos. A más tardar desde la introducción de la clozapina en EE.UU. en 1990, sólo se habla de antipsicóticos y se distingue entre sustancias típicas y atípicas. Sinónimamente, y sobre todo en los libros de texto, se clasifican como antipsicóticos de primera generación (AGP) o antipsicóticos de segunda generación (AGS). Esto no significa una clase uniforme de sustancias, porque los antipsicóticos más nuevos son estructuralmente muy diferentes y tienen un perfil de receptores considerablemente distinto. Básicamente, en la literatura científica en lengua inglesa, todas las sustancias antipsicóticas introducidas después de 1990 se denominan “antipsicóticos atípicos” (Directrices Maudsley, 2018). En los últimos años, el Colegio Europeo de Neuropsicofarmacología (ECNP) ha propagado una nueva nomenclatura que clasifica las sustancias según su farmacología y modo de acción: Nomenclatura basada en la neurociencia (NbN2, 2018). Sólo el tiempo dirá si esta sofisticada clasificación prevalecerá. Después de todo, en su libro de texto estándar de psiquiatría, Kaplan Sadock (2015) se refiere a los antipsicóticos típicos como antagonistas de la dopamina y a las sustancias atípicas como antagonistas de la serotonina-dopamina, ya que tienen en común este principio de acción (desarrollo de la nomenclatura).
¿Qué aporta al paciente esta discusión académica?
Los pacientes suelen ser ante todo escépticos/críticos cuando se les recetan antipsicóticos. Sobre todo, para ellos es importante un efecto eficaz sin reacciones adversas a los medicamentos.
Fabricar o mantener buenos antipsicóticos desde el punto de vista del paciente (extracto):
- Sin síntomas de calambres (EPMS)
- Sin inquietud (acatisia)
- Sin lengua pesada, sin problemas de deglución (EPMS, disquinesia precoz).
- Peso corporal estable
- No sedación/sedación
- Potencia/Libido
- No hay aplanamiento del afecto
- No hay “dependencia
- Ningún “daño genético
Por lo tanto, al seleccionar un antipsicótico debe prestarse atención a una seguridad y tolerabilidad óptimas con una buena eficacia (Visión general 2) . Al mismo tiempo, los criterios mencionados son decisivos para recomendar la medicación más adecuada para el individuo. Es importante proceder en el sentido de la toma de decisiones compartida y tener en cuenta los deseos del paciente.

Para los pacientes psicóticos de primer episodio (FEP = First Episode Psychosis), la mayoría de las directrices internacionales recomiendan la administración de un antipsicótico de la 2ª generación, por la que los de la La 3ª generación también puede englobarse en esto. Esto también se aplica a las recomendaciones de tratamiento suizas (Kaiser et al. 2016/18). Los antipsicóticos de primera generación (por ejemplo, el haloperidol) son ahora la segunda opción en el tratamiento de los trastornos psicóticos. La excepción es el uso en el tratamiento del delirio (Eich PH, Nick B. 2018).
Conclusión
La farmacoterapia moderna del trastorno esquizofrénico debe cumplir múltiples funciones, es decir, la perspectiva del tratamiento en los pacientes es multifocal. Lo hará al mismo tiempo:
- Conozca los antipsicóticos de primera generación y sea consciente de sus ventajas e inconvenientes.
- Ser eficaces con el menor número posible de reacciones adversas a los medicamentos (RAM).
- Ser personalizados, es decir, adaptados a las personas afectadas (si se dispone de indicadores adecuados)
- Ser restaurador con el objetivo: Restitutio ad integrum, es decir, preservar la función y rehabilitar.
- Estar integrado en la atención basada en la comunidad y en las necesidades
Desde una perspectiva clínica, el Antipsicóticos del 2. y 3ª generación claras ventajas sobre las sustancias típicas. En relación con Hipócrates y su principio: “Primum non nocere – secundum cavere – tertium sanare” (primero, no hacer daño/no causar daño – segundo, tener precaución – tercero, curar/contribuir a la curación/traducción del autor), los agonistas parciales de la dopamina, con su favorable perfil de efectos secundarios, son definitivamente fármacos de primera elección.
Mensajes para llevarse a casa
- Los antipsicóticos siguen siendo hoy en día el pilar del tratamiento agudo y a largo plazo de los trastornos esquizofrénicos. Históricamente, en la actualidad disponemos de una gama bastante amplia de sustancias antipsicóticas modernas entre las que elegir.
- El orden del tratamiento farmacológico se basa en la psicopatología y el nivel de sufrimiento de los pacientes afectados. Debe tenerse en cuenta que cuanto antes se inicie el tratamiento antipsicótico, mayores serán las posibilidades de controlar o detener la progresión de la psicosis.
- La falta de adherencia es el factor de recaída más importante.
- El uso de antipsicóticos debe discutirse en la toma de decisiones compartida; un buen conocimiento del modo de acción y de las posibles reacciones adversas es un requisito previo.
- Los antipsicóticos de 3ª generación (aripiprazol, brexpiprazol y cariprazina) son un paso importante en la dirección correcta.
Para saber más:
- Citrome L: Psiquiatría actual, 17(4), abril de 2018
- Eich PH, Nick B: Número especial “Esquizofrenia”, Therapeutische Umschau, 01/2018.
- Kaiser ST, et al: Recomendaciones de tratamiento del SGPP para la esquizofrenia, versión de febrero de 2016; www.psychiatrie.ch/sgpp/fachleute-und-kommissionen
- Kaiser ST, et al: Recomendaciones de tratamiento SGPP para la esquizofrenia, Swiss Med Forum 2018; 18(25): 532-539.
- Taylor D, et al: The Maudsley Prescribing Guidelines in Psychiatry 13th edition, Wiley Blackwell, 2018.
- Nomenclatura basada en la neurociencia (NbN-2R), publicado por el ECNP, 2018.
- Falkai P, Wittchen HU: Diagnostisches und Statistisches Manual Psychischer Störungen DSM-5, APA, 2013; Hogrefe 2015
- Sinopsis de psiquiatría de Kaplan & Sadock, 11ª edición, Wolters Kluwer, 2015.
- Möller HJ, Laux G, Deister A: Psiquiatría, psicosomática y psicoterapia, 6ª edición, Thieme Verlag, 2015.
- Stahl ST: Psicofarmacología esencial, 4ª ed, Cambridge University Press, 2013.
- Woggon B: Behandlung mit Psychopharmaka, 3ª edición, Huber Verlag, 2009.
InFo NEUROLOGÍA Y PSIQUIATRÍA 2019; 17(6): 16-21.














